對《平均相對分子質量對化學平衡判斷的數學證明》一文的商榷
李建濤

摘要:建立模型,從另一個角度運用數學方法解析和探究“在m(總)、n(總)同時向一個方向改變的過程中,平均相對分子質量能否作為平衡標志”,最終得出結論并應用。
關鍵詞:數學解析;平均相對分子質量;化學平衡
文章編號:1008-0546(2019)06-0024-03 中圖分類號:G633.8 文獻標識碼:B
doi:10.3969/j.issn.1008-0546.2019.06.007
化學教與學2017年第10期《平均相對分子質量對化學平衡判斷的數學證明》一文(以下簡稱該文),該文系統探究化學平衡的判斷方法,總結全面、詳細,并從數學角度來證明平均相對分子質量對化學平衡的判斷,分類討論,并以函數圖像形式呈現,形象直觀,思路新穎,是難得一見的好文。但是,筆者發現該文“數學證明部分”存在一定的局限性,結論存在一定偏差,不具有普遍性。
二、存在的局限性和偏差
1.建立的模型不具有普遍性,假設的具體值太多,如A、B相對分子質量的值、反應起始投料比等于反應物化學計量系數之比等,這就使最終得到的結論要受到本身假設條件的限制,具有一定局限性。
2.利用公式2證明過程中,反應起始投料比等于反應物化學計量系數之比,在平衡建立過程中,反應物物質的量之比始終不變,物質A、B兩者的平均相對分子質量始終不變,如果起始投料比不等于反應物化學計量系數之比,在平衡建立過程中,物質A、B兩者的平均相對分子質量始終變化,此結論就無法應用。
基于以上,筆者嘗試運用數學方法從另一個角度分析,重新建立模型,探究“在m(總)、n(總)同時向一個方向改變的過程中,平均相對分子質量能否作為平衡標志”。
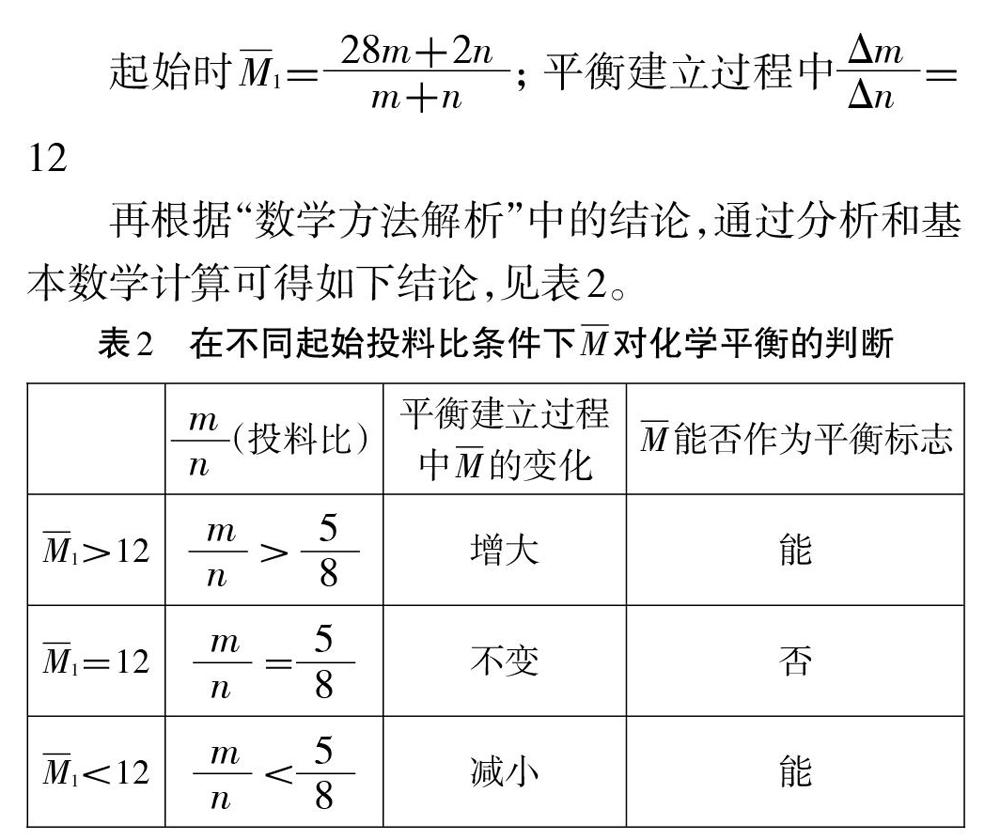
再根據“數學方法解析”中的結論,通過分析和基本數學計算可得如下結論,見表2。
四、啟示
我們在用數學方法解析化學問題時,建立的模型要具有普遍性,解析過程中,應用的物理量及其變量不宜過多,要控制變量,盡量不要將一些化學常數賦予具體值,這樣通過數學分析得出的結論,更具有應用的價值。

