半育耳蕨化學成分及其抑制α-葡萄糖苷酶活性研究
陸 懷,孫靜賢,蔣孟圓,高利斌,陳毅堅,李育逵,黃相中,田 凱,王 韋
(云南民族大學 民族藥資源化學國家民族事務委員會-教育部重點實驗室,云南 昆明 650500)
蕨類植物資源豐富,全球約11 500種, 中國有2 600多種[1]. 該類植物在我國擁有悠久的入藥歷史,不僅可以治療痢疾發(fā)熱、跌打骨折、風寒感冒、小便不利、腹痛等,還能預防流行性乙型腦炎、流行性感冒、流行性腮腺炎等病毒感染性疾病,在民間多用作消炎止痢、祛風除濕、清熱、利尿、止血藥等[2-6].石韋、卷柏、綿馬貫眾等收載于《中國藥典》(2015年版)[7].
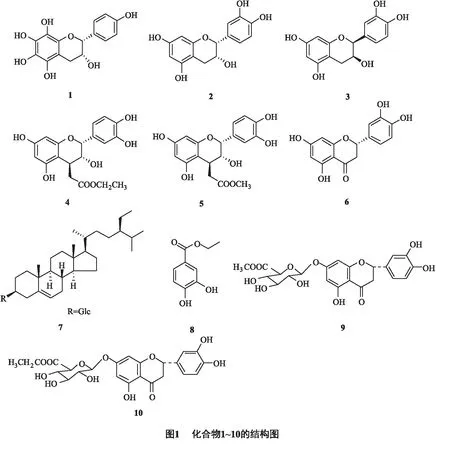
半育耳蕨(Polystichumsemifertile)是鱗毛蕨科(Dryopteridaceae)耳蕨屬植物, 主要分布于印度、尼泊爾及我國四川、云南、西藏等地. 生于海拔1 000~3 000 m 的山坡、河谷、箐溝的林下濕地[8]. 該屬植物具有止痛、潤肺止咳與清熱解毒的功效, 用于治療感冒咳嗽、瘡痛腫毒及周身疼痛等癥[9]. 此外,還有文獻報道同屬植物雞足山耳蕨對大腸桿菌、枯草芽孢菌及金黃色葡萄球菌均有抑制作用[10- 11], 尚未見對半育耳蕨化學成分研究的報道.本課題組研究發(fā)現(xiàn)半育耳蕨的乙醇提取物有較好的抑制α-葡萄糖苷酶活性,為深入了解其藥效成分,本實驗對95%乙醇提取物中的乙酸乙酯部分進行研究,從中分離得10個化合物. 活性篩選結果顯示, 化合物4、5和6具有較好的α-葡萄糖苷酶抑制活性,如圖1所示.
1 實驗部分
1.1 儀器與材料
VG Auto - Spc - 3000 型質譜儀(英國VG 公司); 旋轉蒸發(fā)儀(上海愛郎博儀器有限公司);暗箱式紫外分析儀(鞏義市予華儀器); Bruker AV- 400 核磁共振儀(瑞士Bruker公司); Agilent 1260半制備高效液相色譜儀(美國安捷倫科技公司); Sephadex LH-20凝膠(德國 Merck 公司); MCI gel(日本三菱化學株式會社),柱層析硅膠(100 ~ 200 目,200 ~ 300 目,青島海洋化工廠); HPLC流動相所用的有機溶劑為色譜純(德國默克公司); 阿卡波糖(百靈威公司); 4-硝基苯基-α-D-吡喃葡萄糖苷(PNPG),α-葡萄糖苷酶均購自Sigma公司.
半育耳蕨樣品于2017年7月采于云南新平縣,經(jīng)云南大學陸樹剛教授鑒定為P.semifertile,憑證標本(No. 20170714)存放于云南民族大學民族藥資源化學國家民族事務委員會-教育部重點實驗室的標本室.
1.2 提取與分離
10.0 kg干燥的半育耳蕨粉碎后, 用體積分數(shù)95%的乙醇回流提取3次, 合并濾液, 減壓濃縮回收溶劑, 得1.1 kg浸膏. 將浸膏混懸于適量的水中, 按極性大小依次用石油醚、乙酸乙酯、正丁醇萃取, 將萃取液減壓濃縮分別得到各個部分萃取物.
乙酸乙酯部分(198.0 g)用100~200目硅膠進行柱層析, 流動相洗脫梯度為V(氯仿)∶V(甲醇)=(15∶1~0∶1), 經(jīng)TLC檢測后合并得7個組分(Fr. 1 ~ Fr. 7). Fr. 1經(jīng)硅膠柱色譜,用V(氯仿)∶V(甲醇)=(80∶1~2∶1)進行梯度洗脫,得9個組分(Fr. 1~1 ~ Fr. 1~9). Fr. 1~3經(jīng)硅膠柱色譜V(氯仿):V(甲醇)=(80∶1~10∶1)得化合物6(14.8mg)及其他5個組分(Fr.1-3-1~Fr.1-3-5). Fr. 1-3-3經(jīng)洗脫劑為V(氯仿)∶V(甲醇)= 1∶1的Sephadex LH-20凝膠柱分離后得2個組分(Fr. 1-3-3-1~Fr. 1-3-3-2). Fr. 1-3-3-2經(jīng)硅膠柱V(石油醚)∶V(氯仿)∶V(甲醇)=(1∶1∶0~0∶1∶0~0∶40∶1)梯度洗脫得化合物8(6.5 mg). Fr. 1~4經(jīng)洗脫劑為甲醇Sephadex LH-20柱色譜及半制備HPLC純化得到化合物1(38.3 mg). Fr. 1~6經(jīng)硅膠柱色譜V(氯仿)∶V(甲醇)=(40 ∶1~2∶1)得5個組分(Fr. 1-6-1~Fr. 1-6-5). Fr. 1-6-3經(jīng)洗脫劑為V(氯仿)∶V(甲醇) =1∶1的Sephadex LH-20柱色譜洗脫后得化合物4(47.5 mg)及另外一個組分Fr. 1-6-3-1.Fr. 1-6-3-1用39%的甲醇做流動相HPLC純化得化合物10(36.3 mg).Fr. 1-6-4經(jīng)洗脫劑為甲醇的Sephadex LH-20柱色譜分離得7個組分(Fr. 1-6-4-1~Fr. 1-6-4-7), Fr. 1-6-4-5經(jīng)HPLC制備純化得化合物9(9.5 mg)和Fr. 1-6-4-5-2. Fr. 1-6-4-5-2再用洗脫劑為甲醇的Sephadex LH-20柱色譜純化得化合物3(63.0 mg). Fr. 1-6-5經(jīng)硅膠柱色譜V(氯仿)∶V(乙酸乙酯)=(4∶1~0∶1)進行梯度洗脫, 用乙酸乙酯重復洗滌得化合物2(43.0 mg). Fr. 1~8依次經(jīng)硅膠柱色譜、凝膠柱色譜、半制備HPLC及硅膠柱色譜得化合物5(27.1 mg). Fr. 3用30%~100%甲醇洗脫反相MCI柱色譜得化合物7(30.0 mg).
1.3 α-葡萄糖苷酶抑制活性
參照文獻[12]采用PNPG法測定單體化合物對α-葡萄糖苷酶的抑制活性. 實驗設置4個組, 每組3個復孔, 總體積為150 μL, 加緩沖液補足總體積. 各孔分別加入50 μL磷酸緩沖鹽溶液、10 μL DMSO溶解的待測液溶液和20 μL葡萄糖苷酶溶液, 37 ℃恒溫反應5 min后各孔均加入2.5 mmol·L-1PNPG溶液20 μL, 30 ℃下繼續(xù)恒溫反應15 min, 加入0.2 mol·L-1Na2CO3終止液50 μL, 于400 nm波長下測定吸光值. 化合物對α-葡萄糖苷酶抑制活性計算公式:抑制率(%)=[(B-B0)-(A-A0)]/(B-B0)×100%, 進一步計算其半數(shù)抑制濃度(IC50)值.其中, 樣品組(A):適量PBS緩沖液+10 μL DMSO溶解的待測樣品溶液+20 μLα-葡萄糖苷酶溶液+20 μL PNPG溶液+50 μL Na2CO3終止液; 樣品對照組(A0):適量PBS緩沖液+10 μL DMSO溶解的待測樣品溶液+50 μL Na2CO3終止液; 酶活性組(B):適量PBS緩沖液+10 μL DMSO+20 μLα-葡萄糖苷酶溶液+20 μL PNPG溶液+50 μL Na2CO3終止液; 酶空白組(B0):適量PBS緩沖液+10 μL DMSO+50 μL Na2CO3終止液.
2 結果與討論
2.1 結構鑒定
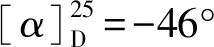


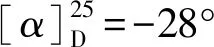
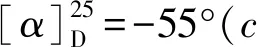
化合物6黃色粉末, 溶于甲醇. ESI-MS(m/z):287 [M﹣H]﹣,分子式為C15H12O6.1H NMR(400 MHz, C5D5N)δ:7.53(1H, d,J=1.9 Hz, H-2′), 7.29(1H, d,J=8.1 Hz, H-6′), 7.09(1H, dd,J=8.1, 1.9 Hz, H-5′), 6.47(1H, d,J= 2.0 Hz, H-8), 6.38(1H, d,J=1.8 Hz, H-6), 5.48(1H, dd,J=12.7, 2.9 Hz, H-2), 3.30(1H, dd,J=17.0, 12.8 Hz, H-3a), 2.90(1H, dd,J=17.0, 3.0 Hz, H-3b).13C NMR (100 MHz, C5D5N)δ:196.9(C-4), 169.1(C-7), 165.5(C-5), 164.4(C-9), 148.3(C-4′), 147.9(C-3′), 131.0(C-1′), 119.0(C-6′), 116.9(C-5′), 115.7(C-2′), 103.2(C-10), 97.6(C-6), 96.5(C-8), 80.2(C-2), 43.8(C-3). 以上數(shù)據(jù)與文獻[18]報道對照, 故鑒定化合物6為eriodictyol.
化合物7白色粉末, 溶于吡啶. ESI-MS(m/z):577 [M﹢H]﹢, 分子式為C35H60O6.1H NMR(400 MHz, C5D5N)δ:5.35(1H, brs, H-6), 5.05(1H, d, J=7.7 Hz, H-1′), 4.56(1H, d,J=11.1 Hz, H-6′a), 4.41(1H, dd,J=11.7, 5.2 Hz, H-6′b), 4.29(2H, m, H-3′, 4′), 4.06(1H, t,J=7.9 Hz, H-2′), 3.96(2H, m, H-3, 5′), 2.48(1H, t,J=11.6 Hz, H-17), 1.00(3H, s, H-27), 0.98( 3H, s, H-9), 0.93(3H, s, H-21), 0.89(3H, s, H-29), 0.87(3H, s, H-26), 0.66(3H, s, H-18).13C NMR(100 MHz, C5D5N)δ:141.3(C-5), 122.2(C-6), 102.9(C-1′), 78.9(C-3), 78.8(C-3′), 78.5(C-5′), 75.6(C-2′), 72.0(C-4′), 63.2(C-6′), 57.2(C-14), 56.6(C-17), 50.7(C-9), 46.4(C-24), 42.8(C-13), 40.3(C-4), 39.7(C-12), 37.8(C-1), 37.3(C-10), 36.7(C-20), 34.6(C-22), 32.5(C-7), 32.4(C-8), 30.6(C-2), 29.8(C-25), 28.9(C-16), 26.8(C-23), 24.9(C-15), 23.7(C-28), 21.6(C-11), 20.3(C-27), 19.8(C-26), 19.6(C-19), 19.4(C-21), 12.5(C-29), 12.3(C-18). 以上數(shù)據(jù)與文獻[19]報道對照, 故鑒定化合物7為daucosterol.
化合物8白色粉末, 溶于甲醇. ESI-MS(m/z):183 [M﹢H]﹢, 分子式為C9H10O4.1H NMR(400 MHz, CD3OD)δ:7.41(2H, t,J=7.6 Hz, H-2, 6), 6.80(1H, d,J=8.1 Hz, H-5), 4.29(2H, q,J=7.1 Hz, H-8), 1.35(3H, t,J=7.1 Hz, H-9).13C NMR(100 MHz, CD3OD)δ:168.4(COOH), 151.7(C-3), 146.2(C-4), 123.6(C-6), 122.9(C-1), 117.4(C-5), 115.8(C-2), 61.7(C-8), 14.7(C-9). 以上數(shù)據(jù)與文獻[20]報道對照, 故鑒定化合物8為3, 4-二羥基苯甲酸乙酯.
化合物9黃色固體, 溶于甲醇. ESI-MS(m/z):479 [M﹢H]﹢, 分子式為C22H22O12.1H NMR(400 MHz, C5D5N)δ: 7.50(1H, s, H-2′), 7.29(1H, d,J=8.0 Hz, H-5′), 7.06(1H, t,J=6.1 Hz, H-6′), 6.59(2H, m, H-6, H-8), 5.93(1H, m, H-2),5.41(1H, d,J=12.5, 1.92 Hz, H-1″), 3.60(3H, d,J=5.2 Hz, OMe), 3.27(1H, m, H-3a), 2.87(dd,J= 17.1, 2.5 Hz, H-3b).13C NMR(100 MHz, C5D5N)δ:197.8(C-4), 170.5(C-6″), 166.4(C-7), 164.8(C-5), 164.1(C-9), 148.4(C-4′), 147.9(C-3′), 130.7(C-1′), 119.1(C-6′), 116.9(C-5′), 115.7(C-2′), 104.8(C-10), 101.7(C-1″), 97.8(C-6), 96.6(C-8), 80.3(C-2), 77.8(C-5″), 77.5(C-3″), 74.7(C-2″), 73.2(C-4″), 52.4(OMe), 43.7(C-3). 以上數(shù)據(jù)與文獻[21]報道對照, 故鑒定化合物9為圣草酚7-O-β-D-(6′-甲酯基)-吡喃葡萄糖醛酸苷.
化合物10白色粉末, 溶于吡啶. ESI-MS(m/z):493 [M﹢H]﹢, 分子式為C23H24O12.1H NMR(400 MHz, C5D5N)δ:7.50(1H, s, H-2′), 7.30(1H, d,J=8.0 Hz, H-5′), 7.02(1H, m, H-6′), 6.58(1H, dd,J=1.5, 8.1 Hz, H-8), 6.49(1H, dd, J=1.5, 9.1 Hz, H-6), 5.88(1H, q, H-2), 4.80(1H, dd,J=10.0, 2.4 Hz, H-1″), 4.11(2H, m, OCH2CH3), 3.20(1H, m, H-3a), 2.81(1H, dd,J=17.0, 3.9 Hz, H-3b), 1.04(3H, q,J=7.0 Hz, OCH2CH3).13C NMR(100 MHz, C5D5N)δ:197.5(C-4), 169.8(C-6″), 166.2(C-7), 164.5(C-5), 163.9(C-9), 148.1(C-4′), 147.6(C-3′), 130.4(C-1′), 118.9(C-6′), 116.7(C-5′), 115.4(C-2′), 104.5(C-10), 101.3(C-1″), 97.6(C-6), 96.4(C-8), 80.1(C-2), 77.6(C-5″), 77.4(C-3″), 74.5(C-2″), 72.9(C-4″), 61.6(OCH2CH3), 43.5(C-3), 14.2(OCH2CH3). 以上數(shù)據(jù)與文獻[21]報道對照, 故鑒定化合物10為圣草酚7-O-β-D-(6′-乙酯基)-吡喃葡萄糖醛酸苷.
2.2 α-葡萄糖苷酶抑制活性
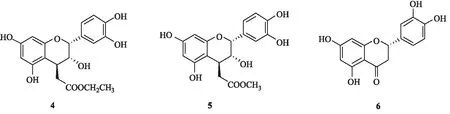
圖2 α-葡萄糖苷酶抑制活性結構
本研究對半育耳蕨的乙酸乙酯部分進行研究, 從中分離得到10個化合物, 所有化合物均首次從耳蕨屬中分離得到. 相對于陽性藥阿卡波糖, IC50為(216.0±8.7) μmol·L-1, 化合物4、5和6在抑制α-葡萄糖苷酶活性的實驗中均顯示較強的α-葡萄糖苷酶抑制作用, 其半數(shù)抑制濃度為(26.2±3.9)、(32.6±2.5)和(51.5±3.6) μmol·L-1, 為半育耳蕨以及耳蕨屬植物的進一步研究奠定了基礎.

