GLP-1受體激動劑/類似物治療2型糖尿病的研究進展
張寧倩,王 清

王清,吉林大學中日聯誼醫院內分泌科主任,主任醫師, 教授, 博士研究生導師。主要從事糖尿病、甲狀腺疾病及腎上腺、垂體、代謝疾病的臨床研究工作。主持衛生部重大課題及國家重點研發計劃項目等國家及省部級課題14項,發表學術論文100余篇,SCI文章12篇,著書8部,獲吉林省科技進步獎和吉林大學醫療技術成果獎多項。中國醫師協會內分泌代謝病分會常務委員,中國微循環學會糖尿病與微循環專業委員會常務委員、學組組長等。
2型糖尿病為臨床上常見的慢性代謝性疾病,《中國2型糖尿病防治指南(2017版)》顯示,我國18歲以上成人2型糖尿病發病率達10.4%,60歲以上的老年人糖尿病患病率均在20%以上。未診斷的糖尿病患者占總數的63%。相關糖尿病并發癥造成患者死亡率逐年上漲,控糖形式不容樂觀。近10年來一些新型降糖藥逐漸問世,其中包括GLP-1受體激動劑/類似物。
1 GLP-1RA的降糖機制及減重作用
GLP-1(Glucagon-like peptide-1,胰高血糖素樣肽-1)是由胃腸道神經內分泌細胞分泌的一種多肽。機體在正常進食后會產生內源性GLP-1來輔助胰島素降糖,但同時其很快被腸道中分泌的DPP-Ⅳ降解,故體內血糖的調控依靠胰島素及胰高血糖素等升糖激素的調節。2型糖尿病患者由于胰島素相對缺乏或胰島素抵抗等原因導致體內血糖處于較高水平,這時體內的輔助降糖物質尤為重要。傳統降糖藥二甲雙胍被推薦作為治療2型糖尿病的一線用藥[1],它能有效降低HbA1c(Hemoglobin A1c,糖化血紅蛋白),控制體重,降低心血管死亡率[1-2]及改善胰島素敏感性[3]。然而,二甲雙胍并不能影響胰高血糖素的水平[4]。研究表明,GLP-1受體激動劑(GLP-1 receptor agonist,GLP-1RA)能夠通過抑制胰島α細胞分泌胰高血糖素[5-6],并且能增加胰島素分泌及適量減重[7],能更好地控制高血糖[8]。同時,其還有延緩胃排空、減輕饑餓感,同時減少食物攝入量[9]的作用。作為GLP-1RA制劑中的一種,利拉魯肽已明確可作為一種降糖藥物長期應用于2型糖尿病的治療[10-13]。一項關于利拉魯肽治療血糖控制尚可的2型糖尿病合并慢性心臟病患者的研究證實,利拉魯肽聯合二甲雙胍治療與安慰劑聯合二甲雙胍治療比較,兩組在治療周期中胰島素敏感性均增加,但利拉魯肽聯合二甲雙胍組B細胞功能較對照組顯著改善,該研究還發現利拉魯肽聯合二甲雙胍治療組降低了餐后胰島素水平[14]。一項在我國進行的對76例體重指數(BMI)大于24 kg/m2的明確診斷為2型糖尿病的患者資料的回顧性分析中[15],根據患者BMI數值將其分為超重組(BMI:24~27.9 kg/m2),肥胖組(BMI:28~31 kg/m2)和嚴重肥胖組(BMI≥31 kg/m2),所有患者接受GLP-1RAs(艾塞那肽或利拉魯肽)3.0~29.0周(平均8.9周)治療,研究結果顯示,3組患者經GLP-1RAs治療后,BMI和內臟脂肪指數(VA)均明顯下降,超重組腰臀比(WHR)明顯降低。與超重組相比,肥胖組和嚴重肥胖組治療后體脂(包括皮下脂肪及內臟脂肪)均明顯下降,同時肌肉重量明顯增加。
2 GLP-1RA的心血管獲益
幾乎2/3的糖尿病患者最終會死于慢性心臟疾病,其中約一半為冠狀動脈疾病[16],通過生活方式干預和藥物治療改變心血管風險是必要的。GLP-1RA可以通過降低血糖、血脂、血壓及血管炎癥等作用機制有效降低心臟風險[17]。2型糖尿病導致冠狀動脈硬化與內皮細胞功能障礙有關,研究表明,GLP-1RA有減弱纖溶酶原激活物抑制劑1型(PAI-1)和血管黏附因子(VAM)在人血管內皮細胞(hVECs)體外表達的誘導作用,并可能對內皮細胞功能障礙(ECD)提供保護[18]。一項分析利拉魯肽治療2型糖尿病效果、并評估其心功能(LEADER)的試驗中,將患者隨機分為2組,每日應用1次利拉魯肽1.8 mg,另一組應用安慰劑,平均隨訪3.8年。結果表明,利拉魯肽具有較好的降糖效果,但未明確其對非致命性心肌梗死和中風的減少有顯著作用[19]。SUSTAIN-6研究顯示,索馬魯肽(Semaglutide)在降低非致命性卒中的風險以及冠狀動脈和周圍血管重建方面顯示出顯著益處[20]。同時,有研究表明,GLP-1 RA除有改善內皮功能外,還有增加心房鈉尿肽、促進鈉的排出、降血壓[21]、抑制心肌細胞凋亡、改善心臟舒縮功能的作用。一項動物實驗表明,飲食誘導的肥胖大鼠用利拉魯肽治療4周后,外周血中TG和極低密度脂蛋白的代謝得到改善,胰島素的敏感性提高[21]。
3 GLP-1RA對腎功能的影響
2型糖尿病是導致慢性腎臟病(CKD)的常見原因,后者可能發展為終末期腎病(透析或/和移植),血糖控制不佳的糖尿病患者發病年齡可能會提前。一項英國的前瞻性糖尿病研究表明,28%的2型糖尿病患者可能在診斷后的15年左右發生腎功能損傷,而腎功能的損傷可能會導致心血管疾病發生的風險[22]。2型糖尿病患者的腎功能常限制了可用的降糖方案。Manie等[23]將隨機選取的279例2型糖尿病患者[HbA1c:7%~10%,BMI:20~24 kg/m2,腎小球濾過率:30~59 ml/(min·1.73 m2)],隨機(1∶1)分為利拉魯肽組(140例,1.8 mg,1次/d皮下注射)和安慰劑組(139例)。治療26周后,血清肌酐與基線比較差異無統計學意義(P=0.26),對eGFR無顯著影響。
4 GLP-1RA劑型
我國自2009年起上市了4種GLP-1RA,均用于調節2型糖尿病患者的血糖情況,作用機制相似,首先其具有葡萄糖依賴性而促進胰島素的分泌,所以患者發生低血糖的情況很少,目前于我國上市的GLP-1RA有艾塞那肽注射液(百泌達)、注射用艾塞那肽微球(百達揚)、利拉魯肽注射液(諾和力)、貝那魯肽注射液(誼生泰)、利司那肽注射液(利時敏),其他劑型還包括度拉糖肽、Semaglutide、Albiglutide等。上述藥物按作用時間可分為短效、長效、超長效等劑型,給藥方式均為皮下注射,常用的幾種GLP-1RA藥代動力學比較見表1、表2。
目前我國上市的4種GLP-1RA均為皮下注射制劑,通過各種方式延長藥物半衰期以期待患者可以減少注射次數并且維持一定的血藥濃度,目前最長可應用1周注射1次的劑型,但受到價格及患者耐受程度等多方面影響,患者依從性仍較差,這時對口服制劑的需求就更迫切,目前,Semaglutide的前景較好,其Ⅱ期臨床研究結果顯示,經26周治療[40 mg/(人·d)]后,T2DM患者的HbA1c水平較初始值下降了1.9%,與皮下注射Semaglutide 1 mg/(人·d)]組相比,差異無統計學意義,目前該分子已經進入Ⅲ期臨床試驗[24]。
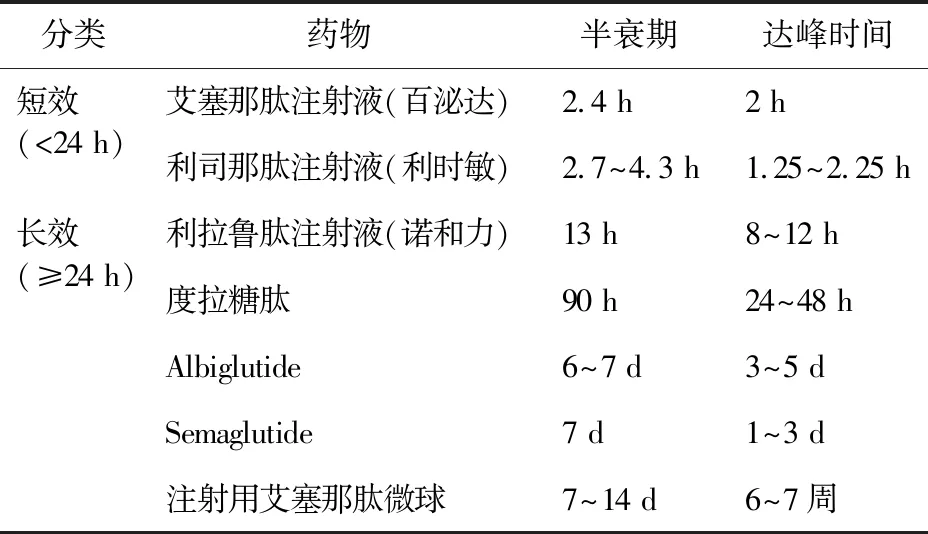
表1 GLP-1RA藥代動力學比較

表2 GLP-1RA結構、劑量、清除等比較
5 結論
結合上述關于GLP-1RA的介紹,希望能給臨床醫生做出一定參考,能夠更恰當地應用各種降糖藥物以延緩糖尿病患者心血管及其他器官并發癥的發生,在可能減輕用藥負擔的同時,能夠更好地降糖,使糖尿病患者的患病率及病死率下降。

