氣相色譜-串聯質譜法測定水果、蔬菜中乙烯利的殘留量
周婷婷,陳盧濤,周 敏,俞璐萍,劉小羽,黎 斌,胡晉峰,朱萌萌,*
(1.綠城農科檢測技術有限公司,浙江杭州 310000;2.安徽農業大學/茶與食品科技學院/茶葉生物與利用國家重點實驗室,安徽合肥 230036)
乙烯利又名2-氯乙基磷酸,是一類人工合成的植物生長調節劑,在植物體內可以通過釋放乙烯來參與調節植物生長的各種生理過程,比如可以催熟西瓜、蘋果、梨等水果,使柿子催熟脫澀,促進棉花增花,使小麥、水稻等作物秸稈矮化等[1]。由于乙烯利屬于低毒類植物生長調節劑,近年來,乙烯利在果蔬催熟中被廣泛使用,已有研究表明,長期食用會對人的健康和生命造成一定的危害,一定濃度的乙烯利可引起局部及頭腦腎損害,導致中樞麻痹,加速人體衰老[2]。歐盟對乙烯利在葡萄、桔子、桑葚等水果、蘿卜、番茄、黃瓜等蔬菜中的最大殘留限量均為0.05 mg/kg;美國對乙烯利在番茄中的最大殘留限量為2.0 mg/kg;我國《GB 2763-2016食品安全國家標準 食品中農藥最大殘留限量》中規定乙烯利在辣椒、番茄中的最大殘留限量分別為2.0、5.0 mg/kg,在葡萄、哈密瓜中的最大殘留限量為1.0 mg/kg,在獼猴桃、荔枝、芒果、香蕉、菠蘿中的最大殘留限量為2.0 mg/kg。
目前,國內外對果蔬中乙烯利檢測分析方法主要有頂空氣相色譜法結合氫火焰離子檢測器(HS/GC-FID)[3-6],此類方法易產生假陽性結果。另外一類方法是將乙烯利用重氮甲烷進行甲基化衍生化后形成乙烯利二甲酯,結合氣相色譜火焰光度檢測器進行檢測(GC-FPD)[7],而重氮甲烷在制備和存儲過程中易燃易爆,且具有較強的毒性和刺激性,但其反應速度快,效率高,產生雜質少。近幾年液相色譜-串聯質譜法(HPLC-MS/MS)較多地用于乙烯利等植物生長調節劑的檢測分析[8-10],但需要特殊的色譜柱及洗脫條件,不具有一定的普遍適用性。此外三甲基硅重氮甲烷[11]、N,O-雙(三甲基硅烷)三氟乙酰胺(BSTFA)[12]也常用于乙烯利的衍生化反應檢測分析中。衍生化試劑MTBSTFA反應性較強,衍生物揮發性較好,易與羥基、羧羥基、一級胺和二級胺中的活潑氫反應,不與脂肪酸反應;可形成特丁基二甲基硅的衍生物,其在質譜中易失去特丁基形成高豐度[M-57]+特征離子,適于MS定量分析,已廣泛用于硝基苯酚、癸醇、二羧酸等化合物的衍生化反應[13]。氣相色譜串聯質譜(GC-MS/MS)具有定性準確度高、抗基質干擾能力強、定量測定靈敏度高等優點,已經廣泛用于農產品、食品、土壤等樣品中農藥殘留、塑化劑、多氯聯苯等化合物的分析檢測。本文擬采用衍生化試劑N-(特丁基二甲基硅烷)-N-甲基三氟乙酰胺(MTBSTFA)、N,O-雙(三甲基硅烷)三氟乙酰胺(BSTFA)結合GC-MS/MS方法對果蔬中乙烯利化合物殘留量進行檢測分析,并比較其差異,旨在探究一種操作簡單、檢出限低、靈敏度高的前處理及衍生化方法,用于果蔬中痕量乙烯利化合物殘留量的檢測分析。
1 材料與方法
1.1 材料與儀器
乙烯利標準品 純度≥96.0%,德國Dr Ehrenstorfer公司;N-(特丁基二甲基硅烷)-N-甲基三氟乙酰胺(MTBSTFA)硅烷化試劑 純度≥97.0%,美國Regis公司;MTBSTFA+1% t-BDMCS 純度≥95.0%,美國Regis公司;N,O-雙(三甲基硅烷)三氟乙酰胺(BSTFA)硅烷化試劑 純度≥99.0%,美國Regis公司;甲醇 色譜純,美國J T Baker公司;甲苯、鹽酸、無水乙醚、吡啶、苯 分析純,國藥集團化學試劑有限公司;試驗室所用水 均為去離子水;微孔有機濾膜(0.22 μm) 天津博納艾杰爾科技有限公司。
氣相色譜-串聯質譜儀:GC-2010 plus-TQ8040,VF-5MS色譜柱(30 m×0.25 mm×0.25 μm) 日本Shimadzu公司;ST-16R型離心機 美國Thermo Fisher 公司;BSA2202S型電子天平 德國Sartorius公司;漩渦混合器 美國Henry Troemner 公司;KQ5200E型超聲波清洗器 昆山市超聲儀器有限公司;AutoEVA-20L型全自動平行濃縮儀 福建睿科儀器有限公司;CHK-121型臺式精密酸度計 北京昌科儀自動化科技有限公司。
1.2 實驗方法
1.2.1 樣品的提取及衍生化 參考文獻[13]的方法,以水果、蔬菜樣品為研究對象,先將樣品切碎混勻均一化制成勻漿,然后稱取制備好的試樣10.00 g于50 mL聚乙烯離心管中,加入20.0 mL提取溶劑甲醇,渦旋器振蕩1.0 min,加入一定體積的鹽酸水溶液(V/V=1∶1,調節pH),在200 W功率下超聲提取20 min,在5000 r/min下離心3.0 min,取上清液于50.0 mL聚乙烯容量瓶中,殘渣再次加入20.0 mL甲醇,在200 W功率下超聲提取20 min,合并提取液于50.0 mL聚乙烯容量瓶中,用甲醇定容至50.0 mL,待衍生。
取10.0 mL萃取液于15 mL聚乙烯離心管中,在35 ℃水浴條件下緩緩氮吹至液面不再下降,即甲醇全部揮發,向離心管中加入5.0 mL無水乙醚,渦旋3.0 min,靜置10 min,將乙醚層液體轉移至另一聚乙烯離心管中,殘留液加入5.0 mL無水乙醚,重復提取一次,合并提取液,35 ℃水浴條件下緩緩氮氣吹至乙醚完全揮發。向該離心管中加入100 μL甲苯,渦旋30 s,加入衍生化試劑MTBSTFA 10 μL,渦旋30 s后,蓋嚴塞子,60 ℃水浴反應30.0 min后,用甲苯定容至1.0 mL,渦旋后過0.22 μm有機相濾膜,進GC-MS/MS分析。
1.2.2 標準溶液的配制及衍生化 稱取乙烯利0.0101 g,用色譜純甲醇定容至25.0 mL,得到387.84 mg/L標準儲備溶液;用甲醇稀釋為10.0 mg/L的標準工作溶液,于0~4 ℃保存。
取一定體積的乙烯利標準工作溶液至于具塞離心管中,緩緩氮氣吹至甲醇完全揮發,向該離心管中加入100 μL甲苯,渦旋30 s,加入10 μL衍生化試劑MTBSTFA,其余步驟同1.2.1衍生化過程,圖1為乙烯利與MTBSTFA的衍生化反應原理。由于MTBSTFA對水分敏感,在與乙烯利反應前必須除去樣品中的痕量水,主要是通過和甲醇重復共蒸發來實現的。
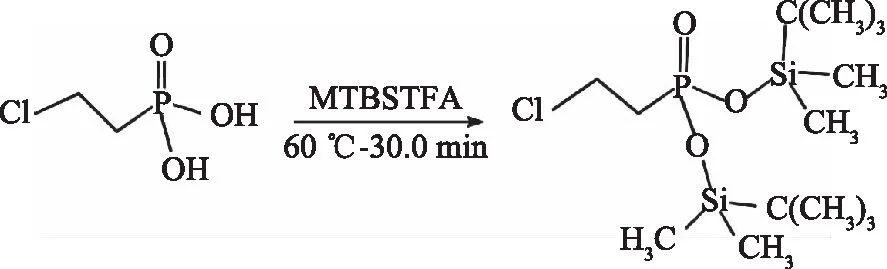
圖1 乙烯利與MTBSTFA的衍生化反應
1.2.3 提取條件的優化
1.2.3.1 提取溶劑的選擇 乙烯利具有較強的極性和親水性,在水中的溶解度大于1000 g/L,易溶于水、甲醇、乙醇、丙酮、乙醚,微溶于苯和二氯乙烷,不溶于石油醚,常用的提取溶劑有水、甲醇、乙醇、丙酮等。由于MTBSTFA對水分敏感,不能用水作為乙烯利的提取劑,本試驗考察了甲醇、乙醇和丙酮3種提取溶劑對乙烯利提取效果的影響。按照1.2.1節所述方法分別加入3種提取溶劑:甲醇、乙醇和丙酮進行提取,加入衍生化試劑MTBSTFA 10 μL,用甲苯定容至1.0 mL,渦旋后過0.22 μm有機相濾膜,檢測回收率。
1.2.3.2 提取pH的優化 乙烯利在室溫、pH<3.0的條件下比較穩定,本試驗以甲醇為提取溶劑,MTBSTFA作為衍生化試劑,比較了不同pH條件下的提取效率。稱取10.00 g葡萄樣品,加入20.0 mL甲醇,渦旋器振蕩1.0 min,加入一定體積的鹽酸水溶液(V/V=1∶1,調節pH),調節樣品溶液pH分別為1.0、2.0、3.0、4.0、5.0、6.0,按照1.2.1節所述方法進行提取和衍生,用甲苯定容至1.0 mL,渦旋后過0.22 μm有機相濾膜,檢測回收率。
1.2.4 衍生化條件的優化
1.2.4.1 衍生化試劑的考察 幾種硅烷化試劑如N-甲基-N-(三甲基硅烷)三氟乙酰胺(MSTFA,CAS:24589-78-4)、N,O-雙(三甲基硅烷基)三氟乙酰胺(BSTFA,CAS:25561-30-2)常用于磷酸或羧酸基團的衍生化反應[15],但MTBSTFA在衍生化產物的得率和重復性上效果較其它衍生化試劑要好。本試驗比較了BSTFA、MTBSTFA和MTBSTFA+1% t-BDMCS三種衍生化試劑用于乙烯利衍生化反應的優劣。在3個具塞離心管中分別加入10.0 mg/L的乙烯利標準工作溶液0.1 mL,在常溫條件下,氮氣流緩緩吹干有機溶劑,向離心管中加入100 μL甲苯,渦旋30 s,分別加入衍生化試劑BSTFA、MTBSTFA和MTBSTFA+1% t-BDMCS 10 μL,渦旋30 s后,蓋嚴塞子,60 ℃水浴反應30.0 min后,用甲苯定容至1.0 mL,渦旋后過0.22 μm有機相濾膜,檢測乙烯利衍生化產物的響應。
1.2.4.2 衍生化試劑添加量的優化 對衍生化試劑MTBSTFA添加量進行了優化,在6個具塞離心管中分別加入10.0 mg/L的乙烯利標準工作溶液0.1 mL,在常溫條件下,氮氣流緩緩吹干有機溶劑,分別添加衍生化試劑MTBSTFA 5.0、10.0、15.0、20.0、25.0、30.0 μL,按1.2.1操作過程進行衍生化反應,并將最終體積定容為1.0 mL上機分析,檢測乙烯利衍生化產物的響應。
1.2.4.3 衍生化溫度的優化 對衍生化溫度進行了優化,向5個具塞離心管中分別加入10.0 mg/L的乙烯利標準工作溶液0.1 mL,在常溫條件下,氮氣流緩緩吹干有機溶劑,分別設置衍生化溫度為40、50、60、70、80 ℃,按1.2.1操作過程進行衍生化反應,并將最終體積定容為1.0 mL上機分析,檢測乙烯利衍生化產物的響應。
1.2.4.4 衍生化時間的優化 對衍生化時間進行了優化,向6個具塞離心管中分別加入10.0 mg/L的乙烯利標準工作溶液0.1 mL,在常溫條件下,氮氣流緩緩吹干有機溶劑,分別設置衍生化時間為10、20、30、40、50、60 min,按1.2.1操作過程進行衍生化反應,并將最終體積定容為1.0 mL上機分析,檢測乙烯利衍生化產物的響應。
1.2.5 儀器條件
1.2.5.1 色譜條件 進樣口溫度:250 ℃;載氣:高純氦氣;碰撞氣:高純氬氣,純度≥99.999%;柱流量:1.0 mL/min;進樣方式:不分流進樣,1.0 min后開閥;進樣量:1 μL;定量方法:外標法;升溫程序:80 ℃保持0 min,以40 ℃/min升至250 ℃,保持0 min,以20 ℃/min升至290 ℃,保持3.75 min。
1.2.5.2 質譜條件 色譜-質譜接口溫度:280 ℃;電離方式:EI;電離能量:70 eV;離子源溫度:230 ℃;檢測器電壓:0.99 kV(+0.4 kV);測定方式:MRM多重反應監測模式;定性、定量離子、碰撞能量等參數見表1。
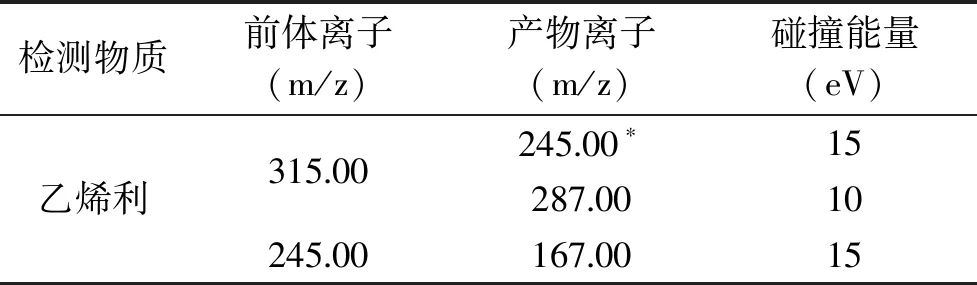
表1 乙烯利質譜檢測參數Table 1 The MS/MS parameters of ethephon
1.2.6 方法學考察
1.2.6.1 基質效應(ME) 由于食品樣本基質背景復雜,且前處理過程用到大量有機試劑、酸和衍生化試劑,可能對目標物的響應產生一定的影響,基質效應成為影響分析結果的精確度和精密度的關鍵因素,為了提高分析結果的準確度,本實驗按照添加法定量評價基質效應強度[16]的方法對基質效應進行考察,分別選取不含乙烯利的4種蔬菜空白樣品:蘿卜、西葫蘆、辣椒、番茄,4種水果空白樣品:葡萄、草莓、香蕉、油桃,按1.2.1前處理方法處理后,通過測定空白提取液與純溶劑中添加相同濃度(濃度:1.00 mg/kg)分析物的離子響應強度,考察不同基質條件對乙烯利化合物響應的影響,ME的計算公式如下:
式中:A為基質標準溶液峰面積;B為純溶劑標準溶液峰面積。
1.2.6.2 線性范圍、檢出限和定量限 采用相應基質匹配標準曲線進行標準定量,配制成0.01、0.05、0.1、0.2、0.5、1.0 mg/L 6個質量濃度的乙烯利化合物,以峰面積為縱坐標,標準樣品的質量濃度為橫坐標繪制標準曲線。分別在空白基質中添加0.200和0.600 μg/kg的乙烯利,按1.2.1前處理方法處理后,測試其信噪比,分別確定檢出限和定量限,以信噪比S/N≥3得到目標物的檢出限(LOD),以信噪比S/N≥10得到目標物的定量限。
1.2.6.3 穩定性實驗 向7個具塞離心管中加入10.0 mg/L的乙烯利標準工作溶液0.1 mL,按1.2.1操作過程進行衍生化反應,并將最終體積定容為1.0 mL,分別于0、2、4、6、8、10、12 h進樣1.0 μL,測定乙烯利衍生物峰面積,計算其相對標準偏差。
1.2.6.4 添加回收實驗 稱取市售的蘿卜、辣椒、葡萄、草莓、香蕉5個空白樣品中進行3個水平的添加回收實驗,添加濃度分別為:0.0100、0.0200和0.0500 mg/kg,每個添加水平重復3次,按照1.2.1節所述方法進行回收率實驗和精密度實驗。
1.3 數據處理
上述數據經過日本Shimadzu公司的GCMS solution軟件、Excel軟件及美國GraphPad公司的GraphPad Prism 5軟件統計分析并制圖。
2 結果與分析
2.1 提取溶劑的選擇
在所選提取溶劑用量一致的情況下,分別選擇甲醇、乙醇和丙酮作為提取溶劑。結果表明,丙酮的提取效率明顯低于甲醇、乙醇,而甲醇和乙醇的提取效率接近(圖2)。考慮到丙酮毒性較甲醇、乙醇大,且丙酮提取基質中的色素等雜質較多,會對后續凈化效果產生一定的影響;甲醇沸點較乙醇低,在氮吹過程中可節約樣品前處理時間,綜合考慮,選擇甲醇作為提取溶劑。
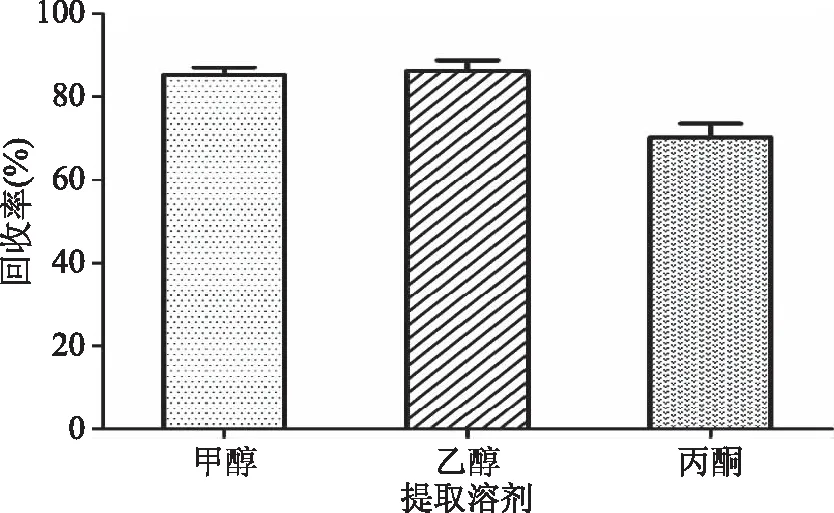
圖2 提取溶劑對萃取效果的影響(n=6)
2.2 提取pH的選擇
乙烯利的穩定性受pH的影響較大,在以甲醇作為提取溶劑的條件下,考察了乙烯利在不同pH提取條件下的回收率(見圖3),結果表明,當乙烯利在pH<4.0的條件下進行萃取,回收率均在80.0%以上,且較為穩定;在pH為4.0時,回收率達到最大;隨著pH的升高,當pH為5.0、6.0時,回收率持續下降,可能是由于乙烯利在pH>4.0的溶液中存在部分降解,導致回收率偏低且不穩定。綜合考慮,選擇pH為4.0的萃取溶液環境。
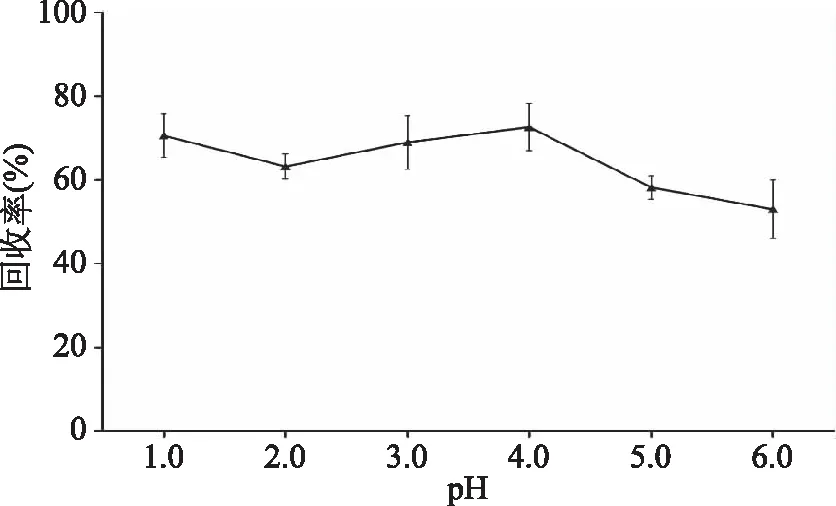
圖3 pH對萃取效果的影響(n=6)
2.3 衍生化試劑的選擇
本實驗最初采用BSTFA用于乙烯利標準工作溶液的衍生化反應,衍生后進GC-MS/MS分析,發現乙烯利經BSTFA衍生后,產物的重復性較差,在進樣口若使用硅烷化、未添加玻璃棉的襯管,RSD<20%;若使用未硅烷化、添加玻璃棉的襯管,RSD>50%,可能一方面是因為未硅烷化襯管表面的硅醇基極易和樣品發生作用,另一方面是因為BSTFA衍生后產物不穩定,導致重復性較差,這與Purdon的實驗結果是一致的[17]。本實驗后采用MTBSTFA和MTBSTFA+1% t-BDMCS用于乙烯利標準工作溶液的衍生化反應,且衍生化效率用峰面積來表示(見圖4),結果表明,乙烯利經MTBSTFA衍生后產物的峰面積是經MTBSTFA+1% t-BDMCS衍生后產物響應的1.16倍左右,說明使用不含1% t-BDMCS的MTBSTFA結合GC-MS/MS法更適合乙烯利的檢測分析,這與Young等人使用MTBSTFA對環烷酸進行衍生化反應得到的結論一致[18]。

圖4 MTBSTFA+1% t-BDMCS與MTBSTFA對衍生化效率的影響(n=6)
2.4 衍生化試劑添加量選擇
衍生化反應一般受衍生化試劑量的影響較大,在衍生化試劑MTBSTFA不同添加量的條件下,考察衍生化效率用用峰面積來表示(見圖5),結果表明,當MTBSTFA的添加量為5.0 μL時,乙烯利衍生后產物的峰面積最小,隨著MTBSTFA添加量的增加,乙烯利衍生后產物的響應逐漸提高,當MTBSTFA的添加量為10.0 μL時,乙烯利衍生后產物的峰面積最大,當添加量>10.0 μL時,衍生后產物峰面積有所降低并呈穩定趨勢。為保證衍生化反應完全,并綜合考慮試驗成本,選擇MTBSTFA的添加量為10.0 μL。
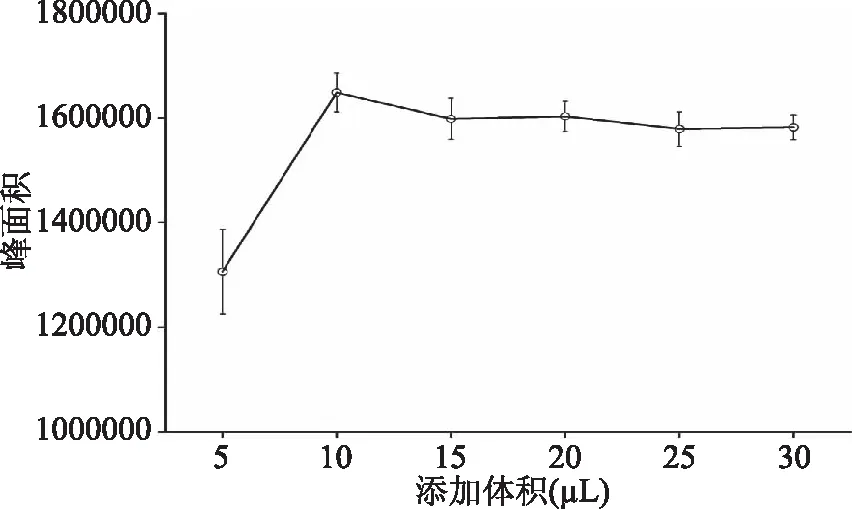
圖5 衍生化試劑添加量對衍生化效率的影響(n=3)
2.5 衍生化試劑溫度選擇
乙烯利是化學性質不穩定的一種化合物,可以通過堿水緩慢釋放出,在室溫或中等堿性條件下,乙烯利的降解比較緩慢,在pH為9的條件下,乙烯利的半衰期僅為1 d,但隨著pH和溫度的升高,乙烯利會發生明顯的降解[13]。在設置不同衍生化溫度的條件下,且衍生化效率用峰面積來表示(見圖6),結果表明,當衍生化溫度為40 ℃時,乙烯利衍生后產物的響應最小;隨著衍生化溫度的升高,乙烯利衍生后產物的響應逐漸提高;當衍生化溫度為60 ℃時,衍生后產物響應達到最高;衍生化溫度繼續升高時,乙烯利衍生后產物的響應又略有降低,可能是由于溫度升高,乙烯利發生部分降解,導致衍生后產物響應降低,溫度越高,降解越明顯。綜合考慮,選擇衍生化溫度為60 ℃。
2.6 衍生化試劑時間選擇
在設置不同衍生化時間的條件下,且衍生化效率用峰面積來表示(見圖7),結果表明,當衍生化時間為10 min時,乙烯利衍生后產物的響應最小;隨著衍生化時間的延長,乙烯利衍生后產物的響應逐漸提高;當衍生化時間為30~60 min時,衍生后產物響應最高并趨于穩定,考慮日常檢測樣品的效率,選擇衍生化時間為30 min。

圖7 衍生化時間對衍生化效率的影響比較(n=3)
2.7 氣相色譜-質譜條件的優化
在電子轟擊離子源(EI)檢測模式下對乙烯利衍生后產物進行一級質譜分析(Q3 Scan),在質譜圖中選擇質荷比較大,絕對強度較大的離子為前體離子(見圖7),M/Z為315的碎片離子相對強度最高;M/Z為287和245的碎片離子相對強度次之,故選擇315、287和245共3個碎片離子作為前體離子進行二級質譜掃描。設定3~45 eV(每3 eV一個間隔)的碰撞能量,對選定的前體離子峰進行二級質譜分析(產物離子掃描),根據二級質譜圖,離子強度最大的245被選擇為定量離子,離子強度次之的287和167被選為定性離子。圖8、圖9分別為使用優化后的氣相色譜質譜條件采集乙烯利衍生后產物的MRM質譜圖和色譜圖。

圖8 乙烯利硅烷化衍生物的全掃描質譜圖
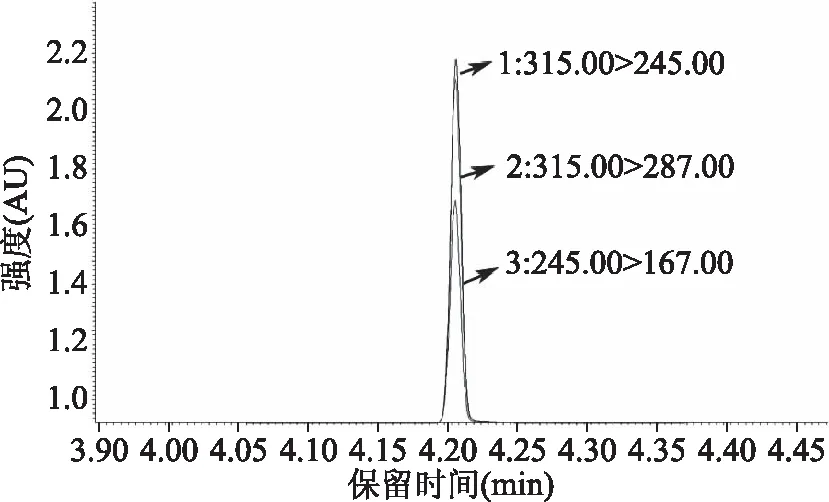
圖9 乙烯利MRM色譜圖
2.8 基質效應的考察
本實驗分別測定空白提取液與純溶劑中添加相同濃度分析物的離子響應強度,考察了在添加1.00 mg/kg條件下,不同基質條件對乙烯利化合物響應的影響。結果表明(見圖10),乙烯利衍生后產物在不同基質中均存在基質增強效應,在蘿卜、西葫蘆、辣椒、番茄中A/B<1.2,基質干擾程度較低。在葡萄、草莓、香蕉中A/B>1.2,說明存在中等程度的基質干擾效應。在水果中的基質效應強于在蔬菜中的基質效應,可能是由于水果中富含葡萄糖、果糖、蔗糖、有機酸、果膠等多種成分,在前處理過程中未得到有效的凈化,而一般熱極性、不穩定、具有氫鍵結果能力的農藥在氣相色譜殘留分析中較易產生基質效應。在基質效應存在的情況下,本試驗選取基質匹配標準曲線定量,可以一定程度上降低基質效應的影響,使定量結果更加準確。

圖10 不同基質對乙烯利的基質效應影響(n=3)
2.5 線性范圍、檢出限和定量限
采用空白基質匹配標準曲線進行定量,以儀器響應峰面積對目標化合物的質量濃度進行線性回歸,線性關系良好(R2≥0.999)。在空白基質中添加0.200、0.600 μg/kg的乙烯利,按1.2.1前處理方法處理后,以信噪比S/N≥3得到目標物的檢出限(LOD),以信噪比S/N≥10得到目標物的定量限,具體見表2。檢出限、定量限分別為0.200、0.600 μg·kg-1。

表2 乙烯利衍生化化合物的線性方程、相關系數、檢出限和定量限Table 2 Linear equations,correlation coefficient,limit of determination(LOD) and limit of quantitation(LOQ)of ethephon derivatization compound
2.6 穩定性
通過測定供試樣品溶液中乙烯利0、2、4、6、8、10、12 h內濃度的相對標準偏差(RSD),其值為2.1%,表明供試樣品溶液中乙烯利衍生物在12 h內保持穩定。
2.7 回收率、精密度
通過在不同基質樣品中添加0.0100、0.0200和0.0500 mg/kg三個濃度水平的乙烯利,每個加標水平平行測定3次,其平均回收率范圍為81.3%~105.0%,相對標準偏差小于5.4%,具體結果(見表3)。
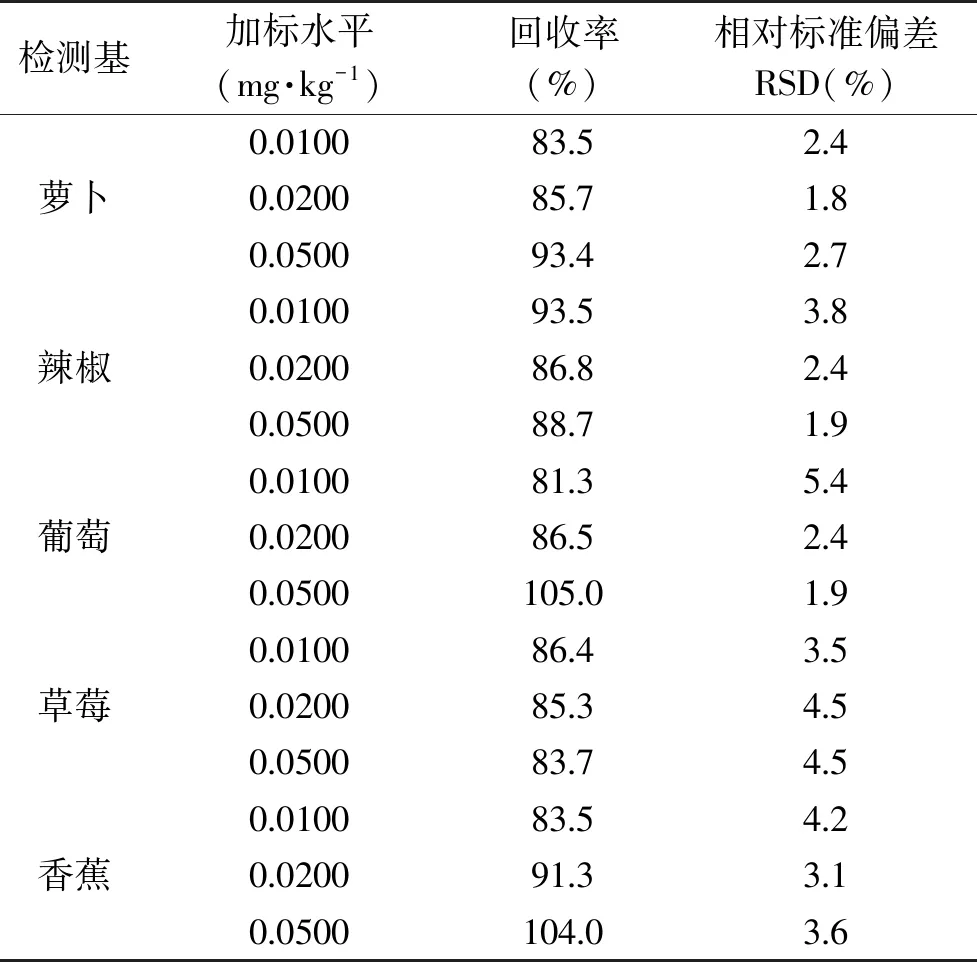
表3 乙烯利加標回收率及相對標準偏差(n=3)Table 3 Recoveries and RSD of ethephon
3 結論
本文比較了衍生化試劑BSTFA、MTBSTFA、MTBSTFA+1% t-BDMCS用于乙烯利衍生化反應的差異,并對前處理方法及儀器色譜條件進行優化,發現在pH為4.0的條件下,以甲醇作為提取溶劑,采用MTBSTFA在添加量為10 μL、60 ℃條件下衍生反應30.0 min,結合GC-MS/MS進行分析檢測,取得較好的效果。在0.1~1.0 mg/L的濃度范圍內,線性關系良好,決定系數大于0.999,檢出限為0.200 μg/kg,定量限為0.600 μg/kg,在三個不同添加水平下的平均回收率為81.3%~105.0%,相對標準偏差小于5.4%。優化后的方法操作簡便,反應溫和,同時避免使用易燃易爆,且具有較強的毒性和刺激性的重氮甲烷進行衍生,可用于水果、蔬菜中乙烯利的定量檢測。

