控制性超促排卵治療對胎盤組織的病理學影響
呂紅娟 朱新玲 袁倩
體外受精-胚胎移植(in vitro fertilization and embryo transfer,IVF-ET)治療的控制性超促排卵(controlled ovarian hyperstimulation,COH)是讓多個卵泡同時發育成熟,體內雌激素水平在一段時間內處于超生理狀態。促排卵導致的卵巢過度刺激征(ovarian hyper-stimulation syndrome,OHSS),特別是重度OHSS是致命的,據統計發生率在0.5%~2%之間[1]。我院以正常妊娠母體為對照,探討控制性超促排卵治療后新鮮胚胎移植以及凍融胚胎移植對胎盤組織的病理學影響。
對象與方法
一、對象
本研究對象來自于2014年1月—2014年12月在青島市婦女兒童醫院產科門診就診的150名孕婦。其中人工助孕組100例(IVF-ET組和凍融組),自然妊娠孕婦(正常組)50例。所有參加者均為自愿參加,填寫知情同意書后,為其建立詳細的病歷登記資料,留存聯系方式。該研究經過單位倫理委員會批準。
納入標準:單胎初次妊娠;年齡20~35歲;血常規、生化、X線胸透和心電圖檢查結果均正常,夫妻雙方染色體核型均正常。人工助孕組(IVF-ET組和凍融組)均要求不孕原因為單純輸卵管因素或男方因素等非免疫因素;凍融組要求自然周期妊娠;正常對照組要求妊娠前3個月未使用任何激素類藥物。
排除標準:排除受孕夫妻任一方有家族遺傳性疾病史及不良妊娠史者;促排卵過程中發生OHSS者;孕中晚期出現產科并發癥,如妊娠期糖尿病、妊娠高血壓或合并甲狀腺功能異常者。
150例孕婦中,7例因后期失訪被剔除,失訪率為4.7%。隨訪過程中剔除妊娠期合并癥孕婦共22例(IVF-ET組9例,凍融組9例,正常妊娠組4例), 剩余121例數據進入統計分析階段。其中IVF-ET組39例,凍融組40例,正常組42例。
二、研究方法
1.胎盤標本采集與處理:胎盤娩出后,在胎盤母體面底板區的中間帶和中央帶不同部位隨機取3塊組織,在 4%戊二醛固定液中切成1 mm3的組織塊,經固定→脫水→滲透→包埋后用 Leica 超薄切片機切片,經醋酸雙氧鈾、硝酸鉛雙重電子染色后,在日立H-7500型透射電鏡下觀察及拍照。
2.終末絨毛的主要觀察指標,包括:絨毛間質(絨毛水腫,纖維素沉積)以及細胞滋養層細胞(cytotrophoblast,CT)、 合體滋養層細胞(syncytiotrophoblast,ST)及其亞結構(微絨毛密度、細胞漿內囊泡、核固縮、鈣化及其他結構)。對所觀察到的各項指標進行定量和半定量評估(表1)。每一例標本隨機選取3個戊二醛固定的組織塊,每一個組織塊隨機選取5個觀測視野,并在5 000×、12 000×和25 000×放大倍數下進行觀察和測量。因此,對于每一例樣本,共獲得15個隨機測定的指標數據,借此減少個體差異。
3. 染色與免疫組化:在胎盤母體面垂直取下約1 cm3大小的組織,立即投入4%中性福爾馬林液中固定24~48 h后,常規脫水、石蠟包埋,待HE染色及免疫組化染色。
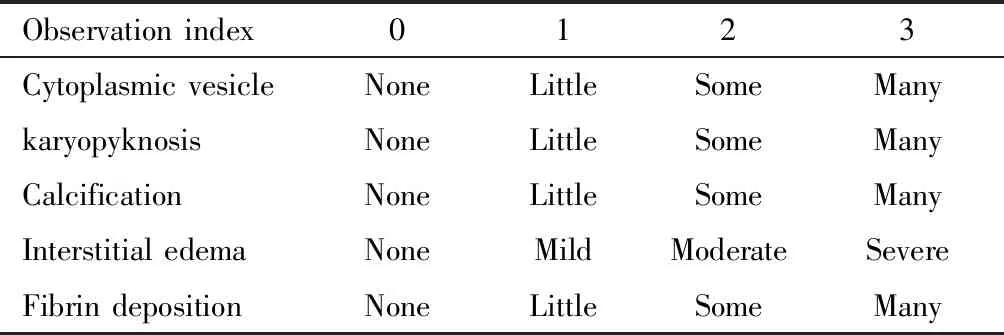
表1 評估合體滋養層細胞細胞漿內囊泡、核固縮、鈣化以及絨毛間質水腫和纖維素沉積的半定量標準Table 1 Semi-quantitative criteria for the evaluation of cytoplasmic vesicles, nuclear shrinkage, calcification, chorionic stromal edema and cellulose deposition insyncytiotrophoblast cells
4.稱重:胎盤取材后,自胎盤臍帶根部剪除臍帶稱取胎盤重量,記錄新生兒出生體重。

結 果
1.孕婦年齡、新生兒體重及胎盤指標比較
正常妊娠組孕婦平均年齡較IVF-ET組和凍融組孕婦低2歲左右,考慮可能與助孕組孕婦年齡相對偏大有關,但三組間差異無統計學意義(表2)。IVF-ET組、凍融組與正常妊娠組比較,胎盤重量、新生兒體重差異也均無統計學意義(表2)。通過線性相關分析,胎盤重量與新生兒體重具有相關性(r=0.78,P<0.05)。
2.三組間胎盤絨毛組織定量比較
IVF-ET組、凍融組與正常妊娠組比較,胎盤末梢絨毛血管數減少,血管占絨毛橫切面積比減小(P<0.05),IVF-EF組與凍融組間差異無統計學意義。三組間絨毛面密度比較,無統計學差異(表3)。
3.三組間胎盤超微結構比較
通過半定量統計對三組胎盤ST細胞漿內囊泡、核固縮、鈣化以及絨毛間質水腫和纖維素沉積進行分析(表4)。和正常妊娠組相比,IVF-ET及凍融組來源胎盤的ST細胞漿內更容易出現囊泡樣及鈣化改變,差異有統計學意義,見圖1;余核固縮、絨毛間質水腫和纖維素沉積差異無統計學意義。

表2 孕婦年齡、新生兒體重及胎盤指標在三組間的分布情況Table 2 Comparison of maternal age, newborn weight and placenta index in three groups

表3 三組間胎盤絨毛組織定量分析比較Table 3 Quantitative analysis of placental villi in three groups
Note:compared with IVF-ET group and freeze-thaw group,*P<0. 05
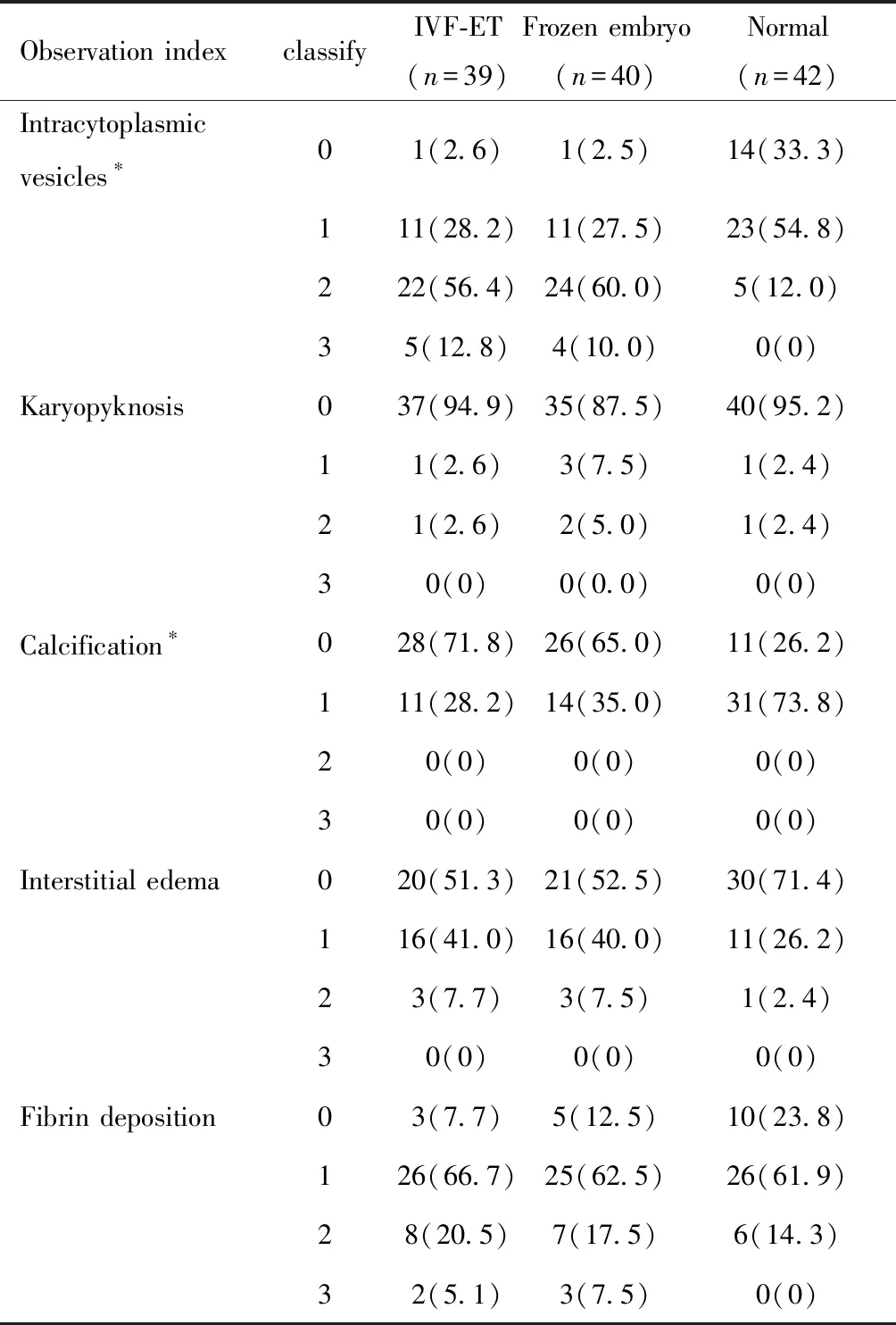
表4 三組的胎盤超微結構觀察情況分析[例(%)]
Note:comparison among the three groups,*P<0.05

圖1 IVF-ET組來源胎盤 ST 細胞漿內出現中等量囊泡樣改變,Bar=2μmFigure 1 Moderate vesicular changes in the cytoplasm of ST cells from placenta derived from IVF-ET group, Bar=2 μm
正常足月胎盤中約88%的絨毛合體滋養細胞表面,均有發育良好的微絨毛覆蓋。 ST頂端微絨毛是參與形成母胎交換界面的重要結構,也是母胎循環之間營養成分和代謝廢物交換發生的主要場所。有報道指出頂端微絨毛密度和滋養層細胞成熟度相關[2],在外界氧氣和營養濃度影響以及體外功能性刺激下發生變化[3]。微絨毛密度的下降出現在胎兒宮內生長受限胎盤[4],先兆子癇胎盤[5]以及其他一些妊娠合并癥胎盤中[2],提示在這些異常妊娠狀態中,胎盤微絨毛密度的下降伴有胎盤代謝交換能力的減退。本研究觀察到IVF來源胎盤出現了明顯的ST頂端微絨毛密度的降低,有些區域甚至發生微絨毛的完全丟失,表明IVF來源胎盤具有較小的屏障交換面積。因此推測人工助孕組胎盤在發生過程中微絨毛密度減少,可能影響胎盤轉運代謝功能。
本研究結果顯示和正常妊娠組相比,IVF-ET 組和凍融組來源胎盤 ST內出現鈣化的發生率明顯低于正常妊娠組胎盤,而Lalosevic等[6]則認為ART胎盤出現絨毛水腫以及微鈣化的幾率提高。IVF-ET 組和凍融組來源胎盤ST細胞漿中出現了中等量的囊泡樣結構。有報道表明在GDM妊娠胎盤中可觀察到廣泛的囊泡樣改變[7]。而一項利用體外培養模型的研究發現從足月胎盤分離得到的滋養層細胞在缺氧條件下培養,滋養層細胞細胞漿內出現了較多的囊泡樣改變,并伴有葡萄糖代謝和轉運的變化[8]。這些被認為是細胞內轉運異常的表現形式之一[9]。IVF-ET組及凍融組胎盤中出現較多的囊泡樣改變提示其胎盤可能存在滋養層細胞轉運異常,并推測這種異常可能是COH周期或胚胎操作過程中局部缺氧所致。但是,到目前為止仍未能有實驗證實缺氧即是引起這些病理改變的直接原因。盡管有上述超微結構的改變,但是IVF-ET組和凍融組胎盤的HE組織學沒有顯著改變,超微結構顯示屏障基本結構正常,反映IVF-ET組和凍融組胎兒發育的宮內環境、營養、屏障等與自然妊娠胎兒是基本相同的,且IVF-ET組和凍融組間差異無統計學意義,因此沒有證據證明COH周期是導致IVF-ET 組和凍融組胎盤出現上述改變的原因,關于胎盤某些超微結構上的差異還需繼續深入研究。

