非金屬摻雜改性納米TiO2光催化性能研究進展
余立志,李京偉,林銀河
(1.中農康大生態環境科技有限公司,北京 100083; 2.中國科學院光伏與節能材料重點實驗室 中國科學院合肥物質科學研究院應用技術研究所,安徽 合肥 230083;3.攀枝花學院 國際釩鈦學院,四川 攀枝花 617000)
二氧化鈦作為典型的光催化劑,因其化學穩定性好、高催化活性、無二次污染、安全無毒、成本低廉等特點,在大氣污染物降解、污水處理、環境自潔凈等領域被廣泛應用。由于二氧化鈦的禁帶寬度為3.2 eV,導致其光吸收波段過窄,且只能在紫外或者近紫外光波段(λ<387 nm)產生光催化響應,從而造成太陽能利用率低;另一方面納米二氧化鈦在光源激發下產生電子-空穴對的復合速率過快,吸附親和力差,與污染物接觸的反應活性位點不足,降低其光催化活性[1],因而限制了納米二氧化鈦光催化技術的發展。為此,如何有效的拓寬納米TiO2的光譜響應范圍和抑制光生電子-空穴對復合的速率成為提高其光催化性能的關鍵。
為了提高納米TiO2的光催化性能和太陽能的利用率,國內外的研究重點是通過改變二氧化鈦的電子結構,將激發吸收光譜范圍由紫外光區間拓展到可見光區域,同時抑制光生電子和空穴對的復合速率。目前針對納米二氧化鈦功能化改性主要的研究方法包括離子摻雜[2]、貴金屬沉積[3]、半導體復合[4]及形貌調控[5]等。其中離子摻雜是提高納米二氧化鈦光催化性能,拓寬光譜響應范圍最有效的手段之一。離子摻雜改性納米二氧化鈦主要包括金屬離子摻雜[6]、非金屬離子摻雜[7]、共摻雜[8]等。本文重點針對近年來國內外關于非金屬離子摻雜對納米二氧化鈦光催化性能研究現狀進行了總結和梳理,通過相關技術的比較分析,為非金屬摻雜改性納米二氧化鈦提供一些參考。
1 TiO2光催化原理
半導體二氧化鈦包含價帶、導帶和禁帶三部分。當太陽光輻射的能量超過TiO2禁帶寬度時,納米TiO2的活性被激發,電子由價帶激發到導帶中,空穴則留在價帶,從而形成電子-空穴對。價帶的空穴具有強氧化性和反應活性(1.0~3.5 V),而導帶中的電子則具有良好的還原性(0.5~1.5 V),利用高度活性的納米二氧化鈦電子-空穴對的氧化還原作用,將有毒有害的有機物最終氧化成二氧化碳和水等無機小分子,從而達到光催化降解污染物的效果,其光催化機理見圖1[1]。
(a)TiO2+hv→h++e-;h++e-→熱能
h++OH-→·OH;h++H2O→·OH+H+
2H2O·→O2+H2O2;H2O2+O2→·OH+H++O2
·OH+dye→…→CO2+H2O
H++dye→…→CO2+H2O
dye:染料或碳氫化合物
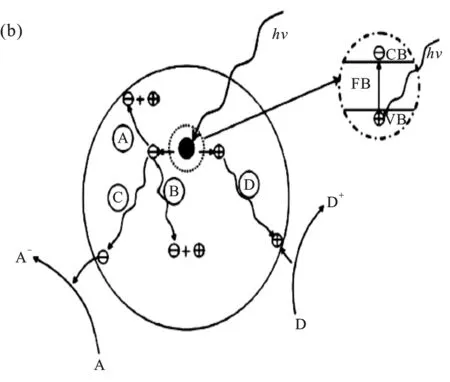
圖1 TiO2光催化反應機理及示意圖[1]Fig.1 The mechanism and diagram describing of TiO2 photocatalysis reaction[1] a.光催化反應機理;b.光催化反應示意圖
2 非金屬元素單摻雜體系對納米二氧化鈦改性影響
非金屬摻雜[7]不僅可以降低納米二氧化鈦的能帶間隙,拓寬可見光的響應范圍,還可以有效抑制光生載流子的復合速率,進而提高其光催化性能;與此同時,非金屬元素具有原料來源廣泛、價格低廉等優點,因此非金屬摻雜納米二氧化鈦成為近年來研究的熱點。
2.1 氮摻雜
氮元素原子半徑與氧原子近似,具有電離能小、穩定性好的特點,能與TiO2進行多種方式摻雜,氮被視為最理想的非金屬摻雜元素。Sato S[9]首次發現氮的引入,可使TiO2具有可見光活性。Dunnill等[10]研究發現TiO2氮摻雜后會產生替代性和間隙性兩種類型的晶體結構,其中替代性結構是氮原子置換氧原子,而間隙性結構則是氮原子進入TiO2晶格中。
何奕明等[11]采用溶膠-凝膠法制備了N-TiO2/PP復合催化膜,通過GC-MS分析中間產物并對甲苯光催化降解機制進行了解析,結果表明氣體停留4.32 s時,可見光條件下甲苯的降解率達77%,去除負荷達到76.5 g/(m3·h)。段秋宴等[12]采用工業TiO2為原料的,研究了不同氨濃度對氮摻雜TiO2光催化性能的影響,結果發現氨氣濃度的變化顯著影響TiO2中氧空位,氮的摻入會在TiO2晶格中產生N—H鍵和N—Ti—O鍵,使得TiO2電子能帶從半導體向金屬過渡,并且TiO2的吸收光譜產生紅移現象;可見光條件下單摻雜二氧化鈦對亞甲基藍的分解率由5%提高到93%。由于氮摻雜可以改變二氧化鈦的能級結構,提高量子效率;氮原子的p軌態與氧原子的2p軌態能級相近且易雜化,所以氮摻雜有利于減小二氧化鈦的禁帶寬度,拓寬光譜響應范圍,進而提高氮摻雜TiO2的光催化效率[13]。
2.2 碳摻雜
張春磊等[14]研究發現碳摻雜TiO2可以促進其結晶性的提高,納米TiO2的吸收波長發生紅移,范圍由紫外光區拓展到可見光區。同時研究發現納米棒組裝而成的花狀結構可以延長光在納米二氧化鈦中的傳輸路徑,進而提高納米TiO2的光吸收和捕獲能力。通過碳摻雜與未摻雜TiO2光催化性能比較發現,碳摻雜在紫外光區域的活性明顯高于未摻雜二氧化鈦。經過摻C/摻N處理后,二氧化鈦表面會形成更多的 —OH基團,使得改性二氧化鈦表面吸附水分子的能力變強,Ti—OH基團的含量越多則越有利于提高TiO2光催化性能[15]。由于N和C的電負性均比O弱,TiO2晶格中的氧被氮和碳取代后,Ti原子周圍的電子密度會增加,因此鈦的結合能也會增加。
2.3 磷摻雜
鮑聞淵等[16]以磷酸為原料采用溶膠水熱法制備了TiO2/MBA/Ag三明治結構的納米材料,獲得了粒徑尺寸在6~12 nm范圍的銳鈦礦型納米顆粒,磷元素以P5+替代了Ti4+,以O—P—O鍵形式進入TiO2晶格中,降低了TiO2的帶隙寬度,豐富了TiO2的表面態,進而促進了TiO2向MBA分子的電荷轉移。通過晶粒形貌的分析可知,P摻雜并不改變TiO2顆粒的形貌,但是晶粒尺寸卻比未摻雜時小,也進一步表明了P摻雜抑制了納米TiO2晶粒的生長。
2.4 硫摻雜
硫元素有多種價態,因此S摻雜進入TiO2中也會存在多種形態。Umebayashi等[17]采用高溫氧化退火工藝制備硫摻雜的納米TiO2。研究發現經過600 ℃退火處理,TiS2會轉化成銳鈦礦型TiO2。S2-取代TiO2晶格中的O,S的3p軌道與價帶的混合可以降低其禁帶寬度,提高TiO2的光催化性能。Zhou等[18]采用機械化學法水解四氯化鈦制備了硫摻雜納米TiO2,研究發現硫摻雜TiO2在400~650 nm的可見光范圍具有較強的吸收能力;可見光對亞甲基藍的分解具有較高的光催化活性。XPS結果表明硫原子以S6+和S4+形態存在于TiO2晶格中,同時S摻雜也可以改善電子空穴對的分離。
2.5 硼摻雜
Zhao W等[19]采用四氯化鈦、鈦酸四丁酯和硼酸為原料,制備了不同B含量的納米TiO2,在可見光條件下可以有效降解和礦化有毒有機污染物如三氯苯酚、苯甲酸鈉等;當硼摻入量1.32%時,改性TiO2的光催化性能最好。B摻雜可使TiO2光譜響應范圍擴展到可見光區域,提高其光催化效率。于愛敏等[20]采用水熱法制備了B摻雜納米TiO2,研究發現經過5 h可見光催化處理,苯酚的降解率可達100%,B以B-O-Ti的形式摻入到TiO2的晶格中,進而有利于提高可見光條件下納米TiO2的光催化性能。
2.6 氟摻雜
Hattori等[21]以NH4F為氟源,采用溶膠凝膠法合成了氟摻雜納米TiO2,結果表明,少量氟化銨的加入可以顯著增強納米材料的光反應活性。當氟化銨與Ti的摩爾比為1.35×10-2時,TiO2對甲基硅氧烷的降解速率達到最大值。X射線衍射分析表明F-引入可以改善銳鈦礦的結晶度,提高其在可見光條件下的光催化性能。Li Di等[22]以H2TiF6水溶液為原料,采用噴霧熱解法制備了摻F的納米二氧化鈦(FTO)粉體,研究發現F摻雜粉體在紫外光和可見光照射下具有極高的光催化活性,究其原因主要是表面酸性的增強、氧空位的產生和活性位點的增加。張理元等[23]研究發現,經過75 min鹵燈輻照,10%氟摻入量時甲基橙的降解率可達91.12%;氟摻雜使得納米TiO2的吸收帶產生藍移,F-可將部分Ti4+轉化成Ti3+,而Ti3+表面態在TiO2的帶隙間產生一個淺勢的施主能級,可以有效捕獲光生電子,進而抑制電子空穴對的復合,提高其光催化性能[24]。
2.7 氯摻雜
陳恒等[25]利用鹽酸水解鈦酸四丁酯制備了氯摻雜納米TiO2粉體,研究發現氯的引入降低了無定形相向銳鈦礦轉變溫度,300 ℃高溫焙燒處理的氯摻雜TiO2具有最佳的光催化性能,吸收波長可擴大至可見光譜范圍,在大于400 nm波長的可見光照射下,經過120 min后苯酚的降解率可達42.5%。同時XPS結果也表明,摻雜過程中氯元素以Cl-形式進入到TiO2的晶格中。郭省學等[26]采用NaCl和Ti(SO4)2為原料,用水熱法制備了具有高催化活性的氯摻雜納米TiO2,其平均粒徑67 nm,研究發現氯摻入量15%時,經過200 min光照處理苯酚的降解率達到90.6%,具有最佳的光催化性能。
2.8 溴摻雜
樊麗霞等[27]以溴化鉀和硫酸鈦為原料,水熱法制備了具有光催化性能的溴摻雜改性納米TiO2粉體,平均粒徑50 nm。結果表明,當溴與鈦的摩爾比0.35時,700 ℃焙燒得到的Br摻雜TiO2具有最佳的光催化活性。與未摻雜相比,Br摻雜TiO2對苯酚的降解率由69%提升至80%。Br摻雜也使得納米二氧化鈦在紫外區的光催化能力得到加強。
2.9 碘摻雜
蔣悅等[28]以碘酸鉀和鈦酸四丁酯為原料,低于100 ℃制備了碘摻雜納米二氧化鈦(I-TiO2)。研究發現,碘摻雜TiO2的光譜響應范圍產生紅移,可以有效降解并礦化有毒的RhB有機污染物,同時在導帶和價帶之間引入了新的雜質軌道,進一步減小了禁帶的寬度,從而提高了其對可見光的利用效率。Hong等[29]則以碘單質作為碘源,采用水解法制備了碘摻雜改性納米二氧化鈦(I2-TiO2),在可見光范圍也具有顯著的光催化性能。
3 非金屬共摻雜體系對納米二氧化鈦光催化性能影響
3.1 N和S共摻雜
楊超等[8]硫脲(CH4N2S)作為原料,采用兩步水解法制備了具有介孔結構的N、S共摻雜納米TiO2粉體,平均粒徑5 nm,比表面積是58.706 m2/g。介孔結構的平均孔徑在15~25 nm范圍,硫脲元素的摻入填充了孔道,從而增加了介孔通道。當硫脲的摻入量50%時,甲基橙的降解率達98%以上。韓松等[30]研究表明,N-S共摻雜改性納米TiO2對甲醛的降解率最高可達97.2%,并且N-S共摻雜TiO2的光催化性能明顯優于氮摻雜TiO2。
3.2 N和B共摻雜
林周園等[31]以硼酸和氨水作為原料制備了N-B共摻雜納米TiO2,然后采用氯化鐵和戊二醛對陰陽膜層進行交聯改性處理,結果表明經過光電催化處理苯酚廢水的降解率達到65%以上。由于B3+的離子半徑比Ti4+和O2-的離子半徑小得多,所以B3+取代Ti4+和O2-比較困難,最終B3+以間隙摻雜的方式進入到TiO2的晶格中[32]。
3.3 N和Fe/Ce/Gd共摻雜
暢曉鈺等[33]以硝酸鐵和尿素為原料,采用溶膠凝膠法制備N-Fe共摻雜納米TiO2,結果表明5%Fe和12%N摻入量時,可見光條件下亞甲基藍的降解效果最好。N-Fe共摻雜二氧化鈦的協同效應使得其光催化性能明顯高于單摻雜樣品和純二氧化鈦。李經方等[34]制備了N-Ce共摻雜TiO2/纖維素復合氣凝膠,結果表明當N-Ce共摻雜TiO2/纖維素復合氣凝膠對亞甲基藍的降解效果并沒有明顯高于單獨摻Ce的效果(85.9%),表明B-Ce共摻雜工藝還需要進一步改進。蔣樂等[35]研究了N-Gd共摻雜TiO2對甲基橙降解的影響規律,結果表明,8.0%N~0.5%Gd摻雜TiO2在可見光照射下,對甲基橙的降解率可達68.4%,比工業TiO2的降解率高了34.9%。
3.4 F和Cu共摻雜
陳贊宇等[36]采用蒸汽熱法制備了F-Cu共摻雜TiO2空心微球,結果表明F-Cu共摻雜可以增大TiO2的比表面積,Cu2+進入TiO2晶格中,而大部分F則以化學吸附態存在于TiO2表面,少部分進入到晶格中。經過30 min可見光光照處理,F-Cu共摻雜二氧化鈦對陽離子藍溶液的降解率可達99.8%,以上結果也進一步表明非金屬與金屬共摻雜可以在催化劑中產生更多的摻雜能級和捕獲中心,產生協同效應,進而提高二氧化鈦的光催化性能。
4 結束語
非金屬離子摻雜作為一種提高納米TiO2光催化活性的有效方法被廣泛研究。非金屬摻雜不僅可以降低納米二氧化鈦的能帶間隙,拓寬可見光的響應范圍,還可以有效抑制光生載流子的復合速率,進而提高其光催化性能。本文詳細總結和梳理了近年來非金屬摻雜二氧化鈦光催化關于的研究現狀,重點梳理了N、C、P、S、B、F、Cl、Br、I及非金屬共摻雜時納米二氧化鈦對有機污染物降解的影響,同時對不同摻雜元素對納米二氧化鈦晶體結構及光譜響應機制進行了比較和探討。不同類型非金屬元素的原子半徑、晶體結構、摻入量都會對改性TiO2的能級結構和帶隙寬度產生差異,進而其對不同有毒有害污染物的光催化性能產生不同影響,需要綜合考慮。目前,非金屬摻雜TiO2的光催化降解特性還處于不斷深入研究階段,對于降解環境污染物,保護和凈化環境具有重要的意義。

