血清淀粉樣蛋白A與急性腦梗死關系的Meta分析
鄭文惠,李 倩,張 磊,李北辰,方 瑗
2019年《Lancet Neurology》雜志發布了2016全球疾病負擔研究( Global Burden of Disease Study,GBD)關于卒中的分析數據,結果顯示:2016年卒中是全球第二大死亡原因(550萬),全球卒中患病人數為8010萬,2016年新增卒中病例1370萬;在所有卒中的患病人數中,84.4%為缺血性卒中,東亞的卒中年齡標化發病率最高,特別是中國(354/10萬人年)[1]。但是目前腦卒中的預后評估尚缺乏良好的生物學指標。血清淀粉樣蛋白A(serum amyloid protein A,SAA)是一種急性時相反應蛋白[2],可通過改變高密度脂蛋白的功能,影響膽固醇的轉運和清除,進而引起脂質沉積,加速動脈硬化進程和動脈粥樣硬化性血管疾病的發生[3]。前期研究顯示SAA可以作為評估和預測冠心病病情和嚴重程度的敏感標志物[4],但在急性腦梗死的研究中尚無明確定論。為了探討SAA與急性腦梗死的關系及其臨床意義,本文薈萃有關SAA與急性腦梗死的文獻進行Meta分析。
1 方 法
1.1 文獻納入標準 (1)研究類型:隊列研究;(2)研究人群:急性腦梗死組符合急性腦梗死的診斷標準,并且經頭部CT和(或)頭部MR確診;(3)文獻數據完整:提供了或通過數據可計算淀粉樣蛋白A的均值及標準差。
1.2 文獻排除標準 (1)完全重復發表或者同一數據發表;(2)資料和統計所需數據不全;(3)實驗設計、操作實施過程有誤或者存在重大缺陷。
1.3 文獻檢索 計算機檢索PubMed、Cochrane Library、中國期刊全文數據庫(China National Knowledge Infrastructure,CNKI)、中國生物醫學文獻數據庫(CBM),檢索時限均為從建庫至2019年4月,語種限制為中文或英文,中文檢索詞為“卒中”或“腦梗死”和“淀粉樣蛋白A”;英文檢索詞為“stroke”OR“ischemic stroke”和“serum amyloid protein A”。同時,追溯納入文獻的參考文獻,避免漏查尚未公開發表的文獻。
1.4 資料提取和文獻偏倚風險評價 (1)資料提取和文獻偏倚風險評價由2名研究者完成,如有分歧討論決定。以EndNote X7 軟件管理文獻,篩選可能符合納入標準的文獻并閱讀全文進行判斷,合并整理后建立文獻數據庫,提取文獻基本信息:第一作者、發表時間、國家。(2)研究對象基本特征:年齡、性別、病例來源時間和樣本量。(3)各實驗室指標結果:均數及標準差。以 Newcastle-Ottawa Scale (NOS)[5]量表評估納入文獻的偏倚風險,包括納入文獻對象的選擇(4分)、可比性(2分)、暴露(3分)3 個方面,≥7分為低度偏倚風險;6分為中度偏倚風險;≤5分為高度偏倚風險。

2 結 果
2.1 文獻檢索結果 共檢索到322篇文獻,10項隊列研究[6~15]納入本文進行Meta分析,共1054例急性腦梗死患者。納入文獻基本情況(見表1)。文獻檢索流程及結果(見圖1)。
2.2 文獻質量評價 采用非隨機研究偏倚風險評估方法(NOS)對納入研究的方法學質量進行評估。NOS包括研究對象選擇(4個條目,4分)、組間可比性(1個條目,2分)和結果測量(3個條目,3分),總共 9 分,6分及以上為高質量文獻。如遇分歧則討論解決,必要時根據第三意見進行商議,最后達成一致性意見。質量評價結果(見表1)。

表1 納入文獻基本信息
2.3 Meta分析結果 急性腦梗死組與健康組血清淀粉樣蛋白A水平比較,共納入10篇文獻包括1470名受試者對血清SAA水平進行了比較,異質性檢驗結果 I2=100%,P<0.00001,提示存在統計學異質性,故采用隨機效應模型。合并效應量結果:(MD=14.86,95%CI=12.09~17.63,P<0.00001),顯示急性腦梗死組血清SAA水平高于健康組具有統計學意義(見圖2)。共3篇文獻在患者入院后行美國國立衛生研究院卒中量表評分(National Institute of Health stroke scale,NIHSS)進行腦卒中嚴重程度評定。其中重度神經功能缺損和中度神經功能缺損的血清SAA水平的Meta分析顯示重度神經功能缺損組的血清SAA水平高于中度組,具有統計學意義(MD=1.17,95%CI=0.32~2.03,P=0.007),其中中度神經功能缺損和輕度神經功能缺損的血清SAA水平的Meta分析顯示中度神經功能缺損組的血清SAA水平高于輕度組,具有統計學意義(MD=0.60,95%CI=0.12~1.08,P=0.02)(見圖3、圖4)。

圖1 文獻篩選流程及結果
3 討 論
通過分析可以得出結論:急性腦梗死患者SSA的水平明顯高于正常健康人,而且SSA的水平跟腦卒中嚴重程度呈正相關。結論由納入的研究進行分析得出,共10項給出了觀察組和對照組的血清淀粉樣蛋白A的水平,均為前瞻性研究,且以均值和標準差的形式給出,從而提取連續性數據進行分析,通過NOS量表對文獻質量進行評估,所有研究均在5分以上。但是上述研究均來自國內文獻,對國外數據庫搜索后得到相關文獻數量很少,且沒有符合納入標準的文獻,所以結論適用范圍有限,對研究的最終結果,我們應該謹慎對待。
SAA主要由肝臟分泌產生,可分為急性期SAA和結構型SAA,急性期SAA包括SAA1和SAA2在炎性急性反應期分泌顯著增加,結構型SAA不參與急性炎癥反應含量基本保持不變[16]。一項大規模前瞻性研究[17],對28263例健康絕經期女性進行隨訪結果顯示,SAA是動脈粥樣硬化相關心血管事件的預測因素,并且大量研究發現SAA在動脈粥樣硬化損傷時表達增加[18~20]。動脈粥樣硬化是一個復雜的動態過程,斑塊內脂質隨著時間的推移逐漸累積并被纖維帽覆蓋,在致炎性物質(如氧化的脂質或炎性因子)的刺激下發生炎癥反應;在觸發因素(應激、血壓升高或神經因素)的協調作用下發生斑塊破裂或糜爛,動脈粥樣硬化與腦梗死的發病密切相關。SAA與腦梗死的關系,其可能機制包括以下幾個方面:(1) SAA通過替換高密度脂蛋白膽固醇(high-density lipoprotein,HDL)中的載脂蛋白A-I(Apo A-I),并與HDL形成新的顆粒,從而失去對卵磷脂膽固醇酰基轉移酶(LCAT)的激活作用,最終影響膽固醇的逆向轉運[3]。進一步研究顯示,SAA對Apo A-I的替換及HDL/SAA復合物的形成,是HDL與肝細胞的親和力減低,而HDL/SAA復合物與巨噬細胞的親和力比單純HDL提升3~4倍,這些脂質進入巨噬細胞促使其轉為泡沫細胞,進一步促進動脈粥樣硬化[21]。(2)SAA被發現在急性和慢性炎癥中均有表達,能促進單核細胞/巨噬細胞的趨化和黏附,增加動脈粥樣硬化斑塊的炎性浸潤[22],還具有促進多種炎性因子的表達及對炎癥相關信號通路的激活作用[23~25]。(3)SAA通過誘導基質金屬蛋白酶的表達,加速纖維帽中細胞外基質的降解,導致纖維帽破裂,進一步造成粥樣斑塊破裂,進一步導致斑塊不穩定性增加[6]。雖然大量研究顯示SAA是形成動脈粥樣硬化的重要原因,但是目前也存在爭議,近期國外一項研究,通過觀察亞臨床頸動脈粥樣硬化的長期病死率,進行12 y的隨訪發現病死組的血清淀粉樣蛋白A的水平高于存活組,但是排除了超敏C反應蛋白的混雜因素后,我們發現這一統計學意義就丟失了,進一步說明可能SAA與動脈粥樣硬化可能并沒有直接的因果關系,也許只是機體炎癥狀態的標志物[26]。這也引發了我們對急性期腦梗死血清淀粉樣蛋白A升高的意義的思考,血清淀粉樣蛋白A的升高僅僅是一種炎性狀態的標志物?還是急性腦梗死發展過程中的一個積極參與者?如果它參與了急性腦梗死的發生,又是通過什么樣的途徑和靶點實現的?目前的研究還不能夠充分解釋,后期需要進一步的高質量的研究去說明,以期對急性腦梗死的預防和治療發揮用處。

圖2 急性腦梗死組與對照組組淀粉樣蛋白A水平的Meta分析
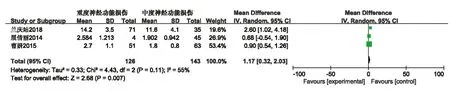
圖3 重度神經功能損傷和中度神經功能損傷組淀粉樣蛋白A水平的Meta分析

圖4 中度神經功能損傷和輕度神經功能損傷組淀粉樣蛋白A水平的Meta分析

