Mo2C@C納米棒的制備及氧還原性能研究
刁金香,邱 雨,郭曉輝
(1.西安航空職業技術學院航空材料工程學院,西安 710089;2.西北大學合成與天然功能分子化學教育部重點實驗室/化學與材料科學學院,西安 710069)
1 引 言
隨著環境污染日益的加劇和人口的增加,開發可持續且綠色的能源轉換和存儲技術,如再生燃料電池,可充電金屬空氣電池和水電解槽等越來越發強烈。迫切尋找可再生的清潔能源。可充電的金屬-空氣電池,例如Zn-空氣電池和Li-O2電池受到了越來越多的關注,由于其高的能量密度和環境友好[1-3]。鋅空氣電池是以空氣中的氧氣為正極活性物質,金屬鋅為負極活性物質的一種新型化學電源。電池在工作中,放電過程中的氧還原(Oxygen reduction reaction)和充電過程中的析氧反應(Oxygen evolution reaction)起著至關重要的作用。然而,Zn-空氣電池和Li-O2電池存在較大的瓶頸,常見的ORR催化劑可以分為鉑基貴金屬催化劑和非貴金屬催化劑,貴金屬價格昂貴,稀缺,限制其規模化的生產[6-7]。
目前碳基材料及過渡金屬的碳化物(Transition metal carbides)(TMC), 例如碳化鐵,碳化鉬,碳化鎢,碳化鈷和碳化鎳等催化劑有近似于貴金屬性能,由于價格低廉引起了科學家的關注和研究。這些催化劑具有較高的電傳導率,熱傳導率和化學的穩定性。這些催化劑中,納米級的Mo2C因具有類似Pt的d帶電子軌道,具有產氫和產氧及電催化性能受到了廣泛的關注[8-10]。Yang等報道了Mo2C納米顆粒分散在碳微米花中,具有優良的產氫性能[11]。Kwak等[12]報道了Mo2C/CNTs 納米復合材料應用于Li-O2電池,具有較低的過電壓,循環穩定性和高的穩定性,然而很少有相關的報道Mo2C及其復合催化劑產氧或者氧還原性能。另外,在選擇催化劑時,催化劑的表面形貌,介孔和面積及材料的分散影響著催化劑的性能,高的比表面積提供了較多的活性點,加強電解質與電極的接觸面積,縮短了電子-離子的分散。
2 實 驗
2.1 原料及儀器
鉬酸銨(NH4)6Mo7O24·4H2O(分析純,西安精細化工有限公司), 乙二胺C2H8N2(分析純,國藥集團化學有限公司),丹寧酸 C76H52O46(國藥集團化學試劑陜西有限公司)。
掃描電子顯微鏡(Quanta 400 FEG,日本日立);X射線衍射分析(Bruker AXS-D8,布魯克(北京)科技有限公司);電化學工作站(CHI 760C,上海辰華公司),投射電鏡(JEM-2100F,日本電子株式會社)旋轉圓盤電極(MSR,美國PINE設備公司)。
2.2 原料MoO3-EDA 制備方法
1.24 g(NH4)6Mo7O24·4H2O溶解30 mL去離子水中,加入890 μL的乙二胺攪拌,然后用2 mol/L HCl 調至pH=4~5,有大量沉淀析出,然后將反應放入50 ℃的水浴中反應2 h,最后用乙醇抽濾沖洗,放入70 ℃的烘箱中烘干即得MoO3-EDA[13]。
2.3 Mo2C@C納米棒的制備
1 g 丹寧酸(TA)溶解在10 mL的H2O中。稱取100 mg MoO3-EDA粉末,加入到10 mL的上述的TA溶液中,然后放在超聲中超聲1 h,1 h后放進冰箱冷凍,冷凍好之后進行冷凍干燥。稱取冷凍得到的樣品稱取281 mg放入瓷舟,以5 ℃/min的升溫速率升到650 ℃在10%氬氫混合氣氛圍下煅燒2 h,自然冷卻,制備Mo2C@C。
2.4 Mo2C@C納米棒電催化性能測試
電化學電催化性能測試采用三電極體系,Mo2C@C納米棒的氧還原性能采用的是旋轉的圓盤電極,工作電極材料為玻碳,飽和的Ag/AgCl電極為參比電極,鉑片電極為對電極[14]。催化劑的擔載量為0.4 mg ·cm-2。電解液采用的是0.1 mol/L KOH溶液,循環伏安法(CV)掃速50 mV·s-1,電壓范圍為0.2~-0.9 V, LSV曲線在不同的轉速下即 400 r/min,900 r/min,1600 r/min,2000 r/min和2500 r/min,掃速5 mV·s-1,電壓范圍為0.2~-0.9 V進行的[15]。

圖1 MoO3-EDA(a)前驅體和(b)Mo2C@C的XRD圖譜Fig.1 XRD patterns of MoO3-EDA(a) and Mo2C@C(b)
3 結果與討論
對于合成前驅體MoO3-EDA、Mo2C和Mo2C@C進行X射線粉末衍射分析,圖1(a)和(b)分別為前驅體與Mo2C和Mo2C@C的X射線粉末衍射分析。由圖1(a)可知,經過與XRD標準圖譜JCPDS#00-050-2402對比,其物相為Mo3O10(C6H8N)2.2H2O)[13]。圖1(b)Mo2C和Mo2C@C的XRD圖譜。與碳化鉬的XRD標準的衍射圖譜(JCPDS#15-0457)對比,其物相組織為Mo2C,其中處于2θ=37.767°、43.692°、63.394°和75.725°分別對應Mo2C的(111)、(200)、(220)和(311)晶面。Mo2C@C譜線與Mo2C譜線相比,除了Mo2C的特征峰以外,在20°~ 30°之間有較為明顯的鼓包,歸結為無定型碳,即Mo2C@C。
圖2為前驅體MoO3-EDA和Mo2C@C-650納米棒的SEM圖,圖2為MoO3-EDA 前驅體,Mo2C@C前驅體和Mo2C@C納米棒的SEM照片,從圖2(a)和(b)為MoO3-EDA前驅體和 Mo2C@C前驅體的電鏡圖看出,前驅體納米棒的直徑為300~450 nm,長度為10~30 μm。表面比較光滑。從圖2(c)Mo2C@C的SEM圖可以看出,與(b) 相比表面覆蓋一層物質,即為無定型碳,與前驅體比較納米棒的長度有所增加。圖3(a)和(b)為Mo2C@C的TEM圖,(a)圖可以看出,納米棒分為兩個部分,顆粒形成的納米棒的和外部覆蓋的致密一層碳,碳物質的厚度為50 nm,兩層具有明顯的分界面。

圖2 MoO3-EDA前驅體(a), Mo2C@C的前驅體(b)和Mo2C@(c)SEM照片Fig.2 SEM images of MoO3-EDA(a), the precursor of Mo2C@C(b) and Mo2C@C(c)

圖3 Mo2C@C的TEM照片Fig.3 TEM images of Mo2C@C
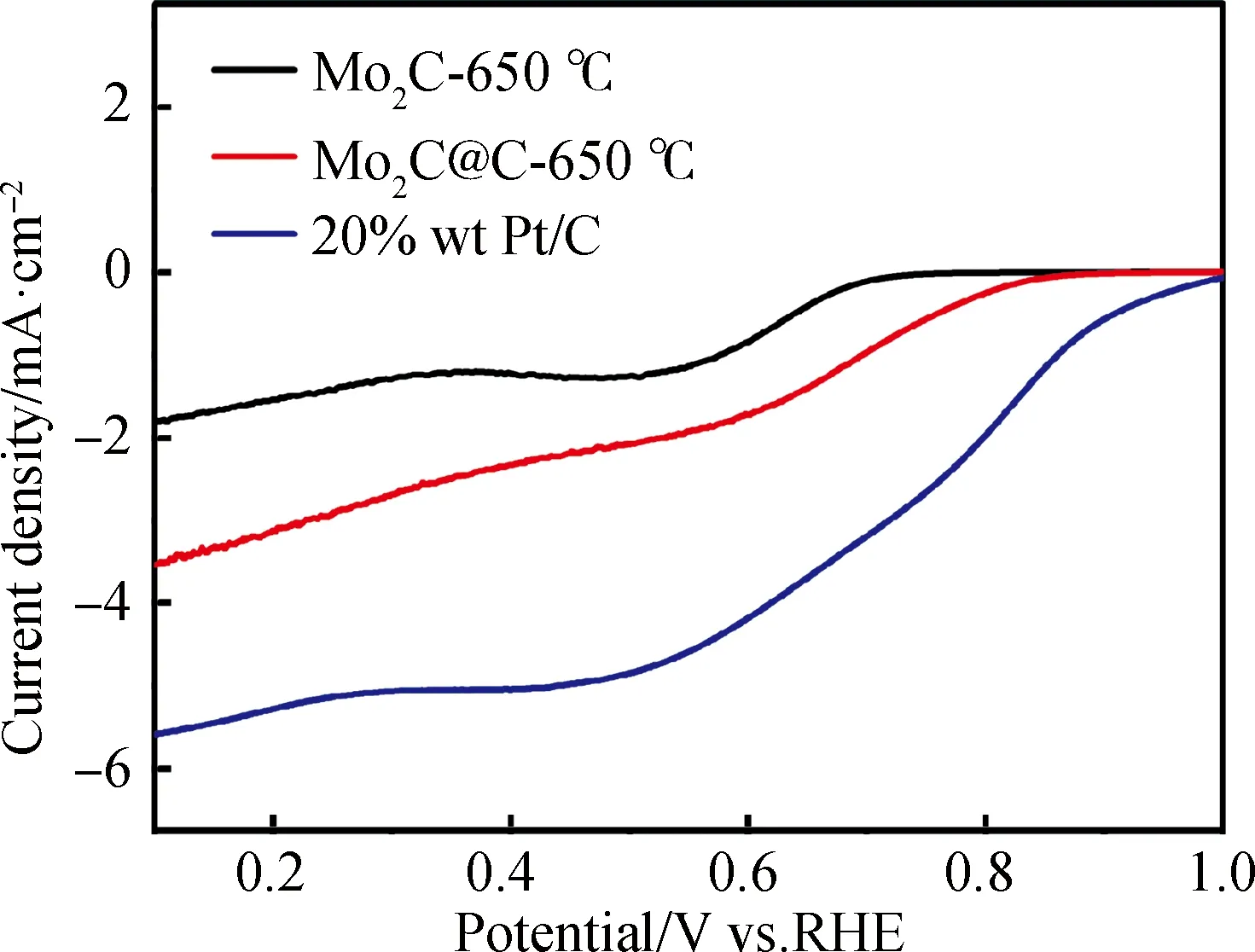
圖4 20% Pt/C, Mo2C 和Mo2C@C-650 ℃催化劑的LSVFig.4 Comparison of ORR catalytic activities recorded at 1600 r/min for 20% Pt/C, Mo2C and Mo2C@C-650 ℃
圖4為20%Pt/C,Mo2C和Mo2C@C在飽和O2氣氛下,在1600 r/min轉速下的極化曲線,20%Pt/C,Mo2C和Mo2C@C的起始電壓為分別為0.986 V, 0.7173 V和0.842 V。20%Pt/C,Mo2C和Mo2C@C的半波電位為0.790 V,0.6056 V和0.720 V。結果表明所合成的催化劑的催化順序Mo2C 圖5(a)和(c)為20%Pt/C和Mo2C@C在飽和O2氣氛下,在不同的轉速下,即400 r/min,900 rpm,1600 r/min,2000 r/min和2500 r/min的極化曲線,Mo2C@C在0.5 V,2500 r/min的極限電流密-4.5 mA·cm-2。當轉速為400 r/min,在0.692 V有個小的還原峰[16],隨著轉速的增加,還原峰消失。圖(b)和(d)為20%Pt/C和Mo2C@C的(Koutecky-Levich)K-L曲線。20%Pt/C 在0.1 V,0.2 V,0.3 V,0.4 V和0.5 V電子的轉移數為4.39,3.94,3.69,3.71和3.94。Mo2C@C在0.1 V,0.2 V,0.3 V,0.4 V和0.5 V電子的轉移數為3.43,3.16,2.93,2.78和2.60。20% Pt/C和Mo2C@C 是典型的4e-途徑,說明催化劑對于氧還原具有良好的選擇性。 圖5 (a)20% Pt/C,(c)Mo2C@C-650 ℃催化劑在不同速率下的極化曲線; (b)20% Pt/C,(d)Mo2C@C-650 ℃催化劑K-L曲線Fig.5 LSV plots of 20% Pt/C(a),Mo2C@C-650 ℃ (c) at different rotating speeding; K-L plots of 20% Pt/C(b), Mo2C@C-650 ℃(d) 催化劑氧還原性能的重要的指標為穩定性。采用計時電流法(i-t)來測定20%Pt與Mo2C@C-650 ℃材料的穩定性能,介質為0.1 mol/L KOH,1600 r/min的轉速。從圖6可以看出,經過了11 h,20%Pt/C電極電流強度降低了27%,Mo2C@C-650 ℃電極電流強度降低了40%,說明具有較好的穩定性。 圖6 20% Pt/C 和Mo2C@C-650 ℃催化劑在0.1 mol/L KOH 溶液中的電化學穩定性Fig.6 Evaluation of ORR stability performance of 20% Pt/C and Mo2C@C-650 ℃ in 0.1 mol/L KOH solution 通過原位生長的方法合成了Mo2C@C納米棒,Mo2C@C納米棒的氧還原性能采用的是旋轉的圓盤電極在0.1 mol/L KOH進行測試,結果表明:Mo2C@C具有良好的氧還原活性,同時在氧還原的過程中主要采用的是4e-途徑,表現出優異的電催化性能和穩定性。

4 結 論

