超聲乳化術中高灌注壓對急性閉角型青光眼患者術后視功能的影響
牛春梅,孔德銘
0引言
急性閉角型青光眼(acute angle-closure glaucoma,AACG)指因前房角被周邊虹膜組織機械性阻塞引起眼壓急性升高,進而造成視力、視野不可逆損害的一類疾病。該病具有起病急、損傷大的特點。小梁切除術是治療該病的主要手術方法,但術后反應重、恢復慢、并發癥多。大量研究表明,白內障超聲乳化摘除術通過摘除混濁晶狀體解除晶狀體的瞳孔阻滯作用,而植入較薄的人工晶狀體可有效緩解前房角的擁擠,前房加深、變寬,房角開放,同時人工晶狀體與虹膜間間隙增大,房水循環阻力降低,后房壓力降低,消除了小梁網粘連與虹膜根部膨隆因素等諸多機制降低患者術后眼壓[1-4]。此類手術創傷小、恢復快、操作簡單、并發癥少,所以在臨床上白內障超聲乳化摘除術被越來越多的眼科醫生用來治療AACG[5]。白內障超聲乳化摘除術后眼壓降低后是否會減少高眼壓對視神經的損傷,尤其是對于有早期青光眼視野改變的患者實施這樣的手術是否利大于弊,因為白內障超聲乳化術中高灌注壓可能會給AACG造成進一步損傷,本研究針對這個問題做了臨床研究。
1對象和方法
1.1對象收集2017-03/2018-10于我院住院的AACG合并白內障的患者35例37眼,其中男9例11眼,女26例26眼,雙眼患病者2例,年齡 54~86歲,入院時眼壓>40mmHg。AACG入組標準:(1)房角關閉2個以上象限;(2)青光眼急性發作次數≤3 次,每次發作持續時間≤5d,病程≤3mo;(3)BCVA<0.5(LogMAR);(4)視野檢查結果需滿足固視喪失<20%,假陽性<33%,假陰性<33%;(5)有早期青光眼視野改變;(6)依從性好。排除標準:(1)曾做過抗青光眼手術、有其他內眼手術史及眼部外傷史患者;(2)眼部炎癥及全身疾病影響本次手術療效患者;(3)術后出現并發癥患者;(4)精神障礙或無法正常交流者。所有患者及家屬均知情同意,本研究通過本院醫學倫理委員會批準。
1.2方法
1.2.1檢查項目入選患者進行常規眼科檢查:BCVA(采用國際標準視力表 LogMAR記錄視力)、非接觸眼壓計測量眼壓、裂隙燈、房角、眼底。輔助檢查:應用Octpus 900 型自動電腦視野計G-top程序檢查視野,記錄:平均視敏度(MS)、平均缺損(MD)和丟失方差平方根(sLV)的值。
1.2.2檢查方法視野檢查在暗室于屈光矯正后正常瞳孔下進行,使用縮瞳藥的患者在檢查前需停用1wk,檢查前給予患者有關視野檢查的注意事項及操作方法的宣教,避免在患者疲勞時做視野檢查,檢查時患者保持頭位正,上瞼遮擋視野者需用膠布拉起。
1.2.3治療方法術前眼壓降至30mmHg以下,術前3d給予氧氟沙星滴眼液滴眼,術前散瞳、沖洗結膜囊、鹽酸丙美卡因滴眼液表面麻醉3次。術中常規消毒、鋪巾,開瞼器開瞼。入組患者均由同一術者應用同一臺超乳機在同一超聲乳化參數設置(核乳化參數設定:瓶高100cm,負壓300mmHg,能量30%;抽吸皮質參數設定:瓶高90cm,負壓450mmHg)下完成手術。手術時間10~20min。于上方透明角膜處做隧道切口,連續環形撕囊,水分離,超聲乳化吸除晶狀體核,I/A完全吸除皮質,囊袋內植入折疊式人工晶狀體。術后從主切口及輔助切口沿房角將黏彈劑360°緩慢注入,達到分離房角的目的。I/A充分吸除黏彈劑,術畢結膜囊內涂妥布霉素地塞米松眼膏,包扎術眼。術后給予局部抗炎治療預防感染,妥布霉素地塞米松滴眼液6次/d,持續使用2wk,妥布霉素地塞米松眼膏1次/晚,持續使用2wk,雙氯芬酸鈉滴眼液4次/d,持續使用1mo。術后隨訪6mo,比較患者術前,術后3、6mo BCVA、眼壓、MS、MD和sLV值的變化。
統計學分析:使用SPSS 17.0統計學軟件進行數據處理,計量資料以均數標準差表示,不同時間點各指標比較采用重復測量數據的方差分析,不同時間兩兩比較采用LSD-t檢驗,P<0.05為差異有統計學意義。
2結果
2.1手術前后BCVA和眼壓比較患者術后3、6mo BCVA較術前顯著改善,差異有統計學意義(t=23.815、30.787,均P<0.001),術后6mo BCVA優于3mo,差異無統計學意義(t=1.896,P=0.71)。患者術后3、6mo眼壓較術前顯著降低,差異有統計學意義(t=11.631、12.392,均P<0.001),術后6mo眼壓低于3mo,差異無統計學意義(t=0.603,P=0.636),見表1。
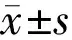
表1 手術前后BCVA和眼壓比較

表2 手術前后視野MS、MD、sLV比較
2.2手術前后視野指數MS、MD、sLV比較患者術后3、6mo MS較術前明顯上升,差異有統計學意義(t=-3.755、-5.856,均P<0.001),術后6mo MS大于3mo,差異無統計學意義(t=-2.517,P=0.11)。患者術后3、6mo MD、sLV較術前明顯下降,差異有統計學意義(tMD=6.552、9.547,均P<0.001;tsLV=3.056、5.147,均P<0.001),術后6mo MD、sLV均低于3mo,差異無統計學意義(tMD=3.399,PMD=0.06;tsLV=2.151,PsLV=0.33),見表2。
3討論
AACG患者多伴有淺前房、晶狀體較厚、位置靠前等特定的解剖學結構,由于晶狀體與虹膜的接觸面積大,所以當房水從后房經過晶狀體與虹膜間隙時受到阻力較大,造成瞳孔阻滯,使得后房壓力增高、虹膜膨隆、房角粘連關閉[6]。隨著年齡增長,晶狀體逐漸混濁、增厚、體積變大,進一步加重瞳孔阻滯,繼而加重前房角粘連,造成房水引流障礙致使眼壓增高,誘發AACG急性發作。白內障超聲乳化摘除人工晶狀體植入聯合房角分離術治療AACG的機制主要是:(1)解除晶狀體的瞳孔阻滯作用,而植入較薄的人工晶狀體可有效緩解前房角的擁擠,前房加深、變寬,房角開放,同時人工晶狀體與虹膜間間隙增大,房水循環阻力降低,后房壓力降低,消除了小梁網粘連與虹膜根部膨隆因素[7]。(2)用黏彈劑的張力和黏性360°分離房角[8-9],分開粘連不緊密和未完全粘連的房角,充分暴露小梁網。(3)超聲乳化術中灌注液液流沖刷及湍流沖擊效應,可分開房角,減輕虹膜前粘連,使術后小梁網通透性增加[10-12]。(4)超聲波使少量睫狀體上皮細胞變性壞死從而使得房水生成減少[13]。
超聲乳化術通過高負壓低能量來減少手術對鄰近組織的損傷,高灌注壓可維持前房的穩定性從而保障手術安全,然而對于術中高灌注壓是否會對已有視神經損傷的AACG患者視功能造成二次損傷并未引起手術醫生的關注。超聲乳化術中高灌注會導致一過性的眼壓升高[14]。Zhao等[15]通過前房植入壓力傳感器測到超聲乳化術中最高眼壓可達96±6.2mmHg,遠超過了視網膜血流灌注壓。王振茂等[16]測得超聲乳化階段最高眼壓為59.64±13.83mmHg,皮質抽吸階段眼壓為39.72±10.04mmHg。Malik等[14]報道,眼壓增加20mmHg并持續5min,將導致健康人視神經、視網膜和脈絡膜的血流量減少。臨床研究表明當眼壓超出一定范圍時,自體調節可能失代償并危及易感眼中視神經和視網膜的血流。越來越多的證據也顯示,一過性眼壓升高可引起眼灌注壓減少從而導致眼內組織缺血缺氧損害[17-18]。白內障術中高灌注壓可導致黃斑和視盤的血管密度、灌注密度降低[19]。
本研究將35例37眼AACG合并白內障患者作為研究對象,觀察并分析超聲乳化術中高灌注壓對AACG患者術后視功能的影響,結果顯示,與術前相比,患者術后3、6mo BCVA顯著改善,眼壓顯著降低,差異有統計學意義(P<0.001),術后組間比較差異無統計學意義(P>0.05),與術前相比,患者術后3、6mo MS明顯上升,MD、sLV明顯下降,差異有統計學意義(P<0.001),術后組間比較差異無統計學意義(P>0.05)。盡管本研究發現患者在眼壓降低后,視野有明顯改善,但其中不乏因白內障摘除后的視野改善會對研究結果造成干擾。由于本研究病例較少,需要在以后的研究中擴大樣本量,進一步探討此問題。
總之,白內障超聲乳化摘除聯合房角分離術對于降低AACG患者眼壓療效肯定,而且可以通過一次手術改善患者視力、降低眼壓、保護視功能,減少并發癥的發生,手術成功率高[20-23]。但是對于已有視神經損傷和其他并發性眼病的AACG患者行白內障超聲乳化摘除聯合房角分離時,我們仍應該盡量縮短手術時間,降低術中瓶高及負壓來減少術中眼壓升高及波動,最大程度地保護患者視功能。

