中西醫結合治療陽虛寒凝型糖尿病遠端對稱性多發性神經病變40例臨床觀察
張海生 侯宇方2 劉 翠2 張志俊 魏 偉
1.山西中醫學院附屬醫院,山西 太原 030024;2.山西中醫藥大學,山西 太原 030024
糖尿病遠端對稱性多發性神經病變(Diabetic distal Symmetric polyneuropathy,DSPN)是糖尿病性周圍神經病變中最常見的臨床類型,DSPN患者感覺神經病變或/和運動神經病變均是導致糖尿病足發病最重要的啟動因素[1],給糖尿病患者生活質量和生存率帶來極大危害。近年來,中醫藥在治療本病方面,進行了諸多探討,取得一定成效,2017年中華中醫藥學會糖尿病分會發布的《糖尿病周圍神經病變中醫臨床診療指南(2016年版)》[2],根據患者臨床表現,將本病分為氣虛血瘀、陰虛血瘀、痰瘀阻絡、肝腎虧虛、陽虛寒凝、濕熱阻絡六型,并給予相應的治療用藥推薦,對于辨證屬陽虛寒凝者,作為Ia級推薦,建議使用陽和湯加減治療。筆者在臨床中以陽和湯與四逆湯之合方陽和四逆湯聯合甲鈷胺治療陽虛寒凝型DSPN取得較好療效,現報告如下。
1 資料與方法
1.1 一般資料 選取于2017年6月至2018年12月在山西中醫學院附屬醫院內分泌科門診或住院治療的陽虛寒凝型DSPN患者80例。其中,對照組中男24例,女16例;年齡40~70歲,平均(57.77±9.29)歲;DSPN病程7~24個月,平均(15.22±5.17)個月。治療組中男22例,女18例;年齡39~70歲,平均(58.75±8.72)歲;DSPN病程個6~24月,平均(15.40±4.68)個月。兩組年齡、性別、病程等一般資料比較,差異無統計學意義(P>0.05),具有可比性。
1.2 診斷標準 ①西醫診斷:參照《中國2型糖尿病防治指南(2013年版)》[3]DSPN診斷標準制定:有明確糖尿病病史;糖尿病診斷之時或之后出現神經病變;有DSPN臨床癥狀(疼痛、麻木、感覺異常等),以下5項檢查(踝反射、針刺痛覺、震動覺、壓力覺、溫度覺)中任1項異常;神經傳導速度檢查提示神經傳導功能異常。②中醫辨證:參照《糖尿病周圍神經病變中醫臨床診療指南(2016年版)》[2]中陽虛寒凝證辨證標準制定,主癥包括:下肢麻木,雙足發涼,下肢疼痛;次癥包括:神疲懶言,腰膝乏力,畏寒怕冷,舌質暗淡或有瘀點,苔白滑,脈沉緊。
1.3 納入與排除標準
1.3.1 納入標準 ①符合DSPN西醫診斷標準及糖尿病周圍神經病變陽虛寒凝證中醫辨證標準;②年齡在30~70歲之間,性別不限;③能夠依從研究者制定的飲食、運動和治療方案;④3月內沒有使用過其他治療DSPN的方法或藥物;⑤知情同意。
1.3.2 排除標準 ①頸腰椎病變、腦梗死、格林-巴利綜合征等疾病所致周圍神經病變;②動靜脈血管性病變、化療藥物神經毒性作用所致的神經損傷;③嚴重心、肝、腎功能不全者;④對治療方案中所使用藥物過敏或不能耐受者;⑤妊娠或哺乳期婦女;⑥血糖控制差,4周以上空腹血糖>9.0 mmol/L或餐后2 h血糖>12.0 mmol/L者。
1.4 治療方法 符合納入標準的患者按就診順序,用隨機數字表法分為對照組和治療組各40例。所有患者均給予糖尿病健康教育,均予皮下注射胰島素降糖治療方案,甘舒霖R(3 mL:300 iu,通化東寶藥業股份有限公司,國藥準字S20020092),起始劑量為0.2U·kg-1·d-1,分3次于3餐前30 min皮下注射,甘精胰島素(3 mL:300 iu,賽諾菲(北京)制藥有限公司,國藥準字J20140052),起始劑量為0.2U·kg-1·d-1,每日22時左右皮下注射1次),每2~3日監測血糖,根據血糖調整胰島素用量,使空腹血糖控制在6.0~9.0 mmol/L,餐后2 h血糖控制在6.5~10.0 mmol/L。對照組給予甲鈷胺序貫治療,即第1~2周予甲鈷胺注射液(衛材(中國)藥業有限公司,0.5 mg/支,國藥準字J20170016),0.5 mg,肌肉注射,3次/周,第3~4周予甲鈷胺片(衛材(中國)藥業有限公司,0.5 mg/片,國藥準字H20143107),0.5 mg,3次/日,口服;治療組在對照組基礎上加服陽和四逆湯,日1劑,水煎分2次溫服。陽和四逆湯組成: 制附子10 g(先煎30 min)、鹿角膠10 g(黃酒烊化),熟地黃20 g,干姜10 g,肉桂5 g,炙麻黃5 g,炒白芥子10 g,懷牛膝15 g,炙甘草6 g。兩組均以4周為1個療程,共治療1個療程。
1.5 觀察指標
1.5.1 中醫臨床癥狀評分 參照《糖尿病周圍神經病變中醫診療規范初稿》[4]制定,由專門醫師對治療前后患者臨床癥狀進行評分,主癥包括:下肢麻木、雙足發涼、下肢疼痛,按癥狀輕、中、重程度,分別計2分、4分、6分;次癥包括: 神疲懶言,腰膝乏力,畏寒怕冷,按癥狀輕、中、重程度,分別計1分、2分、3分;無上述癥狀計0分,舌、脈象不計分。
1.5.2 神經傳導速度(Nerve Conduction Velocity, NCV)測定 分別在治療前后,由我院肌電圖室由專人使用上海諾誠電氣有限公司的NTS-2000肌電圖與誘發電位儀,測定雙側腓總神經、脛前神經運動神經傳導速度(Motor Nerve Conduction Velocity, MNCV)和腓總神經、脛前神經感覺神經傳導速度(Sensory Nerve Conduction Velocity, SNCV),所有患者均以右側肢體檢查結果作為診斷及療效判定指標。
1.5.3 血漿同型半胱氨酸(Homocysteine,Hcy)水平測定 血漿Hcy檢測采用循環酶法,于治療前后空腹抽靜脈血,由我院檢驗科應用奧林巴斯400全自動生化分析儀及相配試劑檢測。
1.5.4 安全性指標 治療前后分別行血、尿常規,肝、腎功能及心電圖等檢查,同時觀察并記錄其他如低血糖等不良反應。
1.6 療效判定 參照《中藥新藥臨床研究指導原則(試行)》[5]制定。顯效:中醫臨床癥狀、體征明顯改善,臨床癥狀評分減少>70%,NCV提高≥5 m/s;有效:中醫臨床癥狀、體征均有好轉,30%≤臨床癥狀評分減少≤70%,NCV提高<5m/s;無效:中醫臨床癥狀、體征均無明顯改善或加重,臨床癥狀評分減少<30%,NCV無明顯改善。總有效率=顯效率+有效率。

2 結果
2.1 兩組各主癥及臨床癥狀總評分比較 治療前,兩組各主癥及臨床癥狀總評分比較,差異無統計學意義(P>0.05);治療后,兩組下肢麻木、雙足發涼、下肢疼痛等主癥評分及臨床癥狀總評分較治療前均有下降,與治療前比較差異有統計學意義(P<0.05);且在改善癥狀評分方面,治療組優于對照組(P<0.05)。見表1。
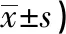
表1 兩組各主癥及臨床癥狀總評分比較 (分,
注:與同組治療前比較,*P<0.05;與對照組治療后比較,#P<0.05。
2.2 兩組血漿Hcy水平,脛前神經、腓總神經MNCV、SNCV比較 治療前,兩組血漿Hcy水平及脛前神經、腓總神經MNCV、SNCV比較,差異無統計學意義(P>0.05)。治療后,兩組脛前神經、腓總神經MNCV、SNCV較治療前提高,血漿Hcy水平較治療前下降 (P<0.05);且治療組在改善血漿Hcy及NCV方面均優于對照組(P<0.05)。見表2。
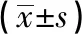
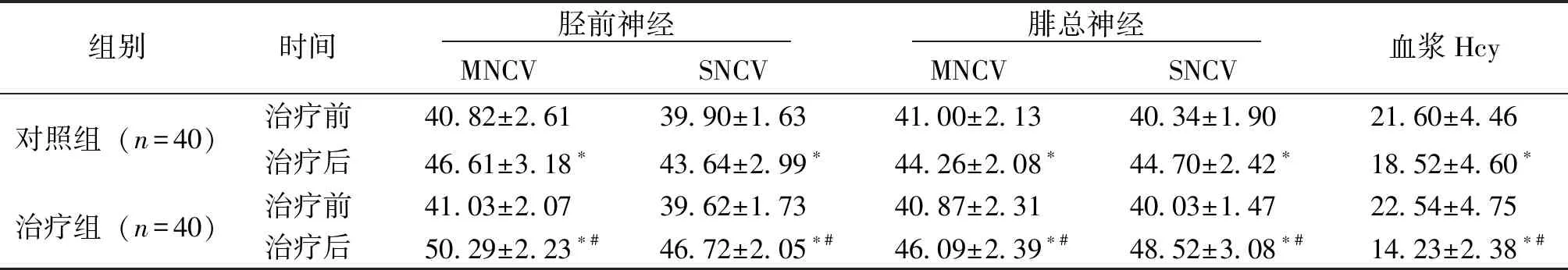
組別時間 脛前神經 腓總神經 MNCVSNCVMNCVSNCV血漿Hcy對照組(n=40)治療前40.82±2.6139.90±1.6341.00±2.1340.34±1.9021.60±4.46治療后46.61±3.18?43.64±2.99?44.26±2.08?44.70±2.42?18.52±4.60?治療組(n=40)治療前41.03±2.0739.62±1.7340.87±2.3140.03±1.4722.54±4.75治療后50.29±2.23?#46.72±2.05?#46.09±2.39?#48.52±3.08?#14.23±2.38?#
注:與同組治療前比較,*P<0.05;與對照組治療后比較,#P<0.05。
2.3 兩組臨床療效比較 治療組總有效率為72.50%,對照組總有效率為47.50%,治療組優于對照組,差異具有統計學意義(P<0.05)。見表3。

表3 兩組臨床療效比較 [例(%)]
注:與對照組比較,#P<0.05。
2.4 不良反應 治療后,兩組血、尿常規,肝、腎功能及心電圖均未見明顯異常,治療期間無嚴重低血糖反應發生。
3 討論
DSPN發病以對稱性的四肢遠端感覺、運動障礙為特征,臨床表現為對稱性肢體麻木、疼痛、感覺異常、肌肉無力等,尤以雙下肢為常見[6]。DSPN發病機制復雜,一般認為是多因素共同作用的結果。近年來,血Hcy與糖尿病周圍神經病變發病之間關系逐漸引起人們關注,相關研究較多,多數研究表明高Hcy與糖尿病周圍神經病變密切相關,是導致糖尿病周圍神經病變發病的重要因素之一[7-9]。另外,研究表明,血Hcy水平與糖尿病周圍神經病變的嚴重程度密切相關,隨著患者神經損傷加重,血Hcy水平有逐漸升高的趨勢[7]。高Hcy可能通過直接的神經細胞毒性作用、通過促氧化應激使血管內皮細胞受損,或通過抑制NO的生成,引起血管平滑肌舒縮功能受損,導致神經纖維缺血和損傷、以及通過刺激vWF等細胞因子分泌,導致凝血和纖溶功能紊亂,促進血管硬化和血栓形成等方式參與糖尿病周圍神經病變的發生及發展,故有效降低血Hcy水平,可以預防乃至阻止的糖尿病神經病變的發生、發展[10]。此外,糖尿病周圍神經病變患者不同中醫證型與血漿Hcy水平之間,兩者也有一定關聯,如高志生[11]研究發現,在糖尿病周圍神經病變辯證為陰虛熱盛-氣陰兩虛-陰陽兩虛等不同中醫證型患者中,血Hcy水平呈現逐漸遞增的趨勢。
甲鈷胺作為治療DSPN的常用藥物,臨床療效較為明確,它能夠促進神經髓鞘主要成分卵磷脂的合成,它還是蛋氨酸合成酶的輔酶, 在神經軸突結構蛋白合成中起重要作用[12]。寧光等[13]研究證實,采用甲鈷胺,先注射后口服的序貫治療方法, 相較單純口服或單純肌肉注射治療,能更快地促進受損神經細胞的修復,具有依從性好,獲效迅速的優勢。張國棟等[14]研究還表明,應用甲鈷胺治療Hcy升高的糖尿病周圍神經病變,除具有能效改善患者臨床癥狀的作用外,對于降低Hcy水平也有一定作用。本研究結果顯示,DSPN患者在給予甲鈷胺序貫治療4周后,患者臨床癥狀較前改善,NCV較治療前明顯提高,血Hcy較治療前明顯下降,與文獻報告結果相似。
中醫學認為DSPN是消渴病“變證”,屬“消渴病痹癥”的范疇,由“消渴病”日久不愈而發病,其病機多為本虛標實之證,本虛以氣虛、氣陰兩虛、脾腎陽虛,陰陽兩虛等多見,標實則有痰濁、瘀血、寒凝等不同。DSPN多纏綿日久難愈,每易耗損人體陽氣,病久及腎,終致脾腎陽虛,陽虛溫煦不足,陰寒之邪痹阻脈絡,致氣血運行失常,肢體失于溫養,而見四肢麻木、疼痛、發涼怕冷。《糖尿病周圍神經病變中醫臨床診療指南(2016年版)》[2]將陽虛寒凝證列為本病六種證型之一,中醫學文獻對于陽虛寒凝在本病發病中作用及臨床表現也早有記載,如《靈樞·本臟篇》云:“腎脆,則善病消癉,腎氣不足,腎陽衰微,陽氣不能達于四末,則四肢厥逆不溫,陽不化氣,四肢失濡。”《王旭高醫案》也載:“消渴日久,但見手足麻木,肢涼如冰”。臨床診療中也常常可見,DSPN患者在出現肢體疼痛、麻木、感覺異常等癥狀時,常會伴有全身或下肢畏寒怕冷,手足發涼,以及疼痛、麻木遇寒加重,得溫痛減等虛寒證的表現,故陽虛寒凝當為本病常見病機。故治療上,針對本病陽虛寒凝病機,應以溫陽散寒、通絡止痹為法,標本并治,方可獲效。陽和四逆湯方中君以制附子溫陽、散寒通絡以扶正祛邪,鹿角膠壯腎陽、益精血以扶助正氣,兩者合用補腎溫陽、散寒通絡,標本并治;臣以熟地補腎益精,干姜、肉桂溫補脾腎、溫經散寒;佐以辛溫之品麻黃發越陽氣、散寒通滯,白芥子溫陽化滯、消痰散結,牛膝補肝腎、強筋骨、引藥下行,使炙甘草調和諸藥,減輕麻黃、附子毒烈之性,諸藥合用共奏補腎溫陽、散寒通絡止痹之效,標本并治,恰中DSPN陽虛寒凝證本虛標實之病機特點,獲效較佳。
本研究發現,陽和四逆湯聯合甲鈷胺治療陽虛寒凝型DSPN,可明顯改善患者的臨床癥狀、提高脛前及腓總神經感覺、運動神經傳導速度,并能有效降低血漿Hcy水平,療效優于單純甲鈷胺治療。對于本方在DSPN治療中遠期療效以及具體作用機制尚需進一步研究。

