114例嗜鉻細胞瘤或腹腔副神經節瘤的臨床觀察
劉 敏,解楊婧,施浩強,何 非
嗜鉻細胞瘤(pheochromocytoma, PCC)和副神經節瘤(paraganglioma, PGL)是分別起源于腎上腺髓質或腎上腺外交感神經鏈的腫瘤,為臨床少見內分泌疾病,國內尚缺乏其發病率數據[1]。該腫瘤合成和分泌大量兒茶酚胺(catecholamine, CA)引起患者血壓升高等臨床癥候群,是繼發性高血壓的重要病因之一,并可造成心、腦、腎等嚴重并發癥。現收集PCC和腹腔PGL患者114例,對其臨床表現、診斷過程、病理表現、治療情況進行回顧性分析,以期提高臨床醫師對其診斷和治療的再認識。
1 材料與方法
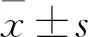
1.1 病例資料選擇安徽醫科大學第一附屬醫院2010年1月~2018年6月經手術和病理證實為腎上腺PCC 104例和腹腔PGL 10例,其中男54例,女60例,男女1 ∶1.11。就診年齡(47.71±13.61)歲,從癥狀出現或體檢發現至來本院就診時間中位數為0.5月(8 h~10年)。位于左側腎上腺49例(占42.98%),右側腎上腺53例(占46.49%),雙側腎上腺2例(占1.75%),腎上腺外腹腔內10例(占8.77%)。
1.2 研究方法回顧性分析全部患者的臨床病歷資料、實驗室檢查結果、輔助檢查結果(心電圖、腹部超聲波、腹部CT掃描、腹部磁共振)、手術治療方式及病理診斷。
2 結果
2.1 臨床表現有典型兒茶酚胺釋放發作癥狀(發作性心悸、血壓升高、頭痛、出汗等)者40例(占35.08%);消化道癥狀為主(發作性惡心、嘔吐、腹痛等)者13例(占11.4%),其中4例以急腹癥表現入院者均被病理證實有瘤體出血壞死。以休克表現入院者1例;非特異性癥狀(經常胸悶、腰酸等)者19例(占16.66%);無癥狀體檢發現者41例(占 35.96%)。有長期高血壓病史者21例(占18.42%),高血壓病程不等(3個月~20年),糖尿病史者9例(占0.79%)。入院時相關陽性體征:血壓高(≥18.62/11.97 kPa)者48例(占42.1%),其中最高血壓達30.59/18.62 kPa;低血壓(<11.97/7.98 kPa)者2例;心率快(>100次/min)者14例;病變部位腎區叩擊痛者6例;觸及腹部包塊者2例。
2.2 實驗室檢查空腹(靜脈)血糖增高(>6.1 mmol/L)者57例(占50%),其中48例(占84.21%)既往無糖尿病史;低血鉀(<3.5 mmol/L)者12例(占10.53%);63例檢測了尿WMA定性,其中僅11例陽性(陽性率17.46%),20例檢測了血CA,其中9例水平增高(多巴胺和去甲腎上腺素增高2例,腎上腺素和去甲腎上腺素增高7例)。
2.3 輔助檢查112例患者完成心電圖檢查,59例異常(占51.75%),主要表現為竇性心動過速、ST-T變化、左室高電壓、房性或室性早搏。52例患者完成腹部超聲波檢查,發現腫瘤占位46例(陽性率88.46%),其中能定位者32例,難以定位者14例。未發現腫瘤占位者6例(陰性率11.54%)。114例患者全部完成腹部CT掃描檢查,均發現腫瘤占位(陽性率100%),其中能定位者109例(占 95.61%),難以定位者5例(占4.39%)。僅15例行腹部磁共振檢查,均顯示腫瘤占位。
2.4 病理檢查結果114例患者全部完成病理檢查,腎上腺PCC 104例,其中良性92例(占88.46%),圖1顯示瘤境界清楚,左上角可見擠壓的腎上腺皮質。惡性12例(占11.54%),圖2顯示瘤細胞形態不規則,浸潤包膜,左上角包膜外血管內可見瘤栓。腹腔PGL 10例,良性8例(占80%),圖3顯示瘤境界清楚,周圍有纖維包膜。 惡性2例(占20%)。
2.5 手術治療情況全部患者均完成手術切除腫瘤治療,經常規開放式手術53例(占46.09%),其中1例患者一次切除雙側腎上腺PCC;經腹腔鏡手術54例次(占46.96%),其中1例患者經腹腔鏡手術先切除左側腫瘤,間隔48 d后再次經腹腔鏡手術切除右側腫瘤;經達芬奇機器人腹腔鏡手術8例(占6.95%)。術前需用口服降壓藥(哌唑嗪、硝苯地平、美托洛爾)控制血壓者81例(占71.05%);手術中觸碰或牽拉瘤體導致血壓急劇升高(最高血壓38.57/22.61 kPa)需應用靜脈滴注降壓藥物(艾司洛爾、酚妥拉明、尼卡地平)降低血壓完成手術者79例(占68.7%);腫瘤摘除中或摘除后血壓降低(最低血壓7.45/3.99 kPa)需靜脈補液和滴注升血壓藥物(去氧腎上腺素、多巴胺、去甲腎上腺素)者33例(占28.7%)。全部患者經恰當補液及合理應用血管活性藥物均完成手術,無死亡病例。
3 討論
2016年中國專家共識和2017年WHO對PCC / PGL做了重要更新[1-2],二代測序技術使這些腫瘤的發現呈指數增長。超過1/3的PCC / PGL與胚系基因突變有關[3],為目前最常見的遺傳性腫瘤,因此應對所有患者行基因檢測[1]。本報道中,1例患者發病年齡13歲,1例患者有家族發病史,2例患者發現雙側腎上腺PCC,均難以排除基因突變。隨著健康體檢中影像學檢查普及,無特殊癥狀在體檢或在診治其他不相關疾病中發現患者并非少見,30%以上患者由此獲得及時診斷,得到及時治療。CT掃描檢查發現占位腫瘤為100%,其中95%以上能明確定位;近半數患者完成腹部超聲波檢查,88.46%發現占位腫瘤,其中難以定位占4.39%。僅15例患者行腹部磁共振檢查,均能顯示占位腫瘤。因此,應把CT掃描檢查結果作為本病最主要的診斷依據。

圖1 腎上腺PCC HE×200 圖2 腎上腺惡性PCC HE×200 圖3 腹腔PGL HE×200
惡心、嘔吐、腹痛等胃腸道癥狀者往往與本病CA導致胃腸小動脈收縮痙攣有關,嚴重時甚至可導致胃腸黏膜缺血、壞死、穿孔[4],4例表現為急腹癥患者,均被病理證實有瘤體出血壞死。罕見以休克為表現發病者,系因腫瘤波動性分泌CA或瘤內出血、壞死、栓塞,在CA分泌減弱或消退后導致低血壓休克[5]。1例休克患者,病理證實為右側腎上腺巨大PCC(14.0 cm×11.5 cm×8.0 cm),并發現瘤栓。有50%患者入院時空腹血糖升高,其中84.21%患者既往并無糖尿病史,與上述機制有關。PCC可引起糖代謝紊亂,CA可促進肝糖原、肌糖原分解和糖異生,并有對抗胰島素作用[3]。PCC導致低血鉀可能與CA促使K+進入細胞內及促進腎素、醛固酮分泌有關[6]。PCC患者心電圖改變較常見[7],但缺乏特征性。
PCC/PGL的傳統定性診斷方法包括測定血和尿腎上腺素、去甲腎上腺素、多巴胺和終末代謝產物香草扁桃酸(VMA) 濃度[1]。本研究中許多患者因腫瘤定位明確后及時手術治療,未檢測血、尿CA及其代謝產物。檢測結果陽性率偏低,除與我們報告的患者中因體檢發現腫瘤,無典型CA釋放癥狀的患者比例高(52.63%)外,與腫瘤分泌釋放CA呈陣發性或分泌后未及時檢測,被多種酶水解有關。有學者認為尿WMA檢測不僅留取標本過程干擾因素多,且有很多因素可影響實驗室檢測結果, 多次反復檢測方有助于診斷[8]。筆者認為,在腫瘤定位明確情況下,不一定等待完成血或尿CA及其代謝產物檢測結果后再進行手術治療,病理診斷更為可靠。
目前除頭頸部PGL和分泌多巴胺的患者外,均應服用α-受體阻滯劑做術前準備,以阻斷CA收縮血管平滑肌作用,使外周阻力血管和容量血管擴張,對PCC摘除后驟然血管擴張容量不足和低血壓有良好的預防作用[1]。本文中半數以上患者在術前應用了選擇性α1-受體阻滯劑哌唑嗪,若加用β-受體阻滯劑控制血壓或心動過速,需在應用α-受體阻滯劑后使用β-受體阻滯劑,反之,有誘發急性肺水腫和左心衰風險[9]。16例加用美托洛爾患者均合并應用哌唑嗪,未發生急性肺水腫和左心衰。在術前適當增加患者液體入量,以增加血容量,可防止腫瘤切除后嚴重低血壓。術中應嚴密監測血壓,及時發現和處理因觸碰或牽拉腫瘤導致的血壓急劇升高,腫瘤切除后的血壓驟降。本文中患者術中血壓驟然升高者占68.7%,腫瘤切除后血壓下降者占28.7%,均通過及時發現和處理保障了手術安全,全部完成腫瘤切除手術。
國內已將腹腔鏡手術成功應用于腎上腺腫瘤切除近20年[10-11]。本研究中患者通過腹腔鏡切除占46.96%,具有創傷小、出血量少等優點。文獻[12]報道腹腔鏡手術仍有術后并發癥風險。54例次經腹腔鏡手術后,7例因病情不穩定而入住ICU。臨床推薦對PGL行開放式手術,對小腫瘤、非侵襲性PGL也可行腹腔鏡手術[1]。本文10例腹腔PGL患者因探查需要,均實行了開放式手術。機器人腔鏡手術較好地克服了傳統腹腔鏡和開放手術的缺點,其高清放大成像系統使手術視野清晰,高自由度機械臂使術中操作更加精細,消除生理顫抖對操作的影響[13-14]。我院近3年來已完成機器人輔助手術切除PCC 8例,切除最大瘤體(囊性)達14 cm×11 cm×8 cm,均獲得手術成功。PCC危象是臨床的危急癥,可導致患者因休克、多器官衰竭死亡[15]。1例剖宮產術后頑固性高血壓伴高熱患者,后經CT掃描發現雙腎上腺實質性占位,臨床診斷為PCC。因剖宮產術前未明確診斷及時給予相關治療處理,術后誘發PCC危象,大量CA持續分泌致血管強烈收縮,腸管壞死,多器官衰竭死亡。因無尸檢病理資料,未納入統計分析。

