獸用生物制品批簽發的流程
楊佳穎/本刊
獸藥產品上市的過程中需要涉及,生產與檢驗用菌(種)苗、主要原輔材料的選擇、生產工藝研究、產品質量研究、中間試劑、臨床試驗、新獸藥注冊、獲得產品批準文號、生物制品批簽發等環節。
現小編著重為大家梳理一下,由中國獸醫藥品監察所承辦的獸用生物制品批簽發的審批程序,及幾個常見問題。
1 獸用生物制品批簽發(辦事指南)
獸用生物制品批簽發依據《獸藥管理條例》(中華人民共和國國務院令第404 號),由中國獸醫藥品監察所實施依據跨層級聯辦,暨聯辦機構為獸用生物制品生產企業所在地省(直轄市、自治區)獸藥檢驗機構。
具體分工為:獸用生物制品生產企業所在地省(直轄市、自治區)獸藥檢驗機構負責批簽發樣品的抽取及雙人雙鎖管理;中國獸醫藥品監察所負責批簽發材料的備案及批簽發日常審核。
中國獸醫藥品監察所應在收到申報資料后7 個工作日內完成審核,提出審核意見。
必要時,中國獸醫藥品監察所在審核批簽發申報資料時可對產品實施全部項目或部分項目的抽查檢驗,抽查檢驗應在當年內完成。根據檢驗結果和申報資料審核結果作出批簽發的決定。
在特殊情況下,經農業部批準,中國獸醫藥品監察所對國家統一調撥的應急獸用生物制品實行應急批簽發。
1.1 受理條件
獸用生物制品生產企業應具有以下條件:《獸藥生產許可證》《獸藥GMP 證書》;申請批簽發產品的《獸藥產品批準文號批件》;申請批簽發產品的質量標準。
獸用生物制品中國境內代理機構應具有以下條件:《獸藥進口許可證》《獸藥經營許可證》;申請批簽發產品的《進口獸藥注冊證書》;申請批簽發產品的質量標準。
獸用生物制品生產企業及代理機構向中國獸醫藥品監察所提供上述資料復印件,中國獸醫藥品監察所審核上述申報資料合格后,向生產企業、代理機構發放《獸用生物制品批簽發通知單》。生產企業、代理機構即可向省級獸藥檢驗機構書面申請批簽發抽樣。完成抽樣和企業自檢后,生產企業、代理機構即可向中國獸醫藥品監察所申報產品批簽發。
1.2 申請材料
首次批簽發申請時應提供以下材料:《獸用生物制品批簽發申請表》或《代理機構獸用生物制品批簽發申請表》;生產企業的《獸藥生產許可證》、代理機構的《獸藥進口許可證》和《獸藥經營許可證》復印件各1 份;生產企業《獸藥 GMP 證書》復印件;申請批簽發產品的《獸藥產品批準文號批件》復印件,或《進口獸藥注冊證書》復印件各1 份;申請批簽發產品的質量標準文件各18 份。
生產企業日常申報產品批簽發應提供以下材料:《批簽發產品目錄單》;《獸用生物制品生產與檢驗報告》2 份;《獸用生物制品批簽發樣品抽樣單》;對有特別要求的生物制品,還應根據要求申報《獸用生物制品檢驗原始記錄表》。
代理機構日常申報產品批簽發應提供以下材料:《批簽發產品目錄單》;《獸用生物制品生產與檢驗報告》英文版2 份;《獸用生物制品批簽發樣品抽樣單》;進口產品若具有生產企業所在國家(地區)相應獸藥管理部門出具的批簽發證明,應連同批簽發證明的中文譯本一并提供1 份。
1.3 辦理基本流程
生產企業(或代理機構)向所在地省(直轄市、自治區)獸藥檢驗機構提出抽樣申請,省(直轄市、自治區)獸藥檢驗機構應在7 個工作日內完成抽樣,抽樣后由企業將抽樣單連同其他相關材料送至中國獸醫藥品監察所業務管理處;
中國獸醫藥品監察所質檢管理員自收到材料1 個工作日內完成批簽發申請受理并進行初次審核,提出書面審核意見;
批簽發申請通過初次審核后,由質檢管理員分發至相關檢測室,如需抽查檢驗的,由質檢管理員下達檢驗任務;
檢驗員和檢測室負責人在3 個工作日內完成對批簽發資料的審核,提出書面審核意見;
質檢管理員在1 個工作日內完成檢測室提出的書面審核意見匯總,進行抽查檢驗的,一并匯總檢驗結果,形成書面審核意見,報業務管理處負責人;
業務管理處負責人在2 個工作日內根據以上審核意見形成最終審核意見;對予以簽發的批簽發資料,將《獸用生物制品生產與檢驗報告》副本寄回申報單位;對不予簽發的批簽發資料,將《獸用生物制品批簽發不符合規定通知單》寄回申請單位和申請單位所在地省級獸藥檢驗機構。
2 常見的問題解答
2.1 獸用生物制品批簽發抽樣數量是多少
滅活疫苗(抗體類)每批抽取10 瓶,活疫苗每批抽取20 瓶,診斷試劑(盒)每批抽取5 套。
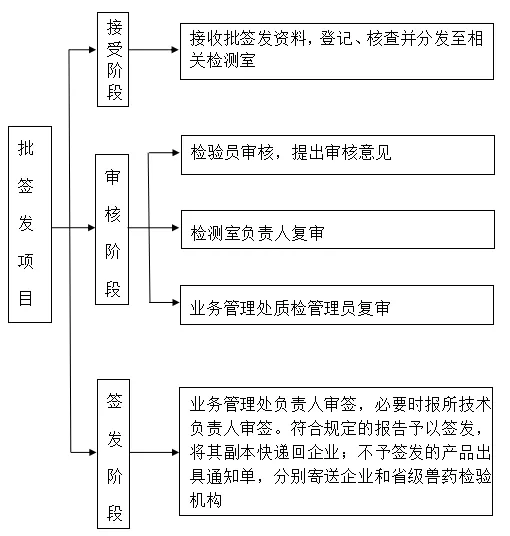
圖1 獸用生物制品批簽發辦理流程圖
2.2 首次申請批簽發時,企業應提供哪些材料?
獸用生物制品生產企業(以下簡稱“生產企業”)和中國境內代理機構(以下簡稱“代理機構”)首次申報批簽發的,應填寫《獸用生物制品批簽發申請表》或《代理機構獸用生物制品批簽發申請表》,并向中國獸醫藥品監察所提交以下資料:生產企業的《獸藥生產許可證》、代理機構的《獸藥進口許可證》和《獸藥經營許可證》復印件;生產企業《獸藥 GMP 證書》復印件;申請批簽發產品的《獸藥產品批準文號批件》復印件,或《進口獸藥注冊證書》復印件;申請批簽發產品的質量標準文件復印件。
2.3 企業對批簽發結果有異議時,應如何處理
生產企業、代理機構有對中國獸醫藥品監察所批簽發審核結果提出異議的,可在接到審核意見后7 個工作日內以書面形式向中國獸醫藥品監察所提出技術復審或仲裁檢驗申請。中國獸醫藥品監察所收到技術復審或仲裁檢驗申請后,應對申請進行審議,確定是否復審或進行仲裁檢驗并通知申請單位。確需復審的,應在7 個工作日內完成復審并通知申請單位。確需仲裁檢驗的,由農業部下達仲裁檢驗任務書,中國獸醫藥品監察所在完成檢驗后7 個工作日內將結果上報農業部。

