不同手術方式治療切口妊娠回顧性分析
劉海紅 王全利 南京中醫藥大學附屬南通醫院,江蘇省南通市 226000
切口妊娠(Cesarean scar pregnancy CSP)是指孕囊、絨毛或胎盤著床于既往剖宮產手術子宮下段疤痕處,隨著妊娠的進展,絨毛與子宮肌層粘連、植入,嚴重者甚至可穿透子宮壁,引起子宮破裂大出血[1]。 CSP為剖宮產的遠期嚴重并發癥之一,近年來隨著剖宮產比例的升高,子宮切口妊娠也越來越常見[2],所以臨床上及時準確診斷及治療CSP顯得尤為重要,失治或誤治可引起大出血危及生命[3]。本文回顧性分析我院近年來處理的78例保留生育功能的切口妊娠患者的臨床資料,從而探討各種治療方式的優點和缺點,為CSP患者提供最佳的個體化治療方案,現匯報如下。
1 資料與方法
1.1 一般資料 回顧性分析2015年1月—2018年1月期間我院收治的78例 CSP患者的臨床資料,根據不同治療方案分為四組:介入組(38例),陰式組(23例),腹腔鏡組(12例),宮腔鏡組(5例)。患者年齡、剖宮產次數、人工流產次數、停經天數、伴隨癥狀、血β-HCE比較,差異無統計學意義(P>0.05)。經超聲檢查診斷為切口妊娠:(1)孕囊位于膀胱與子宮前壁之間;(2)宮腔內無胚胎聲像;(3)矢狀面上子宮前壁不連續[4]。
1.2 治療方法
1.2.1 介入組給予子宮動脈MTX灌注+子宮動脈栓塞(UAE)+清宮術:穿刺右側股動脈,雙側子宮動脈置管并行數字減影血管造影(DSA),向雙側導管內灌注MTX各50mg,再予可吸收性明膠海綿栓塞,經造影證實子宮動脈栓塞滿意。術后72h內,復查血β-HCG較入院時下降≥50%,即在 B超監視下行清宮術。
1.2.2 陰式組給予經陰道前穹窿子宮下段切開取胚+子宮修補術:硬膜外麻醉成功后,分離膀胱子宮間隙,上推膀胱至膀胱腹膜返折處,暴露原疤痕切口,在峽部原子宮切口處可見妊娠組織膨出,為紫藍色,且病灶處肌層組織薄弱,橫行切開此處肌層組織并清除病灶,予吸頭吸宮以排除蛻膜組織殘留,并切除原疤痕組織,可吸收線間斷縫合子宮切口及陰道黏膜切口,手術完畢。
1.2.3 腹腔鏡組給予腹腔鏡下子宮切口妊娠病灶清除+子宮修補術:全麻后,氣腹形成,常規四點穿刺,于宮體注射垂體后葉素6U并與縮宮素20U靜脈滴注,切開子宮膀胱反折腹膜,下推膀胱 ,暴露病灶部位,橫行切開原子宮瘢痕凸起明顯處,清除妊娠組織,并切除原疤痕組織,可吸收線連續縫合子宮下段切口。
1.2.4 宮腔鏡組給予甲氨蝶呤肌注+米非司酮口服+宮腔鏡電切術:術前予MTX 50mg/m2肌肉注射qd,米非司酮25mg 口服bid,連續用藥3d。監測血β-HCG較入院時下降≥50%,陰超檢查提示子宮局部血流明顯減少時,在B超引導下行宮腔鏡電切術,術中可同時予垂體后葉素、縮宮素減少出血量。靜脈麻醉后,行宮腔鏡電切至病灶完全切除(若B超監測提示距漿膜層較近,為避免發生子宮穿孔,需同時行腹腔鏡下切口妊娠病灶清除+子宮修補術);最后創面電凝止血,宮腔無任何殘留組織退鏡,并予交聯透明質酸鈉凝膠3ml(宮安康)宮腔放置預防粘連。
1.3 觀察指標 分析比較四組患者的手術情況(術中出血量、手術時間、住院時間、住院費用),隨訪情況(術后陰道出血時間、月經恢復時間、術后血β-HCG降至正常的時間),術中及術后并發癥、不良反應、術后再次妊娠情況等。

2 結果
2.1 手術情況比較 陰式組在術中出血量及手術時間上均明顯少于其他三組(P<0.05),其中較腹腔鏡組在手術出血量上顯著減少(P<0.01),較宮腔鏡組在手術時間上顯著縮短 (P<0.01);陰式組在住院時間上與腹腔鏡組無明顯差別(P>0.05)與介入組及宮腔鏡組相比,住院時間明顯縮短(P<0.05);陰式組及宮腔鏡組住院費用無明顯差別(P>0.05),與介入組與腹腔鏡組相比住院費用顯著降低(P<0.01),見表1。

表1 四組手術情況比較
注:★P為陰式組與介入組比較,◆P為陰式組與腹腔鏡組比較,▲P為陰式組與宮腔鏡組比較。
2.2 術后隨訪情況比較 陰式組及腹腔鏡組術后陰道出血時間無明顯差異(P>0.05),與其他兩組相比明顯縮短(P<0.05);陰式組及腹腔鏡組術后月經恢復時間無明顯差異(P>0.05),與其他兩組相比明顯縮短(P<0.05);血HCG降至正常時間以陰式組最短,但與其他三組比較無明顯差異 (P>0.05),見表2。
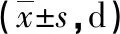
表2 四組術后隨訪情況比較
注:★P為陰式組與介入組比較,◆P為陰式組與腹腔鏡組比較,▲P為陰式組與宮腔鏡組比較。
2.3 術中及術后并發癥 介入組有3例介入后出現發熱、5d內體溫恢復正常;宮腔鏡組有1例術中一并行腹腔鏡下切口病灶清除+子宮修補術;余兩組未出現明顯并發癥。
2.4 術后不良反應比較 介入組有2例、宮腔鏡組有1例出現轉氨酶輕度升高,2周后復查均降至正常值;介入組有4例、宮腔鏡組有1例出現惡心嘔吐,后自行緩解;腹腔鏡組有1例出現肩胛痛、膈肌痛,術后2d自行緩解;陰式組未出現明顯不良反應。
2.5 術后再次妊娠情況比較 隨訪到再次妊娠患者8例,全部患者均未再次發生CSP。
3 討論
子宮切口妊娠發生機制尚不明確,可能因滋養細胞直接侵入子宮肌層,并不斷生長,絨毛與子宮肌層粘連、植入[5],其臨床癥狀表現不典型,易誤診,不恰當的治療可導致子宮穿孔、陰道大出血[6-7]。故臨床上針對有剖宮產手術史,需早期診斷是否為CSP,對于超聲診斷不能明確者,需進一步行盆腔MRI檢查已盡早診斷,HUANG等[8]認為MRI對于臨床分型較超聲有更高的準確率。
若影像學檢查確診為CSP后需立即終止妊娠,故治療原則為止血、清除病灶,且保留患者的生育功能[9]。
通過以上78例CSP患者治療相關情況回顧性分析,筆者可以看出各種治療方案都各有利弊。藥物治療雖然住院費用較其他幾種方式要少,也可有效的治療CSP,但住院時間相對較長,血β-HCG下降較其他方式偏慢,且對于出血風險較大患者不太適合[10]。子宮動脈MTX灌注+ UAE+清宮術有出血量少,局部藥物濃度高,起效快,不受孕齡限制等優勢,對于大出血的患者,介入可迅速達到止血目的,但存在穿刺部位出血、藥物副反應等缺點[11];經陰道前穹窿子宮下段切開取胚+子宮修補術,手術時間短、術中出血量少、住院時間短、住院費用較低且術后各項指標恢復較快,但陰道條件差者不太適合;腹腔鏡下子宮切口妊娠病灶清除+子宮修補術,手術時間短,手術創傷小,術后恢復快,但受到術前血β-HCG水平及病灶包塊直徑影響[12]且費用較高;甲氨蝶呤肌注+米非司酮口服+宮腔鏡電切術,在宮腔鏡直視下可明確胚胎著床位置和大小,可再次檢查了解有無殘留,但有子宮穿孔、病灶一次性難以清除徹底需聯合腹腔鏡等弊端。
綜上,陰式組可以充分暴露術野,在徹底清除異位妊娠病灶的同時可進一步修補子宮切口,避免了再次CSP的可能,腹腔鏡組雖也可以達到陰式組的治療效果,但費用較高;而介入組及宮腔鏡組無法達到修補子宮切口的目的,日后有再次發生CSP的可能性,故我們認為對有再次生育要求的CSP可將經陰道前穹窿子宮下段切開取胚+子宮修補術作為首先方案。

