MTA及iRoot BP Plus對人牙髓干細胞增殖活性的影響
俞琪 鄧淑麗
【摘 ?要】 目的:研究并比較MTA及iRoot BP Plus對人牙髓干細胞(human dental pulp stem cells, hDPSCs)增殖活性的影響。方法:將MTA及iRoot BP Plus制備成濃度稀釋比例為0、0.001、0.01、0.1、0.2、1的條件浸取液,檢測培養1、3、7天時細胞的增殖活性及3、7天時的堿性磷酸酶(alkaline phosphatase, AKP)表達量。結果:使用不同濃度的MTA及iRoot BP Plus浸取液培養hDPSCs時,隨著培養時間的增加,細胞數量顯著增多(p <0.05)。但高濃度(稀釋比例為1)MTA浸取液存在明顯的細胞毒性作用。在相同培養時間下,iRoot BP Plus比相同稀釋比例的MTA更能促進hDPSCs的增殖且高濃度培養無細胞毒性。使用不同濃度的MTA及iRoot BP Plus浸取液培養hDPSCs時,隨著培養時間的增加,AKP表達量顯著增高(p <0.05)。但在高濃度iRoot BP Plus組中,hDPSCs的AKP表達量隨時間明顯下降。在相同濃度下,iRoot BP Plus組的第3天AKP表達量普遍高于MTA組;但低濃度(稀釋比例0.001)AKP表達量低于MTA組(p <0.05)。在低濃度下(比例為0.001及0.01),iRoot BP Plus組第7天的AKP表達量普遍高于MTA組(p <0.05);但高濃度(比例為0.1、0.2和1)的AKP水平低于MTA組(p <0.05)。結論: MTA對hDPSCs的促礦化能力較強,但高濃度下存在一定的細胞毒性作用。iRoot BP Plus相較MTA具有更好的生物相容性,不會抑制hDPSCs增殖分化。但兩者均對細胞的AKP表達量具有一定的抑制作用,且隨著培養時間的增加,高濃度時iRoot BP Plus的抑制作用更為顯著。
【關鍵詞】牙髓干細胞;MTA;iRoot BP Plus;堿性磷酸酶;細胞活性
【中圖分類號】R181.3+2 ??【文獻標識碼】A???【文章編號】1004-7484(2019)10-0184-03
牙髓干細胞(Dental Pulp Stem Cells,DPSCs)是位于牙髓內的成體干細胞,由神經嵴發育而來[1,2]。DPSCs廣泛存在于成熟及年輕恒牙根尖底部,可以定植在根管壁上,進而分化為成骨細胞,能形成牙本質- 牙髓樣結構,在牙髓再生術中發揮著重要作用[3,4]。
生物陶瓷材料MTA(Mineral Trioxide Aggregate)及iRoot BP plus作為新興的髓腔修補及蓋髓材料,相較傳統修復材料具有更好的生物相容性、穩定性、抗菌性和細胞安全性。MTA可誘導細胞成骨、硬組織形成[5-7],但同時也存在著操作不便、著色等問題[8]。iRoot BP plus相較MTA具備更好的生物相容性和促進牙本質形成鈣化橋的能力[8,9],且無著色問題。
本實驗擬探討iRoot BP Plus相較MTA對hDPSC的增殖及促成骨能力的影響,以期為臨床決策作一定的參考。
1 ?材料與方法
1.1 ?實驗材料 PROROOT MTA (Dentsply,美國),iRoot BP Plus (Innovative Bioceramic Inc. 加拿大);CCK-8試劑盒(BestBio,中國),堿性磷酸酶測試盒(南京建成生物)
1.1 ?DPSCs的分離、提純和鑒定 選取在浙江大學附屬口腔醫院12~24歲的患者,因正畸或阻生拔除的完整恒牙(無牙周及牙體疾病)。拔除前后牙齒表面充分消毒,置入4℃含青霉素及鏈霉素的磷酸鹽緩沖液(phosphate-buffered saline,PBS)中轉運至實驗室進行取樣(所有操作均經患者及其監護人同意)。分離牙冠后用改良組織塊酶消化法[10]行原代培養,培養至P3代備用,并進行成脂成骨誘導能力的鑒定。
1.2 材料浸取液的制備 MTA及iRoot BP Plus調拌后37℃硬化48h后取出,5ml 含10%FBS的α-MEM培養液浸取培養48h后過濾,制備成不稀釋、1:5、1:10、1:100及1:1000比例稀釋的條件浸取液備用。
1.3 ?CCK-8測定不同濃度MTA及iRoot BP Plus對hDPSCs細胞增殖活性的影響 取生長良好的P3代hDPSCs,充分消化計數后以每孔50個細胞接種,培養24h后換成上述不同稀釋比例的MTA及iRoot BP的浸取培養液。10%FBS的α-MEM培養液作陰性對照,隔天換液。分別在培養1d、3d、7d時用酶標儀于450nm處測量吸光值。
1.4 不同濃度MTA及iRoot BP Plus對hDPSCs堿性磷酸酶表達量的影響 ?取生長良好的P3代hDPSCs,充分消化計數后以105 /ml接種,培養24h后更換不同濃度的MTA及iRoot BP培養基。10% α-MEM培養液作對照,隔天換液。分別在培養3d、7d時酶標儀于520nm處測量吸光值,562nm處測定蛋白含量,校準AKP測定值誤差。
1.5 數據統計與分析 所測數據用SPSS 24.0(IBM) 進行統計分析。結果用±s表示,計數資料使用單因素方差分析和t檢驗。使用Graphpad Prism 5 繪制統計圖。p <0.05視為具有統計學意義。
2 結果
2.1 不同濃度MTA及iRoot BP Plus對hDPSCs細胞增殖活性的影響
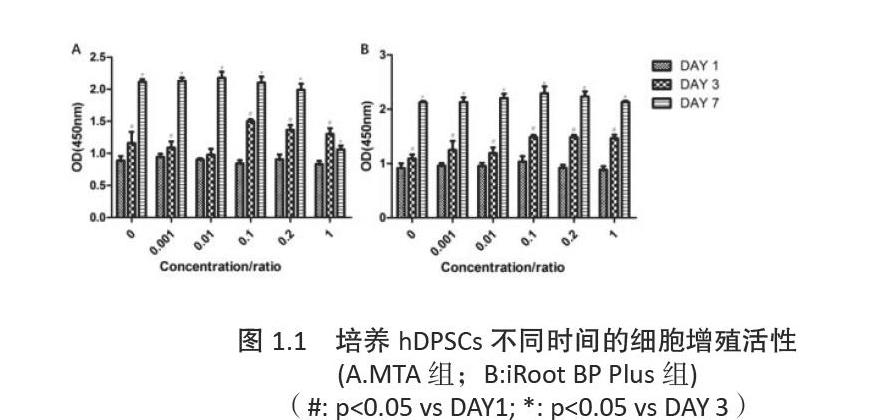
不同濃度的MTA及iRoot BP Plus條件浸取液培養hDPSCs,隨著培養時間的增加,細胞數量顯著增高(p <0.05)。未經稀釋的MTA浸取液(比例為1)在培養7天后對細胞活性存在明顯的抑制作用(p <0.05)(圖1.1A)。不同培養時間,iRoot BP Plus對細胞增殖活性的影響存在一濃度依賴的正態分布曲線,且當比例為0.1~0.2時對hDPSCs的促進作用最強(圖1.1B)。
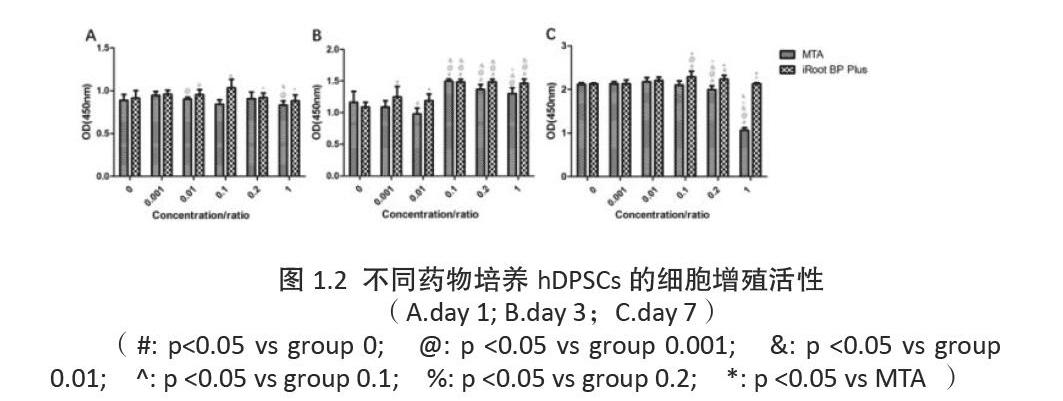
在相同培養時間下,iRoot BP Plus比相同比例的MTA更能促進hDPSCs的增殖,且長時間培養時,在高濃度區段(稀釋比例為0.1/0.2/1)未產生細胞抑制(p<0.05)(圖1.2)
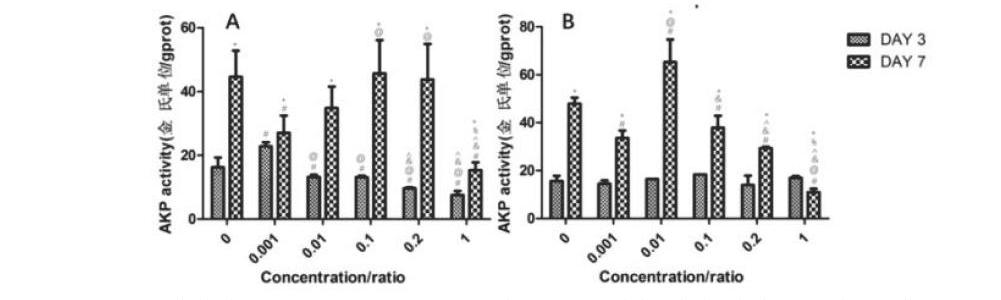
2.2 不同濃度MTA及iRoot BP Plus對hDPSCs堿性磷酸酶表達量的影響 ?不同濃度的MTA及iRoot BP Plus條件浸取液處理hDPSCs,隨著培養時間的增長,AKP表達量顯著升高(p<0.05)(圖2.1)。
培養3天后,稀釋比例為0.001的MTA組AKP表達量高于對照組,其余組低于對照組(p<0.05),且隨著濃度的增加,表達量越低;iRoot BP Plus組不同濃度浸取液對hDPSCs的AKP表達量影響較對照組無統計學差異(圖2.2A)。培養7天后,MTA組稀釋比例為0.001及1時, AKP表達量顯著低于對照組(p <0.05),其余組較對照組無差異(圖2.2B);iRoot BP Plus組的AKP表達量較對照組顯著下降(p<0.05)且在高濃度區段(0.1/0.2/1),隨著濃度的增加,AKP表達量越少。但比例為0.01的處理組, hDPSCs的AKP表達隨時間增加(p<0.05)。
相同稀釋比例的浸取液培養hDPSCs,培養3天時,iRoot BP Plus組AKP表達量普遍高于MTA組,但稀釋比例為0.001時,表達量低于MTA組(p<0.05)(圖2.2A)。培養7天后,低濃度(0.001/0.01)的iRoot BP Plus組AKP表達量普遍高于MTA組,僅0.01組具有統計學差異;高濃度(0.1/0.2/1),表達量較低(圖2.2B)。
3 討論
本實驗中,相同稀釋比例的iRoot BP Plus比MTA更能促進細胞增殖,且高濃度時未出現細胞抑制。該結果表明iRoot BP Plus不會抑制細胞生長或增殖,且其生物相容性優于MTA。類似研究[12]將hDPSCs分別接種于MTA、iRoot BP Plus上,MTA存在明顯的細胞毒性,而iRoot BP Plus在培養早期顯著增加細胞活性,但隨著培養時間增長,其細胞增殖活性下降。Zhang[13]等比較了MTA和iRoot BP Plus的體內外生物學活性,發現iRoot BP Plus相較MTA能組裝更多羥基磷灰石,且可濃度依賴性促進牙髓干細胞的黏附及遷移,牙本質橋形成及牙源性蛋白(DSP/DMP1)及黏附相關分子(Vincullin/p-Paxillin)的表達。而Samyuktha[14]等的研究卻發現iRoot BP 處理人成骨細胞及牙周膜細胞后,細胞毒性高于MTA。 MTA內含三氧化二鉍,對細胞毒性影響較大[15]。其機制在于鉍類化合物可直接作用DNA,下調Bcl-2等蛋白表達,誘導細胞凋亡[16]。iRoot BP Plus用氧化鉭及氧化鋯代替三氧化二鉍,因此無細胞毒性。
AKP參與硬組織的礦化和形成,是檢測細胞成骨分化的早期指標之一[17]。本實驗中,低濃度(稀釋比例為0.001~0.1)的MTA及iRoot BP Plus均能促進hDPSCs的AKP表達,表明iRoot BP Plus和MTA均有一定的促礦化作用。有研究表明[18,19],MTA可通過NF-κB、ERK/p38通路誘導根尖牙乳頭干細胞成牙及成骨分化。培養7天后,MTA及iRoot BP Plus中多組濃度的AKP表達量出現明顯下降。這可能與細胞數量增多有關。鏡下觀察到細胞呈堆疊狀生長,無法有效接觸培養液,因此影響了生長代謝。加上高濃度MTA的細胞毒性作用,細胞數量明顯下降,AKP代謝減少。高濃度MTA組的AKP表達量高于iRoot BP Plus組可能因為高濃度iRoot BP Plus雖會促進細胞增殖,但也會抑制胞內AKP代謝,這與一些研究結果類似。Dedeus G[20]等研究推測iRoot BP對細胞代謝水平的影響高于其對細胞密度層面的影響。Modareszadeh M R[21]等發現在不同培養時間下,iRoot BP Plus顯著降低細胞AKP水平。
材料塊及條件浸取液的制備過程可能是導致不同研究實驗結果存在偏差的原因。Hakki[22]利用MTA的上清液研究其對成牙骨質細胞的作用,這一方法使得材料的濃度得以量化。而iRoot BP Plus作為預調膏劑可直接使用,兩者雖浸取比例相同,但其真實濃度無法完全一致。在濕潤環境下,iRoot BP Plus其內的硅酸鈣可以水解生成硅酸鈣水合物凝膠及氫氧化鈣,后者與磷酸鹽反應生成羥基磷灰石和水,水又可繼續參與反應[23]。相較于根管內環境,本實驗的iRoot BP Plus材料塊固化過程中只有一底面接觸濕潤環境,其余面濕化不足,材料塊內、外表面的固化程度存在差異[24],造成浸取液濃度誤差。另外iRoot BP Plus材料塊在48h后體積膨脹明顯,增加了其浸取表面積/浸取液體積比值,使浸取液濃度增高。Walsh RM[25]等研究結果證實了iRoot BP固化過程中的體積膨脹。而MTA固化后因水分蒸發,會出現一定的體積收縮,浸取表面積減小,使浸取濃度偏低。
4 結論
MTA對hDPSCs的促礦化能力較強,但高濃度下存在一定的細胞毒性作用。iRoot BP Plus相較MTA具有更好的生物相容性,不會抑制hDPSCs增殖分化。但兩者均對細胞的AKP表達量具有一定的抑制作用,且隨著培養時間的增加,高濃度時iRoot BP Plus的抑制作用更為顯著。
參考文獻
[1] ?Ramalhosantos M, Willenbring H. On the Origin of the Term “Stem Cell” [J]. Cell Stem Cell, 2007, 1(1): 35-38
[2] ?Yasui T, Mabuchi Y, Toriumi H, et al. Purified Human Dental Pulp Stem Cells Promote Osteogenic Regeneration[J]. Journal of Dental Research, 2015, 95(2).
[3] ?Gronthos et al. Stem Cell Properties of Human Dental Pulp Stem Cells. J Dent Res 81(8) 2002:531-535
[4] ?Lovelace TW, Henry MA, Hargreaves KM, Diogenes A (2011) Evaluation of the delivery of mesenchymal stem cells into the root canal space of necrotic immature teeth after clinical regenerative endodontic procedure. Journal of Endodontics 17, 133 –8.
[5] ?Utneja S, Nawal R R, Talwar S, et al. Current perspectives of bio-ceramic technology in endodontics: calcium enriched mixture cement - review of its composition, properties and applications[J]. Restorative dentistry & endodontics, 2015, 40(1):1-13.
[6] ?Peter Z Tawil,et al. MTA: A Clinical Review. Compend Contin Educ Dent[J]. 2015 April ; 36(4): 247–264
[7] ?Kulan P, Karabiyik O, Kose G T, et al. The effect of accelerated mineral trioxide aggregate on odontoblastic differentiation in dental pulp stem cell niches[J]. International Endodontic Journal, 2017.
[8] 李羽弘,韋曦. iRoot BP和iRoot BP Plus應用于牙髓治療的研究現狀[J]. 中華口腔醫學研究雜志電子版, 2016, 10(3):208-211.
[9] ?Liu S, Wang S, Dong Y. Evaluation of a Bioceramic as a Pulp Capping Agent InVitro and InVivo[J]. Journal of Endodontics, 2015, 41(5):652-657.
[10] 麻丹丹,高杰,吳補領.改良組織塊酶消化法培養人齲損牙髓干細胞的實驗研究[J].牙體牙髓牙周病學雜志, 2011(7):371-374.
[11] 封艷,牛巧麗, 尹宏斌,等. 有限稀釋克隆法培養分離人牙周膜干細胞實驗研究[J].新疆醫科大學學報, 2014(8):989-994.
[12] Zhang S, Yang X, Fan M. BioAggregate and iRoot BP Plus optimize the proliferation and mineralization ability of human dental pulp cells[J]. International Endodontic Journal, 2013, 46(10):923.
[13] Zhang J, Zhu L X, Cheng X, et al. Promotion of Dental Pulp Cell Migration and Pulp Repair by a Bioceramic Putty Involving FGFR-mediated Signaling Pathways[J]. Journal of Dental Research, 2015, 94(6):853.
[14] ?Samyuktha V, Ravikumar P, Nagesh B, et al. Cytotoxicity evaluation of root repair materials in human-cultured periodontal ligament fibroblasts[J]. Journal of Conservative Dentistry,2014, 17(5):467.
[15] ?Camilleri J,Montesin FE,Papaioannou S,et al. Biocompatibility of two commercial forms of mineral trioxide aggregate[J]. Int Endod J,2004,37 (10):699?704.
[16] 陳懿.有機鉍(銻)配合物的合成、表征及其促肺腺癌細胞凋亡的相關研究[D].中南大學, 2014.
[17] ?Tsukamoto Y, Fukutani S, Shin-Ike T, et al. Mineralized nodule formation by cultures of human dental pulp-derived fibroblasts[J]. Archives of Oral Biology, 1993, 37(12):1045-1055.
[18] ?閆明. 無機三氧化聚合物調控根尖牙乳頭干細胞分化的機制研究[D]. 南京醫科大學, 2012.
[19] ?楊琳. ERK/p38信號通路在MTA誘導的人根尖乳頭細胞分化過程中的作用[D]. 山東大學, 2014.
[20] ?Dedeus G, Canabarro A, Alves G G, et al. Cytocompatibility of the ready-to-use bioceramic putty repair cement iRoot BP Plus with primary human osteoblasts.[J]. International Endodontic Journal, 2012, 45(6):508-513.
[21] ?Modareszadeh M R, Di F P, Tipton D A, et al. Cytotoxicity and alkaline phosphatase activity evaluation of endosequence root repair material[J]. Journal of Endodontics, 2012, 38(8):1101-5.
[22] ?Hakki S S, Bozkurt S B, Hakki E E, et al. Effects of mineral trioxide aggregate on cell survival, gene expression associated with mineralized tissues, and biomineralization of cementoblasts.[J]. Journal of Endodontics, 2009, 35(4): 513-519.
[23] ?Leal F,De?Deus G,Brand?o C,et al. Similar sealability between bioceramic putty ready?to?use repair cement and white MTA[J].Braz Dent J, 2013, 24(4):362?366.
[24] ?Charland T,Hartwell GR,Hirschberg C,et al. An evaluation of setting time of mineral trioxide aggregate and EndoSequence root repair material in the presence of human blood and minimal essential media [J]. J Endod, 2013, 39(8): 1071?1072.
[25] ?Walsh RM, Woodmansey KF,Glickman G Net al. Evaluation of compressive strength of hydraulic silicate-based root-end filling materials[J]. J Endod,2014,40(7): 969?972.
浙江省醫藥衛生科技項目(基金號:2016KYA118)

