理中枳術湯治療便秘型腸易激綜合征的療效及對HPA軸的影響
周軍惠,喬敬華
(上海市奉賢區中醫醫院,上海 201499)
腸易激綜合征(IBS)是一種常見的功能性腸病,主要表現為反復腹痛,便秘,或者腹痛與便秘交替出現等一系列的排便習慣改變[1]。便秘型腸易激綜合征(IBS-C)主要伴隨大便干結,排便周期增長,排便困難,排便不暢等排便習慣改變[2]。其發病機制復雜,現有研究主要集中在腸道局部,對中樞神經系統的影響報道甚少。現有的研究認為IBS與腦-腸軸為基礎的神經-免疫-內分泌(NEI)具有一定的聯系,而小丘腦-垂體-腎上腺(HPA)軸是引起NEI紊亂的重要環節[3]。IBS-C的治療主要西藥為主,但效果仍不理想,而中醫藥對IBS具有一定的療效。我院采用理中湯合枳術湯治療IBS-C取得了一定的療效,并發現可對HPA軸產生一定的影響,現報告如下。
1 資料與方法
1.1 一般資料
選擇2017年1月—2018年12月在我院就診并診斷為IBS-C患者112例,根據隨機數表法將患者分為觀察組和對照組,每組各56例。其中觀察組男31例,女25例,年齡25~60(42.38±10.35)歲,病程1~12(6.32±2.15)年;對照組男33例,女23例,年齡25~60(41.95±9.46)歲,病程1~12(6.29±1.86)年。兩組在性別、年齡和病程等一般資料方面比較,差異無統計學意義(P>0.05),具有可比性。
1.2 診斷標準
西醫診斷標準:1)IBS的診斷標準:癥狀出現至少6個月,并且近3月內至少有3天出現腹痛或者腹部不適的癥狀,并合并以下2條以上即可診斷:發病時具有排便次數改變(<3次/周)、排便形狀改變(外觀改變)、排便后緩解。2)IBS合并以下癥狀即可診斷為IBS-C:排便急迫感和排便不盡感;硬或者塊狀便不少于25%,水樣便或者稀便小于25%;排便費時費力;腹脹腹痛。
中醫診斷標準:主證:大便干,便出不爽,黏膩或者困難;納呆;腹痛腹脹;次證:口干不喜飲;疲乏,肢冷;舌質淡,苔白膩;脈沉遲。符合主證2項以上,次證1項以上和舌脈征象,即可診斷。
1.3 納入標準
符合西醫診斷和中醫診斷;入組前未接受治療或者停止治療的時間已經超過1個月以上;所有患者均簽署知情同意書;經醫院倫理委員會審核通過。
1.4 排除標準
胃腸道其他原因疾病;盆底性疾病,藥物性便秘和器質性病變;腹部有手術史患者;心、肝、腎、肺等重要臟器功能障礙者;精神性疾病和智力障礙者;孕婦和哺乳期婦女。
1.5 治療方法
對照組予以常規西醫治療,觀察組在對照組的基礎上予以理中湯合枳術湯治療。
常規治療:入院后多攝入纖維素,少食高脂肪和產氣食物,對有焦慮和睡眠障礙的患者予以心理干預。予以馬來酸曲美布汀 0.2 g 口服每天3次;并且予以雙歧桿菌三聯活菌腸溶膠囊 420 mg 口服,每日3次。
理中枳術湯組方:生白術60 g,枳實20 g,炙甘草、紅參和干姜各10 g,伴隨寒痛者加附子9 g,呃逆或者噯氣者加10 g,每日1劑,由我院煎藥室統一煎煮,400 mL分早晚2次服用。治療4周為1個療程,2個療程后進行療效評價。
1.6 療效評價標準
兩組均治療2個療程后進行療效評價。癥狀消失為痊愈;癥狀改善超過80%為顯效;癥狀改善50%~80%為有效;癥狀改善不到50%為無效。
總有效率(%)=(痊愈+顯效+有效)/總病例數×100%
1.7 癥狀評分
使用結腸問卷量表對中醫癥狀積分進行評價,根據表格中的6個指標,分別為腹痛時間、腹痛次數、腹脹時間、排便異常比率、黏液便比率和排便通過異常比率。每項最高分為3分,無癥狀為0分,總分18分,分數越高,癥狀越嚴重。
1.8 血清標本的采集和指標檢測
治療前和治療后6月后抽取空腹肘靜脈血,約5 mL,所有靜脈血放置在室溫靜置20 min,再通過離心機離心,離心半徑15 cm,離心速度為3 000 r/min,離心10 min,分離出血清約3 mL,放置在冰箱-80 ℃待檢測。促腎上腺皮質激素釋放激素(CRH),促腎上腺皮質激素(ACTH)和皮質酮(CORT)采用酶聯免疫吸附法進行檢測,采用上海基免實業有限公司試劑盒,按照使用說明書進行操作,主要步驟為:將生物素標記二抗和酶標試劑加入標準品和樣品,反應60 min,溫度37 ℃。洗板后,再加入顯色液AB反應10 min,反應溫度在37 ℃;再加入終止液,在15 min內檢測吸收密度值;通過Elecsys軟件定標曲線計算出CRH、ACTH和CORT水平。
1.9 觀察指標
比較兩組治療后的療效,兩組治療前后自主排便、完全自主排便、中醫癥狀評分、血管活性腸肽、胃動素、生長抑素、CRH、ACTH和CORT水平的變化。
1.10 統計學分析
所有的數據輸入到Excel表,采用SPSS15.0軟件表進行統計分析。正態資料的計量資料采用均數±標準差表示,治療前后比較采用配對t檢驗,獨立因素兩組比較采用t檢驗。計數資料采用率表示,兩組率的比較采用χ2檢驗。檢驗水準α=0.05,P≤0.05為差異有統計學意義。
2 結果
2.1 兩組治療后臨床療效的比較
從表1可知觀察組的總有效率89.28%,明顯高于對照組的66.07%(χ2=7.415,P<0.05)。
表1兩組治療后臨床療效的比較

組別例數痊愈顯效有效無效總有效率(%)觀察組5618266689.28?對照組561015121966.07
注:與對照組比較,*P<0.05。
2.2 兩組治療前后自主排便、完全自主排便和中醫癥狀評分的比較
從表2可知兩組治療前自主排便、完全自主排便和中醫癥狀評分差異無統計學意義(P>0.05),治療后兩組自主排便和完全自主排便均較治療前明顯升高(P<0.01),而中醫癥狀評分較治療前明顯降低(P<0.01),且觀察組優于對照組(P<0.01)。
2.3 兩組治療前后血管活性腸肽、胃動素和生長抑素水平的比較
從表3可知,兩組治療前血管活性腸肽、胃動素和生長抑素水平差異無統計學意義(P>0.05),治療后血管活性腸肽和生長抑素較治療前明顯降低(P<0.01),而胃動素較治療前明顯升高(P<0.01),且觀察組優于對照組(P<0.01)。
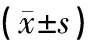

組別例數自主排便(次)完全自主排便(次)中醫癥狀評分(分)治療前治療后治療前治療后治療前治療后觀察組561.93±0.634.68±1.86a0.38±0.153.54±1.57a15.34±1.375.72±1.68a對照組561.89±0.713.65±1.69a0.36±0.182.12±0.95a15.48±1.159.64±2.63at值0.3153.0670.6395.7910.5869.400P值0.7530.0030.5240.0000.5590.000
注:與本組治療前比較,aP<0.01。
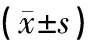

組別例數血管活性腸肽(pg/mL)胃動素(pg/mL)生長抑素(pg/mL)治療前治療后治療前治療后治療前治療后觀察組5641.67±6.1530.48±3.48a135.65±56.34243.94±37.18a22.34±3.4612.64±2.86a對照組5642.18±5.6736.15±4.64a131.76±49.67198.15±42.67a23.28±2.9815.86±3.12at值0.4567.3160.3886.0551.5415.693P值0.6490.0000.6990.0000.1260.000
注:與本組治療前比較,aP<0.01。
2.4 兩組治療前后血清CRH、ACTH和CORT水平的變化
從表4可知兩組治療前血清CRH、ACTH和CORT水平差異無統計學意義(P>0.05),治療后兩組均較治療前明顯降低(P<0.01),且觀察組優于對照組(P<0.01)。
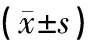

組別例數CRH(ng/L)ACTH(ng/L)CORT(μg/L)治療前治療后治療前治療后治療前治療后觀察組569.56±2.375.76±1.28a23.64±3.6512.78±2.64a234.65±24.39186.46±27.15a對照組569.67±2.197.61±1.39a22.93±2.9616.39±3.16a241.47±28.46206.37±29.43at值0.2557.3271.1316.5611.3623.721P值0.7990.0000.2610.0000.1760.000
注:與本組治療前比較,aP<0.01。
3 討論
IBS-C發病機制復雜,大多數專家認為其與內臟感覺和胃動力發生異常等相關,目前主要集中在調節內臟感覺,導瀉和促進胃腸動力方面的治療。馬來酸曲美布汀具有雙向調節胃腸道動力作用,通過提高胃腸道平滑肌的興奮,作用肌間神經叢的阿片受體,促進乙酰膽堿的釋放,促進胃腸運動和減輕胃腸功能的失調[4]。研究發現,腸道菌群失調與IBS-C發病具有密切關系,益生菌在腸道菌群失調方面已經被逐漸重視,臨床研究證實益生菌能夠改善IBS-C癥狀,可能與益生菌為腸道內的原籍細菌,具有產酶能力強,繁殖能力較強的特點有關,能夠很快適應腸內環境[5]。目前單純西藥治療取得了一定的療效,但長期療效仍不理想,容易復發,而中醫藥治療IBS-C得到一定的認可,尤其聯合西藥治療IBS-C取得了初步療效。本研究觀察理中枳術湯聯合西藥治療IBS-C,其療效明顯優于對照組,并且發現觀察組在提高自主排便和完全自主排便次數,降低中醫癥狀評分明顯優于對照組,說明理中枳術湯具有提高療效,改善IBS-C的癥狀。生白術的主要成分為蒼術酮和白術內酯等成分,現代藥理學認為其具有促進胃腸排空,小腸推進作用;枳實具有行氣、散結、化痰和除痞的功效,現代藥理學認為其對在體胃腸平滑肌具有興奮作用,對幽門螺桿菌具有殺滅作用,具有抗疲勞、鎮痛和鎮靜作用;炙甘草主要成分甘草酸、甘草苷等成分,具有抗炎、解痙、抗酸和腎上皮質激素樣作用,調節免疫和抗心律失常作用;紅參的化學成分主要為皂苷和揮發油,現代藥理學認為具有提高腦和體力活動能力,增強抗應激、抗腫瘤、抗疲勞和抗衰老等作用;干姜主要化學成分為揮發油和姜辣素,現代藥理學認為其具有殺菌、抗氧化、抗血小板,提高免疫力,調節腸張力,節律和蠕動的作用,可以調節消化道機能[6-9]。
本研究顯示,理中枳術湯聯合西藥治療IBS-C能夠明顯降低血清血管活性腸肽,說明理中枳術湯能夠明顯降低IBS-C患者中的血管活性腸肽。血管活性腸肽主要分布在胃腸道的神經叢和平滑肌層中,對胃腸道平滑肌具有一定的舒張作用[10],在針對IBS-C研究中發現,血管活性腸肽參與了IBS-C的發生發展過程,高水平的血管活性腸肽通過神經遞質釋放,對腸蠕動起到抑制作用[11]。同時本研究發現,理中枳術湯聯合治療能夠明顯降低IBS-C血清生長抑素,說明理中枳術湯通過降低血清生長抑素水平,從而達到治療效果。生長抑素廣泛分布于中樞神經系統和胃腸道神經叢中,對胃腸道生理功能具有一定的抑制作用,具有抑制胃腸道運動和胃腸道激素的分泌,促進營養物質和電解質的吸收,從而達到治療的目的[12]。本研究還發現理中枳術湯聯合治療可升高IBS-C患者血清胃動素水平,胃動素是多肽型胃腸激素,能夠加快胃腸道營養和電解質的轉運,在胃動素缺乏時胃腸道功能受到明顯抑制[13]。說明理中枳術湯通過降低血管活性腸肽和生長抑素水平,提高機體的胃動素水平,從而達到治療IBS-C的目的。
理中枳術湯聯合西藥治療IBS-C能夠降低CRH、ACTH和CORT水平,說明理中枳術湯治療IBS-C療效與機體激素CRH、ACTH和CORT水平降低有關。IBS-C的發病機理仍不清楚,可能與多種機制相互關聯,均是以腦腸軸為基礎的NEI,在這些重要的神經網絡中,以HPA軸最為重要,各種致病因素引起中樞和外周神經系統匯集到下丘腦,引起CRH從小丘腦釋放到垂體門靜脈系統,作用于垂體前葉,導致垂體是釋放ACTH釋放入血,引起更多的CORT釋放入血[14]。故CRH、ACTH和CORT水平是反映HPA軸的激活狀態,HPA過度激活狀態是應激過程的重要特征,IBS-C疾病中HPA激活是應激反應激活的特征性表現,多種HPA軸相關的激素大量釋放入血。腎上腺皮質是HPA軸的靶組織,機體處于應激時,垂體分泌大量的ACTH作用與腎上腺皮質,導致機體合成大量的CORT釋放入血,從而對糖脂代謝和穩定溶酶體膜的作用[15];同時垂體激活后同樣也導致大量的CRH釋放。可見理中枳術湯聯合西藥治療IBS-C能夠降低機體的CRH、ACTH和CORT水平,調節HPA軸的激素紊亂,改善胃腸道的高敏狀態,從而起到治療IBS-C作用。
總之,理中枳術湯治療IBS-C療效顯著,具有改善癥狀,糾正胃腸激素紊亂,穩定HPA軸的作用。

