鈣劑聯合新斯的明對婦科腹腔鏡手術術后肌松恢復的影響
張 萍 顏 明 陳 鳳 尹海玲
肌松藥是全射麻醉手術中必不可少的一部分,可以提供滿意的氣管插管條件以及術中維持良好的肌肉松弛效果。術畢神經肌肉阻滯作用逆轉不完全,將會導致肌松殘余(residual neuromuscular blockade,rNMB,定義為TOFr<0.9)。我國氣管拔管時rNMB的發生率約為57.8%[1],麻醉后恢復室(postanesthesia care unit,PACU)中rNMB發生率約為31.0%~55.9%[2~4]。rNMB和一些臨床不良結局相關,是術后肺部并發癥(postoperative pulmonary complications,POPCs)的主要危險因素[5~7]。離子鈣在神經肌肉信號的傳遞中起著重要作用,鈣可以刺激運動神經末梢釋放乙酰膽堿,也能降低乙酰膽堿誘導的運動終板去極化反應的程度[8~10]。臨床實踐證明,血清鈣濃度的增加可能與對神經肌肉阻滯的抵抗有關[11,12]。本研究將評估葡萄糖酸鈣聯合新斯的明是否可以加快神經肌肉功能的恢復,降低POPCs發生率,目前這方面研究較少。
資料與方法
1.研究對象及試驗設計:本研究為單中心隨機對照雙盲試驗,于中國臨床試驗中心注冊(注冊號:ChiCTR1800017027),經筆者醫院倫理學委員會批準(受理號:XYFY2018-KL041-01),術前簽署知情同意書。選取2018年4月~2018年9月在全身麻醉下行擇期婦科腹腔鏡手術的患者:①ASAⅠ~Ⅱ級;②年齡45~65歲;③BMI為18.5~23.9kg/m2。排除標準:①困難氣道;②既往哮喘、慢性阻塞性肺疾病;③術前肝、腎功能異常;④有神經肌肉疾病的患者,正在服用會影響神經肌肉阻滯藥物作用時間和強度的藥物;⑤孕婦,哺乳期女性;⑥高鈣血癥;⑦對于所使用的藥物高敏;⑧對于新斯的明以及阿托品有使用禁忌證的患者。剔除標準:①手術時間小于2h;②中轉開腹手術;③術畢入ICU者。納入患者采用隨機數字法分為葡萄糖酸鈣聯合新斯的明組(C組)和新斯的明組(N組),每組30例。
2.麻醉方法:兩組均采用全身麻醉氣管插管。入室后,建立靜脈通道,連接多導聯監護儀,局部麻醉下左側橈動脈穿刺置管行連續動脈血壓監測,常規監測ECG、BP、SpO2、HR、熵指數、食管溫度及肌松監測側手掌體表溫度。靜脈注射咪達唑侖(0.05mg/kg)、泵注右美托咪定(0.5μg/kg,15min泵完),待患者睫毛反射消失后,行肌松監測。采用Ohmeda GE E-NMT-00壓電法(kinemyography,KMG)監測肌松,使用TOF監測,頻率為2Hz,波寬0.2ms,電流強度60mA,每個成串刺激間隔20s。基線穩定5min后靜脈注射依托咪酯(0.3mg/kg)、舒芬太尼(0.5μg/kg),羅庫溴胺(0.9mg/kg)(浙江仙琚制藥有限公司,產品批號:180303),當TOF計數為0時,進行氣管插管并行機械通氣,呼吸參數設置為潮氣量6~8ml/kg、呼吸頻率10~12次/分,維持PETC0235~45mmHg。術中采用丙泊酚4~10mg/(kg·h)、瑞芬太尼0.1~0.3μg/(kg·min),持續泵注,將狀態熵(SE)維持在40~60,且RE、SE兩差值保持在10以內。根據血壓及心率變化使用血管活性藥物。采取保溫措施,使患者食管溫度≥36.5℃,體表溫度≥32℃。
模擬閉環靶控輸注方式,待TOF計數為1后開啟微量注射泵,持續輸注羅庫溴胺5μg/(kg·min),使TOF計數維持在1~2,若TOF<1則暫停泵注,直到TOF≥1后繼續泵注,并以1μg/(kg·min)的速率減藥,若TOF>2,則迅速推注羅庫溴胺0.1mg/kg,直到TOF≤2后繼續以5~10μg/(kg·min)速率泵注。進行腹腔沖洗時,停止羅庫溴銨泵注,當TOF計數為3時,予以40μg/kg新斯的明加20μg/kg阿托品,C組予以5%的葡萄糖酸鈣注射液20mg/kg,將10%葡萄糖酸鈣注射液(華潤雙鶴利民藥業有限公司,產品批號:17020505-2)加入等容積10%葡萄糖注射液中稀釋,以5ml/min的速率泵注,N組予以等容積0.9%氯化鈉注射液等速度泵注。手術結束后停用瑞芬太尼,TOFr≥0.7后停用丙泊酚。待TOFr≥0.9,自主呼吸、咳嗽和吞咽反射恢復,通氣量恢復到術前水平,予以拔除氣管導管,送入PACU,PACU停留期間予以面罩吸氧2L/min。
3.觀察指標:主要觀察指標:觀察從給予新斯的明到TOFr≥0.9的時間,PACU停留期間低氧血癥的發生情況,記錄在PACU中,發生中度(最低SpO2為90%~93%)以及嚴重低氧血癥(最低SpO2<90%)的人數。次要觀察指標:TOFr≥0.9后15min,評估患者肌力相關的11項體征及2項癥狀,觀察患者能否完成以下指令:抬頭5s,用力握手5s,睜眼5s,伸舌5s,微笑,吞咽,講話,咳嗽,用眼睛追蹤物體,深呼吸,壓舌板試驗,不能完成為陽性,能完成為陰性,詢問患者是否有視物模糊、復視的癥狀,有為陽性,沒有為陰性,在完成測試后,讓患者評估在做指令動作的過程中所感受到的肌無力的程度,評分為0~10分,0分為患者所經歷的最嚴重的肌無力體驗,10分為沒有肌無力感覺。其他:記錄予以新斯的明前(T1)、予以新斯的明后10min(T2)時的HR、MAP以及游離血鈣濃度。觀察患者在PACU停留期間是否有惡心、嘔吐、胸悶、皮膚瘙癢等不適癥狀。患者術后住院時間、住院期間肺炎發生情況(指患者術后住院期間有咳嗽、咳痰等臨床表現,胸部X線片示肺部炎癥改變)。記錄患者的一般情況、麻醉時間、羅庫溴銨總用量、食管溫度等。
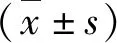
結 果
1.患者一般資料的比較:兩組患者年齡、身高、體重、ASA分級、給藥時的體溫、羅庫溴銨總用量、麻醉時間、術前是否化療、術中是否使用順鉑等一般資料比較,差異無統計學意義(P>0.05),詳見表1。
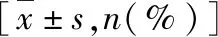
表1 兩組患者一般情況比較
2.安全評價:兩組患者術前、術后總鈣濃度以及T1時游離鈣濃度比較差異無統計學意義(P>0.05),T2時游離鈣濃度分別為N組1.10±0.06mmol/L、C組1.21±0.06mmol/L,差異有統計學意義(P<0.05),給葡萄糖酸鈣后,游離鈣濃度增高,但是在正常值范圍內,兩組患者T1、T2時HR、MAP比較差異無統計學意義(P>0.05,表2),患者PACU停留期間,惡心、胸悶情況,差異無統計學意義(P>0.05,表3)。沒有患者出現嘔吐、皮膚瘙癢癥狀。
3.神經肌肉阻滯的恢復情況:在C組中明顯快于N組,C組患者的從給藥到恢復的時間比N組縮短了27%,分別為1065(810,1150)s和775(540,860)s(P<0.05),予以鈣劑聯合新斯的明后,患者肌無力自主評分分別為5.71±0.71分和6.22±0.93分,差異有統計學意義(P<0.05),TOFr≥0.9后15min

表2 給新斯的明前后兩組鈣、HR、MAP變化

表3 PACU停留期間不良反應發生情況 [n(%)]
測得肌力恢復相關癥狀和體征,差異無統計學意義(P>0.05),詳見表4。 在C組,約85%(23/27例)的患者在15min內神經肌肉阻滯恢復,最早恢復時間為480s,相對于在N組,僅約50%(14/28例)的患者在15min內肌松恢復達滿意程度,最早恢復時間為590s,詳見圖1。

表4 兩組患者肌松恢復情況的比較

圖1 患者TOFr恢復至0.9的累積百分比(%)
4.PACU停留期間低氧血癥發生情況:兩組患者比較,差異無統計學意義(P>0.05),詳見表5。

表5 兩組患者PACU停留期間低氧血癥發生情況[(n(%)]
5.術后肺炎及住院時間:兩組患者比較,差異無統計學意義(P>0.05),詳見表6。
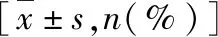
表6 兩組患者術后肺部并發癥及住院時間比較
討 論
游離鈣離子是機體內調節細胞內酶的活性、促進腺體分泌、傳遞信號以及參與激素-受體的結合、激活凝血途徑等生命活動所必需的。其在神經肌肉的轉遞中起著關鍵性的作用,鈣劑在突觸前后以不同的方式增強或者減弱神經肌肉信號的傳導[8~10]。鈣既可以刺激運動神經末梢釋放乙酰膽堿,使接頭部乙酰膽堿濃度增高,也可以穩定突觸后膜,降低其對乙酰膽堿的敏感度,并且參與橫紋肌興奮-收縮耦聯,調節肌纖維的舒張等。Waud等[11]研究發現,甲狀旁腺功能亢進癥的患者,具有較高的血清鈣離子水平,縮短了阿曲庫銨的作用時間,鈣離子濃度增加能降低機體對于非去極化肌松藥物的敏感度,可能與對神經肌肉阻滯的抵抗有關。維拉帕米和氨氯地平使健康受試者的神經肌肉傳導受損,鈣離子通道拮抗劑增強了非去極化神經肌肉阻滯的作用[12]。因此,予以鈣劑可能會加快乙酰膽堿酯酶抑制劑誘導的神經肌肉阻滯恢復的速率。
本研究術中維持C組神經肌肉阻滯恢復時間比N組縮短約27%。表明鈣劑可能對于肌肉神經阻滯的恢復是有益處的。C組相對于N組,患者肌力恢復情況有所改善,術后肺部并發癥例數較少,但是差異無統計學意義,這可能是因為樣本量較小所致,尚需開展大規模的前瞻性的研究來比較C組和N組的臨床結局之間是否存在差異。由于兩組患者均在TOFr≥0.9以后拔管,可能在沒有肌松監測設備的情況下,鈣劑將發揮更大的作用。
Hristovska等[13]納入了41項研究,共4206例患者,統計分析了在TOFr為2時使用0.05mg/kg新斯的明逆轉神經肌肉阻滯作用,恢復時間均值為774s,與本試驗比較,時間相差較大,可能由于本研究中所有患者均為女性,其對羅庫溴銨的敏感度明顯高于男性,作用時間延長,部分癌癥患者術前進行化療,術中腹腔局部應用化療藥物順鉑,加之氣腹使羅庫溴銨代謝減慢,從而使肌松效應維持時間延長,恢復緩慢[14~16]。
羅庫溴銨特異性的拮抗藥物sugammadex,考慮其經濟性,目前尚未在臨床大規模開展使用,因此缺乏大量的臨床研究和循證醫學數據[17]。迄今為止,沒有證據表明使用sugammadex后術后肺部嚴重并發癥的發生率比使用新斯的明低。sugammadex潛在的嚴重過敏反應、導致QTc間期延長、出血風險增加和神經毒性等尚需進一步研究[18]。圍術期多模式的肌松管理策略需要鈣劑的參與,鈣劑也可能可用于提高非氨基甾體類肌松藥物的術后神經肌肉阻滯恢復速率。
本研究將rNMB定義為TOFr<0.9,近期有研究建議當使用KMG法監測肌松時,可以將TOFr≥1.0,作為安全拔管的指標[19]。鑒于現存參考文獻均使用TOFr≥0.9為參考指標,而且尚無研究證明手術結束后達到TOFr≥1.0拔管,患者臨床預后有所改善,因此本研究繼續沿用TOFr<0.9作為肌松殘余的指標。
考慮到醫學倫理學的限制,對患者安全的保障以及麻醉復蘇的臨床需要,本研究并未設計單純空白對照組觀察婦科腹腔鏡手術術后肌松自然恢復情況和單獨鈣劑干預組進行比較,對于這些問題尚需進一步研究解決。綜上所述, 葡萄糖酸鈣聯合新斯的明能加快術后神經肌肉阻滯恢復,改善患者主觀感覺,可安全用于婦科腹腔鏡手術的患者。

