食品及食品接觸材料中烴類礦物油分析技術進展
鄭建國,陳燕芬,鐘懷寧*,李 丹,吳梓潼
(1.廣東省動植物與食品進出口技術措施研究重點實驗室,廣東 廣州 510623;2.廣州海關技術中心,廣東 廣州 510623;3.廣州市天河外國語學校,廣東 廣州 510627)
烴類礦物油(Mineral oil hydrocarbons,MOH)是一類由多種烴類物質組成的復雜混合物,主要由原油經蒸餾、萃取、酸處理、加氫反應等過程或是由天然氣、煤及其它生物材料通過合成反應制成。MOH主要包括環烷烴、直鏈及支鏈的飽和烴類礦物油(Mineral oil saturated hydrocarbons,MOSH)及由烷基化合物組成的芳香烴類礦物油(Mineral oil aromatic hydrocarbons,MOAH)。由于碳原子數小于10的烴類礦物油具有揮發性,殘留并污染食品的可能性小;而碳原子數大于50的烴類礦物油分子量大,不易被人體吸收。因此,現階段的風險評估主要關注碳原子數范圍為C10~C50的礦物油。對于礦物油的毒性,國外已有諸多研究,但仍然存在較大爭議。研究表明,烷烴類礦物油具有生物蓄積效應,目前普遍認為C16~C35具有最高風險,主要蓄積在脂肪組織、淋巴結、脾臟和肝臟等器官中[1];而芳香烴類礦物油具有致突變性,高度烷基化的芳烴可能會誘發腫瘤,一些結構簡單的芳烴有細胞毒性[1],含有3個以上苯環的芳烴有遺傳致癌性[2]。因此,礦物油的污染不容忽視。調查研究表明,礦物油大多存在于有印刷的食品包裝紙和回收紙包裝材料中,通常以氣態擴散或直接接觸的方式遷移到食品中,是目前食品中礦物油污染的主要來源[3]。
烴類礦物油成分復雜,且干擾物質較多,采用現有技術檢測存在較大的局限性。多年來,研究者在前處理技術的簡化、干擾物質的排除、MOSH和MOAH的有效分離及定性和定量分析、儀器配置的開發和應用等方面進行了不斷探索和優化。本文綜述了國內外近十年來礦物油檢測技術的研究進展,及其在食品及食品包裝材料中的應用,旨在為相關企業和機構的檢測工作提供方法與技術參考。
礦物油測定時需要對MOSH和MOAH的總量進行定量分析,其一般檢測流程如圖1所示:提取凈化后,對MOSH和MOAH進行分離,采用GC/FID定量(必要時采用GC-MS進行定性分析)。

圖1 礦物油的常規檢測流程Fig.1 Routine detection process of mineral oil
1 樣品前處理技術
食品中的很多物質與礦物油結構相近,在色譜上難以與礦物油實現分離,從而對檢測產生較大干擾。因此要得到準確的定量結果,必須實現礦物油的有效提取、凈化和分離。
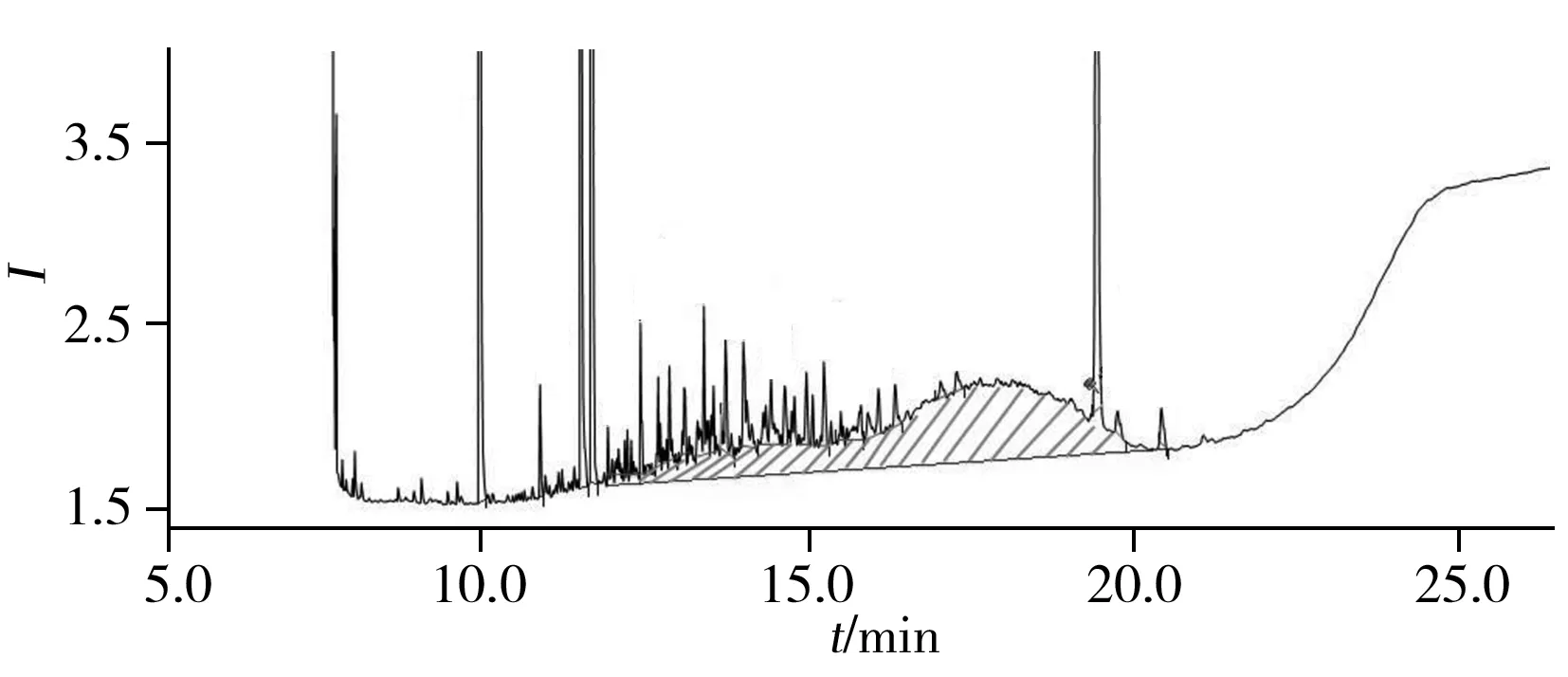
圖2 MOSH的色譜圖Fig.2 Chromatogram of MOSH
1.1 提取及濃縮方法
食品及食品接觸材料的傳統提取方法是采取正己烷或正己烷-乙醇提取,根據測試對象種類選擇不同的提取時間,如奶粉為靜置過夜提取,而紙制品中礦物油含量的提取時間為2 h[4-5]。而針對含油脂的食品,通常需要皂化去除甘油三酯等,導致分析凈化步驟繁瑣、費時,且消耗大量的試劑。為了提高效率,Moret等[6]采用微波皂化萃取法將提取、皂化在高溫高壓微波下同步完成,節約了試劑,簡化了濃縮步驟,實現了快速提取。也有研究通過快速溶劑萃取法[7]大大縮短了礦物油的提取時間。
礦物油為一大類同系物質,在色譜上通常以“駝峰”的形態出現,如圖2。為避免前處理過程中低碳鏈礦物油的損失,需選用合適的方式對提取液進行濃縮。Fiorini等[8]建立了植物油和干性水果食品中礦物油的檢測方法,研究了不同濃縮方式對檢測結果的影響,發現相比氮吹濃縮法,旋轉蒸發濃縮法(40 ℃)造成的目標物損失更少,效果更優。
1.2 凈化方法
植物油中的甘油三酯、原生烴類和烯烴物質是在對植物油中的礦物油進行測定時的主要干擾物質。
1.2.1 皂化法——去除甘油三酯的干擾甘油三酯作為植物油的主要成分,能與礦物油成分共存于有機溶劑中,且沸點較礦物油高,在FID色譜上的出峰相對靠后,既可能掩蓋目標物,也容易造成色譜柱和檢測器的污染,無法實現樣品的準確分析,如圖3。因此,對于植物油類或含油脂成分較高的樣品,需采用皂化法去除油脂的干擾[6,9]。
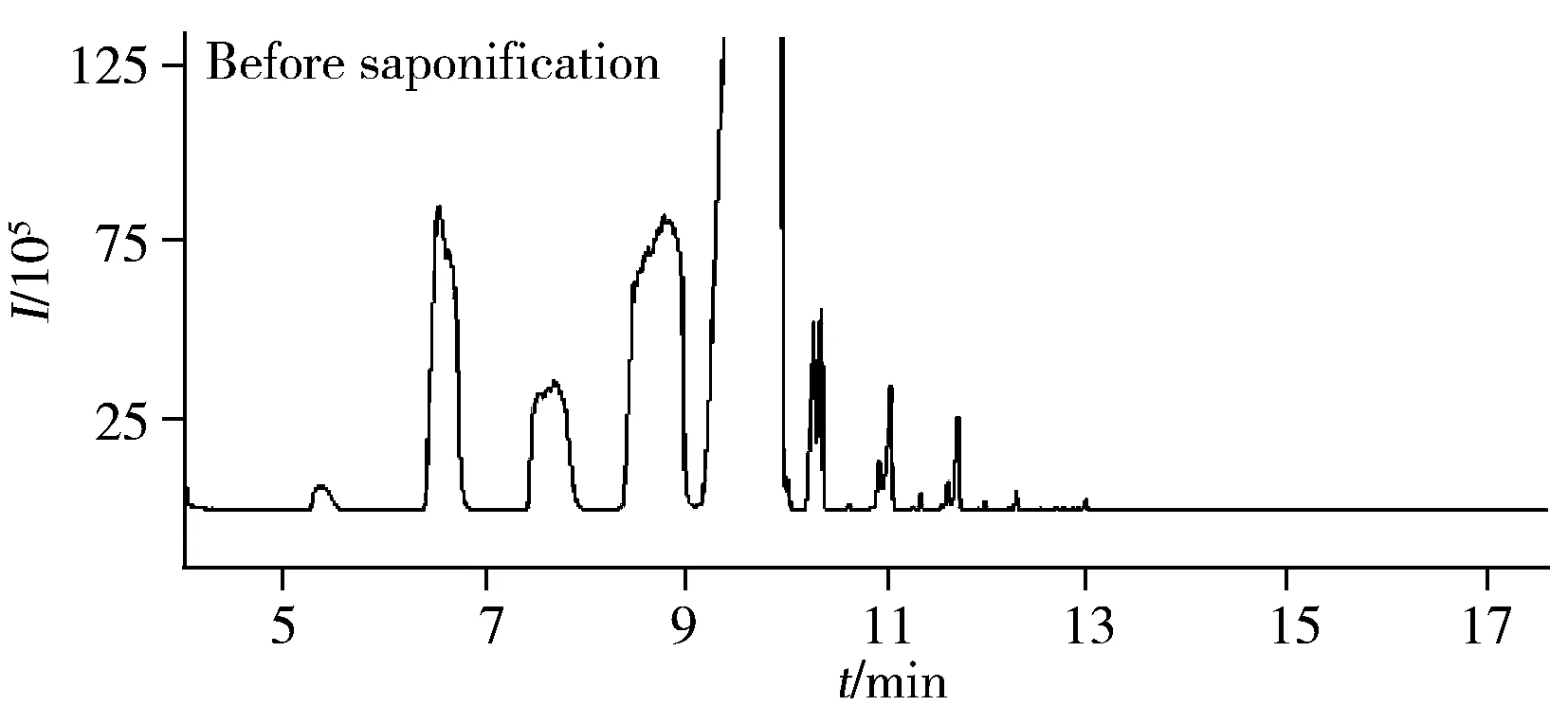
1.2.2 氧化鋁法——去除原生烴類物質的干擾原生烴類物質主要為奇數碳的正構烷烴(C23~C33),其性質與MOSH相同,常規的前處理步驟無法將兩者有效分離。樣品中存在該類物質時,其色譜峰往往豎立于MOSH之上,對MOSH的定性和定量造成干擾,或導致假陽性結果。活性氧化鋁對正構烷烴具有一定的滯留作用,可去除該類物質對礦物油檢測的干擾,已廣泛應用于油脂類食品的檢測[10-11]。但也有研究表明,氧化鋁法在有效降低干擾的同時,會造成一定程度的礦物油目標物的損失[12-14]。實際應用時是否使用活性氧化鋁應視具體情況而定:當原生烴類物質的出峰對MOSH干擾較小時,可不進行氧化鋁的凈化步驟,直接通過手動積分扣除“駝峰”輪廓以上的原生烴類物質(尖峰);而當原生烴類物質含量過高,會對MOSH所產生的“駝峰”造成“壓迫”,導致定量不準確時,則需選擇氧化鋁去除原生烴的干擾。
1.2.3 環氧化法——去除烯烴類物質的干擾植物油中含有的角鯊烯、胡蘿卜素、萜烯、植物甾烯等烯烴類物質的干擾是礦物油分析時需解決的難題之一。目前一般通過環氧化反應和溴醇反應等方法將烯烴物質氧化除去。其中,環氧化反應的應用較為普遍,其原理是采用過氧化物,如間氯過氧化苯甲酸(M-chloroperoxide benzoic acid,mCPBA)[14]與烯烴反應使雙鍵環氧化,環氧化物極性強于MOAH,可更好地滯留在銀硅膠柱上,洗脫過程中不再與MOAH共流出,從而實現兩者分離。同樣,環氧化也會因樣品基質的不同,造成不同程度的目標物損失[14-16]。目前采用此方法對樣品凈化的報道不多,其適用范圍、精密度、回收率等尚處在探索之中。
1.3 MOSH與MOAH的分離方法
由于硝酸銀具有保留烯烴和MOAH的能力,因此,目前主要采用硝酸銀硅膠填料進行凈化。先通過正己烷對MOSH進行洗脫,收集MOSH組分后,再以一定比例的正己烷和二氯甲烷混合溶劑解除固相萃取柱對MOAH的吸附,從而實現兩者的分離。目前該方法已經得到了廣泛的應用[4-5,12,17-21]。在LC-GC分析中,有研究采用含銀的液相色譜柱,實現了在線分離,有效提高了凈化效率[22]。
2 礦物油檢測方法
2.1 氣相色譜法(GC)
GC/FID是目前公認的礦物油檢測方法。根據FID檢測原理,FID幾乎對所有烴類化合物有一致的響應,無明顯的歧視效應。礦物油的烴類化合物在色譜圖上表現為一定沸程的連續“駝峰”。礦物油來源和提煉手段的不同,導致其種類繁多,由于缺乏標準對照物進行一一定量,只能采用與礦物油性質相似的特定物質作為參照,依據保留時間對連續的“駝峰”進行分段和半定量(如采用雙環己烷對MOSH進行定量)。目標峰的積分面積為水平基線及“駝峰”上端輪廓之間的面積(如圖2的陰影部分),輪廓以上的尖峰不屬于礦物油成分。
采用硝酸銀硅膠柱分離MOSH和MOAH,GC/FID進行定量的方法在食品及食品接觸材料的礦物油分析中得到了廣泛應用[4-5,11-12,17-21,23]。李克亞等[18]建立起了紙制品包裝材料中礦物油的SPE/GC方法,并將其應用到6類食品包裝材料的檢測中,SN/T 4895-2017[24]方法即是在該方法的基礎上進行優化和改善而建立的。
GC/FID結合大體積進樣技術,能有效提高檢測靈敏度和降低檢出限,相比于LC-GC聯用技術,該方法可操作性強,成本低,實用性更強[21,25]。
2.2 氣相色譜-質譜法(GC-MS)
質譜技術通過測量離子質荷比對目標物質進行定量。質量相同,結構不同的烴類物質,在色譜圖上的響應不同,使得GC-MS在礦物油的檢測中往往只能作為MOSH和MOAH定性的輔助方法,目前應用GC-MS 法對礦物油進行定量的報道較為少見,僅有Lionel等[9]采用GC-MS方法對巧克力和谷物類食品中的礦物油進行了同時鑒定和定量,并將測定結果與LC-GC/FID進行了對比,證明了該方法具有一定的可行性。
2.3 液相-氣相色譜聯用法(LC-GC)
LC-GC采用液相色譜柱,成功實現了對MOSH和MOAH的在線分離,在近幾十年來,該方法得到廣泛使用和完善[7,16,26-33]。液相色譜柱一般采用硅膠正相柱,如 LiChrospher Si60 和 Supercosil LC-Si,分離原理與SPE小柱相同。另外,溶劑蒸發濃縮技術及Y接口技術[34]的開發和運用,實現了不同檢測器的連接組合,LC-GC儀并聯兩根氣相色譜柱及雙檢測器,可實現多種組合,如LC-GC/FID/FID、LC-GC/FID/MS或LC-GC/FID/FID/MS等,使得從液相色譜柱流出的MOSH 和 MOAH組分分別流入兩根氣相色譜柱中,進行同步的定性定量分析,滿足了不同實驗室的檢測需求,并大大提高了分析效率。
LC-GC 聯用儀具有明顯的優勢。首先,其靈敏度高:經液相色譜柱的分離凈化后,MOSH和MOAH 依次流出,通過LC-GC的接口技術將全部礦物油餾分送入GC后,進入大體積進樣系統,揮發除去大部分的溶劑即可使MOSH和MOAH得到在線的濃縮,提高檢測靈敏度,降低檢出限。其次,LC-GC實現了在線的全樣品分析,自動化程度高,節省了人工操作和成本,降低了樣品損失和引入外來污染的風險,提高了方法的可靠性。再者,LC-GC可有效減少樣品和溶劑的用量,具有環境友好的優點。然而LC-GC成本高,儀器維護及運行成本較高,對操作人員的技術要求較高,目前國內僅有極少數的檢測機構擁有該技術。
2.4 其他技術
2.4.1 二維氣相色譜法(GC×GC)在GC×GC檢測中,試樣進入第一根色譜柱后,化合物根據沸點不同進行分離,因沸點相近而未充分分離的化合物在第二根色譜柱中根據極性大小進行縱向的分離,檢測器采集到的信號形成三維立體圖或二維輪廓圖。根據化合物所屬類型,GC×GC譜圖被分割成不同的區帶,每一區帶代表特定的族,同族化合物在其區帶內按照沸點不同進行分離,如烷烴、環烷烴、單環芳烴和多環芳烴等,這為食品中礦物油來源的分析提供了方法。近年來,該技術被用于植物油[35]、回收紙[36]、食品和化妝品[4,32,37]和人體器官中礦物油的污染來源分析[2,38],為礦物油的溯源和管控提供了有力的依據。
2.4.2 核磁共振技術烴類樹脂和裂解汽油中的礦物油由于結構中含有苯環,使用核磁共振分析時具有更好的選擇性。目前已有研究使用核磁共振方法實現了不同類型礦物油的定量分析[39]及食品中熱熔膠遷移量的研究[40]。而二維氣相色譜結合核磁共振技術,也為礦物油的來源分析開辟了新的路徑[40]。
3 食品及食品接觸材料中礦物油的研究
3.1 食品中礦物油的檢測
目前,礦物油的檢測技術已經廣泛地用于食品中。歐洲食品安全局(European Food Safety Authority,EFSA)在2012年發布的評估報告[41]中指出,MOSH幾乎存在于所有食品中,在收集的1 000多份食品的檢測數據中,不同類別食品中MOSH的平均含量依次為:面包>谷物>非巧克力類糕點>植物油>魚類罐頭>油籽>動物油脂,原因可能是,面包和谷物在加工過程中使用了含有高濃度烴類礦物油的脫模劑和拋光劑。
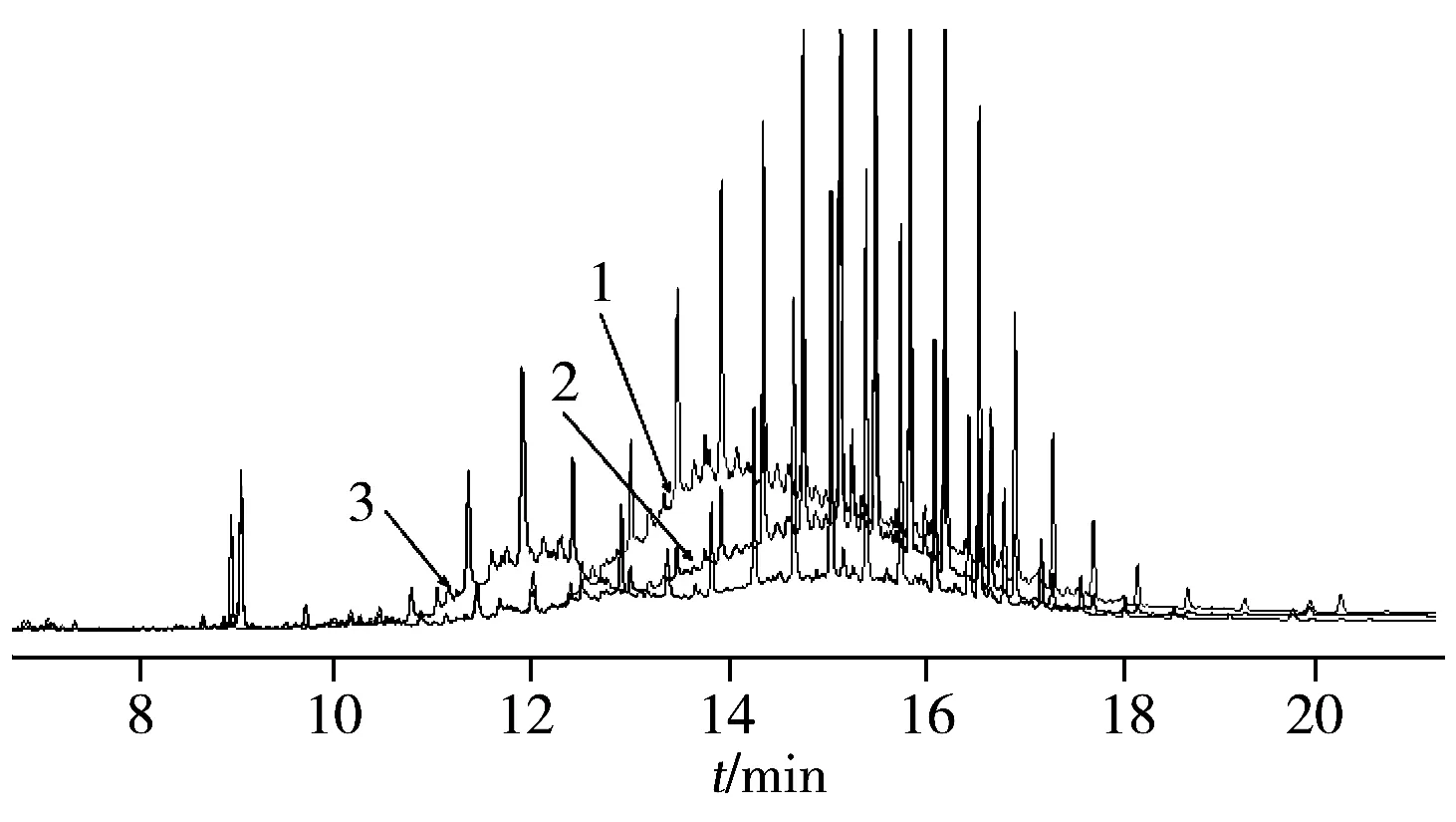
Van Heyst等[42]對比利時市場上的198種食品進行調查,其中142種食品中檢出MOSH,糖果的最大檢出值為85 mg/kg;23種食品中檢出MOAH,含量為0.6~2.24 mg/kg,其中咖啡、可可、茶等干性食品中的MOAH含量最高。 Canavar等[43]對20種干性食品和食品包裝紙中的礦物油進行計算和分析,發現回收紙中的礦物油是食品中MOAH的主要貢獻來源,29%的食品中MOAH的含量大于1 mg/kg;MOSH( 3.2.1 含量的研究食品接觸材料是食品礦物油污染的一個非常重要的來源,包括:食品包裝油墨中的連接料和脫模劑、食品包裝用的紙和紙板、大宗商品包裝用的黃麻袋、食品包裝生產上用的潤滑劑、加工助劑等。從食品生產到消費的各個環節,礦物油可以通過包裝材料與食品直接接觸而發生遷移,也可以通過氣相傳質方式(揮發、擴散)進入到干性食品中。研究表明,含有回收紙纖維的紙和紙板是食品中礦物油污染的重要來源[44-45,47,49],回收紙制品所用的紙纖維往往為舊報紙和刊物等用紙,盡管使用前已經過化學消解,但仍無法完全去除回收紙制品中的油墨、粘合劑等含烴類礦物油的物質或材料。Biedermann和Vollmer等[44-45]發現采用回收紙制成的食品包裝中礦物油含量最高可達3 800 mg/kg,遠超由糧農組織/世界衛生組織食品添加劑聯合專家委員會(Joint FAO/WHO Expert Committee on Food Additives,JECFA)給出的臨時每日允許攝入量(Acceptable daily intake,ADI)值所推導的0.6 mg/kg安全限值,而回收紙直接接觸的食品中礦物油的含量明顯高于該類食品本身礦物油的含量,說明回收紙的使用存在加大礦物油遷移污染的可能性。 3.2.2 遷移行為的研究烴類礦物油向食品發生的遷移受組分特性、環境和材料阻隔性等多種因素的影響。研究表明[45-47],在缺乏功能阻隔層的情況下,礦物油可從食品接觸材料向干性食品中遷移,經過漫長貨架期之后,外層包裝材料中的礦物油也能夠透過內層包裝袋進入內容物中,因此在對食品進行檢測時,應取貨架期最后階段樣品的測試結果進行合規判定。 采用干性模擬物對包裝材料中礦物油的遷移行為進行研究[28]時發現,隨著溫度的升高,聚丙烯層阻隔效果逐漸下降。Lorenzini等[46]研究了紙包裝中礦物油遷移至干性食品的規律,結果發現,長期貯存下,60%~80%的低沸點礦物油( 目前,行業對礦物油的定義存在分歧,如法典委將礦物油按粘度大小來劃分,認為安全風險集中在中低黏度的礦物油中,主要關注的碳鏈范圍為C10~C50,認為該范圍的礦物油會對人體健康造成危害[1,48]。而EFSA將其劃分為MOSH和MOAH,關注的是C16~C35。我國GB 2760-2014中則規定白油可以用作油脂加工工藝的助劑,包括消泡劑、潤滑劑和脫模劑等。對于該類物質是否應歸屬于礦物油的管控范圍,在檢測過程中是否需進行區分,目前仍存在爭議。因此行業呼吁權威機構進一步明晰礦物油的定義,以便更好地區分污染來源與天然來源的烴類物質,進行必要的管控。 現階段,針對烴類礦物油毒理學評估的數據較為缺乏,來自動物實驗的毒理學數據能否外推至人體也存在較大爭議。此外,已有研究多集中于MOSH,對于MOAH的毒理評估報道較少。EFSA使用暴露邊界閾值評價方法對不同人群的膳食暴露量進行評估,考慮到部分MOAH具有致癌性,認為人群暴露于礦物油的健康風險值得關注。 鑒于以上情況,筆者認為,開發能夠定性定量分析不同組分烴類礦物油的技術,并對混合以及特定組分礦物油的毒理學研究和暴露進行評估[41],完善對礦物油的科學評估和立法尤為重要。 圖4 不同紙制品中礦物油的色譜圖Fig.4 Chromatograms of mineral oil for different food packaging paper1.printed corrugated paper(印刷瓦楞紙);2.brown wrapping paper(牛皮外包裝紙);3.gray wrapping paper(灰色外包裝紙) 盡管礦物油的檢測技術多種多樣,但其檢測仍存在較大的局限性和挑戰。首先,由于礦物油本身成分復雜,干擾物質多,除來自于食品或包裝材料的基質干擾之外,不同來源的礦物油會在色譜圖上呈現不同的形態,峰形各異[7,49-50]。如圖4,不同紙制品中礦物油成分不同,需要對樣品進行逐一分析。而對礦物油進行準確的定量和污染源的分析,需要掌握不同生產工藝下礦物油副產物的碳鏈范圍、性質特征等情況,并針對全供應鏈上可能存在的風險點進行排查和分析,這對研究機構提出了極高的要求。 其次,盡管使用了凈化手段,但礦物油中仍然存在很多無法去除的干擾物,如食品植物油中的不可皂化物(高級脂肪醇、甾醇、蠟酯、色素、維生素等),來自于包裝材料的添加劑和原料(如油墨使用的松香、色料、濕潤劑、干燥劑、穩定劑等),均屬于烴類有機化合物,無法與目標成分進行有效分離,也無法通過質譜識別一一剔除。另外,采用手動積分的方法進行定量時,無法避免由主觀因素所帶來的誤差和結果差異。 最后,目前除SN/T 3495-2017針對紙制品的遷移量建立了檢測標準外,國內對于不同基質中礦物油的檢測方法尚缺乏統一的操作標準,如定量內標物質的選擇、加入量、碳鏈的分段等。目前大部分檢測機構的檢測方法是依據德國聯邦風險評估研究所(Bundesinstitut fur Risikobewertung,BfR)推薦的方法及已報道的測試方法[11,17]而建立,因此對于樣品的測試結果,實驗室間存在較大的差異和爭議。 食品和食品接觸材料是消費者烴類礦物油暴露的重要來源,烴類礦物油能夠通過直接接觸或間接傳質方式污染食品,其引發的食品安全問題亟需關注。烴類礦物油成分復雜,分析難度較大,對現有檢測技術仍然存在較大的挑戰。針對烴類礦物油分析的分離和凈化技術,色譜峰的積分定量技術,礦物油來源鑒定技術等還需進一步的優化和完善。為完善對烴類礦物油的科學風險評估和風險管理,需進一步改進和規范烴類礦物油的檢測技術。這將為我國食品和食品接觸材料中烴類礦物油的安全標準制定和行業風險管理工作提供科學依據。3.2 食品接觸材料中礦物油的檢測
4 存在的問題及挑戰
4.1 礦物油的定義與毒理評估
4.2 礦物油的分析方法
5 總結與展望

