大鯢低聚糖肽對葡萄酒發酵香氣成分影響的研究
何鳳梅,余睿智,吳全球,胡斯杰,佟長青,李 偉
(1.大連海洋大學食品科學與工程學院,遼寧大連 116023;2.寧夏塞上圖葡萄酒有限公司,寧夏銀川 750000)
在葡萄酒釀造過程中,釀酒酵母進行一系列復雜的代謝和生物轉化過程,產生了醇類、酯類、酸類等許多重要的香氣化合物[1]。目前,葡萄酒中已鑒定出800多種呈香物質,按結構可分為醇類、酯類、酚類、有機酸、羥基化合物(酮和醛)、萜烯類化合物和含硫化合物六大類,不同的香味物質對葡萄酒香氣品質的影響是不同的[2-3]。釀酒酵母的種類、釀造工藝、萃取劑的種類、添加酵母助劑、殼聚糖及可同化氮素,對葡萄酒香氣化合物合成均有影響[4-10]。溶劑萃取法、蒸餾萃取法、超臨界CO2流體萃取法、攪拌棒吸附法、固相萃取法頂空固相微萃取是提取分離香氣成分的主要方法,氣相色譜法(Gas chromatography,GC)、氣相色譜-質譜聯用技術(Gas chromatography-mass spectrometer,GC-MS)、氣相 -嗅聞測定聯用技術(Gas chromatography-olfactometry,GC-O) 已廣泛應用于葡萄酒香氣成分檢測[11-14]。形成具有獨特風格的葡萄酒,是葡萄酒釀造產業的理想和追求。另一方面的研究表明,肽類活性物質在釀酒酵母香氣合成過程中發揮著復雜的作用,并非只是作為簡單的氮源[15-16]。
大鯢低聚糖肽是利用海洋微生物酸性蛋白酶從大鯢體表黏液中制備出來的低分子量糖肽[17]。大鯢低聚糖肽具有多種多樣的生物活性,如促進小鼠免疫功能的提高[18]、清除自由基活性[17]、抑制血管緊張素轉換酶活性[19]、抗疲勞作用[20]、對CCl4導致小鼠肝損傷具有保護作用[21]等。但迄今為止,還鮮有將大鯢低聚糖肽應用于葡萄酒釀造過程中的報道。通過分析大鯢低聚糖肽對葡萄酒香氣成分的影響,以期獲得一種具有獨特風格的葡萄酒。
1 材料與方法
1.1 材料與試劑
大鯢低聚糖肽按照曲敏[17]的方法制備。在55℃條件下,利用Aspergillus sp.酸性蛋白酶酶解大鯢黏液3 h,即可獲得其時間飛行質譜(m/z)小于3 600的大鯢低聚糖肽。大鯢低聚糖肽具有O-連接糖肽鍵結構,其總蛋白含量為80.01%,總糖含量為15.15%[17]。
赤霞珠葡萄,采自銀川賀蘭山葡萄園;葡萄酒活性干酵母(Saccharomyces cerevisiaea) RV002,安琪酵母股份有限公司提供;葡萄糖、硫代硫酸鈉、重鉻酸鉀、碘化鉀(分析純),天津市大茂化學試劑廠提供;淀粉(食品級),購于黑石礁大商鮮生超市。
1.2 儀器與設備
ZDP-A2160A型曲線控制恒溫培養箱,上海智城分析儀器制造有限公司產品;LDZX-30KBS型立式壓力蒸氣滅菌器,上海申安醫療器械廠產品;LYT-330型手持折光儀,上海淋譽貿易有限公司產品;722E型可見光分光光度計,上海光譜儀器有限公司產品;PHS-3C型精密pH計,上海儀電科學儀器股份有限公司產品;7890B型氣相色譜儀(GC∶7890B)、5977B型四極桿飛行時間氣質聯用儀(GC/Q-TOF:5977),美國安捷倫公司產品。
1.3 試驗方法
1.3.1 釀酒酵母活化
將1 g葡萄酒活性干酵母RV002加入到100 mL質量分數為2%葡萄糖的無菌水中,在35℃條件下活化30 min,得到酵母懸液。
1.3.2 葡萄酒制作過程
將擠碎的赤霞珠葡萄1 000 g放入6個大錐形瓶中,原料的總糖度為22 Brix。分別放入5 mL活化酵母懸液、0.05 g偏重亞硫酸鉀與1 g果膠酶,然后分別加入0,0.5,1.0,1.5,2.0,2.5 g大鯢低聚糖肽,向其中充入氮氣,蓋上塞子放于搖床30℃,轉速140 r/min發酵10 d;去除發酵液表面的殘渣,在10℃繼續發酵5 d;將發酵液在5℃陳釀2個月,進行過濾除菌,即得大鯢低聚糖肽葡萄酒。
1.3.3 大鯢低聚糖肽葡萄酒指標測定
(1) pH值測定。使用精密pH計對大鯢低聚糖肽葡萄酒的pH值進行測定。
(2)糖度測定。使用手持型糖度計對發酵液的糖度進行測定。
(3)乙醇產量測定。乙醇的產量通過化學氧化法測定[22]。
1.3.4 葡萄酒香氣成分的測定
采用固相微萃取-氣相色譜-質譜聯用法(SPME-GC-MS)對大鯢低聚糖肽葡萄酒和不加入大鯢低聚糖肽獲得的葡萄酒香氣成分分別進行測定。
(1)SPME樣品處理。取4 mL樣品,置于20 mL的固相微萃取樣品瓶中,于80℃下平衡20 min,萃取吸附5 min,吸附后的萃取頭于GC進樣口熱解析15 min后自動進樣,用于GC-MS分析。
(2) 氣相色譜(GC) 分析條件。TG-5SILMS型色譜柱(60 m×250 mm×0.25 μm),分流進樣,分流比20∶1,進樣口溫度270℃,傳輸線溫度280℃,載氣為氦氣(He),流速2.0 mL/min;升溫程序為初溫40℃,保持5 min,再以15℃/min升到280℃,保持5 min,再以25℃/min升溫到305℃,保持5 min,共用時32 min。
(3)質譜(MS)條件。電子轟擊離子源(EI),電子能量70 eV,四極桿溫度150℃,離子源溫度230℃,溶劑延遲0.5 min,SCAN掃描范圍29~550 amu。
(4) 定性定量方法。對采集到的質譜圖利用NRST譜庫檢索,并用歸一化法對氣相色譜峰面積進行定量,從而計算出各香氣成分在2個酒樣中的相對含量。
2 結果與分析
2.1 大鯢低聚糖肽葡萄酒指標測定
將大鯢低聚糖肽加入到赤霞珠葡萄中,與釀酒酵母共同發酵、陳釀,對獲得的大鯢低聚糖肽葡萄酒進行各項指標測定。
大鯢低聚糖肽用量對酵母增殖的影響見圖1。

圖1 大鯢低聚糖肽用量對酵母增殖的影響
從圖1中可以看出,隨著大鯢低聚糖肽用量的增加,發酵液中酵母增殖的量增加,在加入2.5 g大鯢低聚糖肽時,OD600nm達到0.77。與對照組相比,在用量為2.0,2.5 g時,發酵液中酵母增殖顯著(p<0.05)。結果表明,高劑量添加大鯢低聚糖肽具有促進釀酒酵母增殖的作用。
大鯢低聚糖肽用量對葡萄酒pH值的影響見圖2。
從圖2中可以看出,添加不同量大鯢低聚糖肽的各組葡萄汁,發酵結束后,發酵液pH值在3.5左右,變化不大,因此大鯢低聚糖肽用量對發酵液pH值的影響不顯著 (p>0.05)。
大鯢低聚糖肽用量對葡萄酒糖度的影響見圖3。
從圖3中可以看出,添加不同用量大鯢低聚糖肽的各組葡萄汁在發酵結束后,葡萄酒糖度變化較大,且隨著大鯢低聚糖肽用量的增加,殘糖含量降低顯著(p<0.05),結果表明大鯢低聚糖肽具有促進釀酒酵母利用葡萄汁中糖的作用。
大鯢低聚糖肽用量對葡萄酒中乙醇含量的影響見圖4。

圖2 大鯢低聚糖肽用量對葡萄酒pH值的影響
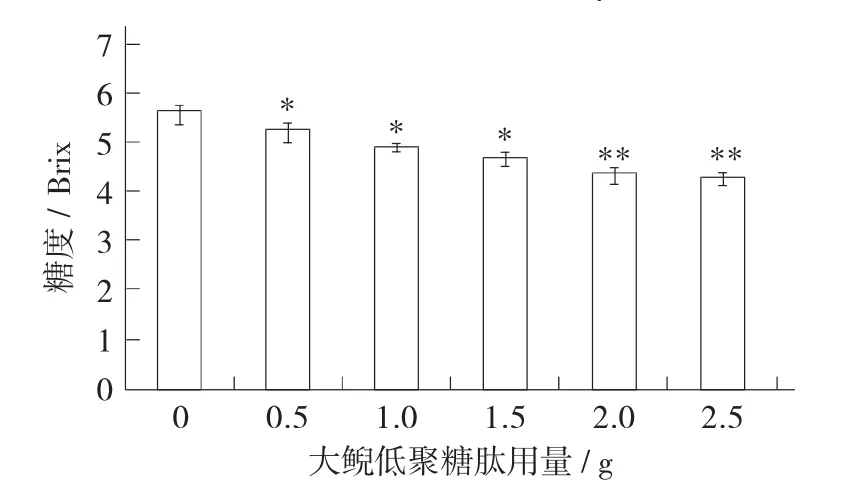
圖3 大鯢低聚糖肽用量對葡萄酒糖度的影響

圖4 大鯢低聚糖肽用量對葡萄酒中乙醇含量的影響
從圖4中可以看出,添加不同用量大鯢低聚糖肽的各組葡萄汁在發酵結束后,葡萄酒中乙醇含量具有增加趨勢,且大鯢低聚糖肽用量為2.0,2.5 g時,大鯢低聚糖肽葡萄酒中乙醇含量顯著高于對照組(p<0.05)。結果表明添加大鯢低聚糖肽后,釀酒酵母利用糖的效率增加,產生了更多的乙醇。
2.2 大鯢低聚糖肽葡萄酒香氣測定
采用固相微萃取-氣相色譜-質譜聯用法對大鯢低聚糖肽葡萄酒(添加2.5 g大鯢低聚糖肽的樣品)及不加入大鯢低聚糖肽獲得的葡萄酒的香氣成分分別進行了測定。
葡萄酒香氣成分總離子流圖見圖5。
利用該方法從大鯢低聚糖肽葡萄酒中共檢測到30種香氣成分,包括7種醇類物質、9種酯類物質和2種同類物質。與不添加大鯢低聚糖肽的葡萄酒相比較,大鯢低聚糖肽葡萄酒中產生了較高含量的乙醇、異丁醇、異戊醇、2-甲基丁醇、苯乙醇和3,4-二甲基苯甲醇。葡萄酒中高級醇的數量影響葡萄酒的感官品質,低于300 mg/L的高級醇對葡萄酒的品質具有積極作用[23]。其中,大鯢低聚糖肽葡萄酒中苯乙醇的含量是不加大鯢低聚糖肽獲得的葡萄酒中含量的2.68倍。天然形成的苯乙醇非常珍貴,能給葡萄酒帶來淡雅細膩的玫瑰香味[24],大鯢低聚糖肽增強了釀酒酵母合成苯乙醇的能力。
大鯢低聚糖肽葡萄酒香氣成分分析見表1。
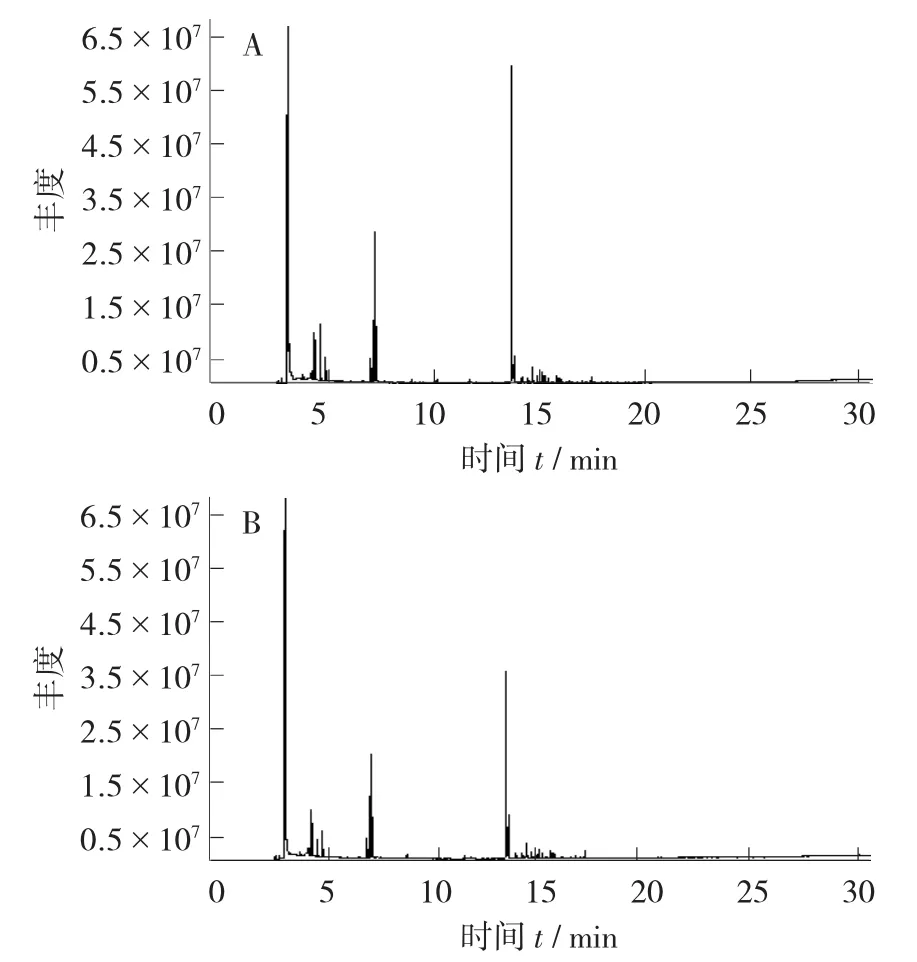
圖5 葡萄酒香氣成分總離子流圖
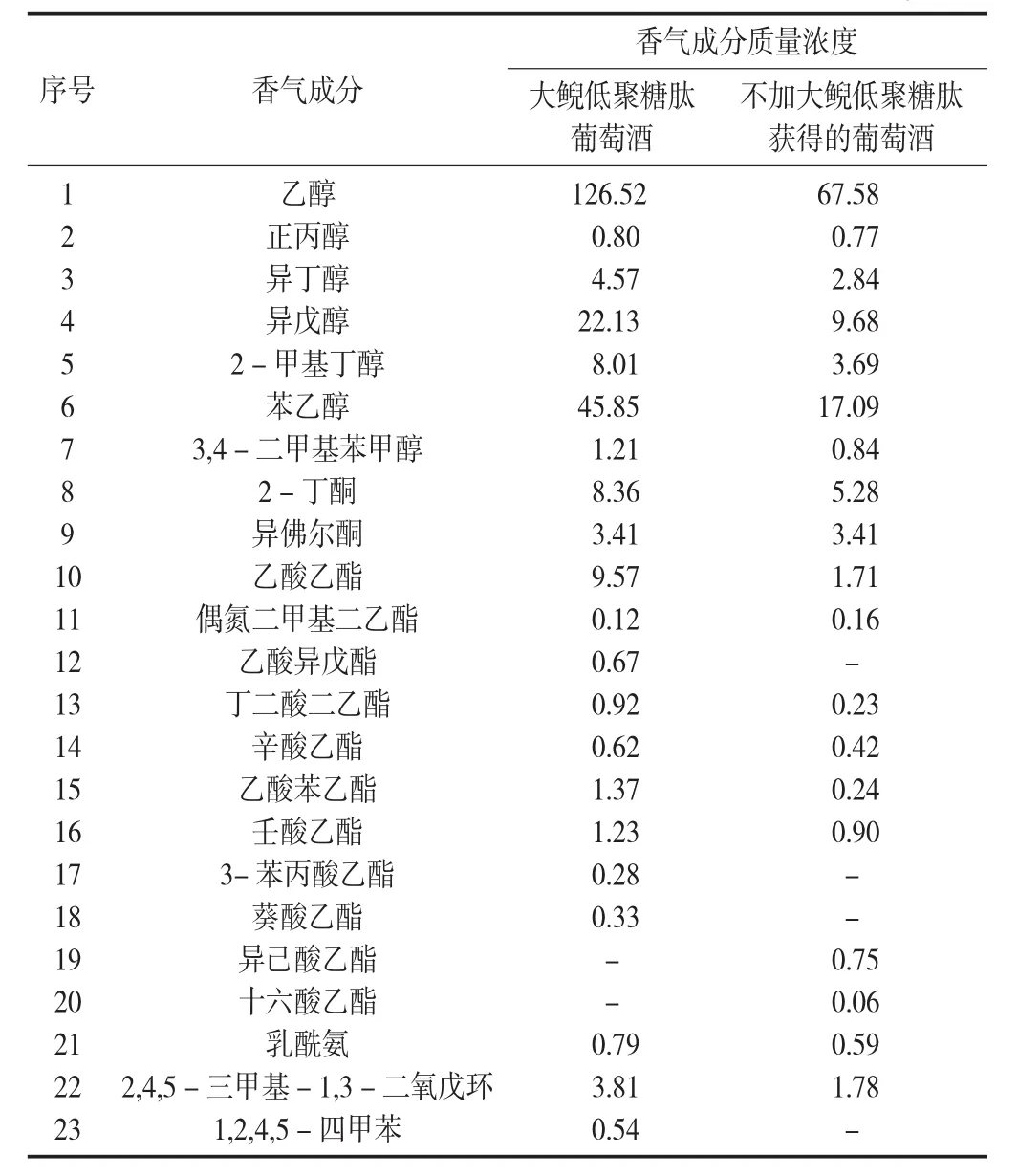
表1 大鯢低聚糖肽葡萄酒香氣成分分析/mg·L-1
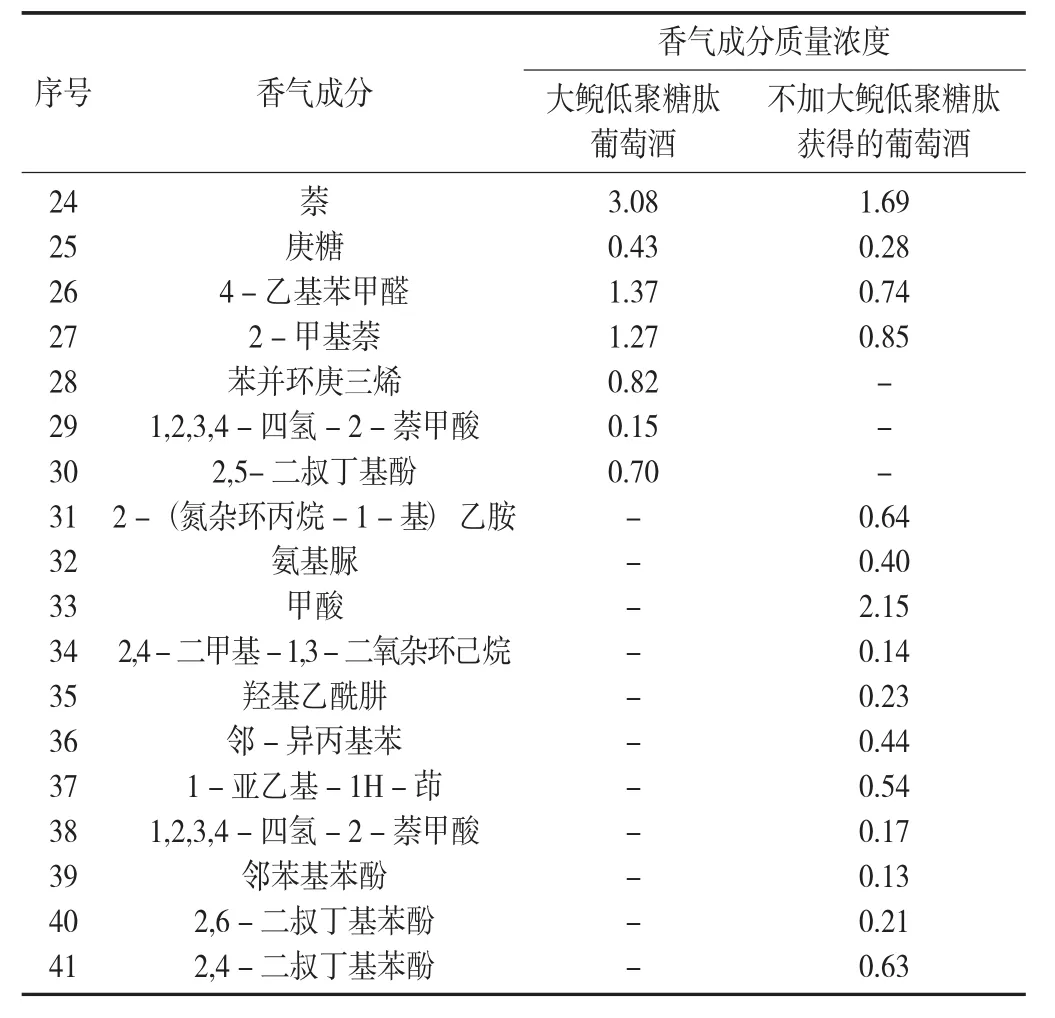
續表1
大鯢低聚糖肽葡萄酒中酯類香氣成分濃度高于不加大鯢低聚糖肽獲得的葡萄酒中酯類香氣成分的濃度,其中乙酸乙酯及丁二酸二乙酯濃度均高于對照的樣品,乙酸乙酯具有柔和的果香和奶油味。丁二酸是合成丁二酸二乙酯的原料,是葡萄酒中的主要酸類之一,可以產生令人愉快的復雜酸味。因此,大鯢低聚糖肽增強了釀酒酵母合成乙酸乙酯及丁二酸二乙酯的能力。
目前,國內在葡萄酒生產過程中廣泛使用活性干酵母進行發酵,造成了葡萄酒的同質化現象。改變葡萄酒的同質化現象,需要加強利用野生的葡萄酒酵母。另一方面,通過添加肽類活性物質影響活性干酵母的代謝過程,使其產生更多的具有積極作用的香氣成分,是提高葡萄酒品質的一個有效手段。
3 結論
大鯢低聚糖肽與赤霞珠葡萄共同發酵、陳釀,獲得大鯢低聚糖肽葡萄酒。結果表明,隨著大鯢低聚糖肽添加量的增加,發酵液中釀酒酵母增殖的量增加,耗糖量增多,乙醇量增加。這表明添加大鯢低聚糖肽的發酵液中,釀酒酵母利用糖的效率大大增加。大鯢低聚糖肽葡萄酒中共檢測到30種香氣成分,包括7種醇類物質、9種酯類物質和2種同類物質。與不添加大鯢低聚糖肽的葡萄酒相比較,大鯢低聚糖肽葡萄酒具有較高含量的乙醇、異丁醇、異戊醇、2-甲基丁醇、苯乙醇和3,4-二甲基苯甲醇,乙酸乙酯及丁二酸二乙酯。因此,大鯢低聚糖肽是一類潛在的可以影響釀酒酵母香氣化合物合成的活性物質。

