超聲內鏡聯(lián)合CT檢查對直腸癌術前分期的臨床價值
宋豐前 熊甲英 葉春華 曾異鋒 付曉霏 高帆

【摘要】 目的 分析超聲內鏡(EUS)聯(lián)合計算機斷層掃描(CT)檢查在腫瘤患者術前浸潤深度(T)、淋巴結轉移情況(N)及遠處轉移(M)分期的臨床診斷價值。
方法 搜集2015年11月~2018年1月符合入組條件的患者共99例,均在手術前2周內完善經直腸超聲內鏡及CT檢查。以術后病理分期為金標準,分別對比EUS和/或CT檢查對腫瘤TNM分期的準確率。
結果 EUS的T分期準確率為83.3%~90.0%,N分期為25.0%~84.2%,而EUS聯(lián)合CT檢查的N分期則有88.2%~88.9%。
結論 EUS及CT檢查對腫瘤的TNM分期均有較好的分辨,而EUS聯(lián)合CT檢查能大大提高術前腫瘤TNM分期的準確率,從而為直腸癌患者的治療方案選擇提供更多依據(jù),以達到最好的治療效果。
【關鍵詞】 直腸癌;超聲內鏡;腫瘤TNM分期;CT
中圖分類號:R735.3+7 文獻標志碼:A DOI:10.3969/j.issn.1003-1383.2019.11.005
To evaluate the value of endoscopic ultrasonography with CT in preoperative staging of rectal cancer
SONG Fengqian,XIONG Jiaying,YE Chunhua,ZENG Yifeng,F(xiàn)U Xiaofei,GAO Fan
(Department of Gastroenterology,Loudi Central Hospital,Loudi,Hunan 417000,China)
【Abstract】 Objective To analyze the clinical value of endoscopic ultrasonography(EUS) combined with computed tomography(CT) in the accuracy of tumor invasion depth(T),lymph node metastasis(N) and distant metastasis(M) in preoperative stages of tumor patients and improve the prognosis of rectal cancer.
Methods Transrectal endoscopic ultrasonography and CT examination were performed 2 weeks before surgery on 99 patients eligible for enrollment in Loudi central hospital from November 2015 to January 2018.Postoperative pathological staging was used as the criteria to compare the accuracy of EUS and/or CT in tumor TNM staging.
Results The T staging accuracy of EUS was 83.3%~90.0%,N staging was 25.0%~84.2%,while the N staging of EUS combined with CT was 88.2%~88.9%.
Conclusion Both EUS and CT can distinguish the TNM stage of the tumor,while EUS combined with CT can greatly improve the accuracy of TNM stage of the tumor before surgery,provide more evidence for the choice of treatment for colorectal cancer patients and achieve the best therapeutic effect.
【Key words】 rectal cancer;endoscopic ultrasonography;tumor TNM stage;computed tomography(CT)
直腸癌是全世界范圍內最常見的消化道惡性腫瘤之一。據(jù)統(tǒng)計,2012年全球估計結直腸癌新發(fā)病136萬,而其中近70萬人死于結直腸癌,結直腸癌已成為世界男性第三位高發(fā)惡性腫瘤,而在女性則為第二位[1]。隨著我國居民生活水平提高,飲食結構發(fā)生變化,其發(fā)病率呈逐年上升的趨勢,成為危害生命健康的主要疾病之一。目前手術根治性切除仍是最有效的治療方法[2]。直腸癌預后主要相關因素有:腫瘤的位置及浸潤深度、淋巴結轉移數(shù)目及腸壁周圍組織器官是否受累,預后往往依賴于疾病的早期診斷、干預和合適的治療方式。而基于黏膜浸潤深度的腫瘤術前分期對于確定是否需要在術前進行新輔助化療意義重大[3~4]。這就需要找到一種能精確進行腫瘤術前分期的方法,區(qū)分腫瘤風險高低,以確保患者能夠從新輔助化療當中受益[5~6]。在直腸癌中,CT檢查可以在腫瘤大小、浸潤深度及遠處轉移中提供有效信息[6~7],這些都能夠為準確有效的術前分期提供有力證據(jù),而經直腸超聲內鏡(EUS)作為一種可以較為準確地定位腫瘤浸潤深度的檢查方法被廣泛應用[8]。
1 資料與方法
1.1 一般資料
研究2015年11月至2018年1月在我院行腸鏡檢查診斷為直腸癌,且在本院行外科手術并符合入組條件的直腸癌初治患者共99例。男54例,女45例,平均年齡62.6歲(27~78歲)。入選標準:確診直腸癌且計劃選擇行手術治療,年齡≥18歲并簽署知情同意書。排除標準:入選前行術前放化療,擬行內鏡下切除術,懷孕,未能提供知情同意書,嚴重的凝血障礙和/或傳染性疾病。所有醫(yī)療記錄均反復確認以確保實驗的真實準確。所有入選患者均有明確的病理診斷作為確診依據(jù),均在術前完善EUS及CT檢查,并在2周內安排手術。因腸管狹窄、患者拒絕而無法行EUS檢查者及重度腎功能不全、對碘劑過敏無法行增強CT者均除外。
1.2 正常腸壁超聲內鏡分層
正常腸壁的EUS圖像分為5層,腸腔由內向外依次為,第1層:高回聲帶——界面波及黏膜層;第2層:低回聲帶——黏膜肌層;第3層:高回聲帶——黏膜下層;第4層:低回聲帶——固有肌層;第5層:高回聲帶——漿膜下層及漿膜層(腹膜折返以下直腸相當于外膜層)。
1.3 腹部螺旋CT及EUS檢查
使用德國西門子256層高檔雙源CT(型號 Flash)進行檢查,檢查前患者禁食6~8小時,檢查前30 min囑飲水500~800 mL,未服用瀉藥,掃描層厚3~4 mm,層距3~4 mm,先行全腹平掃定位全腹后再予碘克沙醇(規(guī)格62.5 g/100 mL)靜脈注射,以獲取動脈增強期及靜脈期影像。使用奧林巴斯CV260超聲內鏡EU-ME2(型號 UE260-AL5;UM-3R)行超聲內鏡檢查,術前禁食禁水6~8小時。
1.4 直腸癌分期
根據(jù)NCCN最新版指南(第八版)[9]在患者完善CT及EUS檢查后,依據(jù)分期標準進行臨床TNM分期,分期方法如下。
原發(fā)腫瘤(T):Tx原發(fā)腫瘤無法評價;T0無原發(fā)腫瘤證據(jù);Tis原位癌:局限于上皮內或侵犯黏膜固有層;T1腫瘤侵犯黏膜下層;T2腫瘤侵犯固有肌層;T3腫瘤穿透固有肌層到達漿膜下層,或侵犯無腹膜覆蓋的結直腸旁組織;T4a腫瘤穿透腹膜臟層;T4b腫瘤直接侵犯或粘連于其他器官或結構。
區(qū)域淋巴結(N):Nx區(qū)域淋巴結無法評價;N0無區(qū)域淋巴結轉移;N1有1~3枚區(qū)域淋巴結轉移;N1a有1枚區(qū)域淋巴結轉移;N1b有2~3枚區(qū)域淋巴結轉移;N1c漿膜下、腸系膜、無腹膜覆蓋結腸/直腸周圍組織內有腫瘤種植(tumor deposit,TD),無區(qū)域淋巴結轉移;N2有4枚以上區(qū)域淋巴結轉移;N2a有4~6枚區(qū)域淋巴結轉移;N2b有7枚及更多區(qū)域淋巴結轉移。
遠處轉移(M):M0無遠處轉移;M1有遠處轉移;M1a遠處轉移局限于單個器官(如肝、肺、卵巢、非區(qū)域淋巴結),但沒有腹膜轉移;M1b遠處轉移分布于一個以上的器官;M1c腹膜轉移有或沒有其他器官轉移。
1.5 觀察指標及其計算方法
準確率=真陽性人數(shù)/(真陽性人數(shù)+真陰性人數(shù))×100%;靈敏度=真陽性人數(shù)/(真陽性人數(shù)+假陰性人數(shù))×100%;特異度=真陰性人數(shù)/(真陰性人數(shù)+假陽性人數(shù))×100%。
1.6 統(tǒng)計學方法
使用SPSS 12.0統(tǒng)計學方法,用卡方檢驗對各組數(shù)據(jù)之間的差異進行統(tǒng)計學檢驗,檢驗標準:α=0.05,雙側檢驗。
2 結果
2.1 直腸癌的T分期
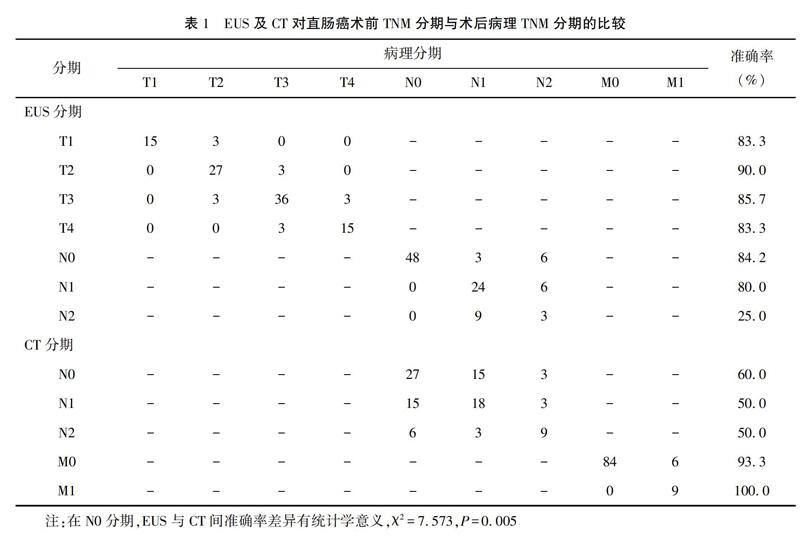
與手術病理結果比較,EUS的T分期中,T1、T2、T3、T4的準確率為83.3%(15/18)、90.0%(27/30)、85.7%(36/42)、83.3%(15/18),各參數(shù)間比較無統(tǒng)計學意義(P>0.05)。見表1。因費用等問題未行CT薄層掃描(每0.1 cm掃描),僅根據(jù)增強CT(每0.5 cm掃描)難以進行腫瘤T分期。
2.2 直腸癌的N分期
與手術病理結果比較,EUS的N分期準確率為84.2%(48/57)、80.0%(24/30)、25.0%(3/12),CT的N分期準確率為60.0%(27/45)、50.0%(18/36)、50.0%(9/18),在N0分期中,EUS與CT的準確率差異有統(tǒng)計學意義(χ2=7.573,P=0.005)。見表1。
2.3 直腸癌的M分期
與手術病理結果比較,CT的M分期準確率為93.3%(84/90)、100.0%(9/9),相對敏感及準確程度高。見表1。
2.4 EUS聯(lián)合CT檢查對直腸癌TNM分期的準確率評估
兩者相結合后,在N2分期中,聯(lián)合分期的準確率88.2%(15/17)及靈敏度100.0%(15/15)較EUS分期準確率25.0%(3/12)、靈敏度20.0%(3/15)明顯提高,差異有統(tǒng)計學意義(P<0.01)。見表2。
3 討論
直腸癌術前臨床TNM分期是醫(yī)生為直腸癌患者選擇治療方式時最為關注的問題,也可能關系到直腸癌患者的預后。目前用于直腸癌診斷和分期的方法有很多,而CT和EUS在目前的臨床TNM分期中意義重大[2]。
CT的明顯優(yōu)勢是可顯示直腸腫瘤與周圍臟器關系及遠處轉移,能通過大范圍掃描結合增強掃描,觀察有無肝臟轉移、淋巴結轉移及腹腔種植等,能夠較好了解直腸癌術后是否復發(fā),同時,CT檢查用時相對較少,并且所形成的影像可以反復觀察得出結論。本病例研究中,CT檢查對于遠處轉移M分期的準確率達到了93.9%和100%,充分說明了CT在M分期中的重要性。同時,本組病例中,CT對直腸癌N分期的準確率只有50.0%~62.5%,說明CT檢查在N分期的局限性,也與文獻報道基本一致[10]。而原因主要是CT檢查不能分辨腸壁各層,同時由于其判斷鄰近臟器受侵是以該臟器與直腸之間的脂肪層缺失為依據(jù),但體瘦、炎癥、粘連等因素均可引起臟器間脂肪層缺失而導致假陽性,對脂肪的顯微浸潤不敏感導致假陰性,因此在直腸癌術前分期中有較大局限性。
EUS結合內鏡和超聲的雙重優(yōu)勢,通過內鏡對消化道管腔內表面進行直接觀察的同時又能在內鏡下行超聲實時掃描,獲得經腹超聲、CT、MRI等所不及的胃腸道層次結構的組織學特征及周圍鄰近臟器的超聲圖像,能準確、清晰地分辨腸壁各層結構和周圍組織器官[8]。隨著頻率增高超聲局部分辨率增高,穿透力減弱,低頻探頭的優(yōu)勢在于能顯示腸周組織及淋巴結轉移,EUS已經成為臨床醫(yī)師評估直腸癌術前分期的一個重要手段[4,11]。本組病例中,EUS在T分期中的準確率(自T1至T4)達到了83.3%、90.0%、85.7%、83.3%,在N分期中的準確率(自N0至N2)也有84.2%、80.0%、25.0%。EUS在T分期及N0、N1分期中有較高準確率,主要是因為EUS可以清楚地顯示腸壁各層次結構和表面小范圍的隆起性病變,分辨出病變位于腸壁的準確位置,對直腸癌的分期做出較準確判斷,為內鏡下微創(chuàng)治療或外科手術提供可靠參考[8,12]。同時,EUS因可以探查最小為3 mm的淋巴結,且可以清楚地評估淋巴結的直徑大小、形態(tài)、邊界清晰度、內部回聲的高低等多個影像學特征,從而做出更為精準地判斷。文獻報道EUS 判斷淋巴結轉移準確率在76%~93%[10]。但是單純的超聲內鏡進行術前分期同樣存在不足,尤其是在N2分期中,準確率僅25%,這是由于超聲小探頭頻率較高、穿透力弱,有時難以顯示病灶的外側邊界,特別是周邊較遠的淋巴結及周圍組織侵犯情況分辨不高。
綜上,CT聯(lián)合EUS檢查可以相互彌補不足。CT的不足在于對腸管層次顯示不清及難以發(fā)現(xiàn)小淋巴結轉移。而EUS則對病灶周邊顯示欠清且難以進行遠處轉移的評估。在本組病例中,聯(lián)合分期中N2分期的準確率及靈敏度較EUS分期明顯提高,說明CT結合超聲內鏡對直腸癌的TNM診斷具有重要價值。
參 考 文 獻
[1]Torre LA,Bray F,Siegel RL,et al.Global cancer statistics[J].CA Cancer J Clin,2012,65(2):87-108.
[2]陳曉靖,蘭凱,汪曉東,等.多層螺旋CT和經直腸超聲在直腸癌術前分期中價值[J].中國普外基礎與臨床雜志,2009,16(9):702-705.
[3]Foxtrot Collaborative Group.Feasibility of preoperative chemotherapy for locally advanced,operable colon cancer:the pilot phase of a randomised controlled trial[J].Lancet Oncol,2012,13(11):1152-1160.
[4]Malmstrom ML,Saftoiu A,Vilmann P,et al.Endoscopic ultrasound for staging of colonic cancer proximal to the rectum:a systematic review and meta-analysis[J].Endosc Ultrasound,2016,5(5):307-314.
[5]Hunter C,Blake H,Jeyadevan N,et al.Local staging and assessment of colon cancer with 1.5-T magnetic resonance imaging[J].Br J Radiol,2016,89(1064):20160257.
[6]Klessen C,Rogalla P,Taupitz M.Local staging of rectal cancer:the current role of MRI[J].Eur Radiol,2007,17(2):379-389.
[7]Rollven E,Holm T,Glimelius B,et al.Potentials of high resolution magnetic resonance imaging versus computed tomography for preoperative local staging of colon cancer[J].Acta Radiol,2013,54(7):722-730.
[8]Puli SR,Reddy JBK,Bechtold ML,et al.Accuracy of endoscopic ultrasound to diagnose nodal invasion by rectal cancers: a meta-analysis and systematic review[J].Ann Surg Oncol,2009,16(5):1255-1265.
[9]National Comprehensive Cancer Network.(NCCN) Clinical Practice Guidelines in Oncology[M].Colon Cancer,Version 8.2018.
[10]Jurgensen C,Dietrich CF.Role of endoscopic ultrasound(EUS)in the staging of rectal cancer[J].Z Gastroenterol,2008,46(6):580-589.
[11]Hunter C,Brown G.Pre-operative staging of rectal cancer: a review of imaging techniques[J].Expert Rev Gastroenterol Hepatol May,2016,10(9):1011-1025.
[12]Badea R,Gersak MM,Dudea SM,et al.Characterization and staging of rectal tumors: endoscopic ultrasound versus MRI/CT[J].Pictorial essay Med Ultrason,2015,17(2):241-247.
(收稿日期:2019-04-11 修回日期:2019-10-11)
(編輯:潘明志)
基金項目:湖南省婁底市科技局項目(婁財企指〔2015〕592號)
作者簡介:宋豐前,男,副主任醫(yī)師,醫(yī)學碩士,研究方向:消化內鏡。E-mail:736896408@qq.com
[本文引用格式]宋豐前,熊甲英,葉春華,等.超聲內鏡聯(lián)合CT檢查對直腸癌術前分期的臨床價值[J].右江醫(yī)學,2019,47(11):821-825.

