不同指征患者胚胎植入前非整倍體篩查的比較
王林玉,施文韜,黃夢楠,師娟子
(1.西北婦女兒童醫院轉化醫學中心,陜西 西安 710061;2.寧夏藥品檢驗研究院,寧夏 銀川 750004;3.億康基因,上海 201499;4.西北婦女兒童醫院輔助生殖中心,陜西 西安 710003)
染色體非整倍體是指染色體數目異常。染色體非整倍體是導致胎兒嚴重智力低下及先天畸形的主要原因之一,在活產新生兒中的發生率約為0.5%[1-2]。目前,尚無有效的治療方法,一旦患兒出生將給家庭和社會帶來沉重的精神和經濟負擔。植入前遺傳學篩查(preimplantation genetic screening,PGS),是在胚胎植入著床之前對早期胚胎進行染色體數目和結構異常的檢測,挑選正常的胚胎植入子宮,以期獲得正常的妊娠,提高患者的臨床妊娠率,降低流產率,預防出生缺陷。同時,由于多次退火環狀循環擴增技術—二代測序技術(MALBAC-NGS)的出現,推動染色體異常的診斷技術不斷向更精確、更快速的方向發展[3-5]。近年來,有文章報道了雙親染色體異常、反復種植失敗和復發性流產(RSA)患者與胚胎非整倍體發生率有關,對此類患者實施PGS均能達到滿意的治療效果,減少了流產率,減少了無效移植次數,提高了妊娠率[6]。基于此,本文就易位、羅氏易位、倒位、非整倍體、Y染色體微缺失、衍生染色體、不良孕產史等其他PGS指征與胚胎非整倍體的關系作初步研究,以期找到更多可以預測非整倍體的指標來輔助臨床工作,并提供正確的臨床咨詢,以使更多患者可以從PGS技術最大獲益。
1資料與方法
1.1研究對象與分組
2018年6月1日至2018年11月30日收集西北婦女兒童醫院生殖中心288例行PGS患者的胚胎,胚胎培養至囊胚期進行活檢,PGS檢測采用MALBAC-NGS方法,比較不同年齡段和不同PGS指征胚胎染色體異常率。PGS檢測在西北婦女兒童醫院轉化醫學中心完成,所有進入臨床PGS周期的患者均簽署知情同意書。最終有效檢出結果的胚胎數為275枚,以女性年齡為分組依據,分為≤27歲(79例)、28~30歲(82例)、31~33歲(62例)、34~36歲(31例)、≥37歲(21例)共5組。
1.2方法
1.2.1囊胚活檢
當囊胚達到活檢標準時,在內細胞團對側用非接觸式激光儀在透明帶上打孔。完畢后繼續將囊胚培養4~6h,使部分滋養層形成疝。活檢時,使內細胞團位于固定針一側,活檢針靠近形成疝的外滋養層細胞緩慢回吸,發射激光,直至活檢的外滋養層細胞(10個左右)全部脫離囊胚。活檢的細胞組織培養液洗滌后放入裝有5μL細胞裂解液的PCR管內,離心后在-40℃凍存待檢。活檢后囊胚冷凍保存。
1.2.2 PGS檢測
采用MALBAC方法將待測樣本進行單細胞全基因組擴增,向待測樣本和對照品的PCR管中分別加入裂解酶,放入設定好參數的PCR儀中,裂解細胞,隨后經過預擴增將微量初始模板進行線性擴增,最后經過指數擴增即完成文庫構建。將構建好的文庫純化后定量,隨后測序文庫與引物、dNTPs、DNA聚合酶、引物載體構建“油包水”PCR反應單元后在DA8600測序平臺完成NGS測序工作。
1.3統計學方法
所有統計分析采用SPSS 23.0進行。計數資料采用率(%)進行統計學描述,組間率的比較采用χ2檢驗,不滿足χ2檢驗條件,則采用Fisher確切概率法檢驗。檢驗水準α設定為0.05。
2結果
2.1基本數據
PGS共活檢288枚胚胎,其中13枚胚胎因質控數據不合格未檢出結果,因此有效檢出結果的胚胎數為275枚。在這275枚胚胎中,整倍體胚胎數目為141(51.27%),非整倍體胚胎數目為134(48.73%)。在染色體異常的胚胎中以異常染色體數目為1條[57/134(42.54%)]和2條[50/134(37.31%)]最為常見,見圖1。若夫妻雙方中僅女方染色體異常,則其產生非整倍體胚胎數目為43(59.72%),若夫妻雙方中僅男方染色體異常,則其產生非整倍體胚胎數目為59(49.17%),見表1。
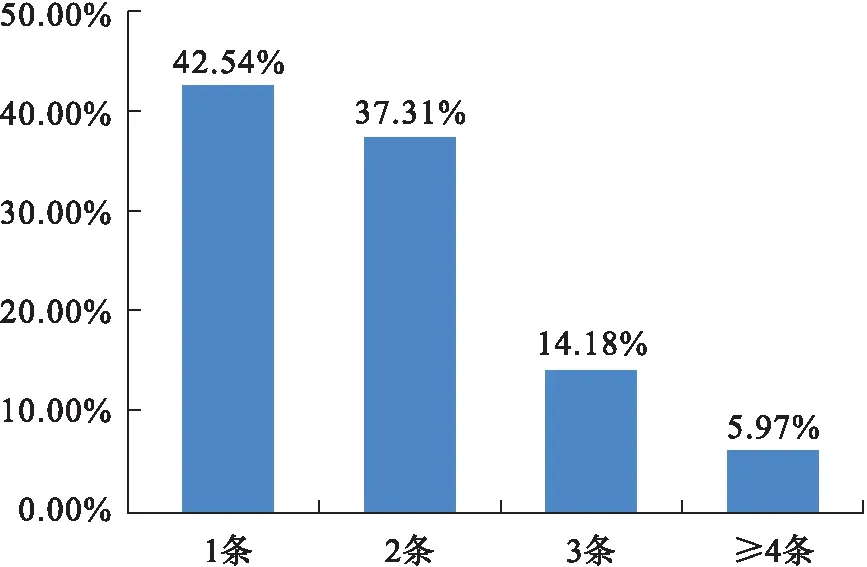
圖1 異常染色體數目的發生頻率Fig.1 The frequency of abnormal chromosome numbers

表1 不同性別的染色體異常患者胚胎整倍體率和非整倍體率的比較 [n(%)]Table 1 Comparison of the rate of euploid and aneuploidy in patients with chromosomal abnormalities of different genders [n(%)]
2.2不同年齡段女性胚胎整倍體率和非整倍體率的比較
以女性年齡為分組依據,分為≤27歲、28~30歲、31~33歲、34~36歲、≥37歲共5組。總體上看,隨著女方年齡的增加,胚胎非整倍體率也隨之增加。然而,不同年齡女性患者的胚胎整倍體率與非整倍體率比較無統計學差異(P>0.05),見表2。
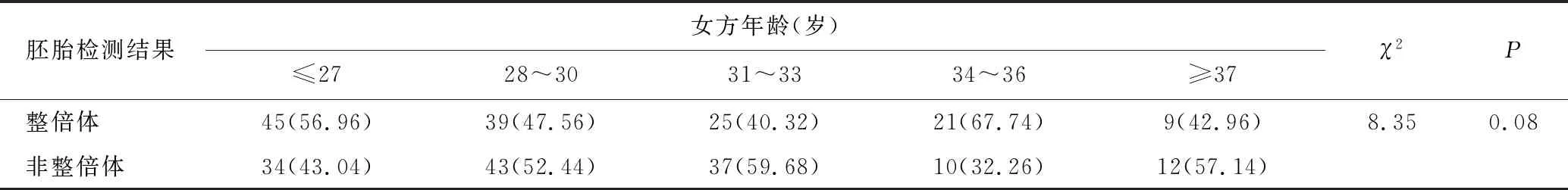
表2 不同年齡段女性胚胎整倍體率和非整倍體率的比較 [n(%)]Table 2 Comparison of the rate of euploid and aneuploidy in different age groups of female [n(%)]
2.3不同PGS指征胚胎整倍體率和非整倍體率的比較
不同PGS指征中,以相互易位(36.84%)和RSA(18.60%)最為常見。PGS指征為染色體相互易位共有105例,其中非整倍體胚胎數目為71個(非整倍體率67.62%);PGS指征為染色體倒位共有3例,其中非整倍體胚胎數目為2個(非整倍體率66.67%);PGS指征為衍生染色體共有9例,其中非整倍體胚胎數目為7個(非整倍體率77.78%);PGS指征為不良孕產史、反復種植失敗、RSA分別有28例、9例、53例,其中非整倍體胚胎數目分別為11個(非整倍體率39.29%)、2個(非整倍體率22.22%)、24個(非整倍體率45.28%)。總體上看,平衡易位、倒位、衍生染色體等雙親染色體異常可能更易導致胚胎非整倍體的發生,見表3。
2.4不同PGS指征單個胚胎各染色體數目或結構異常的發生頻率
胚胎染色體異常中11、13、14、22號染色體及性染色體異常發生率較高(分別占9.19%、10.95%、6.71%、6.01%、8.83%)。發生染色體相互易位的患者胚胎的11、13、14、22、5號染色體異常率較高(分別占9.52%、16.67%、7.14%、6.55%、6.55%);染色體非整倍體患者胚胎的14、2號染色體異常率較高(分別占19.05%、14.29%);不良孕產史患者胚胎的8、21號染色體異常率較高(分別占17.65%、17.65%);RSA患者胚胎的7、11、16號染色體及性染色體異常率較高(分別占7.90%、13.16%、7.90%、15.79%),見表4。
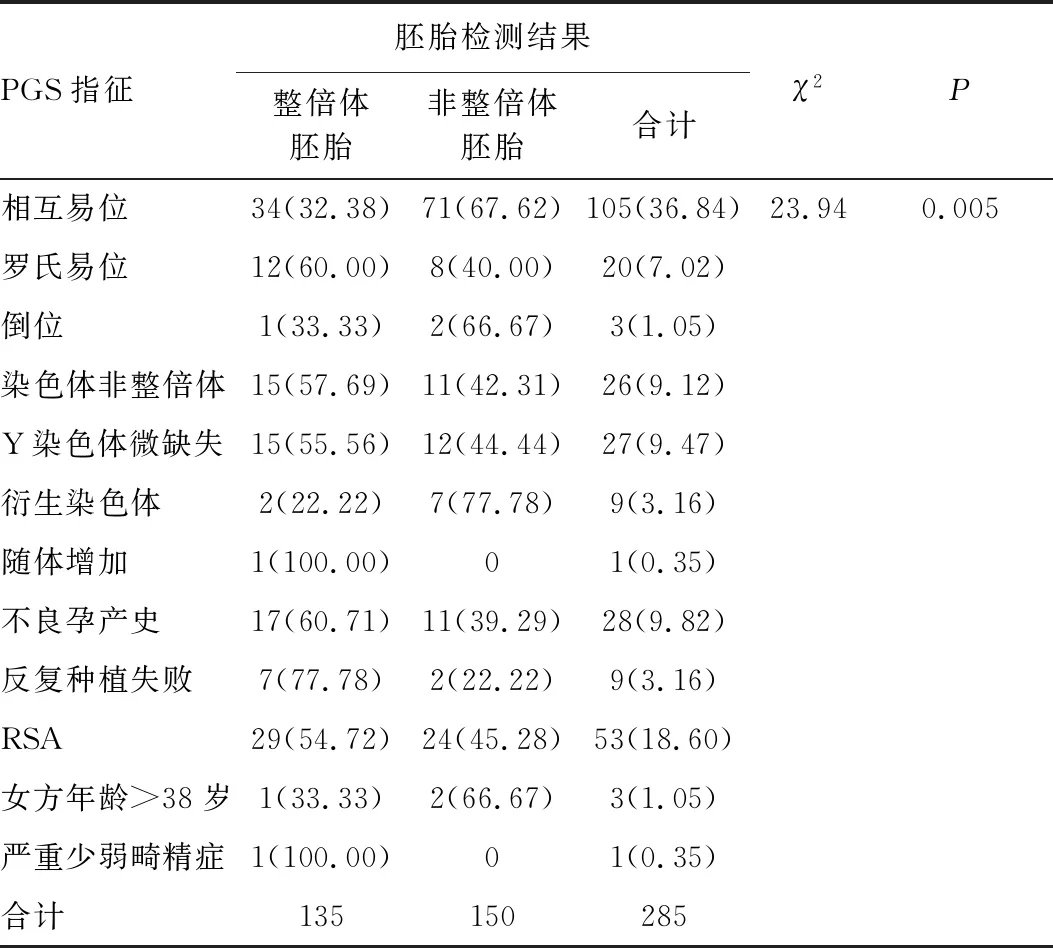
表3 不同PGS指征胚胎整倍體率和非整倍體率的比較 [n(%)]Table 3 Comparison of the rate of euploid and aneuploidy with different PGS indications [n(%)]
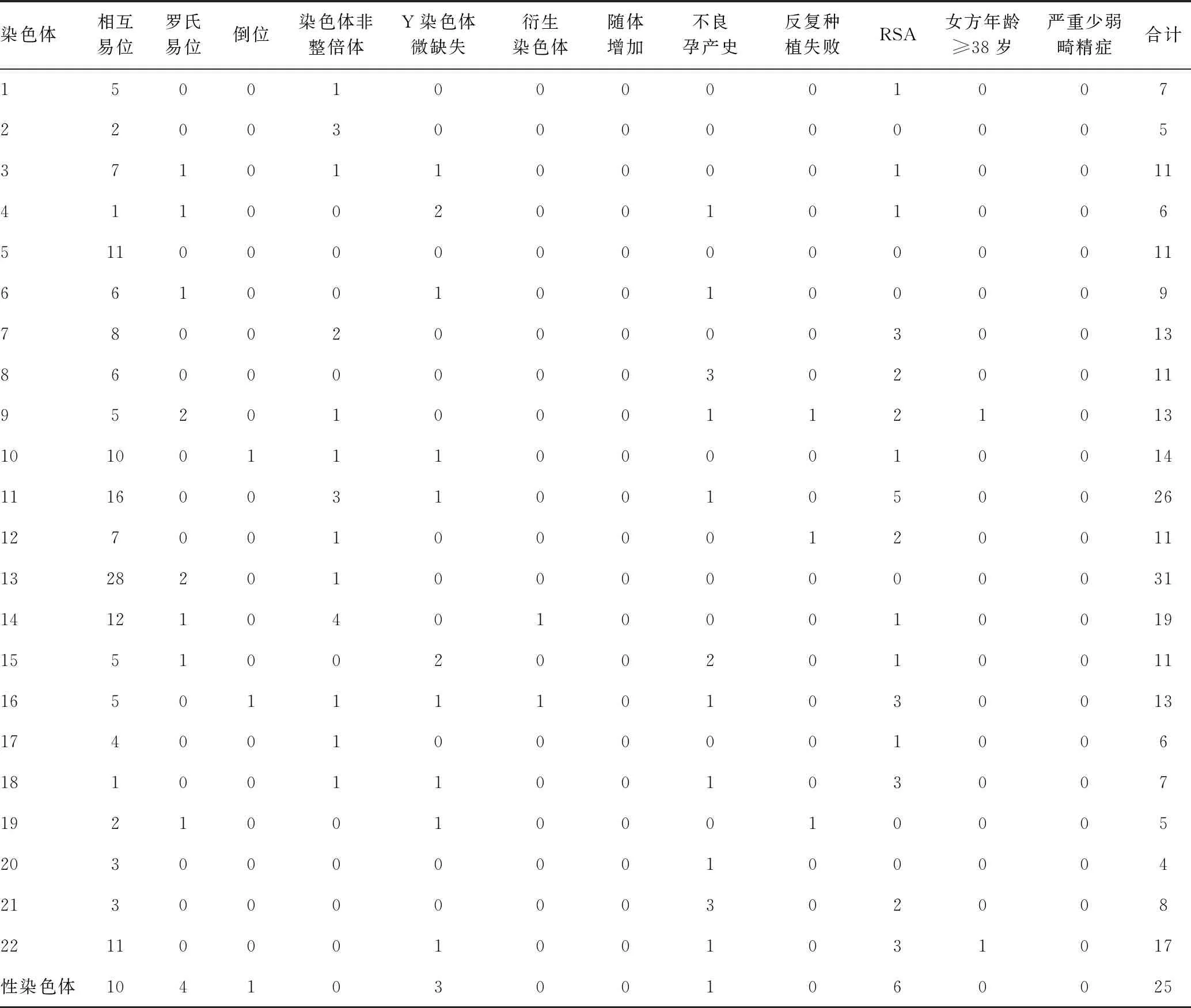
表4 不同PGS指征單個胚胎各染色體數目或結構異常的發生情況 (n)Table 4 Frequency of chromosome numbers or structure abnormal with different PGS indications (n)
3討論
3.1胚胎的非整倍體
非整倍體是最常見的染色體數目異常,發生于卵母細胞或胚胎,可導致胚胎種植失敗、自發性流產和新生兒出生缺陷。據歐洲人類生殖與胚胎學會(ESHRE)10年PGS數據統計,共活檢89 373枚胚胎,僅有33%的胚胎染色體正常,適合移植[7]。有研究報道早期自然流產是健康育齡婦女常見的妊娠并發癥,占臨床妊娠的10%~15%,其病因眾多,以遺傳因素(尤其是胎兒染色體數目異常)最多見,孕婦年齡是迄今唯一被證實的與胚胎非整倍體的發生密切相關的流行病學因素。此外,研究表明反復種植失敗患者可通過PGS獲得臨床妊娠[8-9]。大約50%的RSA患者沒有明確的原因,對流產物的妊娠分析表明染色體非整倍性率很高[10-11]。在向此類夫婦普遍推薦這種治療之前,需要進行研究以確定哪些患者最有可能從PGS中受益。然而相關的研究很少。因此本文就不同PGS指征的患者與胚胎非整倍體之間的關系作橫向比較,以期為臨床工作提供一些幫助。
3.2女性年齡與胚胎非整倍體的相關性
本文共檢測288枚胚胎,有效檢出結果的胚胎數為275枚,其中整倍體胚胎數目為141(51.27%),非整倍體胚胎數目為134(48.73%)。在染色體異常的胚胎中以異常染色體數目為1條(42.54%)和2條(37.31%)最為常見。女方染色體異常者胚胎非整倍體率較高(59.72%),這提示我們,女方染色體異常可能更易引起胚胎染色體異常。
以女方年齡分組后,總體上看,隨著年齡的增加,胚胎非整倍體率也隨之增加。34~36歲及≥37歲組的樣本數相對較少(分別為31、21例),這可能也是造成其非整倍體率較低的原因。
3.3不同PGS指征與胚胎非整倍體的相關性
在不同PGS指征中,以相互易位和RSA最為常見。不良孕產史、反復種植失敗、RSA患者產生的非整倍體胚胎數目分別為11個(45.16%)、2個(22.22%)、24個(45.28%);平衡易位、羅氏易位、倒位、非整倍體及衍生染色體患者產生的非整倍體胚胎數分別為71個(67.72%)、8個(40.00%)、2個(66.67%)、11個(42.31%)和7個(77.78%)。雙親染色體異常可能更易導致胚胎染色體異常,不良孕產史、RSA、Y染色體微缺失患者的胚胎非整倍體率也近乎50.00%。這提示我們在臨床上遇到此類患者要盡可能推薦其做PGS,篩選出正常的胚胎,進而獲得較好的妊娠結局。
同時,由于現代分子生物學的發展,運用于PGS的遺傳學分析技術也在不斷更新。本文所采用的MALBAC-NGS技術,對單細胞全基因組擴增采用的是多次退火環狀循環擴增技術(multiple annealing and looping-based amplification cycles,MALBAC)這一全新的全基因組擴增(whole genome amplification,WGA)方法,采用特殊設計的引物,對整個基因組實現高效而又均衡的全擴增[12-13]。且其作為一項高通量、高度自動化的可用于染色體非整倍體篩查的技術,在精確度、靈敏度、特異性、分辨率等方面都有表現不凡的優勢。

