新輔助食管癌手術前后機體營養狀況變化研究
李國雨,何 明,李國慶
食管癌是全球第六大常見的惡性腫瘤,在癌癥死亡當中排名第四。我國為食管癌高發區,發病率和死亡率均居世界第一位[1],每年因食管癌死亡的人數達40萬以上。目前食管癌的治療以手術為基石的多學科綜合治療為主,對于進展期食管癌,手術治療的5 a生存率僅為30%~40%[2]。新輔助治療近些年來在局部進展期食管癌的治療中迅速開展起來。隨機研究表明,新輔助治療聯合手術的綜合治療模式臨床效果較為肯定,新輔助治療與根治性手術切除相結合,可提高R0切除率[3],一定程度上改善預后,但新輔助治療手術前后患者營養狀態變化仍需進一步探索。本研究就新輔助治療后患者在進行手術治療前后機體營養狀況變化進行探討,為臨床新輔助患者擬行手術治療前增強其營養狀況提供理論依據。
1 對象和方法
1.1 研究對象選擇2017年5月1日至2019年5月31日于河北醫科大學第四醫院胸五科住院治療的食管癌患者,通過電子病歷系統收集患者的臨床病歷資料。入選標準:①年齡≥18歲;②病理證實為食管癌且術前均接受過新輔助治療;③接受過手術治療;④未同時或既往患有其他惡性腫瘤病史;⑤有完整的術前實驗室檢查信息。排除標準:①年齡<18歲的患者;②病理未證實為食管癌或術前未接受過新輔助治療的患者;③未接受過手術治療的患者;④同時或既往患有其他惡性腫瘤病史的患者;⑤資料不完整的患者。
1.2 研究方法研究采用人體測量、營養生化檢查、查閱病歷等方法進行資料收集。
1.2.1 一般資料包括入院日期、入院診斷、病歷號、性別、年齡、新輔助方案(術前輔助放療;術前輔助化療;術前輔助放化療)、腫瘤位置、手術時間、手術方式。
1.2.2 生化測定包括血清前白蛋白(PA)、血清白蛋白(ALB)、總蛋白(TP)、球蛋白(GLOB)、血紅蛋白(HGB)、淋巴細胞總數(TLC)、谷丙轉氨酶(ALT)、谷草轉氨酶(AST)、肌酐(Cr)、尿素氮(UN)。
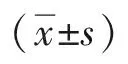
2 結果
2.1 研究人群特征描述按照研究的納入排除標準,對目標人群進行整理和篩選,共收集142例新輔助食管癌患者,排除未做手術的9例,最終入組133例。患者的一般基線特征見表1-2所示。

表1 新輔助治療后手術治療的食管癌患者的分類變量基線特征(n=133) 例(%)
續表

變 量食管癌 有48(36.09) 無85(63.91)吸煙 有69(51.88) 無64(48.12)新輔助方案 術前輔助放療1(0.75) 術前輔助化療123(92.48) 術前輔助放化療9(6.77)腫瘤位置 上段9(6.77) 中段39(29.32) 下段32(24.06) 賁門53(39.85)手術時間 2017年至2018年47(35.34) 2018年至2019年86(64.66)手術方式 左胸①95(71.43) 右胸+腹部②32(24.06) 三切口③6(4.51)
注:①Sweet術式;②Ivor-Lewis術式;③Mckeown術式。

表2 新輔助治療后手術治療的食管癌患者的連續變量基線特征
2.2 手術治療對新輔助食管癌患者的營養狀態的影響133例新輔助治療食管癌患者行手術治療。與手術治療前比較,患者手術治療后相應指標變化見表3-4。其中ALB、PA、TP、HGB、GLOB、TLC水平均明顯降低,差異有統計學意義(均P<0.05)。

表3 新輔助治療食管癌患者手術治療前后測量指標變化比較 例(%)


項 目ALB/(g·L-1)PA/(mg·L-1)TP/(g·L-1)HGB/(g·L-1)GLOB/(g·L-1)TLC/(×109·L-1)手術治療前41.31±2.92235.83±55.6068.21±4.11128.33±14.4726.90±3.551.54±0.52手術治療后31.65±3.47153.31±47.9252.58±5.69120.73±18.4821.17±4.950.73±0.33t/z值-30.45-9.72-29.59-5.99-9.43-18.51P0.0000.0000.0000.0000.0000.000
2.3 手術治療對新輔助治療后食管癌患者的肝腎功能的影響133例患者接受新輔助治療后行手術治療。與手術治療前比較,患者手術治療后ALT、AST水平均明顯增加,差異有統計學意義(均P<0.05);Cr、UN水平均略有增加,但差異無統計學意義(均P>0.05)。見表5。


項 目ALT/(U·L-1)AST/(U·L-1)Cr/(μmol·L-1)UN/(mmol·L-1)手術治療前26.72±21.4424.99±14.6959.34±11.425.00±1.29手術治療后56.50±160.3158.72±78.2761.27±20.916.27±11.37t/z值-4.36-8.73-1.02-0.23P0.0000.0000.310.82
3 討論
惡性腫瘤相關的營養不良是臨床常見問題。美國癌癥中心的營養專家指出,大約40%的腫瘤患者死亡歸咎于營養不良,而并非是腫瘤本身[4]。嚴重的營養不良可影響腫瘤患者的手術治療及其臨床結局。盡管如此,存在營養風險或營養不良的腫瘤患者中僅有30%~60%接受營養干預,還有很大比例未得到及時有效的營養干預[5]。食管癌的營養不良發生率居所有惡性腫瘤第一位,達60%~85%[6]。有文獻報道新輔助治療降低了食管癌患者的生活質量[7]。
食管癌在我國發病率很高,是臨床上常見的惡性腫瘤,既往常規治療方案是手術切除聯合術后放化療,但總體療效欠佳。近些年來新輔助治療迅速開展起來,其有利于腫瘤降期、消滅全身微小轉移灶,對于可手術切除的食管下段及胃食管結合部腺癌患者,新輔助化療能夠提高5 a生存率,而不增加術后并發癥和治療相關死亡率[6]。然而新輔助治療后實施手術患者的營養狀況變化仍需進一步研究。手術對于食管癌患者來說是非常大的打擊,近年來加速康復外科理念越來越受到重視,胸腹腔鏡微創手術在食管癌患者治療中快速發展起來。相較于傳統開胸手術,對胸段食管癌行胸腹腔鏡微創切除手術患者在圍術期實施加速康復措施干預,可減輕術后疼痛、降低術后并發癥、縮短住院時間,但是胸腹腔鏡微創切除手術對于患者來說創傷也是巨大的[8]。手術是目前治療食管癌的主要方法, 但創傷大、出血量多,加之術后并發癥等,以及老年患者機體功能減弱, 所以無論是傳統開放式手術還是胸腔鏡手術都會嚴重降低患者的營養狀況[9],本研究表明新輔助治療后,手術治療顯著降低患者的前白蛋白、白蛋白、總蛋白、淋巴細胞計數及血紅蛋白水平,患者的肝功能也嚴重受到手術的影響。研究發現, 由于食管癌多發于老年群體, 其器官功能衰弱, 且營養攝入量相對較少, 免疫系統呈抑制狀態, 而手術的應激性, 進一步加重了免疫抑制[10],所以無論是接受新輔助治療的患者還是未經任何治療的患者在接受手術治療后,患者的營養狀況都會受到嚴重的影響。食管癌患者圍手術期營養不良是影響預后的重要因素之一。建議為食管癌患者制定最佳的營養干預措施,以防止手術前后營養不良[11]。還有文獻報道食管癌患者在食管癌切除術前接受新輔助治療時應給予額外的營養干預[12]。所以新輔助治療后行手術治療的食管癌患者應盡量改善營養狀況。
綜上所述,新輔助治療后實施手術治療顯著降低了食管癌患者的營養狀況,應及時加以營養干預。

