普通小麥部分同源染色體配對抑制基因 Ph1分子標記的驗證和篩選
李孟軍,周 碩,李亞青,張士昌,彭義峰,張 楠,史占良
(1.石家莊市農林科學研究院/河北省小麥工程技術研究中心,河北石家莊 050041;2.河北省農林科學院遺傳生理研究所,河北石家莊 050051)
小麥的每條染色體都具有與其同源染色體或其他2條部分同源染色體配對的潛力,但染色體配對在很大程度上僅限于同源染色體[1]。普通小麥5BL染色體臂上的Ph1位點是抑制部分同源染色體間配對和重組的主要因子[2-4]。在異源六倍體小麥中,5B染色體上的Ph1位點是在小麥多倍體化過程中產生的,它在減數分裂期間調控類二倍體化減數分裂(diploid-like meiosis),抑制外源種屬的部分同源染色體配對,從而保證小麥異源多倍體基因組的穩定性[5]。雖然在1958 年已鑒定了Ph基因,但由于缺乏等位變異,迄今Ph基因未被克隆[6]。Griffiths等[7]將Ph1定位在5B染色體上1段2.5 Mb區域中,該區域包含1段插入cdc2-like基因簇的亞端粒異染色質片段。cdc2-like基因簇是此區域唯一的多基因簇,其中至少1個成員是5B染色體特有的。因此,cdc2基因是Ph1最可能的候選基因[7]。定位在小麥基因富集區5L0.5的61個標記中,有9個位于Ph1基因區,其中7個標記以相同順序排列定位在水稻9號染色體上450 kb區域上。在水稻450 kb區域中的91個基因中,鑒定出26個Ph1候選基因,其中5個基因與6個減數分裂特異基因(Zip1、Scp1、Cor1、RAD50、RAD51、RAD57)具有相同的結構域[8]。利用VIGS(virus-induced gene silencing)沉默侯選ph1基因C-Ph1(candidateph1gene,C-Ph1)導致了小麥表現出與ph1突變體類似的染色體配對行為。小麥部分同源群中的C-Ph1基因具有不同的結構和表達模式,只有5B染色體上的拷貝在減數分數中期Ⅰ特異性表達[9]。Sears 等[6]通過X-射線處理中國春小麥正常花粉獲得了中國春ph1b突變體,該突變體能夠有效引起部分同源染色體配對和種間、屬間雜種染色體的配對。
在傳統的回交育種過程中,將目標基因轉入輪回親本的同時,往往將非輪回親本攜帶不利性狀基因的染色體片段也轉入輪回親本基因組中。因此,減小攜帶目標基因的外源染色體片段是染色體工程中的重點和難點。為解決上述難題,需要做到以下兩點:(1) 外源目標基因必須以易位染色體形式轉入受體親本,從而提高稀有重組體的出現頻率;(2) 開發高效且成本低廉的分子標記,以便從大量雜交后代中篩選出稀有重組體[5]。
Segal等[12]根據DNA探針WPG90序列開發了分子標記WPG90。Qu 等[13]根據AFLP擴增片段開發了分子標記PSR2120。Roberts等[1,14]根據RFLP標記PSR128和PSR574分別開發了分子標記PSR128和PSR574。王新望等[15]根據RAPD特異片段OPR7936和OPR17524開發了 SCAR標記OPR7和OPR17,又根據大麥RFLP標記Ph920開發了SCAR 標記PhSCAR[16]。Mads是位于CSph1b缺失區的一個基因。雷 昊等[17]根據其DNA序列開發了分子標記Mads,成功地將中間偃麥草攜帶抗黃矮病基因的染色體2Ai-2轉移到ph1b缺失的遺傳背景中。本研究的目的是驗證并比較上述9個PCR分子標記(WPG90、PSR2120、PSR128、PSR574、OPR7、OPR17、Ph920、PhSCAR、Mads)的特異性和穩定性,以期篩選出理想的分子標記,用于利用ph1b突變體的分子輔助育種。
1 材料與方法
1.1 供試材料
中國春ph1b突變體(CSph1b),由山東農業大學孔令讓教授和李興鋒教授提供;六倍體小麥Pavonph1b突變體(Pavonph1b),由山東農業大學吳佳杰博士提供;中國春、中國春缺四體(CSN5AT5B、CSN5BT5A、CSN5DT5B),由中國科學院李義文博士提供;含有ph1的小麥品種師欒02-1、石新828、石4185、鄭麥366、濟麥22和西農979,由河北省小麥工程技術研究中心提供。
1.2 供試分子標記
根據文獻合成Ph1的9對PCR引物(表1),分別用來檢測CSph1b突變體及其轉育的突變體Pavonph1b。PCR引物均由Invitrogen公司合成。
1.3 PCR檢測
PCR反應在Biometra T-Gradient Thermoblock上進行。PCR反應體系(20 μL):2×Taq PCR StarMix(GenStar)10 μL,引物各1 μL(10 μmol·L-1),模板基因組DNA 2 μL(50~100 ng),ddH2O 6 μL。PCR 擴增程序參照文獻并加以優化(表2)。PCR擴增產物采用2.0%瓊脂糖凝膠電泳檢測,緩沖液為1×TAE,溴化乙錠染色觀察記錄。
1.4 序列分析
采用克隆測序方法對PSR128、Mads和PhSCAR三個標記的PCR產物進行了序列分析。PCR反應在Biometra T-Gradient Thermoblock上進行。PCR反應體系(20 μL): 2× LA Taq PCR MasterMix(TaKaRa)10 μL,引物各1 μL(10μmol·L-1),模板基因組DNA 2μL(50~100 ng),ddH2O 6 μL。克隆載體為pMD18-T(TaKaRa)。測序由Invitrogen公司完成。用軟件Lasergene SeqMan II Module (DNAStar; http:/www.DNAStar.com)進行核酸序列組裝、拼接和比對。

表1 PCR分子標記及其引物序列Table 1 PCR marker information and primer sequences
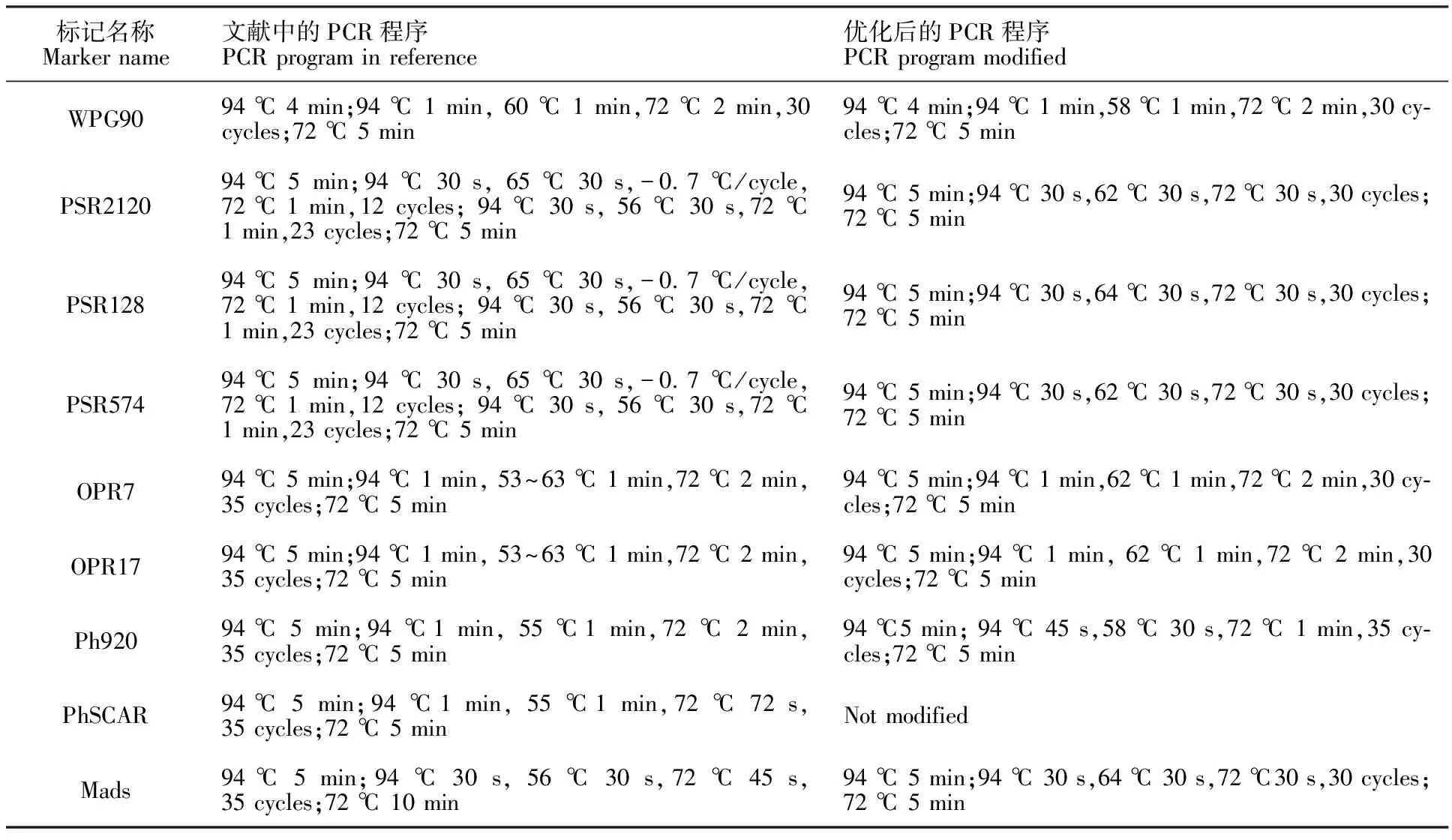
表2 PCR擴增程序Table 2 PCR program
2 結果與分析
通過對相關文獻的分析,選取了其中9個分子標記,以11個基因組DNA為模板,對這9個分子標記進行了驗證和比較。在9個分子標記中,Mads是根據CSph1b缺失區的Mads基因開發的,其余8個標記為根據RFLP、AFLP和PAPD標記開發的SCAR標記。為了簡化PCR操作,提高PCR檢測效率,本研究中PCR擴增均以基因組DNA為模板,采用了相同的PCR擴增體系,并對每個標記的PCR擴增程序進行了簡化和優化(表2)。
PCR擴增結果表明,9個標記中,WPG90、PSR2120、PSR128、PSR574、Ph920、Mads為顯性標記,在CSph1b突變體和Pavonph1b突變體中無擴增,而在含有Ph1的小麥品種中,這6個標記均擴增出特異的單一條帶,片段大小分別為230 bp、232 bp、260 bp、154 bp、920 bp和323 bp(PCR產物直接測序),符合預期[5,12-14,16-17]。CSph1b突變體、Pavonph1b突變體和中國春缺四體CSN5BT5A PCR擴增帶型一致,這表明Ph1位點位于5B染色體上,Pavonph1b突變體來自CSph1b突變體[4](圖1)。標記Ph920采用參考文獻的PCR程序,CSph1b突變體、Pavonph1b突變體和中國春缺四體CSN5BT5A有較弱的非特異性擴增。標記PSR2120有引物二聚體產生,通過調整退火溫度無法消除引物二聚體。標記WPG90對退火溫度非常敏感,僅在58 ℃有微弱的PCR擴增。標記PSR128和標記PSR574擴增條帶特異、清晰、單一,同時,2個標記PCR擴增對退火溫度不敏感,適宜作為多重PCR擴增引物。標記OPR7和標記OPR17在所有DNA模板中均有擴增,無法區分CSph1b突變體和Pavonph1b突變體,是非特異PCR標記,與預期不符[17]。標記PhSCAR在所有DNA模板中均有擴增條帶,但CSph1b突變體、Pavonph1b突變體、中國春缺四體CSN5BT5A三個材料與其他8個材料的PCR擴增帶型不同,與預期不符[16]。標記PhSCAR在CSph1b突變體、Pavonph1b突變體和中國春缺四體CSN5BT5A中擴增出單一條帶,而在含有Ph1的小麥品種中均擴增出2個條帶,這種擴增特征穩定,因此,標記PhSCAR可作為共顯性標記使用(圖1)。
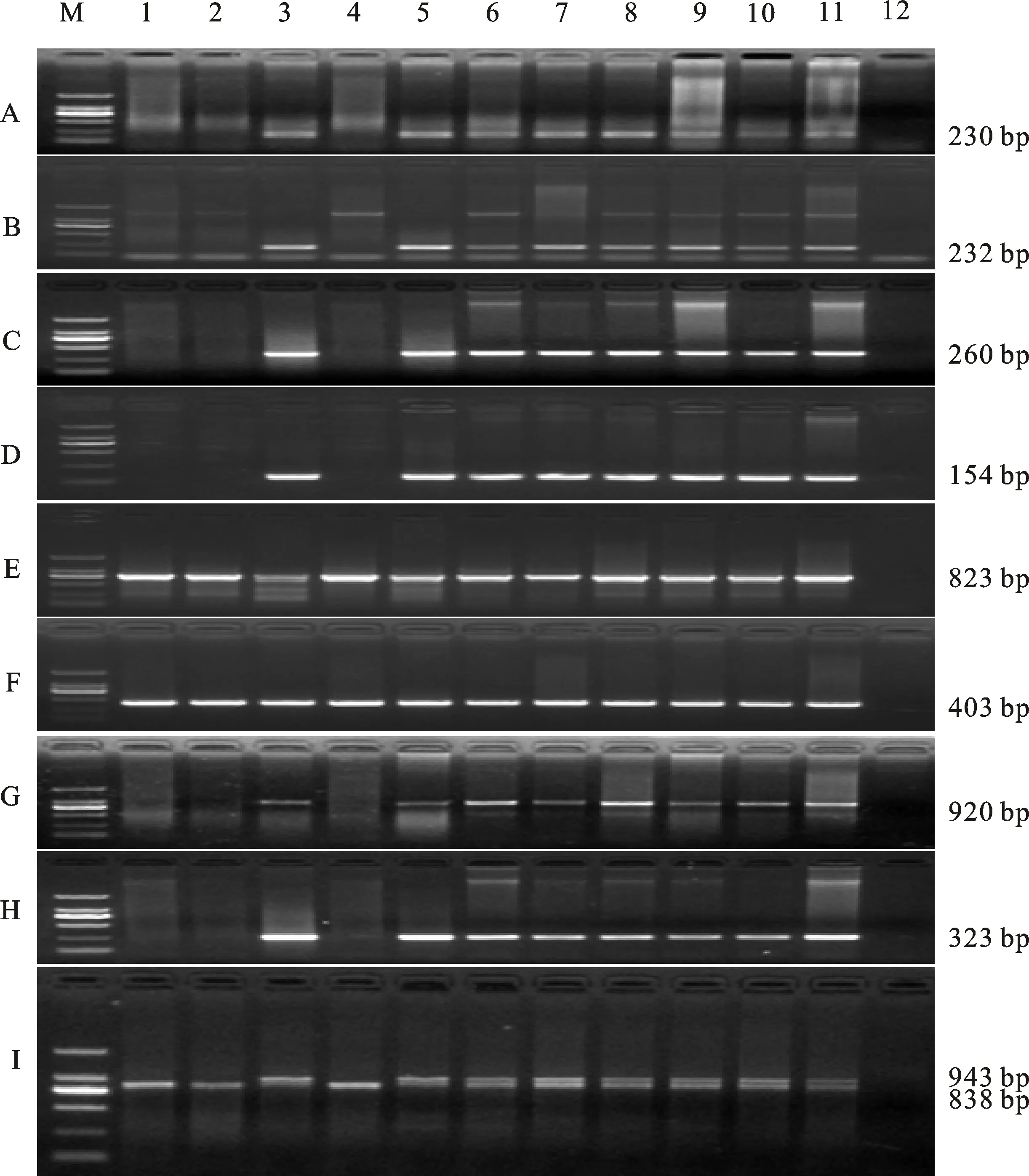
A:WPG90;B:PSR2120;C:PSR128;D:PSR574;E:OPR7; F:OPR17;G:Ph920;H:Mads;I:PhSCAR。M:DNA marker(DL2000);1:CSph1b;2:Pavonph1b;3:CSN5AT5B;4:CSN5BT5A;5:CSN5DT5B;6:師欒02-1;7:石新828;8:石4185;9:鄭麥366;10:濟麥22;11:西農979;12:ddH2O。
A:WPG90; B:PSR2120; C:PSR128; D:PSR574; E:OPR7; F:OPR17; G:Ph920; H: Mads;I:PhSCAR.M: DNA marker(DL2000); 1:CSph1b; 2:Pavonph1b; 3:CSN5AT5B; 4:CSN5BT5A; 5:CSN5DT5B; 6:Shiluan 02-1; 7:Shixin 828; 8:Shi 4185; 9:Zhengmai 366; 10:Jimai 22; 11:Xinong 979; 12:ddH2O.
圖1 9個DNA分子標記的PCR檢測結果
Fig.1 PCR assay amplified with the nine molecular markers
標記Mads擴增中,退火溫度不同,CSph1b突變體、Pavonph1b突變體和中國春缺四體CSN5BT5A PCR擴增帶型不同。擴增產物測序結果表明,PCR帶型的差異是因為標記Mads的上鏈引物和下鏈引物各自分別發生了擴增,擴增片段長度分別為878 bp和1584 bp[17](圖2B)。
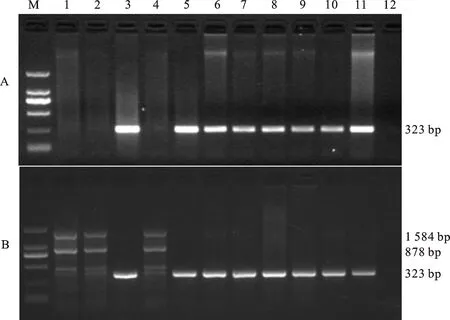
A:Mads (Tm=64 ℃);B:Mads(Tm=56 ℃)。M:DNA marker(DL2000);1:CSph1b;2:Pavonph1b;3:CSN5AT5B;4:CSN5BT5A;5:CSN5DT5B;6:師欒02-1;7:石新828;8:石4185;9:鄭麥366;10:濟麥22;11:西農979;12:ddH2O。
A: Mads (Tm=64 ℃); B:Mads (Tm=56 ℃).M:DNA marker(DL2000); 1:CSph1b; 2:Pavonph1b; 3:CSN5AT5B; 4:CSN5BT5A; 5:CSN5DT5B; 6:Shiluan 02-1; 7:Shixin 828; 8:Shi 4185; 9:Zhengmai 366; 10:Jimai 22; 11:Xinong 979; 12:ddH2O.
圖2 分子標記Mads在不同退火溫度下的PCR檢測結果
Fig.2 PCR assay amplified with Mads at different annealing temperatures
3 討 論
黑麥屬、偃麥草屬、冰草屬、簇毛麥等普通小麥近緣種屬蘊藏著普通小麥缺乏的優良基因,通過遠緣雜交將其優良基因導入小麥基因組中,對普通小麥遺傳改良具有重要意義。Ph1b突變體可誘導普通小麥與近緣物種部分同源染色體的重組[4],通過與部分同源染色體配對重組創制的普通小麥外源染色體小片段易位系,可減少近緣物種攜帶目標基因的染色體片段對小麥農藝性狀的不利影響。CSph1b突變體為春性小麥且農藝性狀較差,通過回交創制適宜本區域農藝性狀優良的ph1b突變體,有利于提高ph1b的育種利用價值[16]。利用ph1b突變體創制普通小麥和外源染色體重組體效率較低,且需采用特定的雜交策略,因此,在回交過程中采用分子標記輔助選擇技術可以顯著加速新種質創制進程,甚至決定新種質選育的成敗[6]。
王新望等[16]以阿勃5B缺體為橋梁親本,京411為受體親本, CSph1b突變體為供體親本,經減數分裂分析和PhSCAR標記輔助選擇,快速地選育了京411的ph1b中間代換系。雷昊等[17]用CSph1b分子標記Mads 及2Ai-2 染色體的分子標記P4和P68高效獲得了小麥-中間偃麥草ph1b-2Ai-2 染色體綜合體。本實驗結果表明,分子標記WPG90、PSR2120、PSR128、PSR574、Ph920、Mads能夠用于ph1b純合單株選擇,其中標記PSR128、PSR574和Mads從特異性、重復性方面考慮適用于分子標記輔助選擇,但標記Mads需要注意退火溫度的選擇。標記PhSCAR與前人研究結果[16]不同,PCR擴增及其產物測序結果表明,標記PhSCAR可作為共顯性標記使用。共顯性標記的PCR分子標記可有效避免顯性分子標記中的假陰性現象。在ph1b株系選擇時,標記PhSCAR與PSR128、PSR574、Mads配合使用可相互驗證,從而減少雜交和選擇的工作量,提高鑒定的準確性。標記OPR7和OPR17無法有效區分ph1b株系,這與前人研究結果[15]不同,具體原因需進一步研究。

