腸鏡下切開引流術治療直腸黏膜下膿腫的初步研究*
蔡平,戴曉宇,李堅炯,周海萍
(中國科學院大學寧波華美醫院 肛腸外科,浙江 寧波 315000)
直腸黏膜下膿腫傳統上行腰麻或者全麻下膿腫切開引流術。近年來,隨著消化內鏡技術與設備的不斷發展,且直腸黏膜對切割無痛覺反應,在無麻醉的情況下,使腸鏡下切開引流術治療直腸黏膜下膿腫成為可能。但目前國內罕見有相關研究報道。本單位在國內較早開展該項技術,至今已積累了一定經驗。現報道如下:
1 資料與方法
1.1 一般資料
選擇2013年1月-2018年12月在中國科學院大學寧波華美醫院收集的直腸黏膜下膿腫病例70 例。其中,男56 例,女14 例;年齡18 ~75 歲,平均43 歲;病程3 ~10 d,平均6 d;首次來診50 例,經抗炎治療無效再診者20 例,70 例患者全部伴有體溫升高,46 例高于38.5℃,44 例感覺肛門墜脹、頻有便意,30例肛周腫痛劇烈且排尿困難,其中16 例伴有糖尿病,空腹血糖在10 ~21 mmol/L。所有患者均在直腸指診時,摸到直腸黏膜下飽滿、柔軟、壓痛之腫塊,肛門外無紅腫、無壓痛、摸不到包塊,術前行盆腔磁共振成像(magnetic resonance imaging,MRI)確診為直腸黏膜下膿腫。
1.2 操作器械
Olympus CV-290 腸鏡、一次性使用圈套器和威利FORCE2 BJ 高頻電刀等。
1.3 手術方法
術前與患者及其家屬談話,告知病情、腸鏡治療方式及替代療法,簽署知情同意書。術前行生理鹽水500 ml 灌腸,使其排盡直腸內糞便,由具有豐富治療經驗的腸鏡醫師進行。術中患者取左側臥位,清醒狀態下鼻導管吸氧,全程心電監護。操作步驟:①行單人腸鏡操作,腸鏡插入直腸內,助手用注射用水充分沖洗直腸,使直腸清潔,仔細觀察直腸黏膜下膿腫部位,可見局部黏膜下隆起明顯,如觀察困難必要時可倒鏡觀察,尋找最佳切開引流部位;②助手置入一次性使用圈套器,并連接威利FORCE2 BJ 高頻電刀主機,將電流模式調至混切30 W、噴凝式凝血30 W,圈套器金屬頭部露出約3 mm 左右,使用混切模式縱行逐層切開直腸黏膜層、黏膜下層,注意切開過程需逐步進行,切忌一蹴而就,如有創面出血,及時改用噴凝式凝血模式徹底充分止血,當全層切開后可見膿液自切口涌出;③吸盡膿液后,圈套器繼續縱行延長切口,并套除部分直腸黏膜,使膿腔開窗不易閉合,達到充分通暢引流的目的,注意止血徹底;④如膿腔巨大,腸鏡可進入膿腔,吸出膿液并徹底沖洗膿腔,如膿腔較小,則腸鏡沖水口對準膿腔后,徹底沖洗膿腔即可;⑤再次確認創面無活動性出血后,退出腸鏡,手指引導下置入引流管或引流條至膿腔內,并固定妥當。直腸黏膜 下膿腫腸鏡下表現及切開引流的操作過程見附圖。
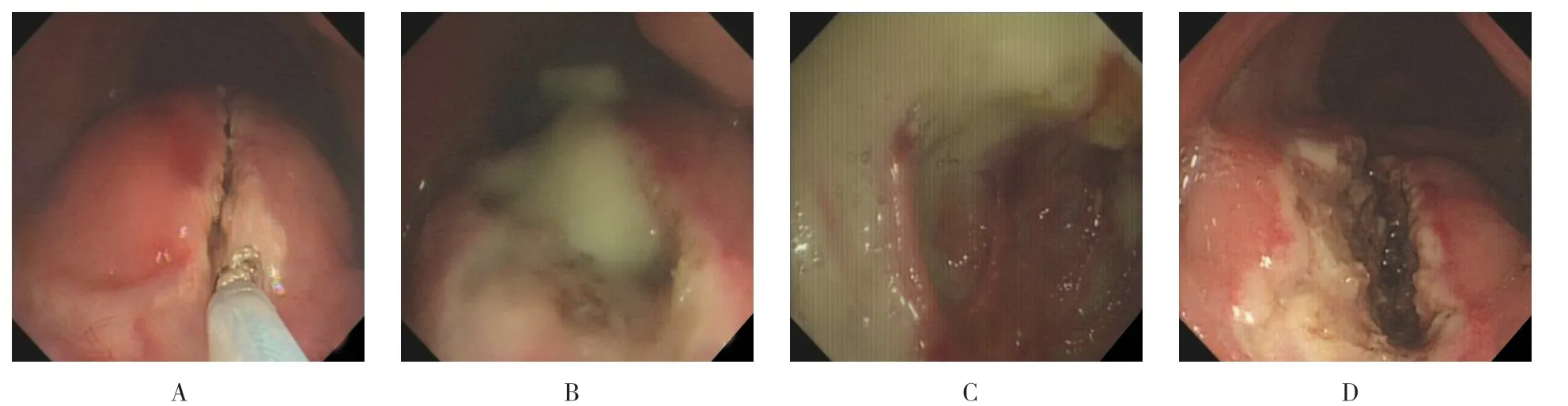
附圖 直腸黏膜下膿腫腸鏡下表現及切開引流的操作過程Attached fig.Enteroscopic presentation of rectal submucosal abscess and the procedure of incision and drainage
1.4 術后處理
患者術后臥床休息,當天禁食禁飲,常規給予補液、抑酸、止血及抗感染等治療。密切觀察患者癥狀和生命體征,注意有無腹痛、發熱加重、氣腹、消化道出血和腹膜炎等并發癥出現。對糖尿病患者注意控制血糖,空腹血糖控制在6.0 ~8.0 mmol/L。動態觀察血常規、血生化等指標。術后觀察引流情況,必要時沖洗膿腔,每日直腸指診,將手指放入開放的膿腔中做分離和清理動作,以防開放的膿腔兩邊粘連而形成假愈合,時刻保持肛周清潔干燥。術后3 d 左右確定無明顯膿液后,拔除引流管或引流條。
1.5 隨訪
患者出院后囑其前6 個月每個月來門診復診1 次,術后7 ~12 個月每3 個月門診復診1 次,均進行肛門查體,并詳細記錄查體結果,明確有無復發及形成肛瘺。隨訪觀察12 個月未再復發即確認治愈,為隨訪終點。
2 結果
70 例直腸黏膜下膿腫患者,均成功行腸鏡下膿腫切開引流術,平均操作時間(15.0±5.2)min。24 例患者膿腔巨大置入引流管,46 例患者膿腔較小置入引流條,3 d 后拔除引流管及引流條。70 例患者均治愈出院,無明顯并發癥發生,無1 例死亡。術后隨訪12個月,7 例患者術后3 個月確診形成肛瘺,9 例患者術后6 個月確診形成肛瘺,確診條件必須同時符合以下2 點:①肛門指診發現手術區域可觸及條索狀硬結;②盆腔MRI 明確形成肛瘺。以上16 例患者均行肛瘺手術后治愈,54 例患者未再復發。
3 討論
直腸黏膜下膿腫是肛門直腸膿腫的一種,是膿腫位于直腸黏膜下與肌層之間的感染發展成為膿腫。其發展迅速,患者出現周身不適、疲倦和畏寒發熱等,甚至出現敗血癥危及生命[1]。局部以直腸刺激癥狀為主,有里急后重、下墜感、排尿困難、便次多或便意感等,盆腔MRI 及直腸腔內超聲可以確診[2-3]。
直腸黏膜下膿腫發生于各種人群,男多于女,以青壯年為多,可能是青壯年飲食偏向辛辣刺激食物及飲酒多有關,容易造成肛竇充血、水腫和感染[4]。直腸黏膜下膿腫形成后,僅有很小部分通過抗生素應用得到控制,大部分都需要手術才能治愈,傳統的手術方式是切開引流術,切開膿腔將膿液引流干凈[5-7]。但是,因為直腸黏膜下膿腫位于直腸內,且位置較高,手術操作視野差,往往切開不夠徹底,同時止血困難,導致形成肛瘺高達90.0%以上。形成肛瘺后,再進行第2 次手術治療,患者痛苦大,疾病的總愈合時間大大延長[8]。
筆者采用腸鏡下直腸黏膜下膿腫切開引流術,既符合疾病本身的治療原則,同時與傳統手術相比又具有以下優勢:①適用范圍廣:操作時,因直腸黏膜對切割無痛覺反應,故無需麻醉,對于無法耐受麻醉及外科手術的患者尤為合適;②操作視野好:因在腸鏡下操作,可以對直腸進行注氣,使腸腔充分擴張,黏膜下膿腫的范圍及嚴重程度清晰可見,便于徹底切開引流沖洗,不留死腔;③手術微創:傳統手術有時因為膿腫位置高無法行直腸內切開引流,往往選擇在肛周切開切口直達黏膜下膿腔來引流,手術創面大,術后患者換藥疼痛明顯,而腸鏡下膿腫切開引流患者無明顯疼痛,且患者術后活動不受限,耐受性好,生活質量高;④安全有效:70 例腸鏡下直腸黏膜下膿腫切開引流患者,僅有16 例形成肛瘺,一次性治愈率達77.1%,遠高于傳統手術,且并發癥少,顯示出較好的臨床療效和安全性。是一種頗具應用前景的處理直腸黏膜下膿腫的治療手段。
進行腸鏡下直腸黏膜下膿腫切開引流術需注意以下7 點:①術前必須進行灌腸,術中需徹底沖洗直腸,使創面清晰暴露,避免盲目切開;②切開要徹底,需在膿腫最明顯的位置縱行全層徹底切開,并且切除部分黏膜以達到膿腫開窗的效果,避免膿腔閉合;③止血要徹底,在切開黏膜的過程中要步步為營,邊切開邊止血,切勿操之過急,切開過快過深,會導致創面出血,從而影響后續操作;④膿腔沖洗要充分,當膿腔巨大時,腸鏡需進入膿腔進行徹底沖洗,使膿液完全流出,并放置引流管或引流條,方便術后沖洗及通暢引流[9];⑤術后換藥沖洗要及時,每次換藥消毒要嚴格,將膿腔內分泌物沖洗干凈,引流條要放到膿腔底部,保證創口由內向外愈合,防止創口假性愈合[10];⑥術后應用敏感抗生素,直腸黏膜下膿腫往往由肛隱窩感染所致[11-12],多為需氧菌和厭氧菌混合感染,一般采用頭孢類和奧硝唑聯合應用,再根據細菌培養及藥敏實驗結果及時調整抗生素[13-14];⑦積極治療肛隱窩炎和肛乳頭炎,防止便秘和腹瀉,及時腸鏡檢查排除腸道特異性疾病,如腸結核、克隆病、潰瘍性結腸炎等,并積極治療[15]。

