內鏡下減壓融合經皮椎弓根釘內固定治療退變性腰椎Ⅰ、Ⅱ度滑脫
王向前,李軍,郭廣銘,郭洋洋,宋中學,刁文博,刁文杰
(河南省周口協和骨科醫院 骨科,河南 周口 466000)
腰椎滑脫病因復雜,Wiltse 和Rothman 把長期存在的節段間失穩導致的滑脫稱之為退變性腰椎滑脫,最常發生于腰5 椎體,其次是腰4 椎體[1]。按Meyerding 分度法共分為4 度,后來國際上把完全滑脫定為Ⅴ度。隨著我國醫療條件的改善,Ⅲ度以上的退變性滑脫已經明顯減少,而Ⅰ、Ⅱ度退變性滑脫仍較為常見。對伴有進行性神經癥狀加重或腰部疼痛影響行走的患者,腰椎后路椎間融合(posterior lumbar interbody fusion,PLIF)椎弓根螺釘內固定仍然是最常用的手術方式[2]。然而隨著脊柱開放手術內鏡化為代表的微創理念的推廣和手術工具的改進,Ⅰ、Ⅱ度腰椎滑脫內鏡下減壓、復位、椎間融合、椎弓根螺釘內固定已初步可行,該術式不剝離后側肌肉,對軟組織損傷小、出血少,目前國內外尚無對腰椎滑脫實行該手術方式的文獻報道,本院率先實行該手術方式,就初期臨床效果進行回顧性總結,現報道如下。
1 資料與方法
1.1 一般資料
回顧性分析 2018 年1 月至2018 年6 月本院收治的16 例腰椎Ⅰ度滑脫、7 例腰椎Ⅱ度滑脫患者的臨床資料為微創組。通過嚴格檢查和篩選,術前腰椎過伸過屈位X 線光片、腰椎CT、磁共振成像常規檢查;在無手術禁忌和手術指征明確的情況下實行內鏡下減壓、復位、椎間融合、椎弓根螺釘內固定手術。另回顧性分析同期行PLIF 椎弓根螺釘內固定術治療的18 例腰椎Ⅰ度滑脫、12 例腰椎Ⅱ度滑脫患者的臨床資料為對照組,術前檢查和手術指征同微創組。兩組患者均為單節段并伴有不同程度的腰椎退變,所有手術均經患者及家屬知情同意。術后對兩組患者隨訪3~9 個月,平均隨訪4.8 個月和5.1 個月。對兩組患者的手術時間,術中出血量,術前、術后1 個月、術后3個月視覺模擬評分 (Visual Analogue Scale,VAS)及 Oswestry 功能障礙指數(Oswestry disability index,ODI)進行統計分析。
1.2 手術方法
微創組:常規采用俯臥位、全身麻醉(全麻),透視定位了解椎體滑脫復位情況,經皮植入追弓根螺釘,內鏡下進行常規減壓,必要時行雙側減壓,減壓完成后內鏡下處理椎間盤,追弓根螺釘單側上棒,透視了解復位情況,確認復位滿意后繼續內鏡直視下處理終板到可看到松質骨,融合器試模,植入自體骨和融合器,透視確認融合器位置及大小,查看融合器及神經,退出內鏡,同側追弓根上棒,縫合傷口術畢。對照組:常規全麻俯臥位,后正中切口暴露椎板和關節突關節,打入追弓根螺釘,去除椎板進行減壓并處理椎間盤,復位椎體固定釘棒,植入融合器和自體骨,再次探查神經,沖洗留置負壓引流,術畢。
1.3 統計學方法
采用SPSS 13.0 統計軟件對數據進行處理。計量資料以均數±標準差()表示,行t檢驗;計數資料以構成比或率(%)表示,行χ2檢驗。P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者一般資料比較
兩組患者一般資料比較差異無統計學意義(P>0.05),見表1。
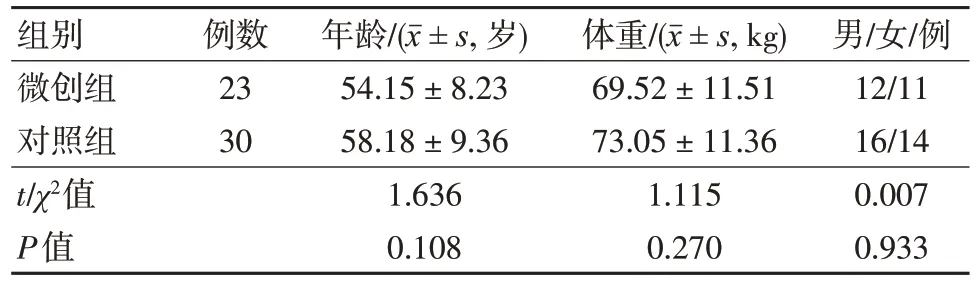
表1 兩組患者一般資料比較
2.2 兩組術前、術中、術后相關指標比較
微創組平均手術時間長于對照組,差異有統計學意義(P<0.05);微創組術中出血量少于對照組,差異有統計學意義(P<0.05);兩組患者術后1 個月、術后3 個月的VAS 評分、ODI 與術前相比均有明顯改善,差異有統計學意義(P<0.05);兩組間術前、術后1 個月及術后3 個月VAS 評分、ODI 比較差異均無統計學意義 (P>0.05)。見表2。
表2 兩組術前、術中、術后相關指標比較 ()
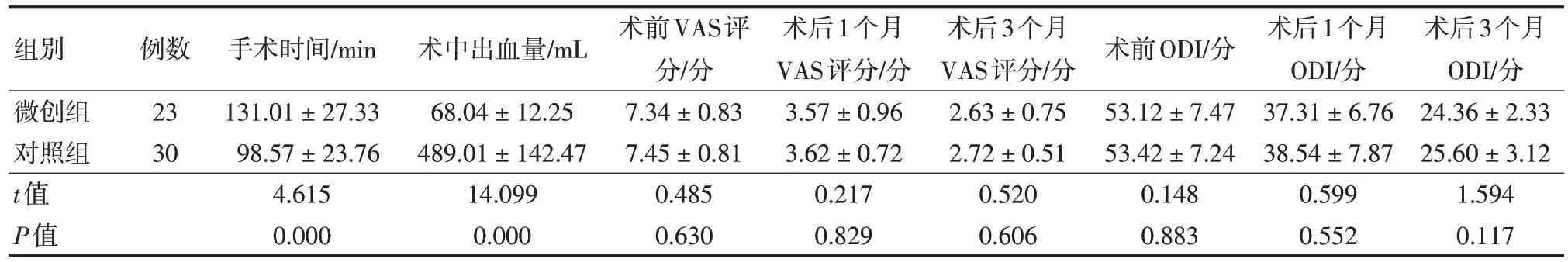
表2 兩組術前、術中、術后相關指標比較 ()
組別微創組對照組t值P值例數23 30手術時間/min 131.01±27.33 98.57±23.76 4.615 0.000術中出血量/mL 68.04±12.25 489.01±142.47 14.099 0.000術前VAS評分/分7.34±0.83 7.45±0.81 0.485 0.630術后1個月VAS評分/分3.57±0.96 3.62±0.72 0.217 0.829術后3個月VAS評分/分2.63±0.75 2.72±0.51 0.520 0.606術前ODI/分53.12±7.47 53.42±7.24 0.148 0.883術后1個月ODI/分37.31±6.76 38.54±7.87 0.599 0.552術后3個月ODI/分24.36±2.33 25.60±3.12 1.594 0.117
3 討論
腰椎滑脫病因復雜,根據病因學分為發育性和獲得性兩大類[3]。本文根據Wiltse 和Rothman分類法把腰椎滑脫分為5 個類型,其中Ⅲ型為退變性,是由于長期存在的節段間失穩所導致。伴有進展性神經障礙和步態異常的嚴重腰骶后凸為絕對適應證,相對適應證則包括輕微的非進展性神經障礙,神經根性和跛行癥狀,非手術治療無效的機械性腰痛。治療該病的目的主要有:①防止滑脫的進一步進展[4];②穩定病變節段;③矯正腰骶部后凸;④緩解腰腿疼痛;⑤逆轉神經障礙[5]。
PLIF 椎弓根螺釘內固定是目前臨床最常用的手術方式,該術式存在暴露清晰、減壓充分、易于復位等優點,但PLIF 后側肌肉剝離較多、出血量大、創傷較大,容易造成肌肉失神經支配、肌肉萎縮甚至是長期慢性腰痛。近年來以脊柱內鏡為代表的微創技術得到迅猛發展,包括后路椎間盤鏡技術和經皮椎間孔鏡技術,兩種術式在手術入路和手術適應證方面有所不同。經皮椎間孔鏡技術以楊氏脊柱內鏡技術(Yeung endoscopic spine system,YESS)和經椎間孔脊柱內鏡技術(transforaminal endoscopic spine system,TESSYS) 應用最為廣泛[6-7],但都需要在非可視下進行精準穿刺,存在穿刺技術要求高,盲視操作多,減壓范圍有限等缺點。開放手術思路下的脊柱內鏡操作則有著對穿刺定位精準度要求低,操作范圍廣、減壓充分,操作過程接近全程可視等優點[8-9]。對于習慣直視下完成開放手術的脊柱外科醫生來說更容易接受和學習。目前非融合下的椎間盤突出癥和椎管狹窄手術已經實現完全可視化操作;而鏡下腰椎融合技術也僅剩下通道下鉸刀處理椎間盤、融合器試模、融合器植入還不能完全可視。
本文中微創組患者椎體復位主要靠患者體位和追弓根螺釘的提拉,對于個別復位困難的患者可通過松解后使用鉸刀插入椎間隙進行撬撥以達到復位目的[10-11]。微創組患者手術時間相對對照組較長,這與工具效率受限,手術程序繁瑣及熟練程度不夠等因素密切相關,椎間隙終板的處理尤其費時。在手術并發癥方面,微創組1 例患者術后出現下肢麻木疼痛加重,術后6 周完全恢復,初步認為是由術中套筒壓迫出口神經根所致;對照組1 例出現腦脊液漏,術后采用頭高腳低位后傷口順利閉合。而微創組因術后均未放置引流,所以未觀察到硬膜破裂或腦脊液滲漏。
脊柱內鏡下實現退變性腰椎Ⅰ、Ⅱ度滑脫的減壓、固定與融合代表著脊柱內鏡的較高水平和未來趨勢。該微創手術與傳統開放后路手術相比早期療效顯著,雖然手術時間較長,但出血少、創傷小,患者恢復快且更容易被患者所接受。另外本研究仍存在病例有限、缺乏多中心性等不足,且由于隨訪時間較短,缺乏融合情況的相關評估,有必要進一步研究。

