84例產褥感染的臨床特點及常見致病微生物耐藥性分析
戴宜霏 余春風 孫楊芳
[摘要] 目的 研究產褥感染的危險因素及常見致病微生物耐藥情況,為臨床治療提供參考。 方法 回顧性分析我院2017年1月~2019年12月發生的84例產褥感染病例的臨床資料,與同時期未發生產褥感染的200例產婦進行對照研究,分析產褥感染的影響因素,并對分離獲得的致病微生物進行耐藥性分析。 結果 感染組妊娠糖尿病、產鉗助產、宮口開全后中轉剖宮產患者的分布率高于對照組,差異有統計學意義(P<0.05);經多因素Logistic回歸分析,妊娠糖尿病是產褥感染的獨立影響因素(P<0.05)。本研究中共檢出致病微生物40株,其中革蘭陰性菌13株(占32.50%),革蘭陽性菌10株(占25.00%),支原體16株(占40.00%),衣原體1株(占2.50%),革蘭陰性菌中以大腸埃希菌最常見,對二代頭孢菌素類抗生素耐藥率20%。革蘭陽性菌以金黃色葡萄球菌最常見,對青霉素及頭孢菌素耐藥率高,未發現對亞胺培南及萬古霉素耐藥。 結論 產鉗助產、妊娠糖尿病、宮口開全后中轉剖宮產是產褥感染可能的危險因素,其中,妊娠糖尿病是產褥感染的獨立危險因素。目前臨床常見致病微生物譜及耐藥率未發生明顯變化。
[關鍵詞] 產褥感染;妊娠糖尿病;宮口開全;產鉗助產;病原微生物
[中圖分類號] R714 ? ? ? ? ?[文獻標識碼] B ? ? ? ? ?[文章編號] 1673-9701(2020)31-0130-04
[Abstract] Objective To research the risk factors of puerperal infection and drug resistance of common pathogenic microorganisms, so as to provide reference for clinical treatment. Methods The clinical data of 84 patients with puerperal infection admitted to our hospital from January 2017 to December 2019 were analyzed retrospectively. Compared with 200 patients without puerperal infection in the same period, the related factors of puerperal infection were analyzed, and the drug resistance of isolated pathogenic microorganisms was analyzed. Results The distribution rates of patients with gestational diabetes mellitus, forceps delivery and cesarean section after uterine neck whole opened in the infection group were higher than those in the control group, and the differences were statistically significant(P<0.05). Multivariate logistic regression analysis showed that gestational diabetes mellitus was an independent impacting factor of puerperal infection(P<0.05). A total of 40 pathogenic microorganisms were detected in the research, among which 13 strains(32.50%) were Gram-negative bacteria, 10 strains(25.00%) were Gram-positive bacteria, 16 strains(40.00%) were mycoplasma and 1 strain(2.50%) was chlamydia. Escherichia coli was the most common Gram-negative bacteria, and its resistance rate to second-generation cephalosporins was 20%. Staphylococcus aureus was the most common Gram-positive bacteria, with high resistance to penicillin and cephalosporin, but no resistances to imipenem and vancomycin were found. Conclusion Birth forceps delivery, gestational diabetes mellitus, and cesarean section after uterine neck whole opened are possible risk factors of puerperal infection, and gestational diabetes mellitus is an independent risk factor of puerperal infection. At present, the spectrum and drug resistance rate of common clinical pathogenic microorganisms have not changed significantly.
[Key words] Puerperal infection; Gestational diabetes mellitus; Uterine neck whole opened; Birth forceps delivery; Pathogenic microorganism
產褥感染是分娩過程及產褥期發生的生殖道感染,可引起的局部或全身的感染性,其總體發病率為1.0%~7.2%[1-2],是導致孕產婦不良預后的主要因素。分娩過程中發生的生殖道損傷、致病微生物入侵以及產后免疫力下降是導致產褥感染率增加的原因,如未得到及時有效的控制,則可能引起盆腔炎癥疾病、繼發不孕等后遺癥,嚴重時繼發全身感染、膿毒血癥,威脅產婦生命[3]。隨著生活水平的不斷提高,妊娠糖尿病發病率逐漸增加。二胎政策開放以來,同一產婦剖宮產次數的增多,增加產褥感染的風險,疾病譜的改變及抗生素的廣泛應用引起致病微生物譜的改變,使致病微生物耐藥情況發生變化,傳統的經驗性抗感染治療效果受到影響。在目前的產科實踐中,對于如何預防孕產婦感染尚缺乏有實踐意義的、個性化的決策指導,本研究旨在通過隊列研究探討院內產褥感染的相關危險因素,同時希望通過對院內感染的主要致病微生物及其耐藥性進行分析,對今后的臨床工作提供參考。
1 資料與方法
1.1一般資料
收集2017年 1月~2019年12月我院院內發生產褥感染的孕產婦84例作為感染組,收集同一時期院內未發生產褥感染的200例產婦作為對照組。納入標準:(1)年齡20~40歲,平均(27.5±6.3)歲;孕齡37~41周;(2)符合婦產科學第8版產褥感染[4]診斷標準:產后24 h至產后10 d內,每日測體溫4次,每次間隔4 h以上,體溫有2次以上≥38℃;可伴有畏寒、寒戰、會陰或腹部傷口紅腫疼痛、滲液;下腹部或子宮體壓痛、子宮復舊不良,惡露可有異味;血常規白細胞及中性粒細胞計數增多,降鈣素原升高。排除標準[4]:(1)產前即已存在宮內感染;(2)生殖系統以外的其他系統的感染:如上呼吸道感染、肺部感染、乳腺炎等;(3)原本合并有紅斑狼瘡/強直性脊柱炎等可能引起非感染性發熱的自身免疫系統合并癥者。所有患者均簽署知情同意并符合醫院醫學倫理學原則。
1.2 方法
對上述284例產婦的臨床資料進行回顧性分析,分析產褥感染的危險因素。病原學鑒定采用病原體培養,血培養在體溫上升高峰、使用抗生素前進行采集,嚴格遵守無菌操作規范;陰道分泌物嚴格按照婦科檢測的規范采集宮腔分泌物,操作過程中嚴格執行無菌原則。采用 VITEK-2全自動細菌分析儀對細菌菌株進行分析鑒定,同時支原體、衣原體采用RNA檢測方法進行定量,藥敏試驗采用 KB紙片擴散法。
1.3 觀察指標
產婦的年齡、孕齡、分娩方式、是否產鉗助產、是否為2次或3次以上剖宮產;產婦妊娠期和分娩期是否有妊娠糖尿病、妊娠高血壓、前置胎盤、胎膜早破、胎盤早剝、第二產程延長、急產、產后出血等合并癥及并發癥。
1.4 統計學方法
采用 SPSS 22.0統計學軟件進行數據分析,計數資料以[n(%)]表示,采用χ2檢驗,多因素分析采用Logistic回歸分析,P<0.05為差異有統計學意義。
2 結果
2.1 兩組的臨床資料比較
感染組產婦的平均年齡為(27.6±4.7)歲,孕齡為(39.1±0.8)周,對照組產婦平均年齡為(27.2±5.0)歲,孕齡為(39.1±0.8)周;兩組產婦的平均年齡、孕齡均符合正態分布(P均>0.05),具有可比性。
2.2 產褥感染的單因素分析
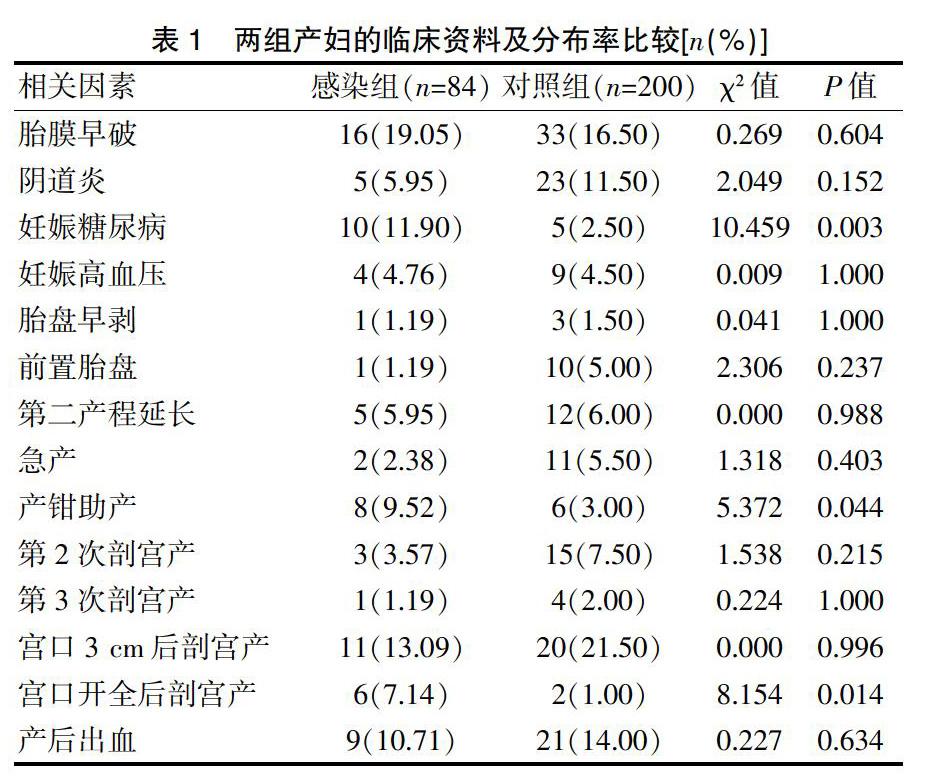
兩組胎膜早破、陰道炎、妊娠高血壓、胎盤早剝、前置胎盤、第二產程延長、急產、產后出血等產科并發癥或合并癥的分布率比較,差異無統計學意義(P>0.05),見表1;兩組多次剖宮產產婦的分布率比較,差異無統計學意義(P均>0.05)。感染組妊娠糖尿病、產鉗助產、宮口開全后剖宮產的分布率顯著高于對照組,差異有統計學意義(P<0.05)。故產鉗助產、妊娠糖尿病、陰道試產失敗宮口開全后中轉剖宮產是產褥感染的危險因素。
2.3產褥感染的多因素分析
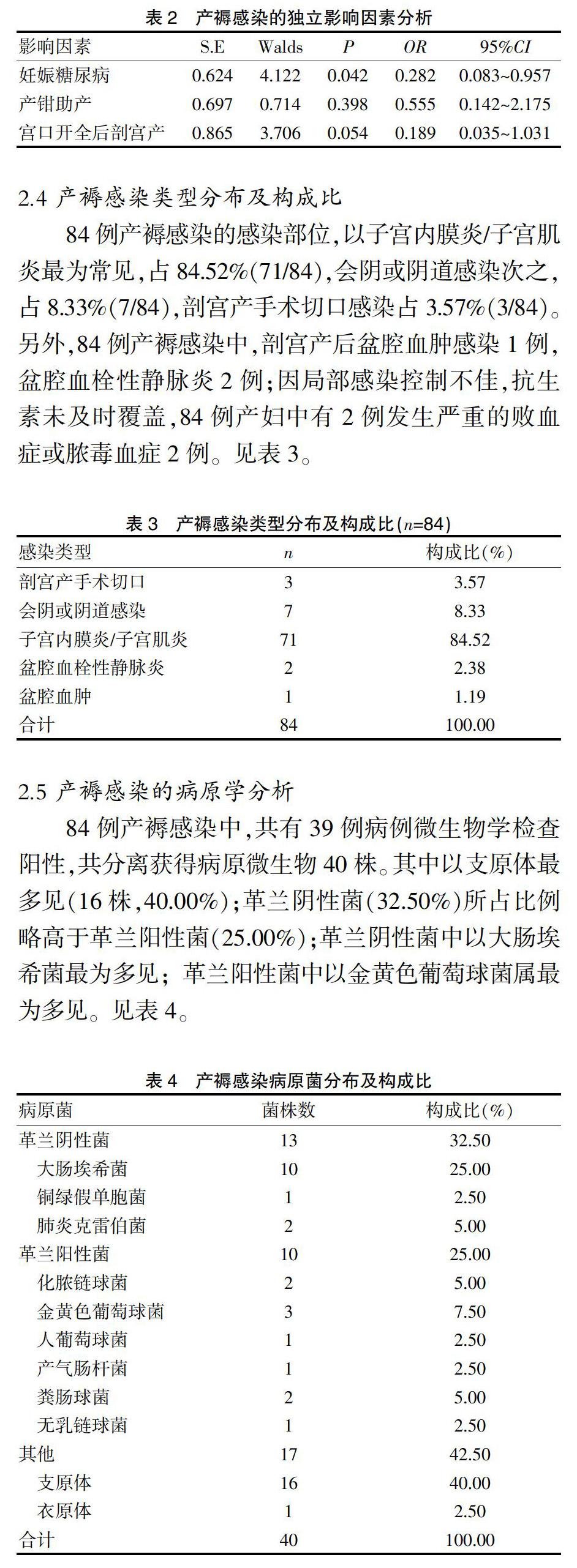
經多因素Logistic回歸分析發現,妊娠糖尿病是發生產褥感染的獨立危險因素(OR=0.282,P<0.05)。見表2。
2.4 產褥感染類型分布及構成比
84例產褥感染的感染部位,以子宮內膜炎/子宮肌炎最為常見,占84.52%(71/84),會陰或陰道感染次之,占8.33%(7/84),剖宮產手術切口感染占3.57%(3/84)。另外,84例產褥感染中,剖宮產后盆腔血腫感染1例,盆腔血栓性靜脈炎2例;因局部感染控制不佳,抗生素未及時覆蓋,84例產婦中有2例發生嚴重的敗血癥或膿毒血癥2例。見表3。
2.5 產褥感染的病原學分析
84例產褥感染中,共有39例病例微生物學檢查陽性,共分離獲得病原微生物40株。其中以支原體最多見(16株,40.00%);革蘭陰性菌(32.50%)所占比例略高于革蘭陽性菌(25.00%);革蘭陰性菌中以大腸埃希菌最為多見;革蘭陽性菌中以金黃色葡萄球菌屬最為多見。見表4。
2.6 產褥感染的致病微生物耐藥性分析
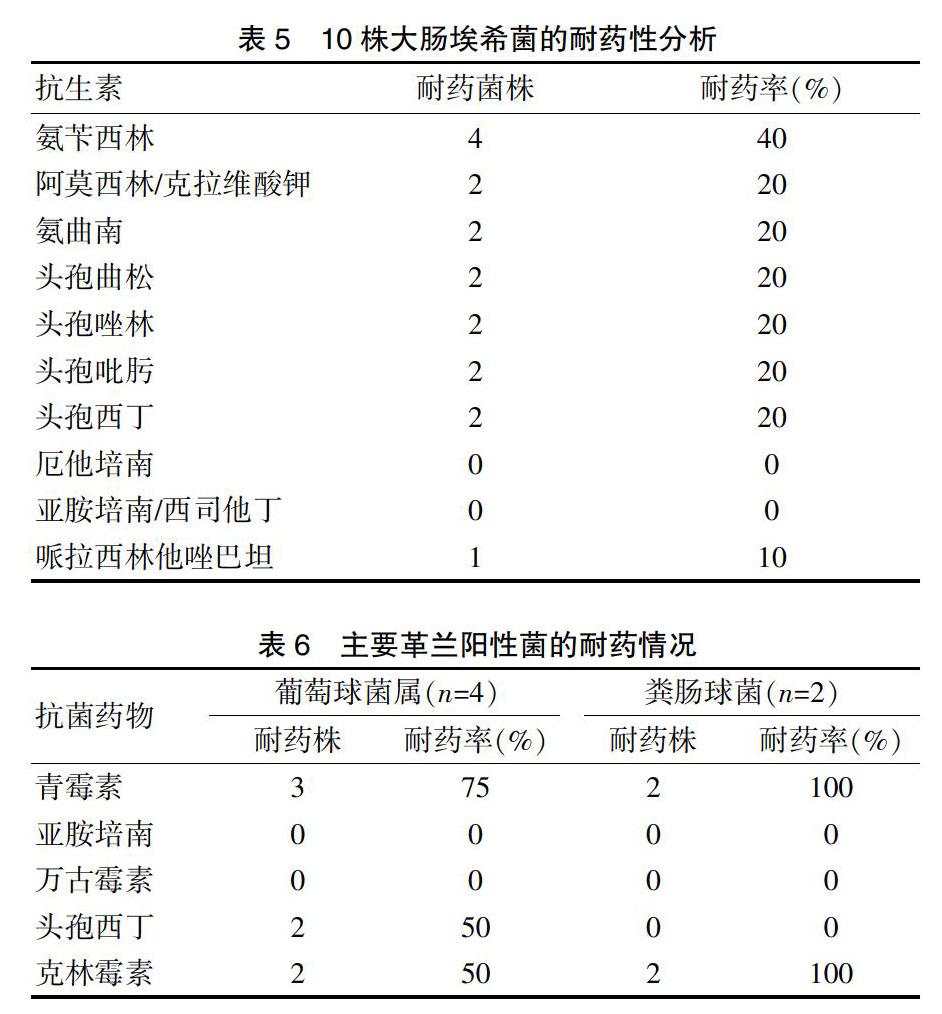
我院分離得到的大腸埃希菌對氨芐西林耐藥率較高,為40%,對頭孢西丁、頭孢唑林、頭孢曲松等產科常用二代、三代頭孢類抗生素的耐藥率均為20%,對哌拉西林他唑巴坦的耐藥率為10%,未發現對亞胺培南/西司他丁耐藥。革蘭陽性菌對青霉素幾乎不敏感,未發現對萬古霉素及亞胺培南耐藥。見表5~6。
3討論
妊娠相關的敗血癥占全球婦女死亡原因的11%[5],雖然隨著醫學水平的不斷提高,妊娠相關的感染在發達地區有所下降,但仍是僅次于產后出血及妊娠高血壓造成妊娠婦女死亡的主要原因。本研究結果顯示,感染組妊娠糖尿病、產鉗助產、宮口開全后剖宮產的分布率顯著高于對照組(P<0.05),故認為產鉗助產、妊娠糖尿病、陰道試產失敗宮口開全后中轉剖宮產是產褥感染的危險因素。本研究中納入的感染病例中有1例產鉗助產時發生會陰直裂,術后會陰創面膿性滲液;另有1例產鉗助產患者發生會陰Ⅲ度裂傷,縫線穿透直腸,術后出現會陰創面膿液培養獲得大腸埃希菌。目前大部分觀點認為,產鉗助產分娩的患者往往有第二產程延長或胎兒窘迫等不良因素,較長的陰道試產會加重產婦疲勞,導致免疫功能下降,同時傷口暴露時間過長,胎先露對產道長時間擠壓,會陰側切也會引起陰道及會陰組織缺血、水腫,增加感染機率[6]。另外,在產鉗助產過程中,醫護人員不規范的操作及多次的內診可能增加生殖道定植細菌逆行感染的發生率[7],因此助產時規范的操作、適當應用抗生素預防感染對減少產褥感染可能有積極意義。
近年隨著我國生活水平不斷提高,妊娠糖尿病的發生率逐年增長,現已成為妊娠期最常見的合并癥之一[8],國內大部分研究認為,妊娠糖尿病增加產褥感染風險[9],其可能的機制有妊娠期孕婦機體分泌過多的胰島素拮抗激素,引起糖耐量下降,血糖水平升高,抑制中性粒細胞的趨化、游走以及吞噬病原體的功能[10];糖尿病機體蛋白質合成減少,分解加快,使免疫球蛋白、補體、抗體等生成減少,淋巴細胞轉換率降低,導致機體免疫功能低下;另外,高血糖水平有利于細菌繁殖[11]。本研究對產褥感染危險因素進一步行多因素回歸分析,認為妊娠糖尿病是產褥感染的獨立危險因素(P<0.05)。
目前國內外對于剖宮產的時機與產褥感染之間的關系研究較少,有觀點認為[12]產程停滯后剖宮產使產褥感染發生率上升。本研究結果顯示,感染組宮口開3 cm后(不包含宮口開全病例)中轉剖宮產患者的分布率與對照組比較,差異無統計學意義,但宮口開全后行剖宮產患者的分布率顯著高于對照組(P<0.05),經進一步多因素回歸分析認為宮口開全后中轉剖宮產可能顯著增加產褥感染的發生率(P=0.054)。這可能與宮口開全后中轉剖宮產患者經歷了較長時間陰道試產、多次內診、會陰陰道組織受壓水腫、組織脆性增加有關,增加感染發生率。在本研究中有1例患者宮口開全后,因持續性枕后位行徒手轉胎頭失敗而中轉剖宮產,同時并發嚴重陰道裂傷,術后陰道創面繼發感染。
有研究[13]認為,胎膜早破可使陰道正常防御系統遭到破壞,感染機率增加,且胎膜早破距離分娩的時間越長,產褥感染的機率越增加,尤其是胎膜早破距離分娩時間超過48 h者,產婦產后感染的風險顯著增加[14-15]。但本研究結果顯示,胎膜早破在感染組中的分布率與對照組無統計學差異,與Baser 等[16]的研究一致。二胎生育開放以來,孕產婦多次剖宮產數量急劇上升,曾有研究顯示,瘢痕子宮再次剖宮產患者術中及術后出血量、產褥感染風險均顯著增加[17]。本研究中產褥感染組與對照組的多次剖宮產分布率無統計學差異,這可能與本研究中納入的三次剖宮產樣本例數較少有關。但值得一提的是,本研究中有1例第三次剖宮產患者,術中盆腔見廣泛炎癥滲出病灶,術后繼發盆腔血腫、敗血癥。因此,胎膜早破及多次剖宮產是否增加母兒感染風險尚需更大樣本研究以明確。
本研究中大部分感染均局限于局部組織或臟器,但有3例發生敗血癥或膿毒血癥,其中1例發生膿毒休克。故及時合理使用敏感的抗生素,對于防止感染擴散尤為重要。本研究對院內感染的致病微生物進行分析,以支原體感染最為常見,解脲支原體可導致羊膜腔內感染[18],增加產后發熱風險[19]。對于院內感染的致病菌,目前仍以革蘭陰性菌為主[20],但革蘭陽性菌占比有所上升(25%),其各自最常見的致病菌仍是大腸埃希菌及金黃色葡萄球菌,上述致病菌的分布情況與國內大部分院內感染調查結果一致,且抗生素的耐藥情況未發生明顯變化[21-23]。
[參考文獻]
[1] Dior UP,Kogan L,Elchalal U,et al. Leukocyte blood count during early puerperium and its relation to puerperal infection[J]. J Matern Fetal Neonatal Med,2014,27(1):18-23.
[2] Creanga AA,Syverson C,Seed K,et al. Pregnancy-Related Mortality in the United States,2011-2013[J]. Obstet Gynecol,2017,130(2):366-373.
[3] Bonet M,Ota E,Chibueze CE,et al. Routine antibiotic prophylaxis after normal vaginal birth for reducing maternal infectious morbidity[J]. Cochrane Database Syst Rev,2017,13:21-37.
[4] 沈鏗,馬丁. 婦產科學(8年制)[M]. 3版. 北京:人民衛生出版社,2015:113-114.
[5] Say L,Chou D,Gemmill A,et al. Global causes of maternal death:A WHO systematic analysis[J]. The Lancet Global Health,2014, 2(6):e323-e333.
[6] 陳佳,羅欣,王龍瓊. 第二產程時間對產后盆底肌力的影響[J]. 實用婦產科雜志,2016,32(1):27-29.
[7] 朱慧芳. 產褥感染的相關因素及預防措施[J]. 中華醫院感染學雜志,2012,22(16):3531.
[8] Ma RCW. Epidemiology of diabetes and diabetic complications in China[J]. Diabetologia,2018,61(6):1249-1260.
[9] 李靜,張富貴,馮琦珍. 圍產期感染相關因素調查分析[J].陜西醫學雜志,2015,44(1):115-116.
[10] Freire MO,Dalli J,Serhan CN,et al. Neutrophil resolvin E1 receptor expression and function in type 2 diabetes[J]. J Immunol,2017,198(2):718-728.
[11] 陳榮月. 糖尿病患者醫院感染危險因素分析[J].中國醫院感染雜志,2002,12:8-10.
[12] Henry DE,Cheng YW,Shaffer BL,et al. Perinatal outcomes in the setting of active phase labor arrest[J]. Obstet Gynecol,2008,112:1109-1115.
[13] Romanik M,Nowosielski K,Poreba R,et al. Streptococcus group B serotype distribution in anovaginal isolates of women in term pregnancy[J]. Neuro Endocrinol Lett,2014,35(4): 301-305.
[14] Navathe R,Schoen CN ,Heidari P,et al. ?Azithromycin versus erythromycin for the management of preterm premature rupture of membranes[J]. Am J Obstet Gynecol,2019, 221(2): 144.e1-e8.
[15] Dundar B,Cakmak BD,Ozgen G,et al. Platelet indices in preterm premature rupture of membranes and their relation with adverse neonatal outcomes[J]. J Obstet Gyaecol Res,2018,44(1):63-67.
[16] Baser E,Aydogan KD,Ulubas ID,et al. The effects of latency period in PPROM cases managed expectantly[J]. J Matern Fetal Neonatal Med,2020,23:1-10.
[17] 曹利娟. 疤痕子宮妊娠再次剖宮產臨床分析[J]. 河南外科學雜志,2014,20(2):66-67.
[18] Kwak DW,Hwang HS,Kwon JY,et al. Co-infextion with vaginal Ureaplasma urealyticum and Mycoplasma hominis increase adverse pregnancy outcomes in patients with preterm labor or preterm premature rupture of membranes[J]. J Matern FETAL Neonatal Med,2014,27(4):333-337.
[19] Lamey JR,Eschenbach DA,Mitchell SH,et al. Isolation of mycoplasmas and bacteria from the blood of postpartum women[J]. Am J Obstel Gynecol,1982,143(1):104-112.
[20] 柯明輝,陸興,張培倫,等. 北京地區近年支原體耐藥情況分析[J]. 中國性學雜志,2018,27(12):122-126.
[21] 房桂青,劉俊平. 婦幼保健機構大腸埃希菌感染的臨床分布及耐藥性分析[J].中華醫院感染學雜志,2017, 27(2):402-403.
[22] 常蕊,王楠,高燕云,等. 產褥期感染患者病原菌分布及耐藥性分析[J].中華醫院感染學雜志,2017,27(20):4758-4760.
[23] 池鴻斐,葉可君,陳雅,等. 糖尿病孕婦分娩會陰切口感染相關因素分析[J].中華醫院感染學雜志,2017,27(16): 3775-3778.
(收稿日期:2020-05-06)

