小茴香揮發油提取工藝優化及抗氧化研究
馬延紅,孫僑生,段志芳,劉文華
(肇慶學院 生命科學學院,廣東 肇慶 526061)
小茴香(FoeniculumvulgareMill.)為傘形科茴香屬多年生草本植物茴香的干燥成熟果實,具有散寒止痛、理氣和胃的功效[1],是《中國藥典》收載的一味傳統中藥,也常作為調味品和香料使用,主要含有揮發油、生物堿、黃酮、脂肪酸、甾醇和糖苷等多種類型的化合物[2]。
揮發油是小茴香的主要有效成分之一,也是發揮生理活性的重要物質基礎[3]。主要是單萜類化合物和苯丙烷類化合物,反式茴香腦作為小茴香揮發油的主要成分,相對含量可達到65%~80%[4]。此類化合物存在于小茴香內,具有強烈的茴香香味,并可隨水蒸氣揮發[5,6]。水蒸氣蒸餾法具有操作簡便、成本低、無溶劑殘留等優點[7],且對揮發油中的微量成分提取效率高,可以得到絕大部分的揮發性香氣成分[8],在小茴香揮發油提取方法中占據優勢,是目前提取小茴香揮發油的主要方法。但水蒸氣蒸餾法的提取效率容易受到物料粉碎粒度、料液比、浸泡時間、提取時間等多種因素的影響。因此,本試驗以小茴香為原料,采用水蒸氣蒸餾法研究不同提取條件對小茴香揮發油提取率的影響,確定最佳提取工藝,為小茴香精油的產業化生產提供一定的參考。同時,利用體外抗氧化試驗測定小茴香精油的總還原能力、羥自由基清除率和DPPH清除率,評定其體外抗氧化能力。
1 材料與方法
1.1 材料與試劑
小茴香:廣州市清平藥材市場;抗壞血酸標準品:廣東光華科技股份有限公司;DPPH:上海源葉生物科技有限公司。
1.2 儀器與設備
BSA124S-CW型電子天平 賽多利斯公司;Q-800D型高速萬能粉碎機 上海冰都電器有限公司;DK-98-II型電爐 天津泰斯特儀器有限公司。
1.3 試驗方法
1.3.1 小茴香揮發油提取工藝優化
1.3.1.1 小茴香揮發油提取流程
將小茴香粉碎、過篩,加入浸提劑,用水蒸氣蒸餾法(依據試驗設計選擇不同的粉碎粒度、料液比、浸泡時間和蒸餾時間)提取小茴香揮發油。經水油分離、無水硫酸鈉除水后,密封保存于4 ℃冰箱中備用。
1.3.1.2 單因素試驗
本試驗選取不同的料液比、粉碎粒度、浸泡時間和蒸餾時間等因素進行單因素試驗。
料液比的確定:準確稱取10 g小茴香粉末,過20目篩,分別加入150,200,250,300 mL蒸餾水作提取溶劑,固定粉碎粒度為20目,浸泡時間為0 h,蒸餾時間為3 h,在以上條件下提取小茴香揮發油。
粉碎粒度的確定:準確稱取10 g小茴香粉末,分別過20,50,60,100目篩,加入250 mL蒸餾水作提取溶劑,固定料液比為1∶25,浸泡時間為0 h,蒸餾時間為3 h,在以上條件下提取小茴香揮發油。
浸泡時間的確定:準確稱取10 g小茴香粉末,過20目篩,加入250 mL蒸餾水作提取溶劑,分別浸泡0,1,2,3 h后提取,固定料液比為1∶25,粉碎粒度為20目,蒸餾時間為3 h,在以上條件下提取小茴香揮發油。
蒸餾時間的確定:準確稱取10 g小茴香粉末,過20目篩,加入250 mL蒸餾水作提取溶劑,固定料液比為1∶25,粉碎粒度為20目,浸泡時間為0 h,分別蒸餾3,4,5,6 h,在以上條件下提取小茴香揮發油。
1.3.1.3 正交試驗
利用正交試驗設計優化小茴香揮發油的提取工藝,在以上4個單因素試驗中,選擇溶劑料液比、物料粉碎粒度、浸泡時間和蒸餾時間進行四因素三水平正交試驗。
1.3.2 抗氧化活性的測定
1.3.2.1 DPPH法
稱取不同量的揮發油于50 mL的容量瓶中,用95%乙醇將樣品配制成0.4,0.8,2.0,4.0,8.0 mg/mL不同濃度的樣品溶液,將1 mL上述藥液加入2 mL濃度為0.5 mmol/L的DPPH 溶液,室溫遮光放置30 min,反應完全后,于517 nm波長處測其吸光度,每個試樣做3個平行樣,取平均值。用對應濃度的抗壞血酸作為陽性對照組,并以抗壞血酸濃度和自由基清除率做標準曲線。樣品結果以每克樣品中所含抗壞血酸相當量來表示[9]。
DPPH清除率=[(A0-A1)/A0]×100%。
式中:A0為未加藥時DPPH溶液的吸光度;A1為抗壞血酸溶液或樣品溶液加DPPH溶液的吸光度。
1.3.2.2 總還原能力的測定
采用鐵氰化鉀還原法[10]。稱取0.4,0.8,2.0,4.0,8.0 mg/mL不同濃度的小茴香揮發油溶液各1 mL加入試管中,依次加入2.5 mL的PBS溶液和2.5 mL 1%的K3Fe(CN)6,混勻,于50 ℃恒溫水浴20 min,加入10% 三氯乙酸溶液2.5 mL,用轉速為3000 r/min的離心機離心10 min,取上清液2.5 mL,再加入2.5 mL蒸餾水和0.5 mL 0.1%的FeCl3溶液,混勻,室溫放置10 min后,于700 nm波長下測其吸光度,每個試樣做3個平行樣,取平均值。以與藥液同樣濃度的抗壞血酸作為陽性對照。
1.3.2.3 羥自由基清除率[11]
取5支10 mL試管,分別加入0.4,0.8,2.0,4.0,8.0 mg/mL不同濃度的小茴香揮發油溶液,再依次向各試管中加入2 mL 6 mmol/L的FeSO4溶液、2 mL 6 mmol/L的H2O2溶液,搖勻后,室溫靜置10 min。再向各試管中加入2 mL 6 mmol/L的水楊酸-乙醇溶液,搖勻,置于50 ℃恒溫水浴30 min,于510 nm波長下測定其吸光度,每個樣品測3個平行樣,取平均值。以與藥液同樣濃度的抗壞血酸作為陽性對照,并以抗壞血酸濃度和自由基清除率做標準曲線。樣品結果以每克樣品中所含抗壞血酸相當量來表示。
羥自由基清除率=[1-(A1-A2)/A0]×100%。
式中:A0為95%乙醇溶液的吸光度;A1為抗壞血酸溶液或樣品溶液的吸光度;A2為用95%乙醇代替水楊酸時樣品溶液的吸光度。
2 結果與分析
2.1 單因素試驗結果
2.1.1 料液比的確定
不同比例的料液比對小茴香揮發油提取率的影響見圖1。
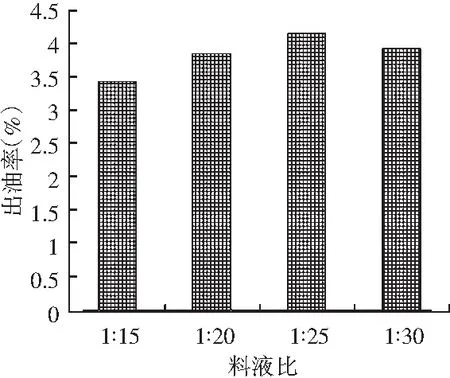
圖1 不同料液比對小茴香揮發油提取率的影響Fig.1 Effect of different ratios of solid to liquid on extraction rates of volatile oils from Foeniculum vulgare Mill.
由圖1可知,當料液比為1∶15~1∶30,揮發油提取率呈現先上升后下降的趨勢,且當料液比為1∶25時,揮發油的得率最大。因此,選擇料液比1∶20、1∶25、1∶30 3個水平進行下一步正交試驗。
2.1.2 粉碎粒度的確定
不同粉碎粒度對小茴香揮發油提取率的影響見圖2。
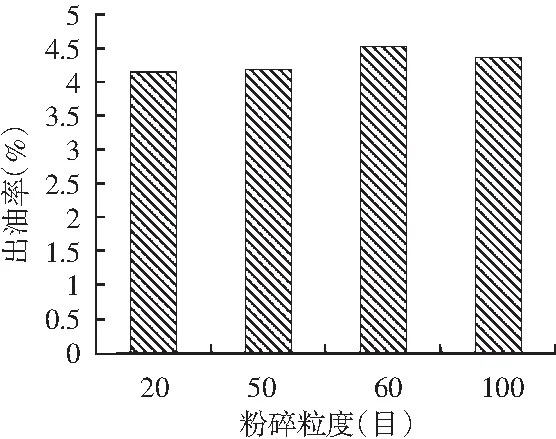
圖2 不同粉碎粒度對小茴香揮發油提取率的影響Fig.2 Effect of different crushing particle size on extraction rates of volatile oils from Foeniculum vulgare Mill.
由圖2可知,在20,50,60,100目條件下,粉碎粒度對小茴香揮發油提取率的影響較小,當粉碎粒度為60目時,揮發油得率最大。選擇50,60,100目3個水平進行正交試驗。
2.1.3 浸泡時間的確定
揮發油提取過程中,浸泡與否及浸泡時間長短會影響揮發油的得率。不同浸泡時間對小茴香揮發油提取率的影響見圖3。
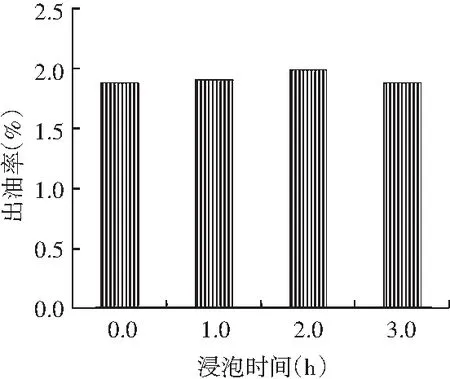
圖3 不同浸泡時間對小茴香揮發油提取率的影響Fig.3 Effect of different soaking time on extraction rates of volatile oils from Foeniculum vulgare Mill.
由圖3可知,當浸泡時間分別為0,1,2,3 h時,揮發油提取率呈先上升后下降的趨勢,但變化較平穩,且在浸泡時間為2 h時,揮發油得率最大。選擇1,2,3 h 3個水平進行下一步正交試驗。
2.1.4 蒸餾時間的確定
不同蒸餾時間對小茴香揮發油提取率的影響見圖4。

圖4 不同蒸餾時間對小茴香揮發油提取率的影響Fig.4 Effect of different distillation time on extraction rates of volatile oils from Foeniculum vulgare Mill.
由圖4可知,當蒸餾時間為3,4,5,6 h時,小茴香揮發油提取率呈緩慢上升趨勢,且當蒸餾時間為6 h時,揮發油得率最大。因此,選擇4,5,6 h 3個水平進行正交試驗。
2.2 正交試驗設計及結果
正交試驗因素水平見表1,正交試驗結果見表2。

表1 小茴香揮發油提取工藝因素水平Table 1 The factors and levels of extraction process of volatile oils from Foeniculum vulgare Mill.

表2 小茴香揮發油提取正交試驗設計與結果分析Table 2 Orthogonal test design and results analysis of volatile oils extraction from Foeniculum vulgare Mill.
以揮發油得率為指標,由表2可知,在小茴香揮發油提取過程中,各因素對揮發油得率的影響大小依次是A>D>C>B,即蒸餾時間>粉碎粒度>浸泡時間>料液比。正交試驗結果表明,小茴香揮發油提取的最佳工藝條件是A3B2C1D3,即蒸餾時間為6 h,料液比為1∶25,浸泡時間為1 h,粉碎粒度為100目時,結果最優。結合試驗中的揮發油提取率結果,證實了在該組合條件下,揮發油得率為3.6412%,優于其他試驗組合。
2.3 體外抗氧化活性測定結果
2.3.1 清除DPPH自由基和羥自由基的能力
通過測定小茴香揮發油對DPPH自由基的清除率和對羥自由基的清除率,評價其體外抗氧化活性。研究結果表明,小茴香揮發油具有較好的體外抗氧化活性,見表3。
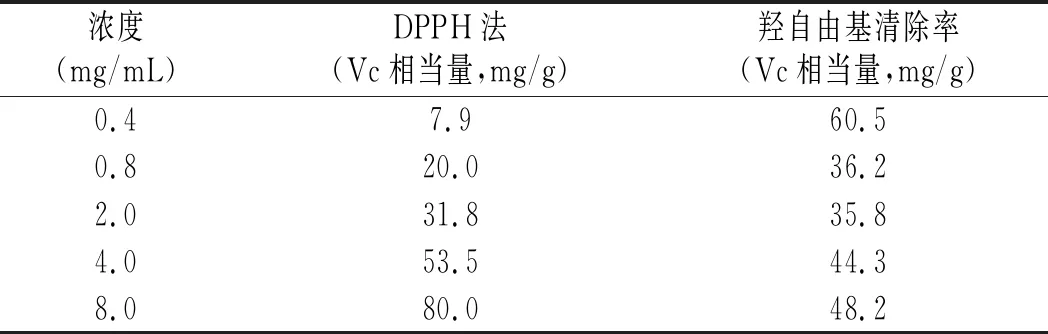
表3 小茴香揮發油清除自由基能力Table 3 The ability of Foeniculum vulgare Mill. volatile oils to scavenge free radicals
小茴香揮發油的抗氧化能力以Vc當量來表示,由表3可知,在0.4,0.8,2.0,4.0,8.0 mg/mL濃度下,小茴香揮發油對自由基清除率(DPPH法)用Vc相當量表示分別為7.9,20.0,31.8,53.5,80.0 mg/g;對羥自由基清除率用Vc相當量表示分別為60.5,36.2,35.8,44.3,48.2 mg/g。
2.3.2 總還原能力
總還原能力的測定是利用樣品的抗氧化性,將赤血鹽還原后,再與Fe3+作用,生成普魯士藍,以普魯士藍的生成量表示樣品的還原能力,并以吸光度值來表示,吸光度值越高,說明樣品的還原能力越強[12]。
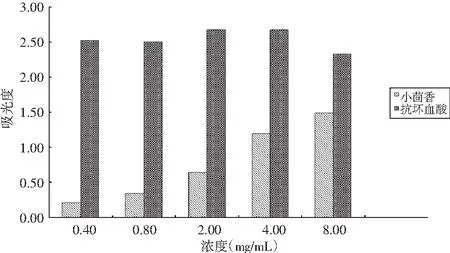
圖5 小茴香揮發油與抗壞血酸總還原能力的比較Fig.5 Comparison of total reducing capacity between volatile oils of Foeniculum vulgare Mill. and ascorbic acid
由圖5可知,小茴香揮發油的還原能力與濃度呈正相關關系,濃度越高,還原能力越強。以抗壞血酸為陽性對照,以此來評價小茴香揮發油的總還原能力。
3 結論
通過單因素試驗和正交試驗方法優化水蒸氣蒸餾法提取小茴香揮發油的提取工藝,最佳提取條件為:蒸餾時間為6 h,料液比為1∶25,浸泡時間為1 h,粉碎粒度為100目。在此條件下提取小茴香揮發油,出油率為3.6412%。并采用3種體外抗氧化活性檢測方法(DPPH法、羥自由基清除率、總還原能力測定)評價小茴香揮發油的抗氧化活性,結果表明:小茴香揮發油具有一定的抗氧化性,且濃度與其抗氧化活性基本呈現正相關性。本研究通過優化小茴香揮發油的提取工藝,為小茴香揮發油的加工生產和科學合理利用提供了一定的理論基礎。小茴香揮發油的抗氧化活性研究對于天然食品來源的抗氧化劑和保鮮劑的開發利用提供了理論依據和支持[13]。同時,小茴香不管是作為常用中藥還是日常調味品,都在人們的生活中占據著重要地位。通過研究小茴香揮發油的體外抗氧化活性對于深入探究其藥用價值具有重要的科學意義。

