我國市場上UHT滅菌乳和巴氏殺菌乳中四種獸藥殘留風險評估
喬勤勤 文 芳 鄭 楠 王加啟 程建波 薛秀恒
(1.安徽農業大學 茶與食品科技學院,合肥 230036; 2.中國農業科學院 北京畜牧獸醫研究所/農業農村部奶及奶制品質量安全控制重點試驗室/ 農業農村部奶產品質量安全風險評估試驗室(北京),北京 100193; 3.安徽農業大學 動物科技學院,合肥 230036)
在奶牛養殖過程中使用獸藥可預防和治療奶牛疾病,提高養殖業生產率[1-3]。然而,獸藥使用不當或休藥時間不足可能會導致牛奶中出現獸藥殘留,危害消費者健康,如引起過敏反應、導致耐藥性增強和致癌等[4-8]。一般獸藥在熱處理下具有高穩定性,獸藥殘留很容易從生鮮乳中轉移到超高溫滅菌乳(UHT乳)和巴氏殺菌乳中[9-11]。因此,歐盟(The European Union)、食品法典委員會(The Codex Alimentarius Commission)和我國農業農村部分別對牛奶中獸藥的最大殘留限量(Maximum residue limits)作出了明確的規定[12-14]。我國農業農村部235公告中明確規定牛奶中氟喹諾酮(Quinolones)、四環素(Tetracyclines)、鏈霉素(Streptomycin)和林可霉素(Lincomycin)的最高殘留限量分別為100、100、200和150 μg/kg[14]。
以酶聯免疫吸附試驗(ELISA)為基礎的可視化微陣列檢測技術作為一種快速、高特異性的分析牛奶中獸藥殘留方法,與傳統檢測方法如液相色譜法(LC)、液相色譜質譜聯用法(LC-MS/MS)和ELISA等相比較,具有操作簡便、特異性強、檢測速度快、檢測通量大,可同時檢測牛奶中多種殘留物等優點[15-18]。該檢測技術已成功應用于檢測多種目標物分析中,如抗生素殘留、硝基呋喃代謝物和乳鐵蛋白等[19-21]。
目前,對我國市場上牛奶中四環素和喹諾酮的殘留進行風險評估的報道較少[22-23],缺乏對于牛奶中鏈霉素和林可霉素的殘留分析的相關研究。因此,本研究擬以從我國25 個省(市)中采集的150 份UHT滅菌乳樣品和50 份巴氏殺菌乳樣品為研究對象,采用ELISA可視化微陣列芯片檢測試劑盒檢測我國奶牛養殖過程中常用的氟喹諾酮、四環素、鏈霉素和林可霉素類等4 種獸藥殘留并進行分析,以檢測我國市場上UHT滅菌乳樣品和巴氏殺菌乳樣品中獸藥殘留并分析風險水平。
1 材料與方法
1.1 樣品采集
2017年3—9月,本課題組分別從我國北京、天津、河北、上海、山東、山西、陜西、湖北、河南、江蘇、江西、浙江、安徽、四川、重慶、甘肅、黑龍江、遼寧、內蒙古、寧夏、新疆、福建、廣東、廣西和云南等25 個省(市)的超市共收集了150 份UHT滅菌乳樣品和50 份巴氏殺菌乳樣品。在分析之前,將UHT滅菌乳樣品在室溫下儲存,巴氏殺菌乳樣品在4 ℃下儲存。所有分析均在樣品保質期到期之前完成。
1.2 試劑及儀器
芯片掃描儀(MRS-4800QA,上海中晶科技有限公司,中國),氮吹濃縮儀(N1-Automatic Nitrogen Concentrator,上海屹堯儀器科技發展有限公司,中國),渦旋振蕩器(Vortex- Genie 2,Scientific Industries,美國),恒溫震蕩孵育器(MTS-2,南京祥中生物科技有限公司,中國),ELISA可視化微陣列芯片檢測試劑盒(南京祥中生物科技有限公司,中國)。
氟喹諾酮、四環素、鏈霉素和林可霉素混合標準液、抗體工作液、二抗工作液、顯色液A、顯色液B、終止液、10×濃縮復溶液、20×濃縮洗滌液、10×濃縮標準液,均購自南京祥中生物科技有限公司。乙酸乙酯(分析純)和正己烷(分析純)購自國藥集團化學試劑有限公司。
1)配制洗滌工作液:去離子水20×濃縮洗滌液按1∶19體積比進行稀釋用于芯片板的洗滌,于 4 ℃ 儲存。
2)配制復溶工作液:去離子水10×濃縮復溶液按1∶9體積比進行稀釋用于芯片板的洗滌,于4 ℃儲存。
3)配制標準工作液:復溶工作液按照1∶9的體積比例稀釋10×濃縮標準液,現配現用。
分析成像結果可以發現,異常出現在兩個球體中央靠近左側質量比較小的球體,這就說明該成像技術在比較淺的地層中異常越明顯,和單個球體成像結果相同。但這種模型對小質量異常體表現得更加明顯,總而言之,這樣的成像技術適合淺源礦體勘探。
1.3 試驗方法
1.3.1樣品前處理
移取1.00±0.05 mL牛奶樣品至50 mL聚苯乙烯離心管中,加入6 mL乙酸乙酯,2 500 r/m轉速下渦旋振蕩,5 000 r/m轉速下離心10 min。離心后,移取3 mL乙酸乙酯至10 mL干凈干燥的玻璃試管中,于50 ℃下用氮吹儀吹干。加入1 mL正己烷,用振蕩儀(2 000 r/m)振蕩1 min。再加入500 μL復溶工作液,用振蕩儀(2 000 r/m)振蕩3 min。移入2 mL聚苯乙烯于離心管中,在 5 000 r/m 轉速條件下離心10 min。去除上層有機相,取下層水相25 μL用于分析。
1.3.2檢測牛奶中四種獸藥殘留
采用ELISA可視化微陣列芯片試劑盒同時檢測牛奶中氟喹諾酮、四環素、鏈霉素和林可霉素殘留。本試驗檢測方法按照試劑盒的說明書進行。方法概要如下:
1)使用前,將試劑盒置于室溫(20~25 ℃)下平衡30 min以上,搖勻所有液體試劑并避光儲存。
2)在微孔支架中插入足夠數量的芯片微孔條,以容納所有標準品、對照品和樣品。并按照對應微孔按序編號,每個標準品、對照品和樣品均做雙孔平行。
3)加樣:依次加入25 μL樣品或標準品和 25 μL 抗體工作液到各自的微孔中,用蓋板膜封板,輕輕振蕩混勻,25 ℃ 600 r/m 振蕩反應30 min。
4)洗板:將液體從孔中倒出,然后將微孔支架上下顛倒3 次,放在吸水紙上以完全除去液體。用250~300 μL洗滌緩沖液填充所有微孔,并如上步驟中所述倒出液體,重復洗滌3 次。
5)向每個孔中加入50 μL二抗溶液,用蓋板膜封板,輕輕振蕩混勻,37 ℃ 600 r/m振蕩速度下反應30 min。取出并重復洗板操作。
6)顯色:將顯色液A和顯色液B以1∶1混合均勻。每孔加入混合液50 μL,37 ℃ 600r/m避光孵育12 min。重復洗板操作。
7)測定:對于比色成像和信號采集,使用微陣列定制的芯片掃描儀(灰度從0到65,535任意單位,分辨率為3 200 dpi)掃描和分析96 孔板,同時進行成像和數據采集,檢測結果報告將自動生成。
本試驗所采用的試劑盒對牛奶中氟喹諾酮、四環素、鏈霉素和林可霉素殘留的檢測限(Limit of detection,LOD)分別為5.00、10.00、10.00和10.00 μg/L,低于檢測限則判定為未檢出。本試驗首先對試劑盒的相關參數進行驗證分析,以確保試驗的準確性。試驗中4 種獸藥標準品濃度見表1,試劑盒相關參數見表2。
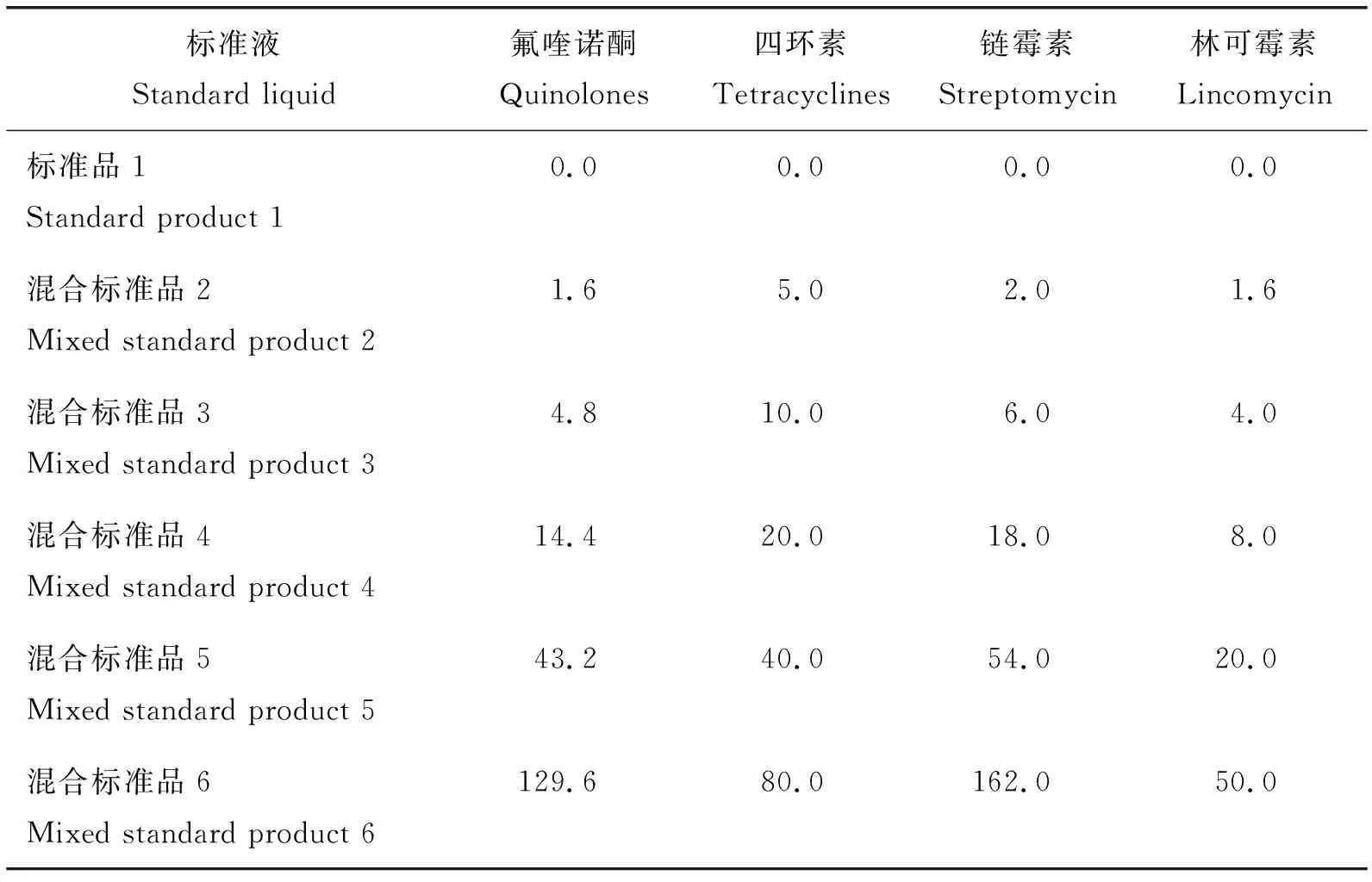
表1 四種獸藥標準品質量濃度Table 1 Standard concentrations of four different veterinary drugs μg/L
1.3.3試劑盒相關參數驗證試驗
氟喹諾酮、四環素、鏈霉素和林可霉素的標準溶液濃度為1 000 μg/L,向1 mL牛奶樣品中添加標準溶液體積為20 μL,牛奶樣品中氟喹諾酮、四環素、鏈霉素和林可霉素加標濃度為20 μg/L。隨機選取24份牛奶樣品,每份樣品進行2次平行試驗。
1.4 統計方法
每份牛奶樣品進行2個平行測定,平均值用于計算獸藥的殘留水平。使用MiELISA軟件(MiELISA v 1.11,南京祥中生物科技有限公司)自動進行圖像分析和定量分析。

表2 試劑盒相關參數Table 2 Related parameters of experiment kit used
2 結果與分析
2.1 試劑盒的相關參數驗證
驗證試劑盒的相關參數的結果表明:氟喹諾酮測定濃度17.02~23.41 μg/L,回收率85%~117%;四環素測定濃度17.00~23.61 μg/L,回收率85%~118%;鏈霉素測定濃度16.34~25.5 μg/L,回收率82%~128%;林可霉素測定濃度17.44~21.88 μg/L,回收率87%~109%。進一步統計發現(表3):牛奶樣品中氟喹諾酮、四環素、鏈霉素和林可霉素測定濃度平均值分別為19.11、20.15、21.22和18.82 μg/L,回收率平均值分別為95.53%、94.94%、106.8%和94.11%。根據我國國家標準(GB/T 27404—2008)[24],這些數值都符合ELISA方法中限定的回收值范圍,說明該試劑盒測定結果可信。
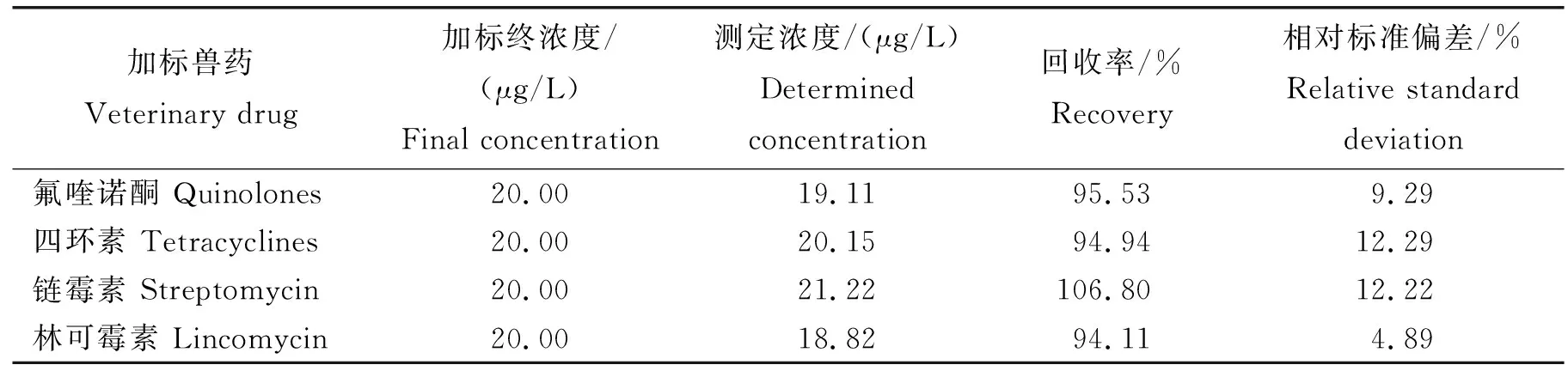
表3 四種獸藥殘留的檢測結果(n=24)Table 3 Test results of four types of veterinary drug residues (n=24)
2.2 我國市場上UHT滅菌乳和巴氏殺菌乳中四種獸藥殘留
我國農業農村部頒布的《全國奶業發展規劃》將奶業產區劃分為東北內蒙古產區(黑龍江、吉林、遼寧和內蒙古)、華北產區(河北、河南、山東和山西)、西部產區(陜西、甘肅、青海、寧夏、新疆和西藏)、南方產區(湖北、湖南、江蘇、浙江、福建、安徽、江西、廣東、廣西、海南、云南、貴州和四川)和大城市周邊產區(北京、天津、上海和重慶)等5個區域[25]。根據奶業產區劃分特點,對從我國市場上收集的150 份UHT滅菌乳和50 份巴氏殺菌乳樣品進行獸藥殘留分析。
獸藥殘留分析表明:收集的150 份UHT滅菌乳樣品中氟喹諾酮、四環素、鏈霉素和林可霉素的檢出率分別為0%、0%、3.3%和0%,其中鏈霉素檢出值為12.49 μg/L;我國生產的100 份UHT滅菌乳樣品中氟喹諾酮、四環素、鏈霉素和林可霉素的檢出率分別為0%、0%、2.0%和0%,其中鏈霉素檢出值為12.49 μg/L,檢出鏈霉素的牛奶樣品均來源于南方產區(2 份);進口的50 份UHT滅菌乳樣品中氟喹諾酮、四環素、鏈霉素和林可霉素的檢出率分別為0%、0%、6.0%和0%,其中鏈霉素檢出值為12.09 μg/L,檢出鏈霉素的牛奶樣品分別來源于德國、法國和澳大利亞(表4)。收集的50份巴氏殺菌乳樣品中氟喹諾酮、四環素、鏈霉素和林可霉素的檢出率分別為0%、0%、8.0%和2.0%,其中鏈霉素和林可霉素檢出值分別為21.16和16.48 μg/L;獸藥檢出樣品均來自國產巴氏殺菌奶,其中檢出鏈霉素的牛奶樣品分別來源于華北產區(2 份)、西部產區(1 份)和南方產區(1 份),檢出林可霉素的牛奶樣品來源于南方產區(1 份);進口巴氏殺菌奶中未檢出獸藥殘留(表5)。


3 討 論
本試驗牛奶樣品中,氟喹諾酮、四環素、鏈霉素和林可霉素的檢出率分別為0%、0%、4.5%和0.5%,其中:鏈霉素殘留在華北產區、西部產區和南方產區檢出率分別為8.0%、3.2%和6.0%;林可霉素殘留在南方產區檢出率為2%,其他產區檢出率均為0%;檢測氟喹諾酮和四環素殘留量最高濃度均低于檢測限,檢測樣品均來源于UHT滅菌乳樣品;鏈霉素殘留量最高濃度為21.16 μg/L,林可霉素殘留量為16.48 μg/L,均來源于巴氏殺菌乳樣品。4 種獸藥殘留量最高濃度均低于歐盟、食品法典委員會和我國標準中規定的最大殘留限量。已有研究相繼報道了我國市場上牛奶樣品中氟喹諾酮和四環素殘留的情況:崔海輝[26]從浙江省內收集的140 份巴氏殺菌乳樣品中四環檢出率為2.8%;張養東等[22]2010年9月從我國市場上收集的94 份UHT滅菌乳樣品和26份巴氏殺菌乳樣品,UHT滅菌乳樣品中氟喹諾酮和四環素檢出率為95.7%和0%,巴氏殺菌滅菌乳樣品中氟喹諾酮和四環素檢出率為61.5%和7.7%,所有液態奶樣品中氟喹諾酮和四環素殘留量最高濃度為20.49和47.7 μg/L;Han等[23]2011年6月從我國市場上收集的180份UHT滅菌乳樣品中氟喹諾酮和四環素的檢出率為100%和0%,其中氟喹諾酮和四環素殘留量最高濃度為58.8 μg/L和<1.5。上述結果表明,液態奶中獸藥殘留量檢出率因檢測方法和檢測限不同而存在差異,但仍可明顯看出氟喹諾酮和四環素殘留在液態奶中經常被檢出。我國市場上也發現牛奶中一些其他獸藥殘留物,例如磺胺類和磺胺二甲嘧啶[12-13]。因此,有必要嚴格實施有效的監管措施,從生產源頭上控制原料奶中獸藥殘留,嚴格執行牛奶質量安全監測體系,堅決貫徹落實食品安全有關部門的決策部署,從根本上保障牛奶的質量安全[27-28]。
4 結 論
本研究發現2016下半年和2017年上半年我國市場上UHT滅菌乳和巴氏殺菌乳樣品中氟喹諾酮、四環素、鏈霉素和林可霉素殘留情況污染的發生率較低,且均未超過歐盟、食品法典委員會和我國標準中規定的最大殘留限量。但是,由于牛奶中某些獸藥殘留仍有檢出,需要嚴格執行有效的監管和控制措施,殘留物控制在安全水平以內,確保牛奶產品安全。

