食品中沙門氏菌能力驗證樣品的鑒定與分析
程瀟 劉娟娟 賈貞


摘要 [目的]掌握食品中沙門氏菌能力驗證中可疑菌落的分離及鑒定,分析食品中沙門氏菌檢驗過程中存在漏檢的可能性及判定方法。[方法]按照沙門氏菌能力驗證作業指導書及GB 4789.4-2016《食品安全國家標準 食品微生物學檢驗 沙門氏菌檢驗》的要求對編號為224號、740號、845號3份能力驗證考核樣品進行沙門氏菌的檢測。[結果]3份樣品中均檢出沙門氏菌,其中224號樣品中檢出沙門氏菌雙相亞利桑那亞種。[結論]3份能力驗證樣品結果均為滿意。
關鍵詞 能力驗證;沙門氏菌;分離鑒定
沙門氏菌是一種無芽孢、無莢膜、需氧或兼性厭氧的革蘭氏陰性菌,易存在于家禽、肉及蛋等食品中,是食品中分布比較廣、危害程度嚴重的食源性致病微生物,可引起惡心、嘔吐、腹痛、腹瀉及發熱等疾病[1]。隨著對沙門氏菌的不斷深入研究,現已發現沙門氏菌超過3 000種血清型[2]。正是由于沙門氏菌具有存在廣泛、種類繁多等特點,且我國每年大多數食物中毒事件都是由沙門氏菌感染引起的,所以食品中沙門氏菌的檢驗對強化食品安全、保障人民衛生健康具有重要意義。
食品微生物能力驗證是通過按照預先制定的準則來考察評價實驗室是否具備從事微生物檢測能力的重要手段。因此,參加能力驗證活動對實驗室質量控制有著非常重要的意義[3]。目前,食品中沙門氏菌的檢測有多種方法,其中比較常用的是GB4789.4的傳統培養方法,此外還有酶聯免疫分析法、環介導等溫擴增法、普通PCR法、實時熒光定量PCR法、序列分析及生物飛行質譜法等[4]。筆者比較了沙門氏菌能力驗證作業指導書及GB 4789.4-2016《食品安全國家標準? 食品微生物學檢驗? 沙門氏菌檢驗》對食品中沙門氏菌能力驗證的結果,為食品中沙門氏菌的能力驗證提供一些參考依據。
1材料與方法
1.1標準菌株
沙門氏菌能力驗證采用的標準菌株為鼠傷寒沙門氏菌(ATCC 14028)和大腸埃希氏菌(ATCC 25922)。
1.2試劑與儀器
緩沖蛋白胨水(BPW)、四硫酸鈉黃綠增菌液(TTB)、亞硒酸鹽胱氨酸增菌(SC)、亞硫酸鉍瓊脂(BS)、三糖鐵(TSI)、營養瓊脂均使用北京陸橋技術股份有限公司產品;沙門顯色培養基使用法國科瑪嘉產品,沙門氏菌屬診斷O及H血清使用寧波天潤生物藥業有限公司產品,VIDAS SLM試劑條及VITEK 2 GN鑒定卡使用法國生物梅里埃產品,所有試劑均為筆者所在實驗室合格供應方提供并在有效期內。
移液器Eppendorf research plus(德國Eppendorf公司)、MSC1.8型生物安全柜(賽默飛世爾科技有限公司)、 恒溫培養箱(德國賓得)、5050型全自動高壓蒸汽滅菌鍋(以色列騰氏公司)、全自動熒光免疫分析儀VIDAS(法國生物梅里埃)及全自動微生物鑒定及藥敏分析系統VITEK 2(法國生物梅里埃)。
1.3檢測方法
檢驗方法主要依據沙門氏菌檢驗作業指導書以及GB 4789.4-2016 《食品安全國家標準? 食品微生物學檢驗沙門氏菌檢驗》的要求進行。
2結果與分析
2.1酶聯免疫分析技術檢驗結果
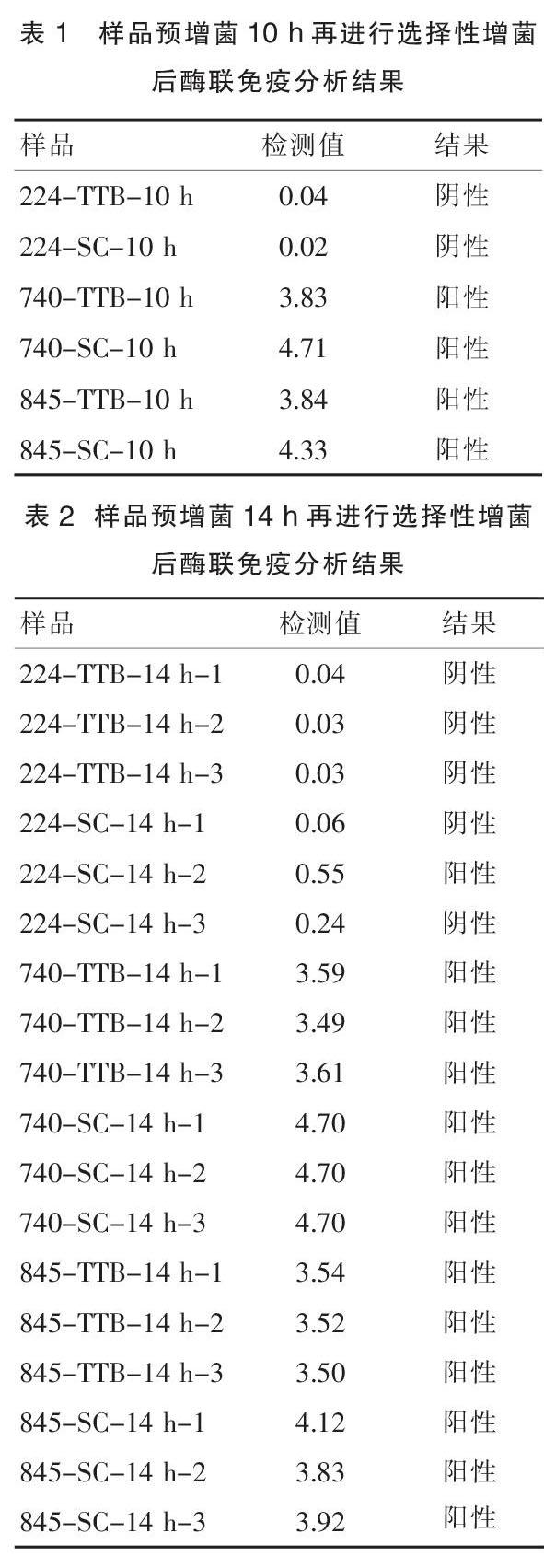
分別將224號、740號、845號3份樣品按照作業指導書的要求接種于BPW后置于36℃恒溫培養箱中培養,分別取培養10、14和18 h后的增菌液接種于TTB和SC進行選擇性增菌,每份樣品各接種3管(其中預增菌10 h樣品僅檢測1管),分別按要求放置于36℃(SC)和42℃(TTB)恒溫培養箱中繼續培養24 h后使用全自動熒光免疫分析儀VIDAS進行檢測(檢測值<0.23為陰性,≥0.23為陽性)。
由表1~3可知,740號、845號2份樣品3個重復在經TTB和SC選擇性增菌10、14、18 h后結果均為陽性,而224號樣品僅有1個重復在經SC增菌14 h后為陽性,其余結果均為陰性,造成這種現象可能是由于224號樣品中含有的多種干擾菌生長旺盛,從而抑制了沙門氏菌的正常生長,導致沙門氏菌的含量低于儀器檢出限。此外試驗結果表明740號和845號樣品經TTB增菌后18 h的檢測值要高于14 h的檢測值,經SC增菌后18 h的檢測值要低于14 h的檢測值,表明TTB相對SC而言對樣品中非沙門氏菌具有一定的抑制性。
2.2常規微生物培養法檢驗結果
分別將接種于TTB和SC的增菌液用接種環轉接至BS瓊脂和沙門顯色培養基后,置于36℃恒溫培養箱中培養24~48 h后觀察結果(圖1),從每塊平板上至少挑取3個可疑菌落接種于TSI瓊脂,同時接種到營養瓊脂上進行純化并置于36℃恒溫培養箱中培養24 h,最后將純化后的菌落用全自動微生物鑒定及藥敏分析系統VITEK 2進行鑒定。可疑菌落經VITEK 2鑒定后顯示740號、845號樣品結果均為沙門氏菌屬(Salmonella group),224號樣品鑒定結果為沙門氏菌亞利桑那亞種(Salmonella enterica ssp. Diarizonae)。
2.3血清凝集試驗結果
樣品分離菌的血清學分型結果見表4。結果顯示,740號和845號2份考核樣品O抗原A-F多價血清和H多價血清均可正常凝集,224號樣品O抗原A-F多價血清不能正常凝集,經過0抗原因子逐一篩查發現O60單因子血清可以凝集,H多價血清在經過誘導后可以產生正常凝集反應。
3結論與討論
結合以上生化試驗和血清學鑒定結果得出,3個樣品均檢測出沙門氏菌,其中224號樣品為沙門氏菌雙相亞利桑那亞種,此次能力驗證結論最終為滿意結果。
目前,國標中要求做食品中沙門氏菌檢驗增菌環節中必須使用TTB和SC 2種增菌液同時進行增菌,在選擇性分離環節中必須同時使用BS瓊脂平板和XLD(或HE、沙門顯色平板)進行分離。這是由于沙門氏菌具有3 000多種血清型,部分沙門氏菌具有比較特殊的生理生化特性,僅使用1種培養基有很大可能造成漏檢;同時有的沙門氏菌在選擇性增菌液中,生長會受到一定的抑制,同時使用2種增菌液會提高檢出率。
此次能力驗證740號和845號樣品在VIDAS上可以得出準確的初篩結果,同時在BS瓊脂平板和沙門顯色平板上均能出現典型可疑菌落;224號樣品在使用VIDAS進行初篩時僅有1管提示為陽性,這可能是由于樣品中含有大量干擾菌造成沙門氏菌雙相亞利桑那亞種在增菌過程中生長受到抑制,導致該樣品中沙門氏菌的含量低于儀器檢出限;此外該樣品在沙門顯色平板上菌落為藍色菌落,不是標準的紫紅色菌落,以上2種情況會造成對該樣品的誤判,導致沙門氏菌的漏檢。因此在檢測沙門氏菌時除對典型菌落進行鑒定外,還必須挑去一些平板上的非典型菌落進行篩查,從而避免漏檢情況的發生。
740號和845號樣品在血清凝集試驗中O多價血清和H多價血清均可凝集,但是224號樣品O抗原A-F多價血清不凝集,由于VITEK 2提示該樣品中含有沙門氏菌雙相亞利桑那亞種,繼而使用O抗血清單因子對該純化菌落進行逐一篩查,最終發現使用O60單因子血清可以獲得凝集反應,這些非典型的特征都會造成該樣品中沙門氏菌的漏檢。通過此次沙門氏菌能力驗證發現個別沙門氏菌僅依靠常規經驗對典型可疑菌落進行判斷是不夠的,在試驗中還必須盡可能多地挑取非典型特征的菌落進行生化鑒定,同時結合VITEK 2生化鑒定系統進行判斷。
參考文獻
[1] 彭易根,張正群.亞利桑那沙門氏菌食物中毒72例臨床分析[J].現代醫藥衛生,2011,27(4):571-572.
[2] GUIBOURDENCHE M,ROGGENTIN P,MIKOLEIT M,et al. Supplement 2003-2007 (No.47) to the White?鄄Kauffmann?鄄Le Minor scheme [J]. Research? in Microbiology, 2010,
161(1):26-29.
[3] 駱海朋,唐頌,陳怡文,等.沙門氏菌能力驗證樣品的研制及其應用[J].食品安全質量檢測學報,2016,7(4):1473-1478.
[4] 羅榮,任秀,崔生輝. 食品中沙門氏菌快速檢測技術研究進展[J].食品安全質量檢測學報,2016,7(4):1468-1472.
責任編輯:鄭丹丹

