三種不同飲食干預建立非酒精性脂肪肝模型
張 丹,呂俊衍,鄧 溢,周 波,耿坐濤,羅粟風,王金香,文 玉,應昀晏,文代艷,馬嵐青
(1)昆明醫科大學第一附屬醫院消化內科,云南昆明 650032;2)昆明醫科大學臨床醫學專業,云南昆明 650500;3)麗江市兒童醫院普外科,云南麗江 530721)
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD)是除外酒精和其他明確的損肝因素所致的脂肪在肝臟堆積所產生的以彌漫性肝細胞大泡性脂肪性變為主要病變的臨床病理綜合征[1],有報道表明NAFLD 在人群中的患病率為20%~40%[2-3]。并且2018 年指南指出:NAFLD 已成為我國第一大慢性肝病和健康體檢肝臟生物化學指標異常的首要原因[4]。
目前國內外常用的NAFLD 動物模型有:(1)營養失調性模型,包括高糖、高脂[5]、膽堿缺乏等誘發模型[6-7];(2)藥物中毒模型,包括CCl4[8]、四環素、乙硫氨酸誘發模型;(3)基因改良模型,有ob/ob 小鼠[9]、FLS 小鼠、PNPLA3 轉基因小鼠、ArKO 小鼠模型;(4)基因飲食復合性模型,有研究用ob/ob 小鼠+MCD 飲食建立齲齒動物NAFLD模型[10];(5)中醫病癥結合模型[11]。NAFLD 動物模型研究不斷取得新進展,但病因機制復雜,尚不能完全闡述其相關的機制,從目前研究看,復合模型在模擬人類NAFLD 的發生發展發揮重要作用,但建模組合繁多,缺乏統一標準。由于中醫模型的特殊性,在推廣和認可上存在一定難度。
因此本文利用3 種不同飲食干預建立NAFLD模型,并進行了對比,旨在為不同病因引起的NAFLD 的發病機制及分子基礎研究提供理想而可靠的動物模型。
1 材料與方法
1.1 材料
1.1.1 實驗動物 雄性C57BL/6 小鼠60 只,日齡42 d,體質量20~23 g,由南京大學-南京生物醫藥研究院提供,SPF 級環境飼養。許可證號:SCXK(蘇)2015-0001,恒溫(20±2)℃及濕度(50±5)%條件,人工照明明暗各12 h,自由進食水,適應1 周后隨機分組。小鼠組織取材在昆明醫科大學動物實驗中心屏障設施內完成,本研究符合昆明醫科大學實驗動物倫理委員會所制定的倫理學標準。
1.1.2 主要儀器與試劑 酶標儀(Thermo Scientific);血糖儀(三諾生物傳感股份有限公司,GA-3型);小鼠胰島素(INS)酶聯免疫吸附測定試劑盒(Elabscience 產品貨號:E-EL-M2614c);甘油三酯(TG)測定試劑盒(Elabscience 產品貨號:E-BC-K238);油紅染色試劑盒(Solarbio 產品貨號:G1261)。
1.1.3 飼料 3 種不同飼料均購自北京博泰宏達生物技術有限公司,高脂飼料自制(總熱量為25.07 kj/g,其熱比為蛋白質20%、碳水化合物20%、脂肪60%);葉酸缺乏飼料自制(普通飼料去除葉酸);高蛋氨酸飼料自制(普通飼料基礎上加2%蛋氨酸);普通飼料購自昆明醫科大學實驗動物中心。
1.2 方法
1.2.1 動物飼養方法 將60 只C57BL/6 小鼠隨機分成4 組,每組15 只,N 組只給予普通飼料;HFD 組只給予高脂飼料;FD 組只給予葉酸缺乏飼料;HCY 組只給予高蛋氨酸飼料,飼料量為每只小鼠(5±1)g/d,飲用高溫滅菌水,不限量。每天觀察食水消耗情況,每周稱體重并做詳細記錄。飼養11 周或14 周后禁食12 h 后,進行下述各項實驗。
1.2.2 空腹血糖及血清胰島素檢測 干預飲食14周后,腹腔注射3%戊巴比妥鈉(100 mg/kg)麻醉后進行心臟取血,測小鼠空腹血糖,取全血樣品于室溫放置2 h 后1 000×g 離心20 min,取上清,利用ELISA 試劑盒檢測血清中胰島素含量,最后計算出各組胰島素抵抗指數(HOMA-IR)及胰島素敏感指數(HOMA-ISI)。計算公式:胰島素抵抗指數=(空腹血糖(mmol/L)×血清胰島素(mIU/L))/22.5;胰島素敏感指數=1/(空腹血糖(mmol/L)×血清胰島素(mIU/L))。
1.2.3 肝指數的計算 迅速取肝臟,稱重記錄,計算肝指數(肝指數的計算方式:肝指數=肝濕重/體質量×100%)。
1.2.4 肝組織甘油三酯檢測 精確稱量組織重量,根據重量(g):體積(mL)=1:9 的比例加入勻漿培養基,在冰水浴中機械勻漿肝組織。以620×g離心10 min,然后取上清液利用GPO-PAP 方法測定肝組織中甘油三酯(TG)含量。
1.2.5 肝組織病理檢測 用10%中性甲醛溶液固定肝臟組織,脫水、包埋、4℃保存,進行常規HE 染色;取新鮮肝組織做冰凍切片,利用油紅O試劑盒染色,光鏡下觀察大鼠肝臟脂肪變性情況。
1.3 統計學處理
采用SPSS 統計軟件處理資料。計量資料用W檢驗進行正態性檢驗,實驗結果數據以()表示,均數多組間比較采用方差分析,以LSD-t 進行組間差異的兩兩比較,P <0.05 為差異有統計學意義。
2 結果
2.1 小鼠的一般狀況、體重體型比較
實驗過程中各組小鼠狀態均良好,食欲佳,性情較為溫順,活動正常。各組小鼠飲水和尿量無明顯差異,HFD 小鼠糞便顏色偏淺黃,HCY 組小鼠排泄物異味較重。各模型組較N 組干預飲食后1周體重差異無統計學意義(P >0.05);干預飲食14 周后HFD 組較N 組體重明顯增加,差異有統計學意義(P <0.0001),HCY 組較N 組體重明顯減輕,差異有統計學意義(P <0.05),FD 組較N 組體重差異無統計學意義(P >0.05),見圖1。干預飲食14 周后,隨機選取小鼠測量臀部最寬處,HFD 小鼠較其他各組較寬,見圖2。
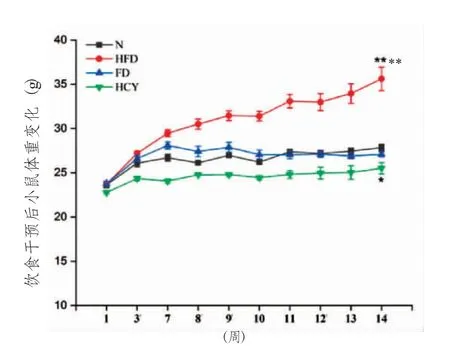
圖1 正常對照組與模型組體重變化趨勢Fig.1 Weight change trend in normal control group and model groups

圖2 正常對照組與模型組體型對比Fig.2 Comparison of body size between the normal control group and the model groups
2.2 小鼠肝濕重及肝指數比較
干預飲食14 周后,取出肝臟,記錄肝濕重,計算肝指數。與N 組比較,FD 組及HCY 組小鼠肝濕重均降低(P <0.001 或P <0.05);與N 組比較,HFD 組及FD 組肝指數顯著降低,差異有統計學意義(P <0.01),見表1。
表1 各組小鼠肝濕重及肝指數變化的比較()Tab.1 Comparison of liver wet weight and liver index of mice in each group()
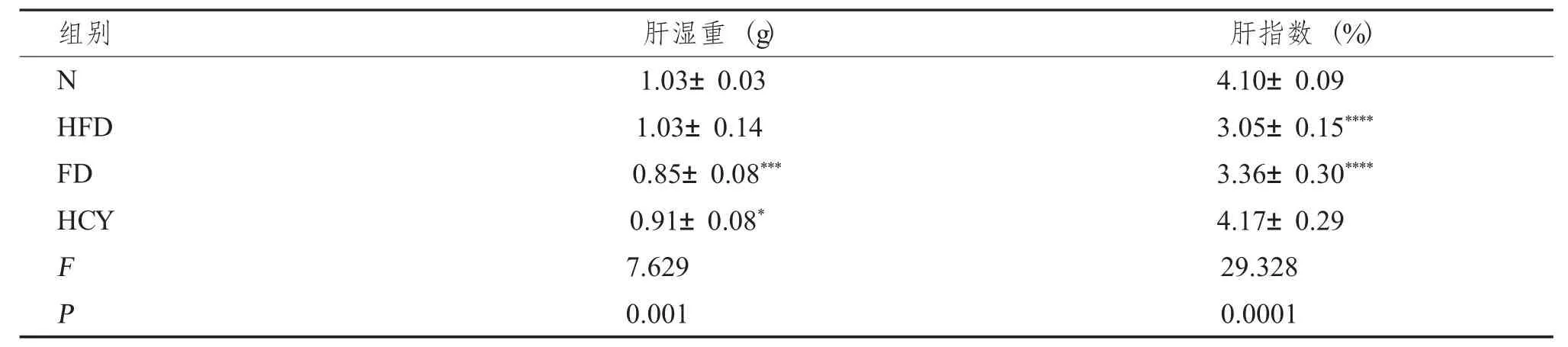
表1 各組小鼠肝濕重及肝指數變化的比較()Tab.1 Comparison of liver wet weight and liver index of mice in each group()
與N 組比較,***P <0.01,****P <0.0001。
2.3 小鼠肝臟大體形態觀察及肝組織病理觀察
2.3.1 肝臟大體形態觀察 干預飲食14 周后,觀察肝臟大體情況,N 組肝表面顏色普遍黯紅,色澤鮮亮,邊緣銳利,無油膩感;模型組肝臟稍黃,切面有油膩感,見圖3。
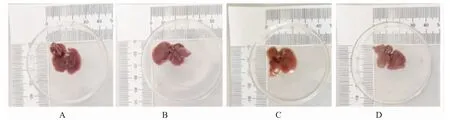
圖3 正常對照組與模型組肝臟大體形態對比Fig.3 Comparison of liver gross morphology between the normal control group and the model groups
2.3.2 肝臟HE 染色結果 光學顯微鏡下觀察肝臟組織HE 染色病理切片,N 組肝組織結構完整清晰、肝小葉結構正常,肝細胞排列成肝索,在中央靜脈周圍呈放射狀分布,細胞中央有大而圓的核,細胞質均勻,無脂肪變性;HFD 組、FD 組、HCY 組均出現脂肪變性,可見肝細胞腫大變圓,胞漿疏松,呈彌散性肝細胞空泡變性,且在干預飲食14 周后的脂肪變性較11 周更明顯,出現大量的脂肪變性空泡,模型組中HFD 組脂肪變性最為嚴重,呈大泡型,而FD 及HCY 組以小泡型為主,見圖4。
2.3.3 肝臟油紅O 染色結果 光學顯微鏡下觀察肝臟組織油紅O 染色結果,與N 組相比,HFD 組、FD 組及HCY 組的胞漿中均有橘紅色脂滴形成,散在分布;且在干預飲食14 周后橘紅色脂滴布滿全視野,較11 周更明顯,且模型組中HFD 組脂肪沉積最為嚴重,見圖5。
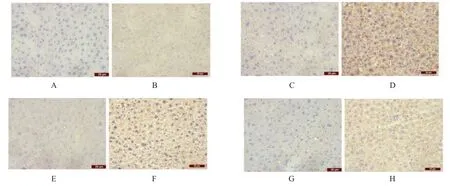
圖5 正常對照組與模型組肝臟油紅O 染色結果(×400)Fig.5 Oil red staining results of liver in the normal control group and the model groups(×400)
2.4 各組小鼠肝組織甘油三酯比較
干預飲食14 周后,HFD、FD 及HCY 組分別與N 組比較肝組織TG 水平顯著增高,差異有統計學意義(P <0.05),FD 組TG 含量最高,分別與其它模型組相比差異無統計學意義(P >0.05),見圖6。
2.5 各組小鼠胰島素抵抗情況比較
干預飲食14 周后,與N 組相比,HFD 組胰島素抵抗指數顯著增高(P <0.01),而FD 組及HCY組較N 組差異無統計學意義(P >0.05),但呈現增高趨勢;HFD 組胰島素敏感指數顯著降低(P <0.05),同樣的,FD 組及HCY 組較N 組差異無統計學意義(P >0.05),但呈現明顯降低趨勢見表2、圖7。
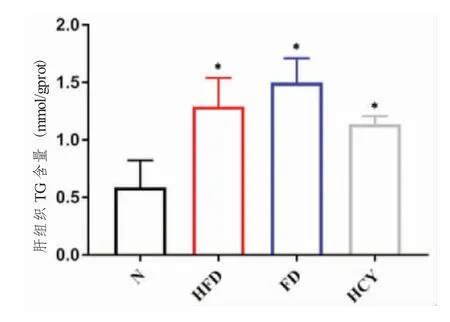
圖6 正常對照組與模型組肝組織TG 比較Fig.6 Comparison of hepatic TG between the normal control group and the model groups
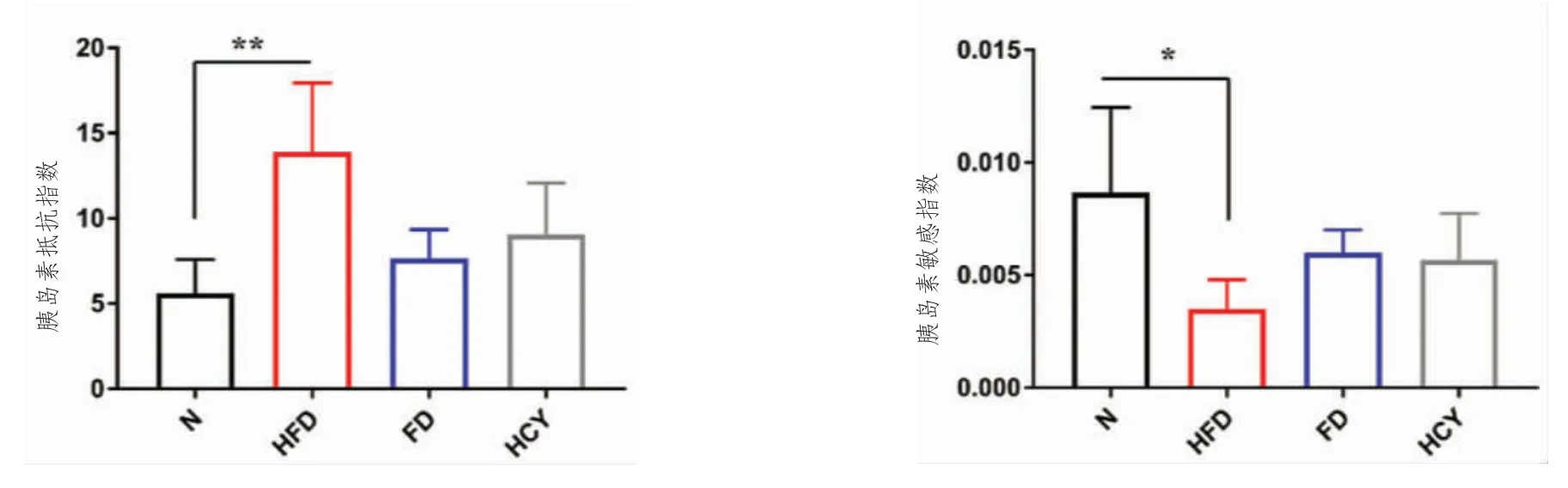
圖7 正常對照組與模型組胰島素抵抗指數及敏感指數比較Fig.7 Comparison of insulin resistance index and sensitivity index between the normal control group and the model groups
表2 正常對照組與模型組胰島素抵抗指數及敏感指數比較()Tab.2 Comparison of insulin resistance index and sensitivity index between the normal control group and the model groups()
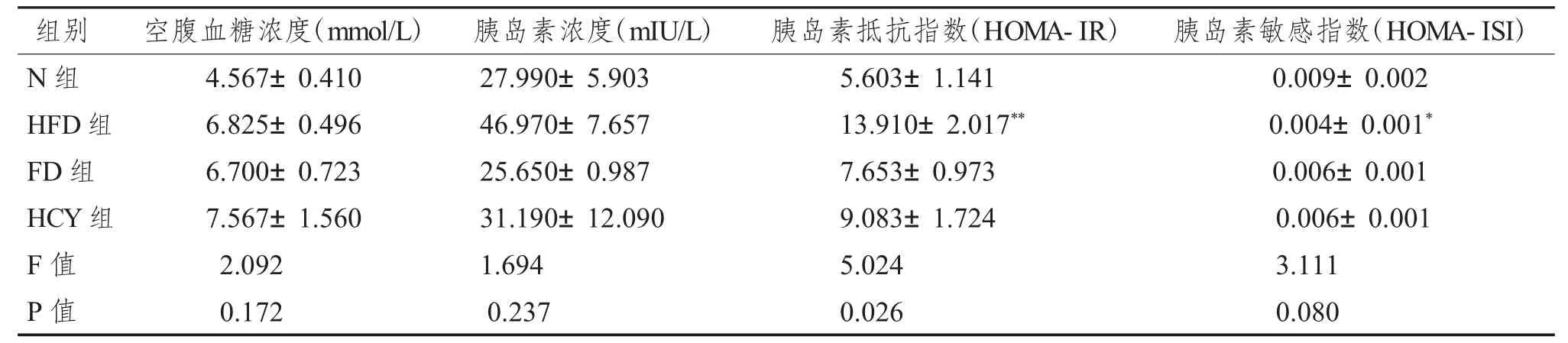
表2 正常對照組與模型組胰島素抵抗指數及敏感指數比較()Tab.2 Comparison of insulin resistance index and sensitivity index between the normal control group and the model groups()
與N 組比較,*P <0.05,**P <0.01。
3 討論
目前尚未有研究做過3 種模型的橫向比較,且對葉酸缺乏及高HCY 導致的NAFLD 研究太少,本研究的價值在于:通過小鼠一般情況監測、肝組織病理學觀察及相關生化指標檢查證實了3 種不同飲食干預均可成功建立NAFLD 模型的同時,對其進行了橫向對比,并結合臨床現狀得出HFD 偏向于模擬超重且較嚴重的NAFLD,FD 偏向于模擬體重變化不大伴營養缺乏的NAFLD,而HCY 偏向于模擬體重不增伴高HCY 的NAFLD,提醒研究者們在今后NAFLD 的病因機制研究中的模型設置方面要全面考慮,根據不同的病因建立適合的NAFLD模型。
經典的HFD 模型:雄性大鼠分別攝入71%的脂肪、11%的碳水化合物和18%的蛋白質,該種建模方法的脂肪含量與美國的平均飲食相同,喂養3周后HFD 大鼠出現脂肪變性、IR、線粒體功能障礙[12]。干預16 周后,脂肪變性、肝細胞膨脹、血糖升高、脂聯素降低和IR[13]。在筆者的研究中,C57BL/6 雄性小鼠攝入蛋白質20%、碳水化合物20%、脂肪60%,干預14 周后體重明顯增加、體型肥胖、IR 顯著增高、ISI 降低、TG 顯著增高;HE 及油紅O 染色均顯示脂肪變性,控制HFD 干預時間建立不同程度脂肪肝模型,可模擬臨床上輕、重度脂肪肝患者。
葉酸缺乏會導致膽堿流失,甲基化能力受損,進而使甘油三酯在肝臟中堆積,葉酸缺乏還能降低一種通過甲基化合成磷脂酰膽堿的酶[14],同時,也有研究表明,磷脂酰膽堿是極低密度脂蛋白很重要的組成成分,它能將甘油三脂運輸出肝臟[15],綜上研究說明葉酸缺乏可導致脂質沉積,這與筆者病理結果相符。生活中,很少人會主動補充葉酸,很有可能增加NAFLD 的患病風險。且目前葉酸缺乏誘導NAFLD 的研究尚少,本文利用葉酸缺乏建立NAFLD 模型,并與其他病因導致的NAFLD 模型進行對比,為預防和治療葉酸缺乏相關NAFLD 的研究提供新思路。
HCY 誘導NAFLD 機制復雜,但越來越多研究發現HCY 與NAFLD 的患病率顯著相關,建立理想的HCY 模型進一步探討NAFLD 機制顯得尤為重要。有研究選用雄性C57BL/6J 給予高蛋氨酸飲食,持續16 周,發現體重與正常對照組無顯著差異[16],而筆者的研究中發現HCY 組14 周后體重不增加反而較N 組降低(P <0.05),在臨床上也發現越來越多的非肥胖患者體檢時會出現NAFLD,這是否與HCY 水平有關,值得進一步研究。
NAFLD 的發病率逐年升高,臨床上,NAFLD形勢十分嚴峻,其確切機制在很大程度上仍不清楚,目前研究者普遍應用高脂、高糖誘導的NAFLD 模型。然而不同致病因素所致脂肪肝模型的機制及病理改變各異,因此尋求復制率高、重復性好、方法較簡便且滿足研究目的的動物模型很有必要。目前文獻報道的高脂飼料誘導的脂肪肝模型,造模耗時較長,且NAFLD 嚴重程度較低;葉酸缺乏誘導NAFLD 的研究尚少,本實驗提供了一種葉酸缺乏導致非酒精性脂肪肝簡單有效的方法,為預防和治療葉酸缺乏相關NAFLD 的研究提供新思路:高同型半胱氨酸可導致高血壓以及動脈粥樣硬化等心血管疾病,這也為臨床上NAFLD 伴動脈粥樣硬化以及高血壓的治療研究提供了最直接的動物模型,除此之外,高同型半胱氨酸對肝臟造成損傷的同時抑制肝細胞再生,這也就提示了HCY 所造成的NAFLD 可能會由單純的非酒精性脂肪肝發展為肝纖維化等肝臟病變,所以,本實驗通過HCY 建立的NAFLD 動物模型對其治療研究具有積極意義。研究結果還表明3 種不同飲食的干預所建立的模型存在差異,尤其體重最為明顯,HFD 模型體重明顯增加,而HCY 模型體重不增反而下降,FD 組體重無明顯變化。眾所周知,肥胖是導致NAFLD 的首要因素,但NAFLD 患者中,不乏體脂正常甚至偏低和營養缺乏的人群,結合本實驗模型,HFD 模型很好的復制了肥胖導致NAFLD 的發病機制,值得進一步思考的是營養缺乏人群的NAFLD 發病機制是否與葉酸缺乏相關,體脂正常甚至偏低的人是否因高同型半胱氨酸導致NAFLD呢?
因此本研究通過比較3 種NAFLD 模型,聯系臨床實際為NAFLD 的病因、機制及防治研究提供合適理想的動物模型基礎。

