PER1對人肝癌細胞BEL-7402輻射敏感性的影響
潘書賢,肖昌浩,黃 皓,胡文濤
(蘇州大學醫學部放射醫學與防護學院, 放射醫學與輻射防護國家重點實驗室, 江蘇省高校放射醫學協同創新中心, 蘇州 215123)
肝癌在全世界的致死性癌癥中排名第三,每年有將近750 000名新增病例[1]。在過去的幾十年間,肝癌潛在的流行病學危險因素一直在增加[2]。隨著肝癌的影像診斷,外科手術和肝移植等技術取得了巨大的進步,肝癌患者的生存率也出現大幅度的提高。然而,肝癌患者的預后情況卻仍然不理想[3]。大約有60%的肝癌病人需要接受放療,但是,肝癌卻被認為是一種輻射抗性腫瘤,其放療效果并不理想,五年生存率只有3%~5%[4]。因此,找到調控肝癌輻射敏感型的目標分子對于提高肝癌的輻射敏感性和改善放療效果是很有必要的。
晝夜節律調節蛋白(period circadian regulator 1, PER1)是調節生物節律的時鐘蛋白,作為生物節律負反饋調節原件參與生物節律的調節,PER1蛋白主要集中在細胞質中與另一種負反饋調節蛋白隱花色素受體(cryptochrome,CRY)結合形成復合體,形成的復合體進一步被PER蛋白激酶CK1酶磷酸化,然后轉位至細胞核與CLOCK:BMAL1結合來抑制其功能,從而對生物節律產生負向調節效應[5-7]。除此之外,Per1基因編碼的蛋白還是生物節律調節的重要限制原件,能夠重置生物節律時相[8,9]。PER1蛋白的表達水平隨著生物節律的波動而變化,而且PER1自身節律的變化在生物節律功能的發揮構成中也是必要的[10]。Niu等[11]研究發現,高水平表達PER1的膠質瘤組織對X射線的敏感性較高,并且在高水平表達的膠質瘤細胞中,X射線引起的凋亡明顯增多,此外,研究還發現,X射線能夠促進PER1的表達,但是在正常組織中并未觀察到類似現象。這提示PER1與腫瘤組織的輻射敏感性有關,然而,其與肝癌細胞輻射敏感性的關系還未曾報道,并且PER1參與調節腫瘤輻射敏感性的具體機制尚不明確。
在本次研究中,我們通過檢測PER1蛋白以及其mRNA在輻射敏感性不同的肝癌細胞系中的表達水平,同時也通過試驗驗證PER1蛋白在肝癌細胞輻射敏感性中的作用,對PER1增強肝癌細胞輻射敏感性的潛在機制進行了初步的研究。結果發現PER1能夠增強肝癌細胞的輻射敏感性。本次研究也為進一步提高肝癌的放療效果提供了試驗基礎。
qRT-PCR用來檢測RA患者滑膜組織P2X7受體和MH7A細胞炎癥細胞因子IL-1β、IL-6相對表達水平。實驗步驟如下:收集處理好滑膜組織或MH7A細胞RNA,逆轉錄后,用SYBER green試劑盒進行實時熒光PCR實驗。PCR條件為:96℃ 30 s,1個循環;PCR反應,96 ℃ 5 s,60 ℃ 15 s,45個循環;溶解,96 ℃ 15 s,65℃ 20s,96 ℃15s,1個循環。PCR結束后,根據相應的公式,以標準曲線進行校正,計算出mRNA的相對表達。
貴州骨干水源工程建設任重道遠,肩負著解決全省工程性缺水問題的重任。國發〔2012〕2號文件明確提出:在安排中央財政轉移支付和中央預算內投資時,加大對貴州水利建設投入力度,支持貴州如期完成“三位一體”綜合規劃提出的水利建設目標。因此,在國家財政和地方財政提供基礎保障的前提下,充分利用好各項優惠政策,以省級水利融資平臺為主,短期內主要依靠金融機構貸款,中遠期采取金融機構貸款、上市融資、發行企業債券等方式融資,可以建立起貴州省骨干水源工程建設投入穩定增長機制。
用雙尾t檢驗分析兩組數據之間的統計學差異,用SPSS9.0軟件錄入數據并進行統計分析。不同組間比較方差齊性,相同指標兩處理組或者多處理組間比較經正態性檢驗后符合正態分布再用t檢驗,P<0.05視為差異有統計學意義。
1 材料與方法
1.1 材料
細胞培養于6孔板,于對數生長期根據試驗說明書進行PER1過表達載體的轉染,每孔載體用量為5 000 ng,Lipo3000脂質體用量為3.75 μL。轉染后過5 h吸去轉染培養基,并更換無轉染試劑的正常培養基進行培養。
1.2 細胞轉染
人肝癌細胞SMMC-7721,BEL-7402和HepG2為本實驗室保存細胞。胎牛血清,青霉素-鏈霉素抗生素混合液,DMEM高糖培養基和RPM1640培養基均購買自美國GIBCO公司。Trypsin-EDTA,BCA蛋白定量試劑盒購買自Bio SHARP生物科技公司。PER1蛋白抗體(鼠抗)購買自美國CST公司。細胞凋亡試劑盒、p53、Bcl-2、Cleaved Caspase-3、HRP標記的山羊抗鼠和一抗稀釋液購買自上海碧云天生物技術公司。PER1過表達載體(pcDNA3.1-PER1)由上海生工設計并構建。反轉錄試劑盒購買自Takara公司,定量PCR試劑盒購買自康潤生物。SMMC-7721,HepG2用含10%胎牛血清的DMEM高糖培養基,BEL-7402用含10%胎牛血清的RPMI1640培養基,均培養于5%CO2,37 ℃恒溫恒濕培養箱中。X射線照射采用美國RAD SOURCE RS-2000X射線儀,劑量率為1.2 Gy/min,細胞照射劑量為0、2、4、6、8、10 Gy,細胞均培養于直徑60 mm的平板培養皿中進行照射。
克隆形成試驗用來檢測過表達PER1的BEL-7402細胞系接受X射線照射后的存活情況。具體方法為接種100、200、400、800、2 000、5 000個細胞于直徑60 mm培養皿中,分別對應X射線劑量為0、2、4、6、8、10 Gy,然后于5%CO2,37 ℃培養箱中培養14 d,接著吸去培養基,用70%乙醇固定后結晶紫染色,計數克隆。試驗重復3次。克隆形成率=克隆集落數量/接種細胞數量×100%。存活曲線利用Graphpad軟件繪制。
(3)某工業廢水中含有少量的As2O3,向該廢水中通入硫化氫可將其轉化為更難溶的As2S3,該反應的化學方程式為____。
1.3 蛋白免疫印跡
TRIzol試劑裂解細胞,提取細胞總RNA,細胞總RNA逆轉錄制備cDNA,PER1的mRNA表達通過GAPDH標準化,試驗重復3次。
1.4 實時熒光定量PCR
RIPA裂解細胞提取細胞總蛋白,用BCA試劑盒進行蛋白濃度定量,聚丙烯酰胺凝膠中添加蛋白為50 μg,以蛋白分子量標準蛋白作為參照,確定目的蛋白的位置,電泳起始電壓為80 V,待樣品到達分離膠后提高電壓至120 V。當溴酚藍指示劑將要跑到凝膠底部時,停止電泳。然后在200 mA,90 min條件下將凝膠中的蛋白濕轉到PVDF膜上。接下來用PBST配置的5%牛奶封閉1 h,加入PER1一抗4 ℃過夜。PBST洗膜8遍,每遍5 min,加入對應二抗,室溫孵育1 h,用PBST洗膜8次,每次5 min,用化學發光成像系統顯影,拍照。最后用Image J軟件進行灰度值定量分析。試驗重復3次。
1.5 細胞凋亡分析
如圖1所示,在照射劑量為0、2、4、6、8、10 Gy情況下,SMMC-7721、BEL-7402和HepG2細胞的存活率都隨著劑量的增加出現降低的趨勢。其中SMMC-7721在三種細胞系中對輻射最敏感,BEL-7402的輻射抗性在三種肝癌細胞系中最高(BEL-7402與HepG2相比P<0.01;與SMMC-7721相比P<0.001)。
1.6 克隆形成試驗以及存活曲線的繪制
四只表演虎間隔2米,成東西方向一字排開,臥于表演場地北側中央,頭南尾北,所有表演者立于虎后,擊鼓人員位于東北方向。
1.7 統計學處理
孩子不在身邊,所幸老人還有個學生,跟進跟出地伺候他。許多人都說:“看這年輕人,放著自己的正事不干,成天陪著老頭子,好像很孝順的樣子。誰不知道,他是為了老頭子的錢。”
2 結果與分析
2.1 細胞存活曲線
消化對數生長期的BEL-7402肝癌細胞,接種于6孔板,每孔接種細胞數為3×105個,轉染PER1過表達載體,5 h后換液,24 h后用5 Gy X射線照射,照射后24 h檢測細胞凋亡情況。
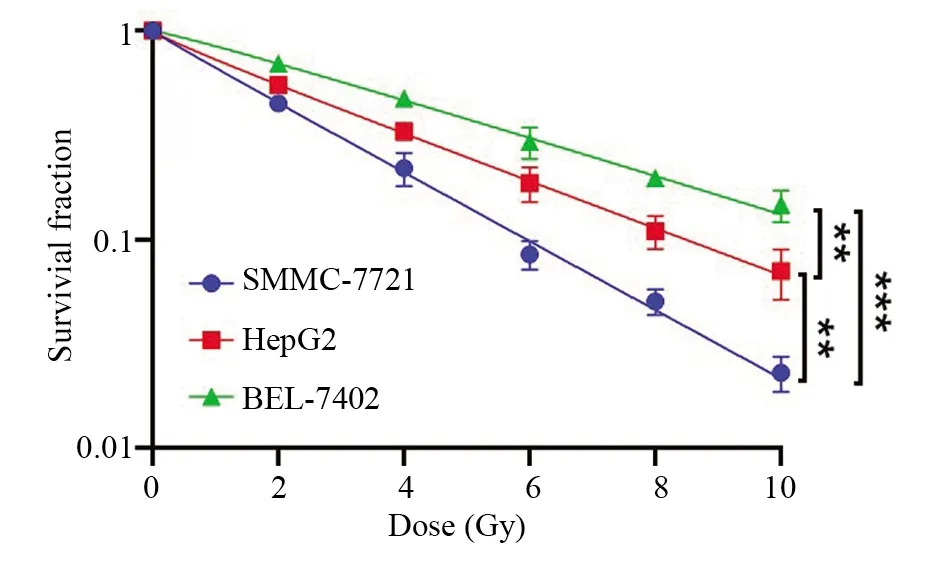
圖1 SMMC-7721,HepG2,BEL-7402三種肝癌細胞系在不同劑量下的存活曲線Fig.1 Survival curves of SMMC-7721, HepG2, BEL-7402 cells exposed to X-ray irradiation of gradient doses*:P<0.05;** :P<0.01;*** :P<0.001*:P<0.05,** :P<0.01,*** :P<0.001
2.2 蛋白免疫印跡試驗和實時熒光定量PCR試驗
經過照射后發現BEL-7402對射線的抗性明顯強于SMMC-7721和HepG2。三種細胞系中SMMC-7721的輻射敏感性最強,我們選用BEL-7402和SMMC-7721兩種細胞檢測PER1蛋白的表達。蛋白免疫印跡結果示于圖2。由圖2可見,BEL-7402中PER1蛋白表達水平明顯低于SMMC-7721細胞中的PER1表達(圖2a、2b,P<0.01)。類似的結果也在定量PCR結果中得到驗證,如圖2c所示,P<0.05。
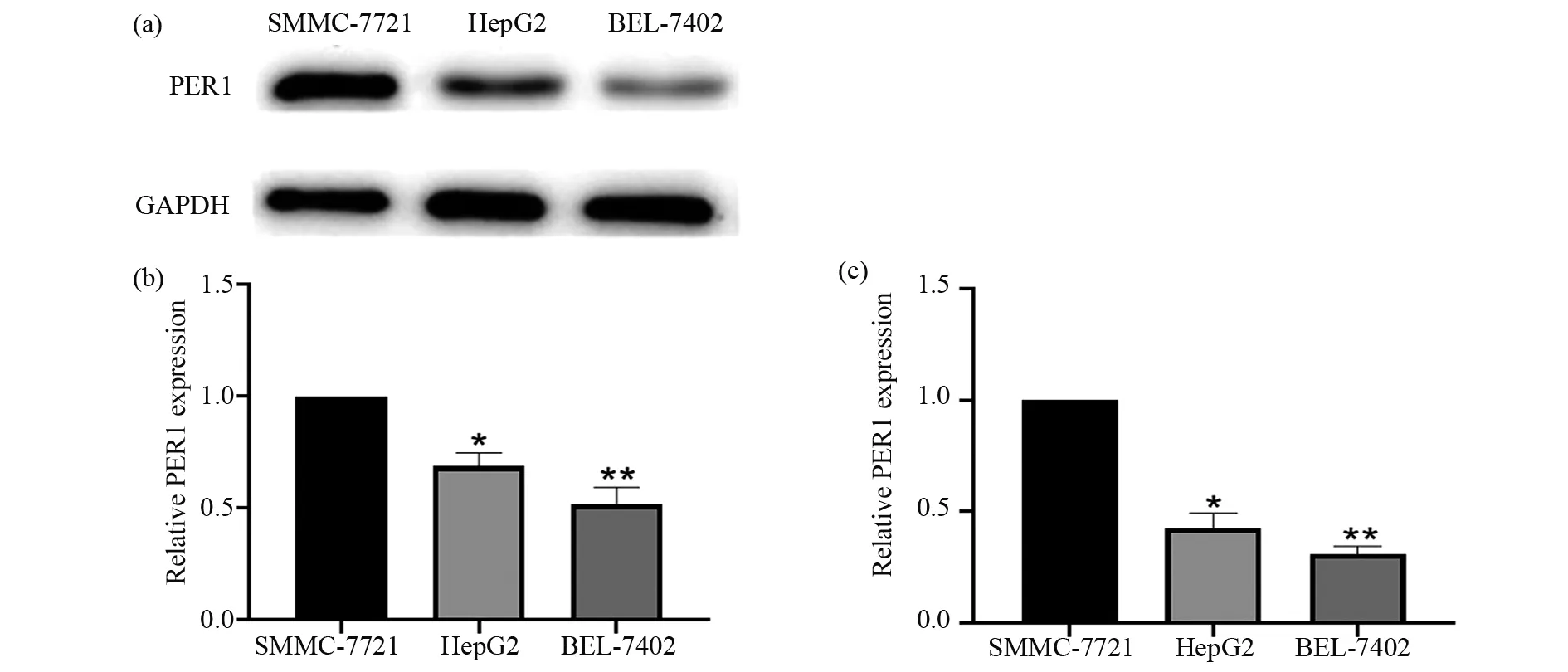
圖2 PER1在SMMC-7721,HepG2,BEL-7402三種肝癌細胞系中的表達Fig.2 The expression of PER1 in SMMC-7721, HepG2, BEL-7402 cells(a,b)PER1蛋白在三種肝癌細胞系中的表達及灰度值檢測;(c)PER1 mRNA 在三種肝癌細胞系中的表達。*:P<0.05,** :P<0.01(a,b)Expression of PER1 protein in the 3 hepatoma carcinoma cell lines;(c)Expression of PER1 mRNA in the 3 hepatocellular cell lines.*:P<0.05,** :P<0.01
2.3 過表達PER1蛋白后的細胞存活曲線
PER1在BEL-7402和SMMC-7721的表達結果顯示,在輻射抗性更高的BEL-7402細胞系中PER1表達水平很低,因此我們選用BEL-7402細胞系研究PER1的輻射增敏作用,結果如圖3所示,過表達PER1后,BEL-7402細胞系中PER1蛋白表達明顯升高,RT-qPCR試驗也得到了同樣的結果(圖3中a~c,P<0.001)。過表達PER1的BEL-7402細胞接受0、2、4、6、8、10 Gy梯度劑量照射處理后,細胞克隆存活率明顯低于未接受PER1過表達處理的對照組(圖3d,P<0.001)。
2.4 細胞凋亡檢測
根據圖2試驗結果,發現PER1在BEL-7402中的表達明顯低于SMMC-7721和HepG2,為了觀察PER1在肝癌細胞系輻射敏感性中的作用,接下來對BEL-7402進行過表達PER1處理,并檢測PER1對X射線誘導的細胞凋亡的影響,結果如圖4a和4b所示,接受X射線照射以后,過表達PER1的BEL-7402細胞凋亡明顯增多(P<0.01)。

圖3 BEL-7402過表達PER1后不同輻照劑量下的存活曲線PER1Fig.3 Survival curves of BEL-7402 cells overexpressing PER1 after irradiation(a~c) BEL-7402過表達PER1后其蛋白及mRNA在細胞中的表達;(d) 過表達PER1后BEL-7402肝癌細胞在不同劑量X射線照射下的存活分數。PER1-OE:過表達PER1的BEL-7402肝癌細胞系;Control:未經過表達處理的BEL-7402肝癌細胞系。*** :P<0.001 (a~c)Verification of PER1 overexpression in BEL-7402 cells by western blot and RT-qPCR;(d)Survival fraction of BEL-7402 cells under different doses of X-rays after overexpression of PER1. PER1-OE:BEL-7402 cells overexpressing PER1;Control:BEL-7402 cells untreated with overexpression. *** :P<0.001
2.5 免疫印跡試驗
為了研究PER1在增強X射線誘導BEL-7402細胞凋亡中的機制,接下來對過表達PER1的BEL-7402細胞進行X射線照射處理。根據圖1結果以及相關文獻報道,選取5 Gy的劑量進行照射,照射后24 h檢測細胞水平抗凋亡蛋白Bcl-2和凋亡執行蛋白Caspase-3以及p53的表達水平。結果表明,過表達PER1后,抗凋亡蛋白Bcl-2的表達明顯降低,而凋亡執行蛋白Caspase-3斷裂增多,同時p53表達明顯升高(圖5中a~d,P<0.01)。
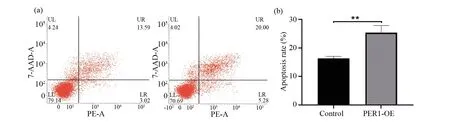
圖4 BEL-7402過表達PER1后細胞凋亡的檢測Fig.4 Apoptosis rate of BEL-7402 cells overexpressing PER1 after irradiation(a)凋亡流式檢測結果;(b)凋亡率統計。PER1-OE:過表達PER1的BEL-7402肝癌細胞系;Control:未經過表達處理的BEL-7402肝癌細胞系。** :P<0.01(a)Representative images of cytometry analysis;(b)Statistical results of apoptosis rates.PER1-OE:BEL-7402 cells overexpressing PER1;Control:BEL-7402 cells untreated with overexpression. ** :P<0.01
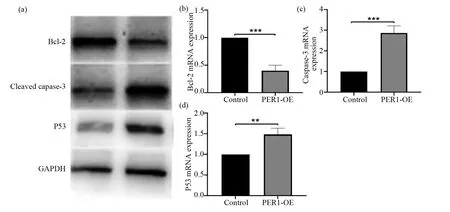
圖5 過表達PER1的BEL-7402接受X射線照射后24 h凋亡相關蛋白檢測Fig.5 Detection of apoptosis related proteins in BEL-7402 cells overexpressing PER1 after irradiation(a)Bcl-2和cleaved caspase-3蛋白表達;(b~d) 蛋白灰度值定量分析。PER1-OE:過表達PER1的BEL-7402肝癌細胞系;Control:未經過表達處理的BEL-7402肝癌細胞系。*** :P<0.001 (a)Expression of Bcl-2 and cleaved caspase3 proteins;(b~d):Quantitative analysis of protein gray values. PER1-OE:BEL-7402cells overexpressing PER1;Control:BEL-7402 cells untreated with overexpression. *** :P<0.001
3 討論
肝癌的有效治療手段包括經皮注射無水乙醇治療、高頻消融、外科手術切除等方法。非外科治療手段,例如動脈栓塞療法,已經廣泛應用于臨床中外科手術不能切除的肝癌[12]。放療作為肝癌非外科治療手段之一,雖然效果有待改善,但是能夠有效地幫助病人取得較好的臨床緩解[13]。在肝癌臨床放療中通過限制照射劑量來減少射線對正常肝臟的損害,這是由正常肝臟細胞對射線的低耐受性以及肝癌細胞自身的抗性所決定的。然而,隨著劑量的減少,肝癌細胞的殺傷作用也隨之減弱[14]。時鐘蛋白已經被證明在多種腫瘤中異常表達[15,16]。PER1作為時鐘蛋白的一種,其功能主要是調節大腦和外周組織的多種生物進程。PER1通過與CRY形成復合體,參與到生物節律的調節中,二者形成的復合體轉移到細胞質內,可被磷酸化酶降解。除此之外,PER1與CRY形成的符合體與CLOCK:BMAL1復合體相互作用,從而抑制CLOCK:BMAL1復合體的功能來延長生物節律周期,從而影響生物節律功能[7,17-19]。研究表明過表達PER蛋白家族會使小鼠更容易發生腫瘤,并且對射線敏感[20],而低氧造成的PER蛋白的降低,會增加細胞自身上皮轉化的功能[21]。另有研究證明PER1的表達與腫瘤的發生發展存在聯系[22],有試驗結果發現,PER1和PER2作為時鐘基因的調節原件,在正常的人大腦和膠質瘤中的表達水平都具有節律性,但是在兩種組織中,生物鐘的變化情況也是不同的。具體表現就是在膠質瘤中生物周期為12 h,但是在正常人腦中的生物周期為24 h[23]。在本次研究中,對PER1在輻射抗性不同的三種肝癌細胞中的表達水平進行了檢測,發現輻射抗性越高PER1的表達水平越低。然后對低表達PER1的細胞系進行PER1過表達處理,發現過表達PER1的肝癌細胞接受輻照后克隆形成率明顯降低,凋亡明顯升高。射線所發揮殺傷細胞的作用,主要依賴其造成的DNA損傷,當DNA損傷發生時,細胞周期明顯延遲,同時啟動細胞凋亡進程[24]。作為重要的時鐘基因,PER1不僅維持生物節律還可以通過調節細胞周期相關基因p53,c-myc等的表達來穩定細胞周期[25]。Fu等[26]研究發現,Per基因缺陷小鼠接受X射線照射以后相對于野生型小鼠免疫細胞凋亡增加了兩倍,此外p53在Per基因缺陷小鼠體內的表達水平也明顯低于在野生型小鼠系內的表達。并且p53在肺癌中的表達也明顯高于正常肺組織,說明了Per基因可以誘導p53的表達。這些結果與過表達Per基因的白血病細胞中的研究結果一致[27]。這些研究證明Per1基因可以通過上調p53水平來促進細胞的凋亡。本次研究也發現,過表達PER1的肝癌細胞受到照射以后,其凋亡比例明顯升高,通過檢測凋亡相關信號通路蛋白發現,過表達PER1后的BEL-7402肝癌細胞接受X射線照射以后,抗凋亡蛋白Bcl-2明顯降低,而凋亡執行蛋白Caspase-3斷裂明顯增多。結合本次研究結果發現,PER1在肝癌細胞系輻射敏感性調節中發揮著重要的作用,能夠明顯增強肝癌細胞的輻射敏感性。因此,此項研究為基于PER1的肝癌放療增敏提供了一定參考。

