氨溴索和糖皮質激素對早產兒BPD 的有效性分析
馬慧偉,張成元
(1.濰坊醫學院,山東 濰坊 261000;2.濰坊市婦幼保健院,山東 濰坊 261000)
支氣管肺發育不良(bronchopulmonary dysplasia, BPD)是早產兒較常見的呼吸系統并發癥,多發于出生后存在呼吸窘迫綜合征且需要進行高濃度氧治療或正壓輔助通氣的早產兒[1]。目前臨床針對早產兒BPD常用的治療方案包含肺表面活性物質治療、機械通氣治療及糖皮質激素治療等[2]。糖皮質激素類藥物是目前對早產兒BPD治療的常用藥物,但是其治療效果仍存在許多爭議,且被許多學者廣泛關注[3]。本研究中采用氨溴索聯合糖皮質激素對早產BPD患兒進行治療,分析其療效及對血液中白介素(IL)-1β、腫瘤壞死因子(TNF)-α水平的影響,現報道如下。
1 資料與方法
1.1 一般資料
選取2017年1月至2018年12月濰坊市婦幼保健院收治的早產兒BPD患兒98例,按照數字表法將其隨機分為兩組,各49例。對照組中男嬰25例,女嬰24例;胎齡為30~36周,平均胎齡(31.1±1.7)周;出生體重1 250.3~2 024.1g,平均體重(1 560.4±242.1)g。研究組中男嬰26例,女嬰23例;胎齡為30~36周,平均胎齡(31.9±1.5)周;出生體重為1 249.3~2 025.1g,平均體重(1 469.8±276.1)g。兩組的性別、胎齡及出生體重方面均無明顯差異(均P >0.05),一般資料有可比性。本研究已獲得醫院倫理委員會批準。
BPD的診斷標準[4]:①任何氧依賴(>21%)>28天的新生兒。②如胎齡<32周,根據矯正胎齡36周或出院時需吸入氧濃度(FiO2)分為:輕度,未用氧;中度, FiO2<30%;重度,FiO2>30%或需機械通氣。③如胎齡≥32周,根據生后56天或出院時需FiO2分為上述輕、中、重度。肺部X 線表現不應作為疾病嚴重性的 評估依據。
納入標準:①入組患兒均符合早產兒BPD的臨床診斷;②患兒在入組前未采取任何治療措施;③入組患兒家屬對本研究內容均知情,且在同意書上簽字。排除標準:①患兒對本研究所用藥物過敏;②患兒胎齡在36周以上;③患兒體重在2 500g以上;④患兒存在先天畸形、中毒性小腸結腸炎、消化道穿孔等情況; ⑤患兒需接受手術治療;⑥患兒家屬選擇放棄治療。
1.2 方法
對照組患兒接受常規治療,具體為:將BPD新生兒放置于培養箱中,給予吸氧治療,在治療期間注意保持患兒呼吸道暢通,并給予營養支持,使用利尿、支氣管擴張及抗感染藥物進行治療,為患兒補充肺泡表面活性物質,注意維持患兒水電解質平衡,密切關注其生命體征變化。
在對照組常規治療的基礎上,研究組患兒接受氨溴索聯合糖皮質激素進行治療。地塞米松的使用方法[5]: 靜脈推注地塞米松注射液(國藥準字:H41021255,規格 1mL∶5mg),0.15mg/kg,1次/日,連續治療3天;將藥量縮減到0.1mg/kg,1次/日,連續治療3天;再將藥量縮減到0.05mg/kg,1次/日,連續治療2天;再將藥量縮減到0.02mg/kg,1次/日,連續治療2天。鹽酸氨溴索的使用方法:靜脈滴注鹽酸氨溴索注射液(國藥準字:H20163230,規格 1mL∶7.5mg),7.5mg/次,2次/日,連續治療7天。比較兩組患兒的療效。
1.3 觀察指標
記錄兩組患兒吸氧時間及機械通氣時間,當患兒在暫停吸氧或機械通氣時,血氧飽和度可保持在88%~93%之間,即認為吸氧或機械通氣暫停時間。
根據患兒臨床癥狀改善情況,結合患兒停氧時間進行療效劃分,顯效∶患兒接受治療5天后停氧;有效:患兒接受治療5~7天內停氧;無效:患兒接受治療7天后仍需接受吸氧治療。有效率 = (顯效+有效)÷總例數×100%。
采集患兒血液樣本,離心獲得血清,采用雙抗體夾心酶聯免疫吸附法檢測兩組患兒治療前后的血清IL-1β和TNF-α水平,嚴格按照試劑盒說明書進行檢測,操作需個人獨立完成,以免交接過程出現誤差。
對兩組患兒治療期間不良反應發生情況進行記錄,主要記錄項目包含惡心嘔吐、腹脹及消化道潰瘍等。
1.4 統計學方法
運用SPSS 24.0軟件分析數據,計量資料以均數±標準差()表示,組間比較采用獨立樣本t 檢驗,計數資料組內對比應用χ2檢驗,以P <0.05為差異有統計學意義。
2 結果
2.1 兩組療效的比較
研究組療效顯著高于對照組,經比較差異有統計學意義(P<0.05),見表1。

表1 兩組療效的比較結果[n(%)]Table 1 Comparison of therapeutic effect between the two groups [n(%)]
2.2 兩組相關因子水平的比較
對照組、研究組的IL-1β和TNF-α水平治療前后組內比較差異均有統計學意義(均P <0.05);治療前,兩組的IL-1β和TNF-α水平比較差異均無統計學意義(均P>0.05);治療后,研究組的IL-1β和TNF-α水平均顯著低于對照組(均P<0.05),見表2。
表2 兩組相關因子水平的比較結果()Table 2 Comparisons of serum levels of IL-1βand TNF-α of the premature infants between the two groups ()
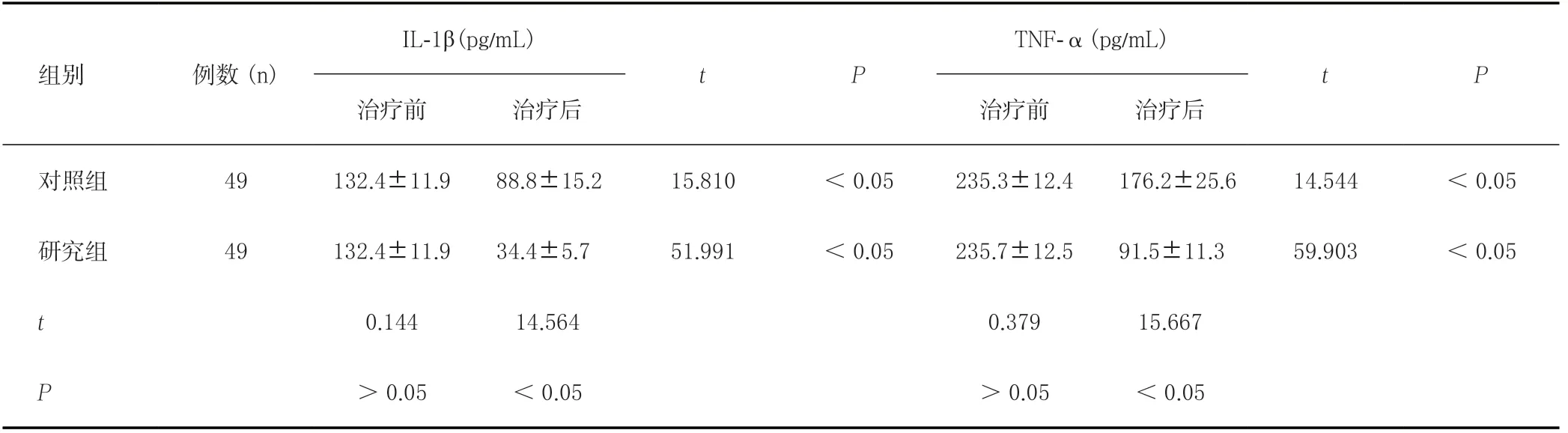
表2 兩組相關因子水平的比較結果()Table 2 Comparisons of serum levels of IL-1βand TNF-α of the premature infants between the two groups ()
IL-1β(pg/mL)TNF-α(pg/mL)組別 例數(n)t P t P治療前 治療后 治療前 治療后對照組 49 132.4±11.9 88.8±15.2 15.810 <0.05 235.3±12.4 176.2±25.6 14.544 <0.05研究組 49 132.4±11.9 34.4±5.7 51.991 <0.05 235.7±12.5 91.5±11.3 59.903 <0.05 t 0.144 14.564 0.379 15.667 P >0.05 <0.05 >0.05 <0.05
2.3 兩組吸氧時間及機械通氣時間的比較
研究組吸氧時間及機械通氣時間均顯著少于對照組,經比較差異均有統計學意義(均P<0.05),見表3。
表3 兩組吸氧時間及機械通氣時間的比較結果()Table 3 Comparisons of oxygen inhalation time and mechanical ventilation time of the premature infants between the two groups()

表3 兩組吸氧時間及機械通氣時間的比較結果()Table 3 Comparisons of oxygen inhalation time and mechanical ventilation time of the premature infants between the two groups()
組別 例數(n) 吸氧時間(d) 機械通氣時間(d)對照組 49 7.5±2.4 13.5±3.5研究組 49 5.1±1.1 8.7±1.6 t 14.267 15.674 P <0.05 <0.05
2.4 兩組不良反應的發生情況
研究組不良反應發生率顯著低于對照組,兩組比較差異有統計學意義(P<0.05),見表4。
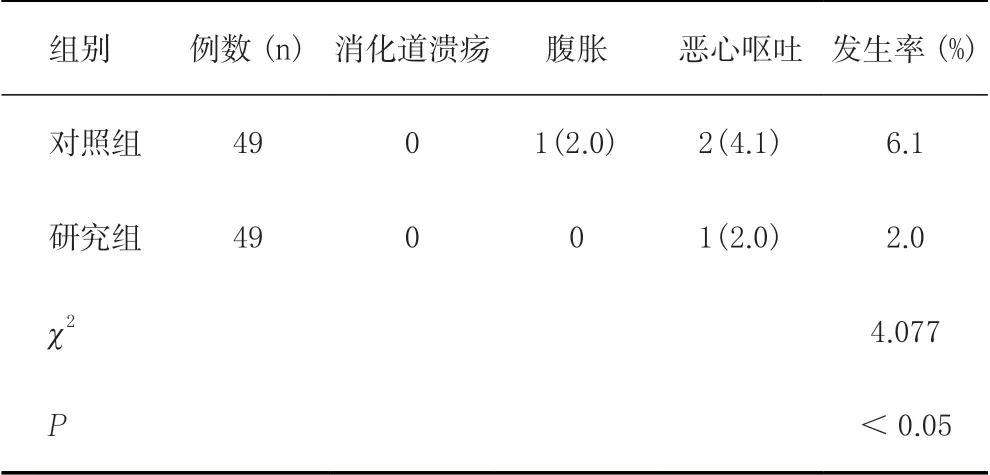
表4 兩組不良反應發生率的比較結果[n(%)]Table 4 Comparison of incidences of adverse reactions of the premature infants between the two groups[n(%)]
3 討論
3.1 BPD 的發病因素及治療現狀
BPD是早產兒中比較嚴重的并發癥之一,對早產兒生命及健康造成了嚴重的影響。據臨床數據統計顯示,早產兒中約有70%會出現BPD[6]。針對該類患兒多需借助呼吸機協助通氣,進而增加了患兒發生肺部感染的幾率。有研究指出,引起早產兒出現BPD的關鍵環節為肺發育不成熟、急性肺損傷及急性肺損傷后異常修復[7]。目前,臨床對BPD常用治療方法有吸氧、營養干預、利尿、機械通氣及糖皮質激素類藥物等[8]。有研究指出,糖皮質激素類藥物治療對于炎癥反應可起到較強的抑制作用,緩解患兒肺纖維化,進而達到改善肺功能的目的[9]。
3.2 糖皮質激素類藥物聯合氨溴索治療BPD 的效果分析
氨溴索是一種黏液溶解劑,可使患兒呼吸道內痰液黏度降低,提高了支氣管纖毛運動,保持呼吸道暢通[10]。在對早產兒BPD患兒治療過程中,氨溴索聯合糖皮質激素可使患兒支氣管和肺部功能得到快速恢復。本研究結果顯示,研究組患兒吸氧時間及機械通氣時間均明顯少于對照組,說明對早產兒BPD患兒采用氨溴索聯合糖皮質激素可縮短治療時間。本研究結果還顯示,使用糖皮質激素聯合氨溴索可提高早產兒BPD的治療效果,且并未增加患兒不良反應的發生。因此認為糖皮質激素在治療早產兒BPD中具有一定的安全性。
3.3 氨溴索聯合糖皮質激素對患兒炎性因子的影響
目前有研究指出,BPD與炎癥反應之間存在密切聯系,IL-1β及TNF-α是機體內比較常見的炎癥啟動因子,對機體炎癥發展可起到促進作用[11]。IL-1β是機體常見的促炎因子,對炎癥發展可起到促進作用,其水平含量上升可加速炎癥反應,加重組織損傷程度。TNF-α屬于機體內常見趨化因子,對肺部組織具有很強的細胞毒性,對炎癥細胞聚集可起到促進作用,加速炎癥細胞的產生,使機體內其他炎癥因子的危害程度增強。本研究結果顯示,研究組的IL-1β及TNF-α水平均顯著低于對照組,說明采用氨溴索聯合糖皮質激素治療早產兒BPD可降低機體炎癥因子水平,緩解機體炎癥發展,促進患兒康復。
綜上所述,對早產兒BPD患兒采用氨溴索聯合糖皮質激素治療可有效提高治療效果,促進患兒機體恢復,臨床上應當進一步推廣應用。

