辣椒種子拮抗青枯病菌內生細菌的分離、鑒定
牟玉梅 范高領 邢丹


摘 要: 為了探究抗青枯病辣椒品種種子中拮抗青枯病菌內生細菌的種群組成及其在青枯病防治中可能發揮的生態學功能,從抗青枯病辣椒品種種子中分離、篩選出拮抗青枯病菌的內生細菌,對其進行抑菌廣譜性分析,測定其對青枯病的生防效果。結果表明,從抗青枯病辣椒品種種子中分離出14株內生細菌,通過平板對峙,篩選出6株拮抗青枯病菌的內生細菌,初步鑒定它們分別為假單胞菌(Pseudomonas)、蒼白桿菌(Ochrobactrum)和微桿菌(Microbacterium)。對6株內生細菌進行抑菌廣譜性研究,所有內生細菌均至少對1種病原真菌有拮抗作用;將6株內生細菌的菌懸液分別對辣椒種子進行浸種處理后育苗,辣椒苗抗青枯病能力顯著提升。辣椒種子中拮抗青枯病菌的內生細菌具有多樣性,用其菌懸液處理辣椒種子后,植株對青枯病具有較好的抗病能力,為開展辣椒青枯病微生物防治提供了理論依據及菌種資源。
關鍵詞: 辣椒; 種子; 內生細菌; 拮抗作用; 生物防治
中圖分類號:S641.3? ?文獻標志碼:A? ?文章編號:1673-2871(2020)02-042-06
Isolation and identification of endophytic bacteria against bacterial wilt in pepper seeds
MOU Yumei, FAN Gaoling, XING Dan
(Pepper Research Institute, Guizhou Academy of Agricultural Sciences, Guizhou 550006, Guiyang, China)
Abstract: This experiment is to investigate the population composition of antagonistic endophytic bacteria and its potential ecological function in the prevention and treatment of green dead pepper varieties. To isolate and screen the endophytic bacteria that antagonize the green dead bacteria from the seeds of pepper varieties with anti-green dead disease, and to analyze their antimicrobial spectrum, to determine their effect on the prevention of green dead disease. Fourteen strains of endophytic bacteria were isolated from the seeds of capsicum varieties resistant to bacterial wilt. Six strains of endophytic bacteria were screened out through plate confrontation. They were identified as Pseudomonas, Pallidobacterium and Microbacterium. Six strains of endophytic bacteria were studied for broad-spectrum bacteriostasis. All endophytic bacteria had antagonistic effect on at least one kind of pathogenic fungi. Six strains of endophytic bacteria were soaked in pepper seeds and then cultured. The ability of pepper seedlings to resist bacterial wilt was significantly improved. The endophytic bacteria that antagonize green pepper bacteria in pepper seeds are diverse. After treating pepper seeds with their suspension, the plants have a good effect on green dead disease, and provide theoretical basis and bacterial resources for the prevention and treatment of pepper green dead disease.
Key words:? Pepper; Seeds; Endophytic bacteria; Antagonistic effect; Biological control.
辣椒是我國種植面積最大的蔬菜作物[1]。辣椒青枯病是我國各辣椒主產區普遍發生的一種毀滅性土傳病害,防治難度較大[2]。采用常規方法選育抗病品種,存在選育周期長、抗性單一的缺點;采用分子育種技術,其過程非常復雜,且在辣椒育種中成功應用的還不多[3];采用化學藥劑又涉及到食品安全性和環境安全性安全評價問題。內生菌生物防治可以較好地解決上述問題[4],不僅可以促進作物生長、增產增收,還可以提高植物抗病性、改善品質以及改良土壤。國內外科研人員針對辣椒青枯病生物防治做了不少研究,篩選了很多新的防控辣椒青枯病的生防菌,但還沒有發現一個成功應用于大批量生產和推廣且能較好防治辣椒青枯病的生防菌。
內生菌是一類生活在植物體內且對植物無明顯不利影響的微生物的總稱[5]。植物攜帶豐富的內生菌資源,這些微生物對植物的生長發育、代謝過程和抗逆抗病等性狀產生重要影響。種子作為植物物種延續的重要繁殖器官,是植物內生菌垂直傳播的重要方式。種子內生菌與植物經過長期、穩定的進化選擇,相比于從其他植物器官中分離的內生菌更易長期定殖生存,也更易演化出與宿主互惠互利的代謝途徑[6]。種子中的內生菌防效具有較為穩定、持久的優點,可作為拮抗菌劑的菌種資源,具有很好的應用前景。
因此,筆者以抗青枯病辣椒品種的種子為材料,從中分離篩選出對辣椒青枯病菌有較強拮抗作用的內生菌株,并鑒定其分類地位,開展抑菌廣譜性研究,以期豐富現有的生防菌種資源,為辣椒種子內生細菌及其生物防治的研究提供一定的理論基礎。
1 材料與方法
1.1 材料
優質地方辣椒種質資源18份(由貴州省辣椒研究所在多年連作重茬的辣椒地自然誘發篩選出的具有較好綜合抗病性的辣椒種質)。青枯病菌為貴州省農業科學院辣椒研究所保存的茄科雷爾氏菌株EP1(登錄號:CP015116.1)。培養基為NA固體培養基、NA液體培養基、固體LB培養基。
1.2 方法
1.2.1 辣椒抗青枯病品種篩選鑒定 對18份地方優質辣椒種質資源進行苗期青枯病抗性表型鑒定,進一步確認材料抗性水平(2016年10月,在貴州省辣椒研究所貴陽試驗基地進行)。將供試材料采用160穴漂浮育苗盤進行育苗,每個品種育苗160株,待幼苗長至5~6片真葉時,選擇健壯的植株移栽至10 cm×10 cm的塑料杯內(數量在70~106株之間),完全隨機排列,置于(26±2) ℃人工氣候室繼續生長,正常肥水管理,待長到7~8片葉期采用傷根灌根接種法接種青枯病菌,進一步篩選高抗辣椒青枯病品種。
青枯病病情調查方法:接種后每天調査和記錄辣椒植株的發病情況,待病情穩定后按病情分級標準統計發病情況,計算發病率和病情指數,參試各種質對青枯病的抗性表型最終評價以第30天的發病率和病情為準。青枯病病情分級標準參照劉富中[7]、黨峰峰[8]等對青枯病的分級標準(表1~2)。發病率/%=發病株數/接種株數×l00,病情指數(DI)/%=∑[(病級×該病級株數)/(最髙病級×接種株數)]×l00。
1.2.2 辣椒種子內生細菌的分離、純化、保存 種子消毒:將辣椒種子在70%酒精中浸泡5 min,0.1%升汞消毒40 s,然后轉入到體積分數2.5%的次氯酸鈉溶液中浸泡5 min,最后用無菌水沖洗3次,將最后一次沖洗用的無菌水涂布分離培養基營養瓊脂平板,置于30 ℃培養3 d,驗證表面消毒情況。
內生細菌分離、純化、保存:將徹底消毒后的種子置于無菌研缽中,加入質量分數0.85%的NaCl溶液充分研磨后,吸取1 mL上清液進行梯度稀釋、營養瓊脂平板涂布,30 ℃培養箱內培養2 d,挑取不同形態、顏色、大小的菌落劃線純化3次,直到平板上菌落的顏色、大小和形態完全一致,然后將純化后的菌株保存在含有20%甘油的菌種保藏管中,-80 ℃凍存。
1.2.3 內生細菌對青枯病菌的抑制作用測定 采用紙蝶法測定內生細菌對青枯病菌的抑制作用,篩選對青枯病菌具有拮抗作用的內生細菌。吸取1 mL濃度為5×l08 cfu·mL-1的青枯病菌懸浮液放入滅菌培養皿中,將45 ℃ NA培養基倒入培養皿中與菌液搖勻,待冷卻后對稱放置2張5 mm滅菌濾紙片,距離培養皿中心距離約為25 mm,每張濾紙片上滴入內生細菌5 μL,每處理重復3皿,以無菌水為對照,置于28~30 ℃恒溫箱中培養48 h,觀察抑菌效果。拮抗作用強弱以“+”表示。“+++”表示拮抗活性很強,抑菌帶寬度大于8.0 mm;“++”表示拮抗活性中等強度,抑菌帶寬度在3.0~8.0 mm之間;“+”表示拮抗活性弱或無活性,抑菌帶寬度小于3.0 mm,或者無抑菌帶,病菌正常生長,且可覆蓋內生細菌。
1.2.4 拮抗青枯病菌內生細菌的鑒定 對青枯病菌具有拮抗作用的內生細菌進行形態學和分子生物學鑒定。
形態學鑒定:在固體LB培養基上劃線接種待鑒定菌株,28 ℃恒溫培養24 h,記錄菌落的顏色、形狀、透明度以及表面邊緣隆起程度等性狀,對細菌進行革蘭氏染色和形態觀察,對種屬進行初步鑒定。
分子生物學鑒定:對菌株16S rDNA 序列進行測定。使用細菌基因提取試劑盒進行基因組DNA提取。以提取的待鑒定菌株DNA為模板,以細菌的16S引物序列27f /1492R進行內生細菌的16S rDNA擴增。PCR以30 μL的體系進行,體系如下:H2O 17.8 μL,Buffer 3 μL,dNTP 2 μL,Primer1 3 μL,Primer2 3 μL,DNA模板1 μL,酶0.2 μL。PCR反應條件為:95 ℃預變性3 min,循環1次;95 ℃變性30 s,55 ℃退火30 s,72 ℃延伸2 min,循環35次;最后72 ℃延伸10 min。用1%的瓊脂糖凝膠電泳檢測PCR擴增結果,利用凝膠成像系統觀察PCR擴增結果。將辣椒種子內生細菌PCR擴增結果送往北京六合華大基因科技有限公司武漢分公司進行分子鑒定,將菌株的測序結果與GenBank數據庫中的序列進行比對。
1.2.5 拮抗青枯病菌內生細菌的抑菌廣譜性研究 對已篩選出的拮抗內生細菌采用平板對峙生長法,測定其對辣椒炭疽病、疫病、立枯病病菌的拮抗作用。
將內生菌株劃線活化培養后,挑取單菌落接種于20 mL LB培養液中,置于30 ℃搖床中200 r·min-1振蕩培養過夜;辣椒立枯、炭疽、疫病病原菌接種到PDA培養基平板上,于28 ℃恒溫條件下培養,待菌絲長滿整個培養皿后,制成5 mm的菌餅備用。
在直徑9 cm的PDA平板中央接入直徑5 mm的病原菌菌餅,視病原真菌生長速度選擇合適時期接種分離到的細菌(炭疽和立枯絲核菌與細菌同時接種,疫霉待菌絲擴增1 cm后再接種待測細菌)。在距中央25 mm處對稱放置2張5 mm滅菌濾紙片,每張濾紙片上滴入活化培養的分離菌株菌液5 μL,28 ℃左右繼續黑暗培養,設不接種分離菌株的處理為對照,每個菌株重復處理3皿,待對照皿中真菌菌絲即將長滿皿時測量抑菌圈大小,計算抑菌率。抑菌率/%=(1-處理菌落直徑)/對照菌落直徑×100[9]。
1.2.6 內生細菌對辣椒青枯病生物防治效果的測定 將辣椒種子置于濃度為109 cfu·mL-1內生細菌菌懸液中浸泡4 h,無菌水沖洗3次后進行漂浮育苗,待幼苗長至5~6片真葉,從育苗盤中選取健壯植株,拔出洗凈根部,分別浸泡在對應的菌株菌懸液中20 min,以LB培養液替代菌懸液浸泡作為對照,每處理6~8株,3次重復。采用傷根灌根接種法接種青枯病菌,觀察記錄發病情況,計算相對防效。相對防效(BE)/%=[(CK的病情指數-試驗處理的病情指數)/CK病情指數]×100。
1.3 數據分析
利用軟件DPS 7.05進行方差分析,利用Excel 2007進行常規數據及表格處理。
2 結果與分析
2.1 抗青枯病辣椒種子樣品的篩選
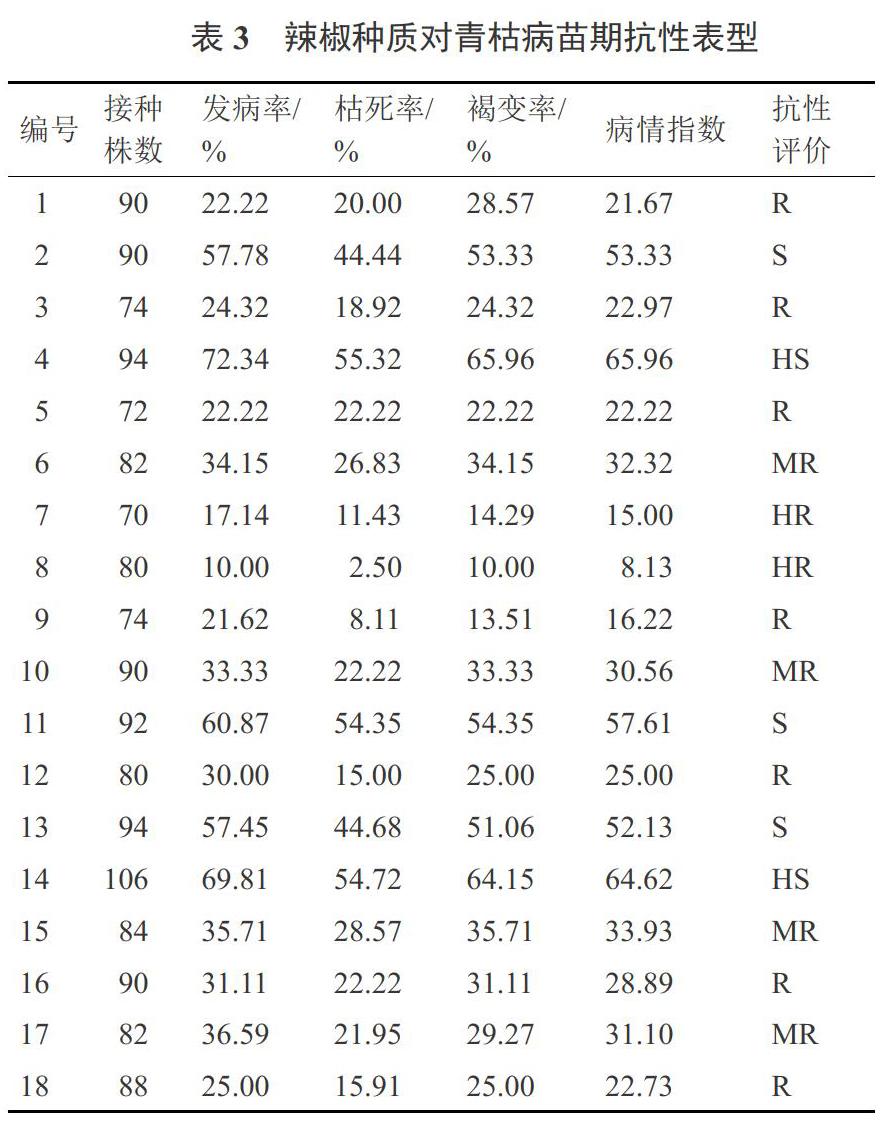
通過苗期青枯病抗性鑒定,從抗性表現良好的18份辣椒種質資源中,篩選出對青枯病抗性最好、最穩定的辣椒種質資源2份(試驗序號為7號、8號),將其種子作為本次試驗的樣品材料(表3)。
2.2 辣椒種子內生細菌的分離純化
將上述抗性最佳的2份抗青枯病辣椒種子經外表消毒殺菌后,混合研磨成漿,在培養基中進行培養、分離、純化,獲得14株內生細菌(編號為gz1~gz14)。
2.3 拮抗青枯病菌內生細菌的篩選
將獲取的14株內生細菌與青枯病菌進行平板對峙,6株內生細菌(gz1、gz6、gz7、gz11、gz13、gz14)對青枯病菌有拮抗作用(表4)。其中,菌株gz6、gz7、gz11、gz13對辣椒青枯病菌的抑菌圈直徑>25 mm,抑菌帶寬度>8 mm,表現拮抗活性很強,抑菌作用強度為“+++”;菌株gz13對辣椒青枯病菌的抑菌圈直徑達到42.22 mm,抑菌帶寬度達到15.60 mm,對辣椒青枯病菌表現出很強的拮抗活性(圖1)。
2.4 拮抗青枯病菌內生細菌的鑒定
對篩選出的對青枯病菌具有拮抗作用的6株內生細菌,進行形態學和分子生物學方法鑒定。
形態學鑒定:gz1菌落呈圓形、光滑、微凸、邊緣整齊、濕潤、菌落顏色為無色、革蘭氏染色結果為陰性、菌體呈桿狀。gz6菌落邊緣光滑、凸起、呈膿液狀、菌落顏色為淺灰綠色、革蘭氏染色結果為陰性、菌體呈球桿狀。gz7菌落邊緣光滑、微凸、呈膿液狀、菌落顏色為綠色、革蘭氏染色結果為陰性、菌體呈桿狀或長絲狀(圖1-A)。gz11菌落多呈圓形、邊緣光滑整齊、微凸、濕潤、菌落顏色為無色、革蘭氏染色結果為陰性、菌體呈桿狀或絲狀。gz13菌落表面光滑、半透明、邊緣整齊、有光澤、菌落顏色為淡黃色、革蘭氏染色結果為陽性、細胞呈球狀或細長、不規則的桿狀(圖1-B)。gz14菌落邊緣光滑、微凸、呈膿液狀、菌落顏色為淺綠色、革蘭氏染色結果為陰性、菌體呈球桿狀。
分子生物學鑒定:6株內生細菌的16S rDNA PCR產物均在750 bp左右,條帶清晰。將6株內生細菌的16S rDNA 序列與GenBank數據庫中的序列進行比對,找到了同源性高的相似菌株序列,結果為:3株屬于或與黏液型銅綠假單胞菌最相似(屬于變形菌門,γ-變形菌綱,假單胞菌目,假單胞菌科,假單胞菌屬);2株屬于或與蒼白桿菌最相似(屬于變形菌門,α-變形菌綱,根瘤菌目,布魯氏菌科,蒼白桿菌屬);1株屬于或與微桿菌最相似(屬于放線菌門,微桿菌科,微桿菌屬)(表5)。
結合形態學和16S rDNA 序列同源性分析,將菌株gz6、gz7、gz14鑒定為黏液型銅綠假單胞菌(Pseudomonas aeruginosa),菌株gz1、gz11鑒定為蒼白桿菌(Ochrobactrum),菌株gz13鑒定為微桿菌(Microbacterium)。
2.5 內生細菌抑菌廣譜性測定
由表6可知,6株內生細菌均至少對其中一種病原真菌有拮抗作用,其中:有3株內生細菌(gz6、gz7、gz14)對3種植物病原真菌均有拮抗作用,有2株內生細菌(gz11、gz13)對2種植物病原菌有抑制作用,有1株內生細菌(gz1)只對1種植物病原菌有抑制作用。總體而言,大部分內生細菌對立枯絲核病菌、辣椒炭疽病菌拮抗作用強。gz6、gz7、gz14對辣椒疫霉菌、立枯絲核病菌、炭疽病菌均有較好抑制作用,且對辣椒青枯病菌也有很明顯的抑制作用,具有廣譜抑菌性,可作為有應用前景的生物資源加以研究。
2.6 內生細菌對辣椒青枯病的生防效果
對6株內生細菌進行辣椒青枯病的溫室控病試驗(表7),結果表明,均具有不同程度的生防效果。6株內生細菌菌株處理后的辣椒植株發病率、病情指數均低于對照。接種28 d時仍有5株株菌具有較明顯的相對防效,其中,相對防效大于60%的有3株,分別是gz7、gz11、gz14;相對防效介于30%~60%的有2株,從大到小依次為gz13、gz6。且有5株株菌能使辣椒推遲發病。
將內生細菌對青枯病菌的抑菌帶寬與它們對辣椒青枯病的溫室控病效果相比較,從圖2可以看出,隨著抑菌帶寬度的增加,相對防病效果并沒有完全呈現增加趨勢,可能是因為種子浸種后部分內生菌株的定殖效果不好,或者菌株生長環境的變化,導致其不能正常發揮抑菌功效,因此,在應用這些菌株前,仍然需要進行大量的驗證試驗。
3 討論與結論
在已有拮抗青枯病菌內生細菌的篩選及其對青枯病生物防治的研究報道中,拮抗內生細菌大部分是從植株根、莖、葉等部位分離的,從種子中分離內生細菌的研究較少,且分離的對青枯病菌具有抗性和生物防效的內生細菌多為芽孢桿菌。如劉杰鳳等[10]從番茄、辣椒和茄子3種茄科果蔬中篩選出的14株對青枯病菌有強拮抗性的內生細菌,分屬為芽孢桿菌屬、埃希氏菌屬、克雷伯氏菌屬、土壤單胞菌屬、歐文氏菌屬、短小桿菌屬,其中芽孢桿菌為優勢種群,而且芽孢桿菌屬菌株對青枯病菌的拮抗作用最強。蔡長平[11]從多年連作重茬的辣椒地健康植株根系中分離的1株內生拮抗細菌PEB-99,對辣椒青枯雷爾氏菌、辣椒疫霉菌、辣椒炭疽病菌、辣椒鐮刀枯萎病菌都有顯著抑制效果,屬于貝萊斯芽孢桿菌。江歡歡等[12]從辣椒根際土壤中分離篩選出1株對青枯病菌具有較強拮抗作用的菌株4S,鑒定為枯草芽孢桿菌。孔凡玉等[13]在福建、廣東、貴州等地感染青枯病的煙株根部及番茄根部分離出的對青枯病具有拮抗作用的內生細菌,3個屬于芽孢桿菌屬,2個屬于假單胞桿菌。
筆者從抗青枯病辣椒種子中分離出14株內生細菌,其中6株內生細菌對青枯病菌有較好的拮抗作用。結合形態學和16S rDNA序列同源性分析,對6株內生細菌進行鑒定,發現3株屬于黏液型銅綠假單胞菌,2株屬于蒼白桿菌,1株屬于微桿菌。6株菌株均具有生防效果,其中菌株gz7、gz11、gz14對辣椒青枯病的生防效果最佳,具有防治疫病、炭疽病、立枯病等多種病害的潛力,是一種潛在的、有效的生防菌株,但未對其進行田間生物防效試驗,需要在后續研究中繼續完成。試驗還發現隨著抑菌帶寬度的增加,內生細菌對辣椒青枯病的控病效果并沒有完全呈現增加趨勢,可能是因為種子浸種后部分內生菌株的定殖效果不好,或者菌株生長環境的變化,導致其不能正常發揮抑菌功效,因此在應用這些菌株前,仍需進行大量的驗證試驗。
筆者從抗青枯病辣椒品種種子中篩選出拮抗青枯病菌的內生細菌6株,并對其進行抑菌廣譜性和辣椒育苗期生防能力研究,為辣椒青枯病生物防治探索了新的途徑、篩選了功能菌種、提供了理論依據。尤其6株拮抗內生細菌均從種子中獲得,種子作為植物物種延續的重要繁殖器官,從中分離的內生菌更易長期定殖生存,也更易演化出與宿主互惠互利的代謝途徑[6],在辣椒生產中應用更為簡便,防效更為穩定、持久,有助于從種子源頭處開展生物防治。
參考文獻
[1] 馬艷青,張西露.湖南辣椒產業現狀及發展思考[J].湖南農業科學,2009(12):94-97.
[2] 黃志農,文吉輝,符偉.湖南辣椒生產概況與病蟲害綠色防控[J].辣椒雜志,2011,9(4):43-47.
[3] 曹坳程.毀滅性土傳病害綜合治理技術體系的構建與創新[J].基層農技推廣,2016(11):108.
[4] 張海利,陳永兵,徐堅.番茄青枯病生物防治研究進展[J].農業科技通訊,2008(8):98-101.
[5] 王志偉,紀燕玲,陳永敢.植物內生菌研究及其科學意義[J].微生物學通報,2015,42(2):349-363.
[6] 焦蓉,劉劍金,楊煥文,等.抑制煙草黑脛病菌和促煙草幼苗生長內生菌的分離與鑒定[J].云南農業大學學報(自然科學),2018,33(6):1037-1045.
[7] 劉富中,連勇,馮東昕,等.茄子種質資源抗青枯病的鑒定與評價[J].植物遺傳資源學報,2005,6(4):381-385.
[8] 黨峰峰,雷玉芬,官德義,等.辣椒種質資源抗青枯病的鑒定與評價[J].植物科學學報,2013,31(4):378-384.
[9] 郎劍鋒,楊蕊,趙榮艷.對玉米莖基腐病菌有拮抗活性木霉菌株的篩選[J].安徽農業科學,2010,38(5):2419-2420.
[10] 劉杰鳳,韓寒冰,張進鳳,等.茄類內生菌的分離及拮抗細菌的篩選[J].安徽農業科學,2009,37(3):1160-1162.
[11] 蔡長平,黃軍,曾艷,等.一株辣椒內生拮抗細菌的篩選及初步鑒定[J].湖南農業科學,2018,(7):1-4.
[12] 江歡歡,程凱,楊興明,等.辣椒青枯病拮抗菌的篩選及其生物防治效應[J].土壤學報,2010,47(6):1225-1231.
[13] 孔凡玉,趙廷昌,張成省,等.防治煙草青枯病生防菌篩選及田間防治試驗研究[C]//中國植物保護學會會員代表大會暨學術年會,2005.

