經(jīng)導(dǎo)管主動脈瓣置入手術(shù)在主動脈瓣狹窄合并二尖瓣反流治療中的療效分析
王 圣 黃乾海 程兆云 陳現(xiàn)杰 陸國慶 趙 亮
主動脈瓣狹窄為機(jī)體心臟主動脈瓣局部鈣化、解剖結(jié)構(gòu)異常引發(fā)的一種退行性病變。主動脈瓣狹窄多高發(fā)于高齡人群中,我國≥65歲的患者中鈣化性主動脈瓣狹窄的患病率為0.60%,65~84歲患者中患病率為0.55%,而≥85歲患者中為1.41%[1]。另有報道顯示,≥65歲人群中主動脈瓣狹窄的發(fā)生率為16.9/1 000,65~84歲人群中發(fā)生率為15.7/1 000,而≥85歲患者中為42.6/1 000[2]。
隨著病情進(jìn)展患者的左心室流出道會逐步阻塞,以至于心臟搏出量下降,甚至?xí)l(fā)生心力衰竭及其他不良事件而死亡[3]。一旦出現(xiàn)臨床癥狀,該病患者的2年死亡率可超過50%[4],因此及時給予有效地治療干預(yù)具有非常重要的意義。由于主動脈瓣狹窄患者的年齡普遍較高,傳統(tǒng)開放性手術(shù)的組織創(chuàng)傷大,術(shù)中血流動力學(xué)波動顯著,手術(shù)風(fēng)險性高。隨著醫(yī)療技術(shù)的發(fā)展,目前經(jīng)導(dǎo)管主動脈瓣置入手術(shù)為重癥高齡高危主動脈瓣狹窄患者的常用治療方法。
主動脈瓣狹窄患者中二尖瓣反流(mitral regurgitation,MV)的比例處于較高水平,MR通常是由于局部組織鈣化、左心室重構(gòu)或瘤樣病變等因素導(dǎo)致的病變,MR會進(jìn)一步加重患者的主動脈瓣狹窄病情[5]。以往研究者多認(rèn)為,主動脈瓣狹窄合并重度MR多采用主動脈瓣置換術(shù)聯(lián)合二尖瓣修復(fù)/置換術(shù),該類患者不能采用經(jīng)導(dǎo)管主動脈瓣膜置入術(shù)[6]。近年來,有研究發(fā)現(xiàn)經(jīng)導(dǎo)管主動脈瓣膜置入術(shù)能夠治療主動脈瓣狹窄合并MR患者[7],但是經(jīng)導(dǎo)管主動脈瓣膜置入術(shù)對主動脈瓣狹窄合并不同程度MR患者的近遠(yuǎn)期療效尚沒有明確。因此,本研究選取我院自 2017 年5月至2019年5月,就診的主動脈瓣狹窄合并MR患者,分析經(jīng)導(dǎo)管主動脈瓣置入手術(shù)在主動脈瓣狹窄合并MR治療中的療效,為臨床中患者治療方案的確定提供依據(jù)。
資料與方法
1.一般資料 選取我院自 2017 年5月至2019年5月,就診的主動脈瓣狹窄合并MR患者共31例,患者的納入標(biāo)準(zhǔn)為:①符合《心血管病診療標(biāo)準(zhǔn)》[8]中主動脈瓣狹窄以及MR的診斷標(biāo)準(zhǔn);②經(jīng)臨床各科室會診后發(fā)現(xiàn)患者不適合外科開胸手術(shù)或外科手術(shù)高風(fēng)險;③患者或家屬對本研究知情同意。本研究經(jīng)本院醫(yī)學(xué)倫理委員會審核批準(zhǔn)。排除標(biāo)準(zhǔn)為:①近期內(nèi)有心腦血管不良事件或消化道出血等疾病或經(jīng)導(dǎo)管主動脈瓣置入手術(shù)禁忌證者;②對造影劑過敏者;③存在因其他因素影響患者生活質(zhì)量或伴有惡性腫瘤等致死性疾病者。按照患者的MR嚴(yán)重程度將其分為A組(輕度,18例)和B組(中度、重度,13例)。
2.方法 術(shù)前需經(jīng)實驗室和影像學(xué)診斷并經(jīng)各科室會診確定手術(shù)治療方案,按照每例患者的主動脈瓣瓣膜結(jié)構(gòu)參數(shù)分析,確定術(shù)中置入心臟瓣膜的規(guī)格尺寸,并評估手術(shù)風(fēng)險。所有患者均行經(jīng)導(dǎo)管主動脈瓣置入手術(shù)治療,手術(shù)首選經(jīng)股動脈入路,如外周血管狹窄或鈣化迂曲嚴(yán)重,則選擇經(jīng)心尖入路。在雜交手術(shù)室中由心外科醫(yī)師、心內(nèi)科醫(yī)師和麻醉醫(yī)師共同參與手術(shù)過程,入室后常規(guī)鋪巾,全身麻醉,氣管插管,連接呼吸機(jī),并建立深靜脈通路,右心室內(nèi)置入臨時起搏導(dǎo)線,并連接臨時起搏器備用。根據(jù)入路不同手術(shù)流程已在其他文獻(xiàn)中描述,穿刺左側(cè)股動脈置入6 F豬尾導(dǎo)管,注入造影劑給予主動脈根部造影,導(dǎo)管預(yù)裝人工瓣膜,首先對主動脈瓣進(jìn)行球囊預(yù)擴(kuò)張,通過主動脈根部造影反復(fù)核查人工瓣膜和瓣葉所在平面的位置,釋放人工瓣膜的同時提快心率,手術(shù)結(jié)束時再通過經(jīng)食管超聲心動圖以及主動脈根部造影評估人工瓣膜的位置、形態(tài)、瓣周狀況和功能情況。最后取出鞘管,縫合切口,常規(guī)用藥處理。
3.觀察指標(biāo) 記錄并比較兩組患者的并發(fā)癥發(fā)生率,比較兩組在術(shù)前、術(shù)后1個月的心功能指標(biāo)LVEF、LVEDD、MR和美國紐約心臟病學(xué)會NYHA分級,定期隨訪觀察患者的病情變化,叮囑患者在術(shù)后3個月時入院復(fù)查,比較兩組患者在術(shù)后1個月、3個月時的死亡率和生活質(zhì)量。LVEF、LVEDD、MR采用超聲心動圖進(jìn)行測定;生活質(zhì)量采用日常生活能力量表(activity of daily living scale,ADL)進(jìn)行評估,該量表共14項內(nèi)容,評分為16~64分,分值越低則日常生活能力越好。NYHA分級標(biāo)準(zhǔn)為,①I級:體力活動時沒有明顯的臨床癥狀;②II級:日常活動時會出現(xiàn)氣促、心悸等癥狀,心臟結(jié)構(gòu)輕微異常;③III級:輕微活動時會出現(xiàn)氣促、心悸等癥狀,心臟結(jié)構(gòu)存在明顯病變;(4)IV級:休息狀態(tài)下出現(xiàn)心衰等嚴(yán)重癥狀,已經(jīng)處于終末期。
4.統(tǒng)計學(xué)方法 所有數(shù)據(jù)使用統(tǒng)計學(xué)軟件SPSS25.0分析。計量資料以均數(shù)±標(biāo)準(zhǔn)差表示,組間比較采用獨立樣本t檢驗,組內(nèi)比較采用配對樣本t檢驗。計數(shù)資料以頻數(shù)(百分率)表示,采用卡方檢驗。以P<0.05為差異有統(tǒng)計學(xué)意義。
結(jié) 果
1.兩組患者的LVEF、LVEDD、MR和NYHA分級比較 術(shù)后1個月時的LVEF、LVEDD、MR和NYHA分級同術(shù)前相比有統(tǒng)計學(xué)差異(P<0.05);A組在術(shù)后1個月時的LVEF值明顯高于B組(P<0.05);A組在術(shù)后1個月時的LVEDD和NYHA分級明顯低于B組,A組在術(shù)后1個月時的MR程度明顯低于B組(P<0.05,表1)。

表1 兩組患者的LVEF、LVEDD、MR和NYHA分級比較
2.兩組患者的死亡率和生活質(zhì)量比較 A組在術(shù)后1個月時的ADL評分均明顯高于B組(P<0.05);A組在術(shù)后1個月時的死亡率明顯低于B組(P<0.05);兩組患者在術(shù)后3個月時的死亡率和ADL評分均差異無統(tǒng)計學(xué)意義(P>0.05,表2)。
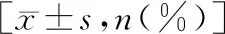
表2 兩組患者的死亡率和生活質(zhì)量比較
3.兩組患者的并發(fā)癥比較 各個并發(fā)癥發(fā)生率均差異無統(tǒng)計學(xué)意義(P>0.05,表3)。

表3 兩組患者的并發(fā)癥比較[n(%)]
討 論
本研究中得出兩組在術(shù)后1個月時的LVEF、LVEDD、MR和NYHA分級同術(shù)前相比差異有統(tǒng)計學(xué)意義(P<0.05);A組在術(shù)后1個月時的LVEF值和ADL評分均明顯高于B組(P<0.05);A組在術(shù)后1個月時的死亡率、LVED、MR和NYHA分級明顯低于B組(P<0.05);兩組患者在術(shù)后6個月時的死亡率和ADL評分均差異無統(tǒng)計學(xué)意義(P>0.05),可見經(jīng)導(dǎo)管主動脈瓣置入手術(shù)可用于主動脈瓣狹窄合并不同程度MR患者的治療中,能夠顯著改善患者的心功能,合并重度和中度MR會提高患者術(shù)后短期的死亡率,而不會影響患者長期的死亡率,此時MR的嚴(yán)重程度對術(shù)后患者遠(yuǎn)期死亡率和生活質(zhì)量恢復(fù)的影響較小。劉先寶等[9]的臨床研究指出,經(jīng)導(dǎo)管主動脈瓣置入手術(shù)可用于主動脈瓣重度反流患者的治療中,促進(jìn)患者心功能的恢復(fù)。一項國外研究中表明,在經(jīng)導(dǎo)管主動脈瓣置入手術(shù)后,合并重度和中度MR患者的LVEF值比未合并者的明顯降低,LVEDI值比未合并者的明顯增高[10],這同本文的結(jié)果相符,該術(shù)式對組織的創(chuàng)傷小,同常規(guī)心臟手術(shù)相比術(shù)中不用進(jìn)行體外循環(huán),術(shù)后可較快改善患者的日常生活能力[11]。
另外,經(jīng)導(dǎo)管主動脈瓣置換術(shù)后多數(shù)合并MR患者的反流程度可能會明顯好轉(zhuǎn),因此,臨床中考慮是否對主動脈瓣狹窄合并MR患者更適用于該術(shù)式,但是仍然有少量患者術(shù)后反流加重,本文中1例患者出現(xiàn)重度瓣膜反流而死亡。既往研究指出,經(jīng)導(dǎo)管主動脈瓣置換術(shù)后一個月內(nèi),合并中度、重度MR患者的死亡率比合并輕度者明顯上升,且兩者在一年內(nèi)的死亡率接近[12],這同本文結(jié)果一致。而D’Onofrio 等[10]的文獻(xiàn)研究發(fā)現(xiàn),在經(jīng)導(dǎo)管主動脈瓣置入手術(shù)后,合并重度和中度MR患者的院內(nèi)死亡率和20個月內(nèi)的死亡率均接近,與本文結(jié)果不一致,分析可能同隨訪時間、病例數(shù)目等因素有關(guān)。
有研究發(fā)現(xiàn),自膨式經(jīng)導(dǎo)管主動脈瓣置換術(shù)在有癥狀的重度主動脈瓣狹窄患者治療中具有良好的療效[13]。但是,該術(shù)式較復(fù)雜,患者年齡較高,術(shù)后可能會發(fā)生房室傳導(dǎo)阻滯、腦血管病變、出血和血小板減少癥等并發(fā)癥[14],本文中兩組患者術(shù)后的并發(fā)癥發(fā)生率均差異無統(tǒng)計學(xué)意義(P>0.05),可見合并不同程度MR的主動脈瓣狹窄患者在經(jīng)導(dǎo)管主動脈瓣置換術(shù)后的并發(fā)癥發(fā)生率接近。血小板減少癥是為了預(yù)防出血使用肝素引發(fā)的,及時處理后血小板計數(shù)水平恢復(fù),而腦血管病變可能會導(dǎo)致患者死亡[15],術(shù)后應(yīng)注意監(jiān)控和處理。
綜上所述,經(jīng)導(dǎo)管主動脈瓣置入手術(shù)可用于主動脈瓣狹窄合并不同程度MR患者的治療中,此時MR的嚴(yán)重程度對術(shù)后患者遠(yuǎn)期死亡率和生活質(zhì)量恢復(fù)的影響較小。

