血栓彈力圖下抗凝干預對心臟瓣膜術后抗凝效果的價值
霍焱,常瑩,車輯
(首都醫科大學附屬北京安貞醫院輸血科,北京)
0 引言
心臟瓣膜術是一種以機械心臟瓣膜替代心臟瓣膜病患者已病變瓣膜的常用外科手術,血栓栓塞作為心外科手術較常見的并發癥,也會給心臟瓣膜術患者帶來較高的二次手術率及病死率[1-2]。本研究選取2016 年9 月至2018 年9 月在我院進行心臟瓣膜術患者200 例作為研究對象,探討TEG 在心臟瓣膜術后對患者凝血功能的評估作用,現將結果報告如下。
1 資料與方法
1.1 一般資料
選擇2016 年9 月至2018 年9 月在我院進行心臟瓣膜術患者200 例作為研究對象,抽簽將其隨機分為觀察組與對照組,每組100 例,比較兩組患者一般資料無統計學意義(P>0.05),具有可比性。患者一般資料比較見表1。
1.2 納入標準
(1)所有患者符合心臟瓣膜病診斷標準,并已進行心臟瓣膜術[9-10];(2)年齡≥18 歲;(3)術前血流動力學穩定;(4)術前肝、腎及血常規經檢查無明顯異常;(5)患者及其家屬同意參與研究并簽署知情同意書。
1.3 排除標準
(1)半年內有活動性出血疾病史或外科手術史;(2)術后嚴重出血或需二次開胸手術;(3)1 周內服用過抗凝藥物;(4)出現活動性出血或慢性貧血。
1.4 研究方法
兩組均在心臟瓣膜置換術后對患者進行抗凝治療:在患者可進食后,服用華法林(北京嘉林藥業股份有限公司,國藥準字H20054247,生產批號20151211,5mg/片),用量為5mg/d,并在術后第2d,注射肝素鈉0.5mg/kg,6h/次。在抗凝治療的基礎上,對照組進行常規凝血試驗(日本Sysmex 公司CS-5100 型血凝儀及其配套質控品、定標品和試劑盒,XE-2100 全自動血液分析儀),觀察組在對照組的基礎上利用TEG 5000 型分析儀(美國Haemoscope 公司)對患者凝血功能進行實時監測,并及時調整抗凝方案:纖維蛋白在血液樣本中形成時間(R)延長時需通過注射新鮮冰凍血漿進行糾正,凝血后血栓彈力圖振幅達20mm 所用時間(K)延長而血凝塊形成速率(α-Angle)減小時需輸注新鮮冰凍血漿來糾正,TEG 最大振幅(MA)值降低需通過輸注血小板進行糾正,30 分鐘內血凝塊幅度減少速率(Ly30)>7.5%時應使用抗纖溶藥進行糾正;華法林用量結合凝血狀況的國際標準化比值(INR)變 化 進 行 調 整:INR<1.0,6.25mg/d;1.0<INR ≤3.0,5mg/d;3.0<INR ≤3.4,3.75mg/d;INR>3.5,停藥;服藥期間每3d 復查一次凝血狀況,停藥期間每天監測其凝血狀況,酌情用藥,服藥期間每3d 復查一次凝血狀況,停藥期間每天監測其凝血狀況,酌情用藥。
1.5 統計學分析
應用SPSS 22.0 統計軟件處理數據,計數資料用百分比(%) 表示,采用χ2檢驗,計量資料以()表示,兩組間比較采用t檢驗,P<0.05 為差異有統計學意義。
2 結果
2.1 兩組患者一般資料比較
比較兩組患者性別、年齡、身體質量指數(BMI)、紐約心臟協會(NYHA)分級、手術類型、瓣膜類型,差異無統計學意義(P>0.05)。見表1。
表1 兩組患者一般資料比較(n,
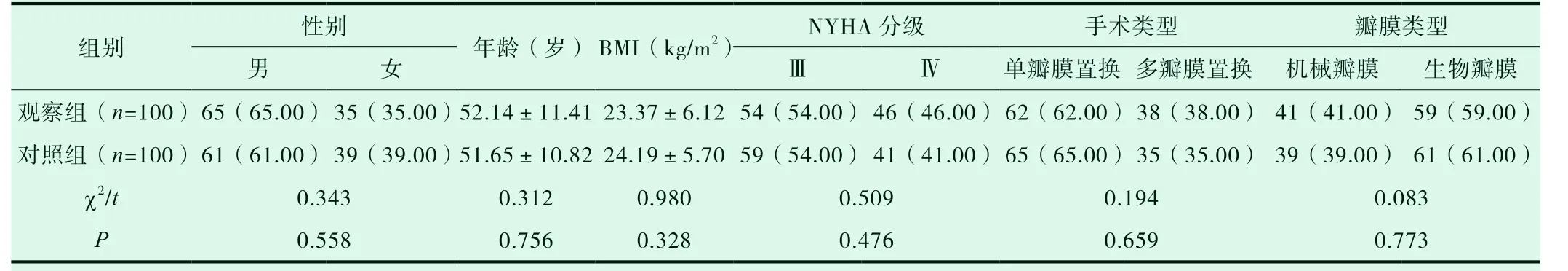
表1 兩組患者一般資料比較(n,
組別 性別 年齡(歲)BMI(kg/m2) NYHA 分級 手術類型 瓣膜類型男 女 Ⅲ Ⅳ 單瓣膜置換 多瓣膜置換 機械瓣膜 生物瓣膜觀察組(n=100)65(65.00)35(35.00)52.14±11.41 23.37±6.12 54(54.00)46(46.00)62(62.00)38(38.00)41(41.00)59(59.00)對照組(n=100)61(61.00)39(39.00)51.65±10.82 24.19±5.70 59(54.00)41(41.00)65(65.00)35(35.00)39(39.00)61(61.00)χ2/t 0.343 0.312 0.980 0.509 0.194 0.083 P 0.558 0.756 0.328 0.476 0.659 0.773
表2 干預前后兩組凝血常規指標比較

表2 干預前后兩組凝血常規指標比較
注:與干預前相比,*P<0.05。
組別 TT(s) INR FIB(g/L) APTT(s) PT(s)干預前 干預后 干預前 干預后 干預前 干預后 干預前 干預后 干預前 干預后觀察組(n=100)27.14±4.81 19.89±3.51* 1.35±0.21 3.41±0.58* 2.01±0.40 3.41±0.61* 40.66±5.51 30.42±6.11*18.14±3.24 11.51±1.84*對照組(n=100)26.59±4.52 21.05±2.71* 1.34±0.19 3.22±0.46* 1.97±0.41 3.12±0.75* 41.04±5.14 33.04±5.25*18.23±3.57 12.25±2.05*t 0.833 2.616 0.353 2.567 0.698 3.000 0.504 3.252 0.187 2.686 P 0.406 0.009 0.724 0.011 0.486 0.003 0.615 0.001 0.852 0.007
表3 觀察組干預前后TEG 監測指標比較

表3 觀察組干預前后TEG 監測指標比較
時點 R(min) K(min) α-Angle(℃) MA(min) Ly30(%)干預前 8.71±1.05 4.05±0.68 48.52±6.24 41.51±8.25 9.52±2.71干預后 8.32±1.01 3.84±0.57 65.12±10.14 53.25±7.52 8.56±1.91 t 2.677 2.367 13.942 10.517 2.896 P 0.008 0.019 0.000 0.000 0.004
2.2 干預前后兩組常規凝血指標比較
兩組干預前凝血常規各指標比較差異均無統計學(P>0.05);干預后,兩組TT、APTT、PT 均有明顯下降,且觀察組低于對照組,而INR、FIB 有明顯上升且觀察組高于對照組,差異有統計學意義(P<0.05)。見表2。
2.3 觀察組干預前后TEG 檢測指標比較
觀察組干預后的α-Angle、MA 均較干預前有明顯升高,而R、K、Ly30 均有明顯降低,差異有統計學意義(P<0.05)。見表3。
2.4 并發癥發生率
兩組術后主要并發癥為血栓栓塞及出血(腦、鼻及口腔出血),觀察組出血15 例,血栓栓塞3 例,總發生率為18.00%(18/100);對照組出血14 例,血栓栓塞6 例,總發生率為20.00%(20/100),兩組并發癥發生率比較差異無統計學意義(χ2=0.130,P=0.718)。
3 討論
心臟手術尤其是心臟瓣膜置換術后異常出血會增加二次開胸手術率及病死率[3]。數據表明,心臟瓣膜術出血率高達40%,病死率則可達19~45%[4-5],因此近年來醫學界興起了針對心外科圍手術期的血液檢測管理,檢測管理包括術中血液回收及凝血檢測。隨著臨床應用的普及,常規凝血檢測雖然能指導患者進行抗凝治療,但仍存在著不足,如對患者凝血功能反應的不直觀不全面等問題,導致患者凝血異常時無法給予有效的關注[6]。TEG 近年來在心臟手術圍手術期有較廣泛的應用,能以圖像的方式反映目標患者較完整、動態的凝血及纖溶整體變化,在臨床醫生對患者凝血功能正確評估及對凝血異常的及時干預上有重要意義。
本研究顯示,兩組TT、APTT、PT 均有明顯下降,且觀察組低于對照組,而INR、FIB 有明顯上升且觀察組高于對照組,觀察組α-Angle、MA 均有明顯升高,而R、K、Ly30 均有明顯降低。提示TEG 及常規抗凝檢測都能用于心臟瓣膜術后抗凝干預的指導,但TEG 對凝血功能的檢測更為直觀且對抗凝干預的指導更有效。心臟瓣膜術后組織及血管內皮細胞受損從而產生較多凝血酶,FIB變為纖維蛋白,大量消耗凝血因子,從而凝血功能紊亂或形成血栓。臨床主要通過雙連抗血小板治療、口服抗凝劑進行治療,而這些會導致術后異常出血,需要通過實施血液保護的管理策略來進行預防[7]。
而TEG 可經由機電轉導系統使血液凝固過程中的血凝塊彈力變化顯現為電信號,經電腦處理形成圖像,因此對凝血功能反應比較直觀且能實時監測,TEG 中凝血因子的缺乏可引起R 值延長,提示FFP 的輸注,并且R 值還受纖維蛋白原水平、血小板、抗凝血酶水平等多重影響,因此其敏感性可能更高;MA 受血小板功能的影響較為敏感,Ly30 的異常表示病人存在纖溶亢進,α-Angle 與K 值存在一定的相關性,都作為反映血凝聚合速率指標,α-Angle能在K 值無法確定的重度低凝情況下進行反映,TEG 展現了血凝塊到形成纖溶這一過程的連續性信息,且還能對一些特定的凝血原因進行辨識,比如凝血因子缺乏、纖溶系統功能亢進、肝素殘留等,因而可以為調整輸血策略提供更精確的指導。與常規凝血實驗檢測不同,其凝血狀況的實時監測更能精準指導輸血,從而使凝血功能更快恢復至正常水平。另外觀察組同時顯示在凝血常規及TEG 指標的變化,提示兩者存在一定相關性,特別是R 值,其對內源凝血因子的反應程度高于外源途徑,這與APTT 機制存在相似之處,而楊婉薇等的研究也表明,R 值同APTT、TT、PT 存在顯著相關性。
綜上,TEG 能及時動態的反映患者凝血功能,對術后指導輸血成分,正確評估凝血功能及抗凝干預都有重要的臨床價值。

