亞低溫聯合促紅細胞生成素對新生兒缺氧缺血性腦病有效性及安全性Meta 分析
許婧,丁周志,劉娜娜,蘇曉宇
新生兒缺氧缺血性腦病(hypoxic ischemic encephalopathy,HIE)是由于圍生期大腦及重要器官缺氧和血液低灌注造成的。據統計,我國每年活產嬰兒中新生兒HIE 的發生率約為3%~6%,其中在新生兒期約20%死亡,而存活者中約30%可能留有不同程度的遠期后遺癥[1]。孫金嶠等運用Meta 分析表明了亞低溫對HIE 具有良好的療效和安全性[2],目前認為亞低溫治療持續時間在72 h,溫度保持在33.5oC為最佳[3]。然而HIE是一個綜合各種因素造成的病理生理過程,單純的亞低溫治療并不能完全阻止腦損傷的整個進程,目前亞低溫與其他神經保護劑聯合治療的研究成為一種趨勢,促紅細胞生成素(erythropoietin,EPO)這種可以迅速通過血腦屏障的神經保護劑,可分別通過激活蛋白激酶A、C、磷酸化核轉錄因子途徑及P13k/Akt途徑,抑制神經細胞凋亡并促進其修復[4]。本研究檢索亞低溫聯合促紅細胞生成素治療的相關文獻行Meta分析,評估聯合治療法對新生兒HIE的有效性和安全性,為臨床應用提供參考。
1 資料與方法
1.1 納入與排除標準
1.1.1 研究類型 所納入研究類型均為臨床隨機對照試驗(RCTs),并除去資料不全或無法獲得完整資料的研究,排除動物實驗、病例分析、薈萃分析,綜述以及非隨機對照的臨床試驗等文獻。
1.1.2 研究對象 均為確診HIE 的足月兒,對于試驗組的性別、出生孕周、出生體重、生產方式、1 min及5 min Apgar評分、妊娠時合并癥及原發病與對照組均差異無統計學意義;并排除先天發育異常、先天代謝異常,宮內感染、產前和產時感染,嚴重的顱內出血及腦膜炎的足月兒。
1.1.3 干預措施 治療組靜脈注射或皮下予以促紅細胞生成素運用,具體用量,療程不限,對照組給予安慰劑治療或空白對照。治療組與對照組均于生后6 h 內行亞低溫基礎治療,48~72 h 后復溫,并輔以吸氧,鎮靜,降顱壓等常規治療。
1.1.4 觀察指標 經治療后血清中樞神經特異蛋白(S100),血清中神經元特異性烯醇化酶(neuronspecific enolase,NSE)含量水平,生后14~28 d新生兒行為神經評估(neonatal behavioral neurological assessment,NBNA)。安全性指標:HIE 治療過程中的病死率、EPO 相關不良事件發生,亞低溫相關不良事件及HIE并發癥等(紅細胞增多癥,低血壓、凝血功能障礙、肝腎功能異常、骨髓抑制、感染、電解質紊亂等)。
1.2 檢索策略 檢索PubMed、Embase、the Cochrance Library、中國生物醫學文獻數據庫(CBM)、中國知網期刊全文數據庫(CNKI)、萬方數據庫,檢索時間均為建庫至2018 年4 月。中文檢索詞為缺氧缺血性腦病、窒息、腦損傷、新生兒、促紅細胞生成素、亞低溫。英文檢索詞為:EPO、erythropoietin、hypothermia、cooling、neonatal asphyxia、hypoxic ischemic encephalopathy、brain injury。采用主題詞與自由詞相結合的方式進行檢索,手工檢索兒科學相關會議論文、納入文獻的參考文獻。
1.3 文獻篩選和質量評價 由2 名研究者獨立雙盲進行質量評價,意見不一致時通過查閱資料或請教專家討論后決定。采用Cochrane 系統評價手冊標準行文獻偏倚風險評估:隨機分配方法,分配隱藏,對試驗實施者、研究對象和結果測量者的盲法,結局資料的完整性(是否描述退出、失訪),選擇性報告研究結果、其他偏倚來源。
1.4 資料分析 制定“文獻基本特征表”進行資料整理,內容包括對象、試驗組和對照組例數、干預措施、對照措施、結局指標。將治療后NSE、S100蛋白的濃度值,NBNA 評分、病死率、不良事件發生率作為效應量,采用Cochrane 協作網提供的Revman 5.3軟件做Meta分析,若各文獻間具有同質性(P>0.1,I2<50%),采用固定效應模型(fixed effect model)進行Meta 分析;若各文獻問存在異質性(P≤0.1,I2≥50%),則采用隨機效應模型(random effect model)。對于連續性變量,采用加權均方差(mean difference,MD)或標準化均方差(standard mean difference,SMD)作為分析統計量;對于二分類變量,采用比值比(odds ratio,OR)作為效應量,各統計量均以95%CI 表示。根據可能出現的異質性因素進行亞組分析,必要時行敏感性分析。
2 結果
2.1 文獻檢索情況及基本特征 檢索數據庫,共檢出822 篇文獻,去除187 篇重復文獻后余635 篇,閱讀題目和摘要對文獻進行初篩,排除非隨機對照試驗、動物實驗和其他主題不相關文獻539篇,對余下96篇閱讀全文后復篩,排除與本文干預措施及觀察指標不相符文獻85 篇,最終納入12 篇文獻進入研究,其中中文10篇,英文2篇,各個文獻的基本特征見表1。
2.2 文獻質量評價 對納入的12篇文獻行文獻偏倚風險評估,有7篇選用的隨機方案為低偏倚風險,有2篇提及“隨機”,但未對方案進行描述;3篇文獻報告分配隱藏及對病人和研究人員采用盲法,其余均未提及盲法;2篇文獻指出結局資料無缺失,其余均未提及數據完整性問題;在12篇文獻中大部分都不能排除選擇偏倚和實施偏倚。
2.3 Meta分析結果
2.3.1 對血清S100 的影響 6 篇文獻報道了亞低溫聯合EPO 與單獨亞低溫治療對HIE 病兒血清S100影響的研究,森林圖見圖1。文獻間異質性檢驗結果為:P=0.002,I2=74%,提示具有異質性,故運用隨機效應模型分析,得到Meta 分析結果示:MD=-0.34(95%CI:-0.43~-0.25,P<0.000 01),提示經治療后聯合治療組S100 濃度均低于對照組。根據EPO 使用劑量不同行亞組分析,大劑量亞組(1 000 U/kg)和小劑量亞組(200~300 U/kg)S100濃度與對照組比較均有統計學意義,隨機效應模型合并MD 值分別為-0.38(95%CI:-0.45~-0.31,P<0.05)和-0.30(95%CI:-0.41~-0.19,P<0.05)。
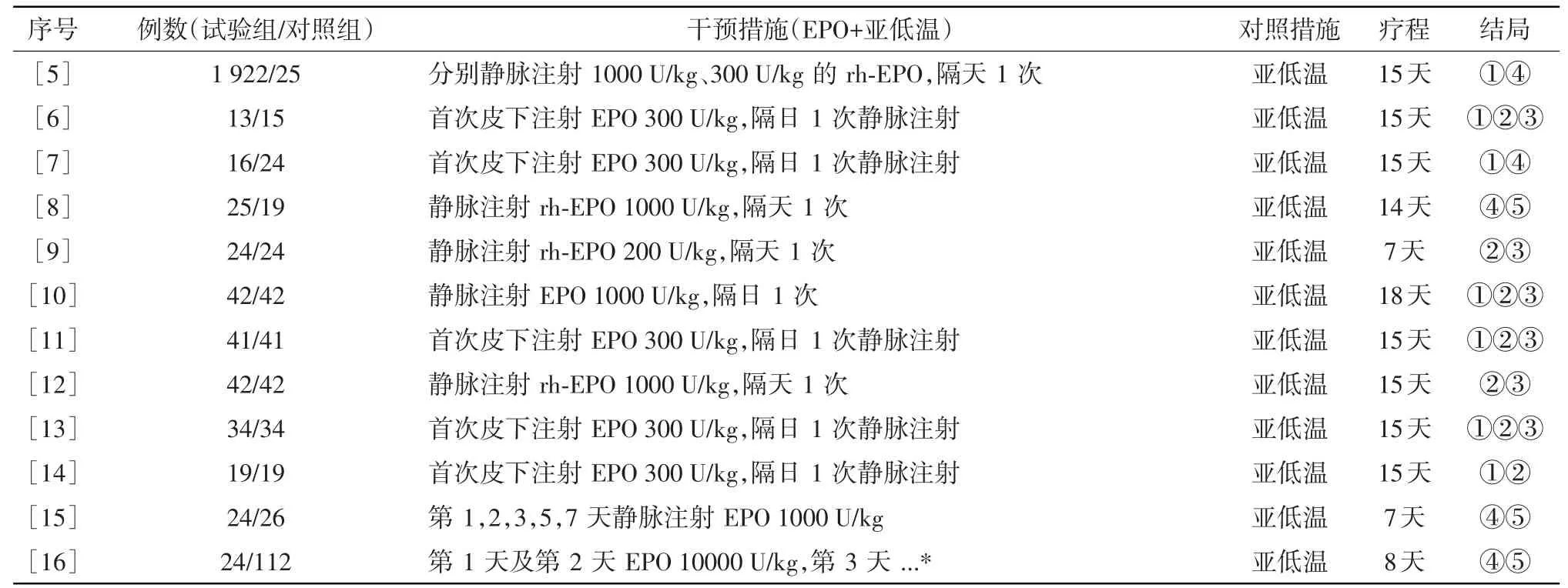
表1 納入文獻基本特征

圖1 血清S100森林圖
2.3.2 對血清NSE的影響 共7篇文獻報道了亞低溫聯合EPO與單獨亞低溫治療對HIE病兒血清NSE影響的研究,森林圖見圖2。文獻間異質性檢驗結果為:P=0.11,I2=43%,運用固定效應模型分析,Meta 分析結果示:SMD=-1.74(95%CI:-1.96~-1.51,P<0.000 01),提示經治療后聯合治療組NSE濃度均低于對照組。大劑量亞組(1 000 U/kg)和小劑量亞組(200~300 U/kg)與對照組比較均有統計學意義,固定效應模型合并SMD 值分別為-1.55(95%CI:-1.90~-1.20,P<0.05)和-1.87(95%CI:-2.17~-1.58,P<0.05)。
2.3.3 NABA 評分 7 篇文獻報道了聯合治療組與亞低溫組NBNA 評分,森林圖見圖3。文獻間異質性檢驗結果為:P<0.000 01,I2=87%,隨機效應模型分析后得到Meta分析結果示:SMD=1.64(95%CI:0.97~2.31,P<0.000 01),提示經治療后聯合治療組比對照組NBNA 得分有明顯提高。另外,亞組分析結果示,大劑量亞組(1 000 U/kg)和小劑量亞組(200~300 U/kg)與對照組比較均差異有統計學意義,SMD值分別為1.00(95%CI:0.30~1.69,P<0.000 01)和1.92(95%CI:1.02~2.81,P<0.000 01)。
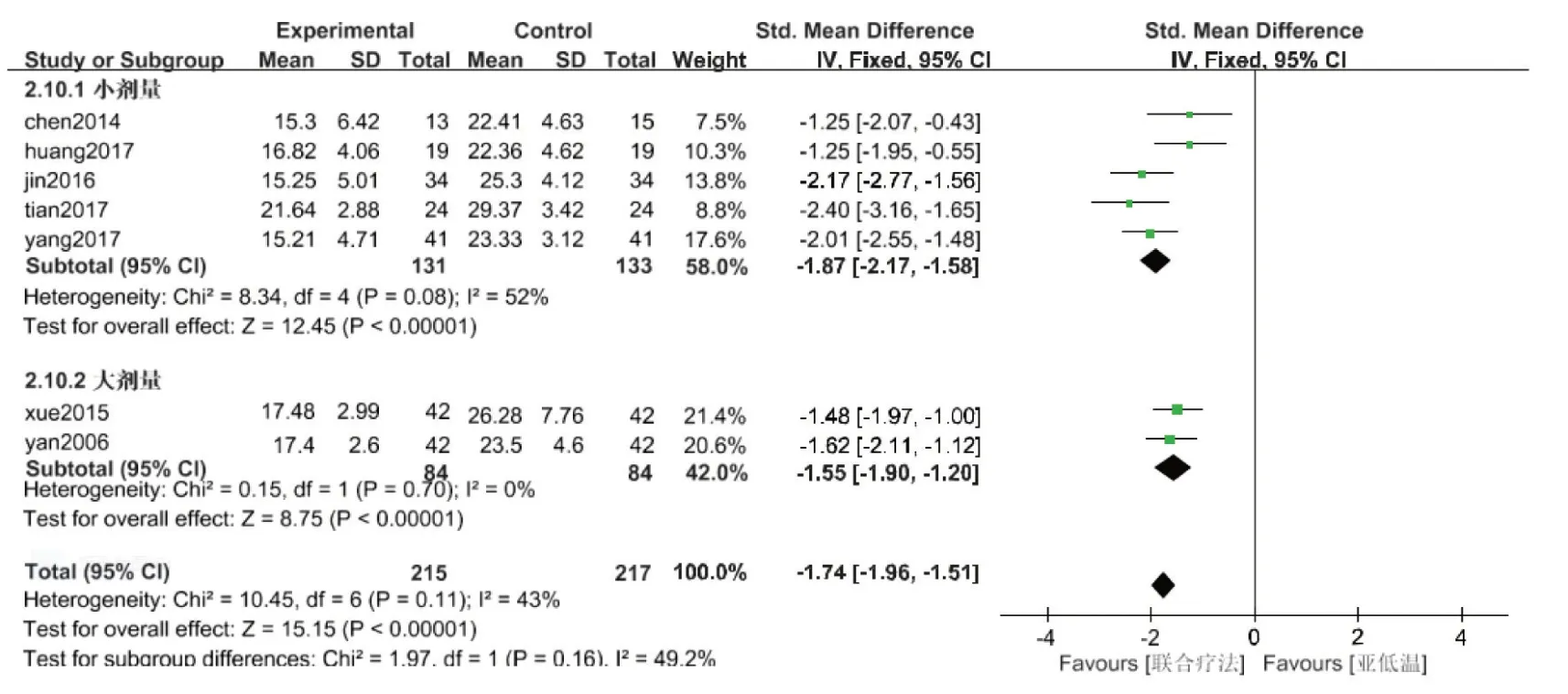
圖2 血清NSE森林圖

圖3 NABA評分的森林圖
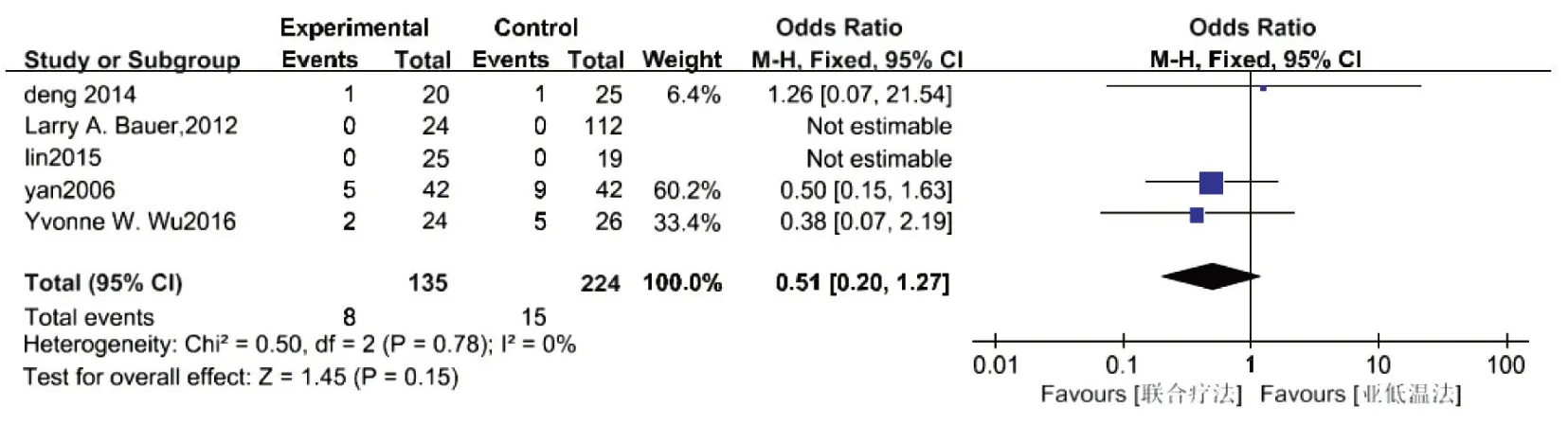
圖4 HIE病兒病死率的森林圖
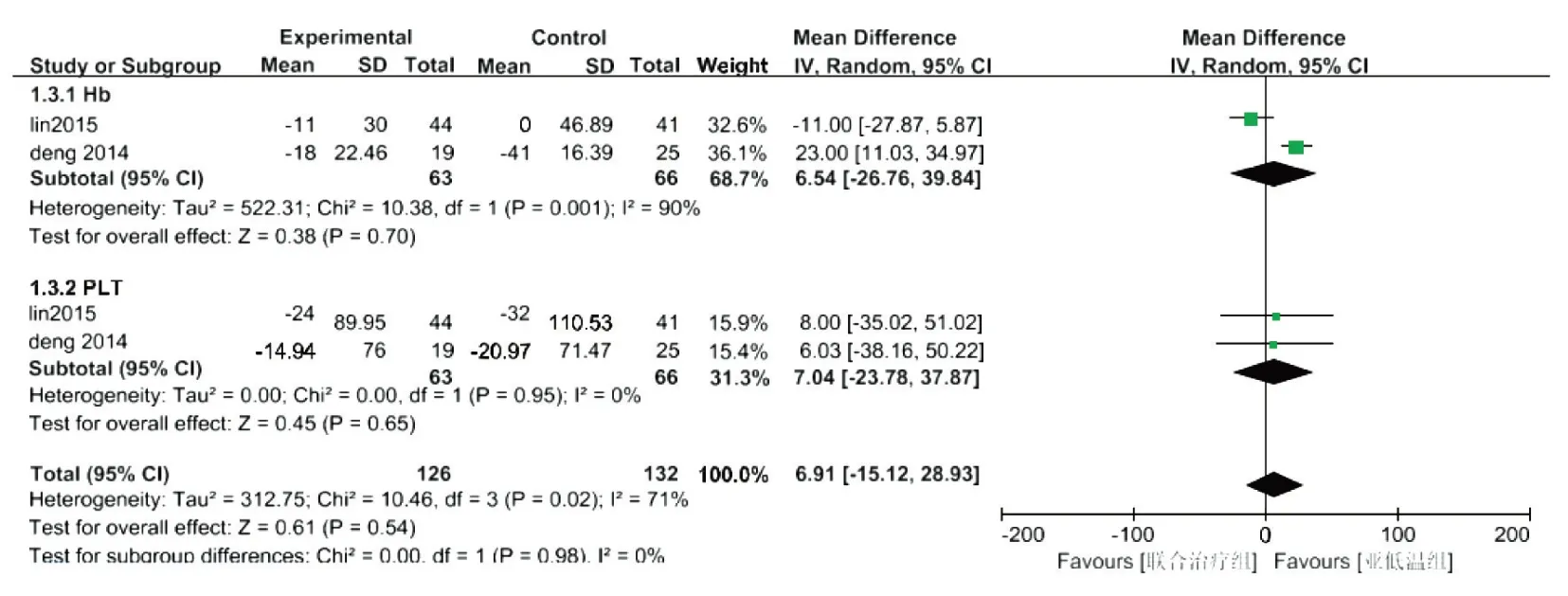
圖5 對HIE病兒治療前后Hb、PLT影響的森林圖
2.3.4 安全性評分 5篇研究報道了聯合治療組與亞低溫組病死率,森林圖見圖4,文獻具有同質性,采用固定效應模型進行Meta 分析,結果示OR=0.51,95%CI:0.20~1.27,聯合治療組與亞低溫組的病死率差異無統計學意義,P>0.05。另外,2 篇文獻報道了治療前后血紅蛋白Hb、血小板PLT 的變化,森林圖見圖5,運用隨機效應模型分析得出治療前后數值差異與對照組無統計學意義,MD 值分別為6.54(95%CI:- 26.76~39.84,P>0.05)和7.04(95%CI:-23.78~37.87,P>0.05)。此外,有3 篇文獻[8,15-16]報告聯合治療組和亞低溫組在治療過程中發生以下不良事件,文獻間具有同質性,均P>0.1,運用固定效應模型分析示,腎功能損害(OR=0.59,95%CI:0.19~1.77)、肝功能損害(OR=1.33,95%CI:0.69~2.55)、骨 髓 抑 制(OR=1.09,95%CI:0.56~2.14)、全身感染(OR=0.48,95%CI:0.13~1.79)、紅細胞增多癥(OR=1.15,95%CI:0.35~3.75)、低血壓(OR=0.87,95%CI:46.00~1.63)及凝血障礙(OR=0.64,95%CI:0.28~1.45),與對照組比較均差異無統計學意義,P>0.05。
3 討論
根據2011 版足月兒缺氧缺血性腦病循證治療指南,對于HIE 病兒除了“三支持,三對癥”的療法外,亞低溫療法是唯一推薦的神經保護治療措施[17]。但是HIE 的發生是由生化級聯反應中的多個環節造成的,亞低溫療法只能將死亡率及重大殘疾率的發生風險降至50%[18]。目前國內外已經開始了亞低溫與其他神經保護劑聯合治療的研究。EPO 在新生兒腦損傷中可促進神經母細胞增殖、遷移和分化,致使受損的基底神經節和皮質神經的重新形成[19]。有證據表明,即使是在新生嚙齒動物受傷后的1周內開始使用,仍然能夠增加軸突的數量,降低腦白質損傷的程度及改善其行為能力[20]。另外隨著使用劑量的增加,腦脊液內EPO濃度也在緩慢上升[16],并且有人發現即使早期加大劑量(3 000 U/kg)重組人促紅細胞生成素對早產兒也是安全的,不會導致死亡或重大不良事件發生[21]。
本研究利用Meta 分析探討亞低溫聯合EPO 對HIE病兒血清NSE、S100蛋白、神經功能評分及不良事件發生率的影響。與單獨亞低溫治療相比較,聯合治療法能顯著降低HIE 病兒血清NSE 和S100 蛋白的濃度,提高NABA評分。血清NSE、S100蛋白作為腦損傷的標志物,其水平的高低可判斷損傷的范圍和嚴重程度[22]。本研究表明聯合治療法對HIE病兒腦損傷的療效顯著,并且有助于提高神經功能水平,具有神經保護作用。
另外本研究不僅分析了兩者聯合的使用療效,還探討了相關并發癥及不良事件的發生。EPO 在治療腦損傷的同時,還有激活血管內皮細胞,促進紅細胞、血小板生成的作用,可能造成血栓及紅細胞增多癥[23]。但本研究發現聯合治療組血紅蛋白、血小板治療前后差值,及紅細胞增多癥的發生率與單獨使用亞低溫治療組比較均無統計學意義。其余不良事件發生率,例如治療過程中的死亡人數,肝腎功能損害、凝血功能障礙、低血壓與對照組差異不明顯,說明與單獨使用亞低溫治療相比聯合治療組并不增加不良事件的發生。
本研究仍然存在著不足:(1)方法學質量均不高,大多研究未報道隱藏分組情況,且未提及對病人及研究者采取雙盲,因此選擇偏倚和實施偏倚無法做出判斷,影響研究結果的真實性和可靠性,故需更多高質量,大樣本的研究提供更加充分的證據;(2)結局指標NABA評分,均由新生兒醫師評定,受個人能力、經驗等主觀影響較大,另外EPO 的療程,使用方法,及亞低溫治療時采取的溫度、方式、持續時間等差異較大,這可能是Meta分析異質性存在的原因,且因納入文獻數量較少,未做劑量反應關系分析,故需要進一步大量的臨床試驗,采用客觀指標進行分析探討;(3)納入的文獻缺少遠期的隨訪,對于HIE病兒今后的生活質量、學習能力及神經系統相關后遺癥缺少證據;(4)僅有3篇文獻報道了可能導致的不良反應,仍需更多高質量的隨機對照試驗證明聯合治療法的安全性。
綜上,亞低溫聯合EPO較單獨亞低溫治療在治療HIE 上臨床效果更加明顯,且是安全可行的。但由于受納入試驗方法學質量限制,本系統評價結果的準確性有待進一步提高,尚需進一步開展設計科學的隨機對照試驗,為亞低溫聯合EPO治療HIE的應用提供證據。

