基于QTL-seq的水稻粒質量QTL定位及候選基因分析
王 豪,張 健,王加峰,楊瑰麗,郭 濤,陳志強,王 慧
(華南農業大學 國家植物航天育種工程技術研究中心,廣東 廣州 510642)
水稻是世界上最重要的糧食作物之一,全球約有一半以上人口以水稻為主食。隨著我國人口數量的不斷增加,耕地面積因氣候環境變化逐年減少,導致糧食安全問題日益嚴峻。只有不斷提高糧食產量,才能從根本上解決糧食問題。水稻千粒質量作為重要的產量性狀一直是育種家關注的重點,同時也會間接影響到品質相關性狀。水稻千粒質量是多基因控制的數量性狀,是由主效基因和一些分布不均衡的微效多基因共同作用的,所以進一步定位和克隆新的控制粒質量的基因是十分必要的[1]。水稻千粒質量由籽粒的體積和飽滿度決定,其中水稻籽粒體積一般由粒長、粒寬和粒厚決定,飽滿度一般由灌漿速率、活躍灌漿期時間等指標衡量[2]。近年來已經有很多控制粒型的基因被克隆,目前克隆的大部分控制水稻粒型的基因是通過轉錄調節因子途徑、油菜素內酯、G-蛋白信號、生長素以及泛素連接酶途徑調控水稻粒型性狀。其中轉錄調節因子調控粒型途徑如GS2(GL2、LGS1)編碼蛋白質可以與DELLA蛋白產生互作,作用于赤霉素信號傳導途徑,可以促進氮元素的吸收和在植物體內的轉運,同時調控植物的光合作用、碳水化合物的代謝和細胞內轉運等,通過促進水稻細胞分裂和膨大調節水稻粒長和粒質量[3-4]。最新研究表明,GS2基因突變可能影響OsGRF-miR396脅迫響應應答,從而增強水稻苗期的耐冷性[5],也表明了GS2基因存在一因多效。GW8編碼包含SBP結構域的轉錄因子,能夠與GW7啟動子結合并抑制其表達,導致水稻籽粒變短圓[6]。GS9編碼轉錄激活因子與OFPs家族蛋白(轉錄抑制家族)OsOFP14和OsOFP8相互作用通過影響細胞分裂調節水稻粒長、粒寬和外觀品質[7]。編碼G-蛋白信號轉導途徑,如GS3負調節水稻粒質量和粒長,蛋白表達主要在水稻幼穗,隨著幼穗的發育表達量逐漸減少,在其他組織如葉片、胚芽、莖端分生組織中有微弱表達,在根中大量表達[8]。泛素連接酶途徑,如GW2編碼環型E3泛素連接酶,通過在細胞質中調節底物與受體酶的結合降解,從而負調節水稻細胞的分裂,影響粒寬和粒質量[9]。GW2等位基因WY3因功能缺失,無法促使底物被識別降解,從而可以激活穎殼外稃的細胞分裂,增加了灌漿速率,顯著增加水稻的粒寬和千粒質量,同時也正調控水稻單株穗數、延長生育期,并顯著地降低每穗粒數和主穗長度[10]。調控生長素轉導途徑,如TGW6編碼IAA-葡萄糖水解酶,控制IAA-葡萄糖的水解,通過影響細胞分裂從而負調控籽粒質量[11]。TGW3(GL3.3)編碼蛋白激酶OsSK41能夠磷酸化生長素應答因子OsARF4(生長素途徑中的轉錄抑制因子)。OsSK41-OsARF4通過負調控生長素信號,調節水稻穎殼中細胞的大小和數量,進而負調控水稻粒長和粒質量[12-13]。同時TGW3與之前發現的GS3存在上位性效應,GS3與TGW3同時存在可以導致水稻粒型的顯著增大[14]。油菜素內酯調控途徑,如GW5編碼蛋白調節油菜素內酯信號傳導,可以通過與GSK2激酶相互作用從而抑制GSK2激酶活性。GSK2激酶可以磷酸化OsBZR1和DLT蛋白,GW5的表達會增加細胞核中未磷酸化的OsBZR1和DLT蛋白的積累,從而調節油菜素內酯響應基因的表達水平和生長響應[15]。QTL-seq是近年來發展起來的一種新型的QTL定位手段,是將傳統的混合分組分析法(Bulk segregant analysis,BSA)和高通量測序結合起來快速定位到性狀相關QTL,節約了大量構建群體的時間,Park 等[16]通過QTL-seq和RNA-seq技術定位了辣椒中影響辣椒素含量的主效基因,Luo等[17]通過QTL-seq和KASP分型技術定位了花生脫殼率的主效QTL。QTL-seq目前已經在水稻粒長[18]、水稻耐寒性[19]、大白菜抗TuMV[20]、鹽脅迫下大麥的籽粒育性[21]與抗病性、西瓜枯萎病[22]、油菜有限花序[23]、鷹嘴豆粒質量[24]、卷心菜和西蘭花開花時間[25]等研究中得到了廣泛的應用,證明了QTL-seq在基因定位中的可行性。現階段大部分水稻粒型定位研究大都是以高世代的RIL群體或染色體單片段代換系為材料,以分子標記或高密度遺傳圖譜作為主要的定位手段進行QTL定位,構建群體時間長,研究成本較高。通過QTL-seq定位的遺傳位點報道較少。對影響粒質量的關鍵表型性狀進行鑒定分析,進一步挖掘可能控制粒質量的候選基因,豐富粒質量性狀多基因調控的理論基礎,以期可以在實際育種中加以應用。
1 材料和方法
1.1 試驗材料與田間處理
材料為國家植物航天育種工程技術研究中心前期收集的優良種質資源重粒親本B233和輕粒親本B91以及雜交繁育的F2群體。于2017年早造進行雜交,2017年晚造種植F1(6株×6株小區),于2018年早造雙壟種植F2506株全部收獲并進行表型考察。
所有的田間處理試驗均在華南農業大學國家植物航天育種工程技術中心試驗田完成,田間種植由實驗室統一管理。
1.2 B91及B233產量相關性狀的考察
收獲2 a四造親本種子在溫室自然風干,對親本進行粒長、粒寬、千粒質量、單株穗數、穗粒數等表型性狀的考察。
1.3 B91及B233籽粒掃描電鏡觀察
1.3.1 穎殼表面掃描電鏡觀察 水稻穎殼用2.5%~5.0%的戊二醛(采用0.1~0.2 mol/L的PBS(pH值6.8)稀釋25%戊二醛至濃度為2.5%~5.0%)固定。為了讓固定液充分浸入材料,當穎殼放入固定液后進行真空處理,然后在4 °C的條件下固定1~3 h后吸出固定液,加入0.1 mol/L pH值6.8的PBS漂洗1 h,期間換漂洗液3~4次;吸出PBS后用乙醇梯度干燥,即30%-50%-70%-80%-90%-100%-100%,樣品在每級乙醇中停留30 min;經無水乙醇干燥后的穎殼用解剖針剖開,使用導電雙面膠粘貼在載物臺上,噴金后使用XL-30-ESEM型號掃描電鏡觀察。
1.3.2 籽粒胚乳淀粉粒掃描電鏡觀察 收獲已經完成灌漿的水稻籽粒(本研究為開花40 d后),將成熟籽粒自然風干后剝除穎殼,用鑷子掰開,留出中部胚乳腹部作為觀察樣本,將觀察樣本的截面用導電膠粘貼置于載物臺上,噴金后使用XL-30-ESEM型號掃描電鏡觀察。
1.4 B233及B91灌漿速率的測定
在水稻孕穗期選取長勢整齊的單株掛牌標記,當穗部露出外葉鞘3 cm時,在此穗的劍葉上標記抽穗日期,統一于15:00開始標記,取樣時間也統一在15:00進行。對標記后的穗子進行跟蹤調查,在穗子中部穎花開放的時間進行定穗,記為開花0 d,并在開花的穎殼上用防水筆標記。自開花的第5天起,每5 d取樣一次,直到開花的第40天粒質量不再發生變化為止。每次每個材料取100粒,取樣均取水稻穗的優勢粒進行測量,保證數據的準確性。取回的穗子立即放入冰袋并帶回實驗室測量鮮質量,在60 ℃的烘箱內烘72 h至恒質量測量干質量。灌漿動態用Richards方程擬合。
1.5 QTL-seq分析
對F2種子進行粒質量考察,在F2群體中篩選出極端輕粒單株30株和極端重粒單株30株,各取葉片2 g,用CTAB法提取葉片DNA,提取后測量DNA濃度和純度,根據濃度等量混合F2群體的DNA。
2個混合池DNA和2個親本DNA建庫進行30×的全基因組重測序,測序得到的原始數據經過過濾后進行SNPs和InDels注釋。以對照親本作為參考,計算每個子代混合池在所有的SNP分離位點的親本基因型頻率,即SNP-index。采用滑動窗口策略來繪制2個子代混合池的SNP-index圖(以2 Mb為窗口,100 kb為步長),并過濾掉2 M范圍內小于10個SNP位點的區域。為了減少測序錯誤和比對錯誤的影響,同時過濾掉子代SNP-index都小于0.3,SNP深度都小于6的位點。得到2個子代混合池的SNP-index圖后,計算分離位點在子代2個極端池中基因頻率的差值(△SNP-index),然后采取滑動窗口的策略繪圖。并進行1 000次置換檢驗,選取99%置信水平作為選取的閾值,超過閾值外的區域為潛在的QTL候選區域。對候選SNPs所在的編碼基因進行統計,發掘潛在的與性狀相關的候選基因。
1.6 注釋基因功能及表達位置分析
通過國家水稻數據中心對于注釋基因的蛋白結構域注釋和預測功能及NCBI網站對候選區域內注釋基因的轉錄組分析進一步篩選候選基因。
1.7 數據處理
表型數據的錄入、整理與柱狀圖由Excel 2016完成,使用SPSS 20完成數據相關性及方差分析等。
2 結果與分析
2.1 親本表型性狀的鑒定和掃描電鏡觀察
2.1.1 B233和B91的表型性狀對比 2 a共四造對B233和B91籽粒形態進行調查(圖1),B91與B233粒長、粒寬、粒厚、千粒質量均具有顯著差異,其中以千粒質量差異最大,所以在F2群體中以千粒質量作為主要考察性狀進行極端單株的篩選,構建混合池。
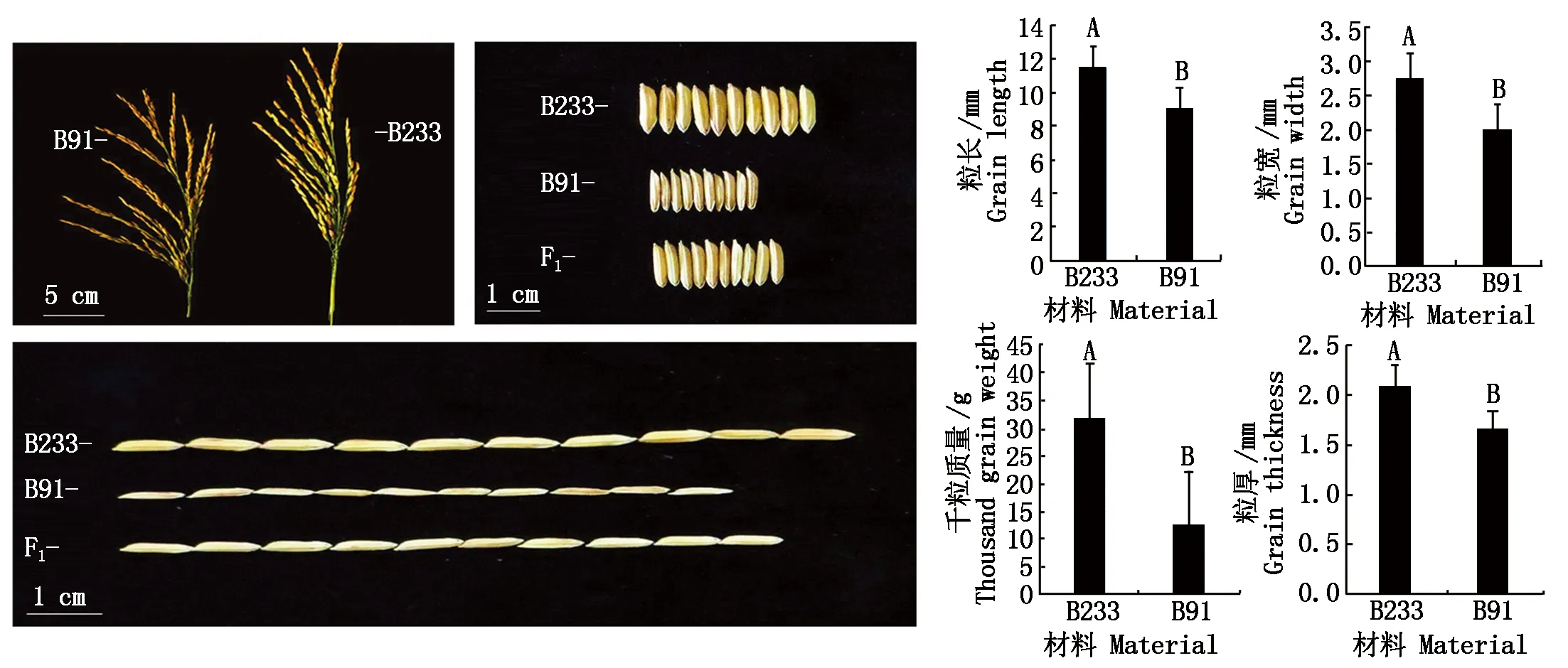
不同字母表示親本間差異極顯著(P<0.01)。 Different letters indicate extremely significant difference (P<0.01)between B233 and B91.
2.1.2 B91與B233灌漿速率對比 灌漿速率等相關指標也會直接影響籽粒充實度并影響到最終粒質量,所以本研究對比了B91及B233灌漿速率(圖2)的相關指標。B91的起始生長勢、活躍灌漿期時間、平均灌漿速率、最大灌漿速率等指標均小于B233(表1)。其中平均灌漿速率、活躍灌漿期等指標都直接或間接影響最終籽粒質量。灌漿動態指標也是導致B233和B91粒質量差異和品質差異的重要因素之一。

圖2 B91和B233灌漿速率的比較Fig.2 Comparison of the filling rates of B91 and B233

表1 Richards方程擬合灌漿參數Tab.1 Richards equation fitting grout parameters
注:A.籽粒終極生長量;R0.起始生長勢;Rmax.最大灌漿速率;Rmean.平均灌漿速率;Dmax.達到最大灌漿速率的時間;Wmax.灌漿速率最大時的籽粒質量;D.活躍灌漿期;R2.方程系數。
Note: A.Grain final growth; R0.Initial growth potential; Rmax.Maximum grouting rate; Rmean.Average grouting rate; Dmax.Time to reach the maximum grouting rate; Wmax.Grain weight when the grouting rate is maximum; D.Active grouting period;R2.Coefficient of equation.
2.1.3 B233和B91穎殼表面和胚乳的顯微觀察和掃描電鏡觀察 由150×、500×和1 000×掃描電鏡視圖(圖3)可以看到,細胞大小和細胞數量在親本間均有明顯差異,表明二者為B91和B233粒型差異的決定因素。根據300×掃描電鏡觀察,單位面積內B91縱向細胞列數與B233縱向細胞列數相比有顯著差異,橫向細胞行數沒有顯著差異;穎殼細胞長和細胞寬均有極顯著差異(表2)。
B91精米細長,米質堅硬,米粒亮透明如玻璃狀,米粒大小均勻,胚乳整齊美觀,無腹白心白,對B91成熟籽粒腹部胚乳細胞的掃描電鏡觀察淀粉粒呈明顯的多邊形、排列緊密、顆粒間基本沒有空隙,

A-C.B91掃描電鏡視圖;D-F.B233掃描電鏡視圖;A,D.觀察倍數150×;B,E.觀察倍數500×;C,F.觀察倍數1 000×。 A-C.B91 scanning electron microscope view; D-F.B233 scanning electron microscope view; A, D. Observation multiple 150 ×;B, E. Observation multiple 500×; C, F. Observation multiple 1 000×.
表2 300×掃描電鏡視圖穎殼單位面積下細胞長寬和細胞數量對比
Tab.2 Comparison of cell length and width and cell number per unit area in 300× scanning electron microscope

樣品Sample 細胞長(平均)/μmCell length 細胞寬(平均)/μmCell width橫向細胞行數(平均)/個 Horizontal cell number 縱向細胞列數(平均)/個Longitudinal cell numberB9121.875±1.567A22.768±2.301A13±0.816A18±0.943AB23331.964±1.413B30.213±1.889B12±0.943A12±0.471B
注:同列不同大寫字母表示樣品間差異極顯著。
Nota:Different capital letter represents extremely significant difference between the two samples.
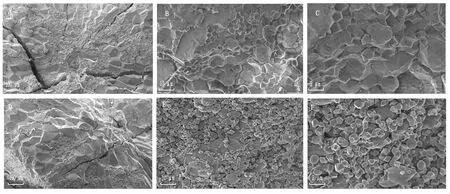
A-C.B91掃描電鏡視圖;D-F.B233掃描電鏡視圖;A,D.觀察倍數300×;B,E.觀察倍數3 000×;C,F.觀察倍數6 000×。 A-C.B91 scanning electron microscope view; D-F.B233 scanning electron microscope view; A,D. Observation multiple 300×; B,E. Observation multiple 3 000×; C,F. Observation multiple 6 000×.
籽粒填充度較好(圖4-A-C)。B233具腹白或心白,稻米品質比B91稍差,對B233成熟籽粒腹部胚乳細胞進行掃描電鏡觀察籽粒淀粉粒多面體的棱角不明顯,部分淀粉粒有橢圓形、排列疏松、顆粒間存在較大空隙、透光性稍差(圖4-D-F)。
2.2 QTL-seq分析
2.2.1 F2群體粒質量分布及遺傳分析 水稻輕粒親本B91和重粒親本B233雜交獲得F1,自交得F2,分別考察粒型相關性狀。F1及F2群體平均粒長、粒寬、粒厚和千粒質量介于兩親本之間(表3),對F2群體共506個單株進行粒質量的考察,粒質量分布呈標準正態分布(圖5),表明在B233和B91中控制親本粒質量性狀的為數量位點基因,F2群體粒質量極端值明顯,是良好的QTL-seq作圖群體。挑選了粒質量極值單株各30株,方差分析顯示,選取的單株粒質量具有極顯著差異,可以用作測序樣本。分別提取單株葉片DNA并留種。

表3 水稻親本、F1(mean)、F2(mean) 粒長、粒寬、粒厚、千粒質量Tab.3 B91 (mean), B233 (mean), F1 (mean), F2 (mean) grain length, grain width, grain thickness, thousand grain weight
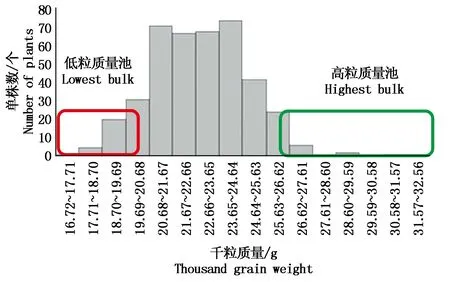
圖5 F2群體粒質量分布Fig.5 Grain weight distribution in the F2
2.2.2 基于雙親分離SNP標記的BSA 將從群體中篩選出雙親分離的SNP作為標記,以便后續進行BSA法QTL定位(QTL-seq)。過濾獲得可以用于后續QTL-seq分析的有效SNP位點共430 762個。SNP窗口總數量為3 620個,SNP數量 ≥ 10的窗口數量為3 234個,占SNP窗口總數量的89.34%。根據雙親分離的SNP標記定位粒質量相關的QTL(圖6)。
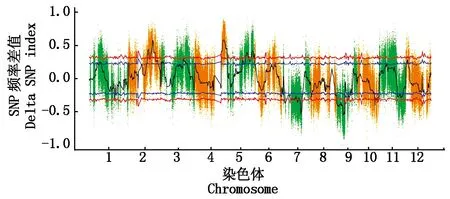
以2個子代SNP-index作差,計算△(SNP-index)。計算過程進行1 000次置換檢驗,獲得各個位點以及窗口的△(SNP index)95%置信區間(藍色閾值線,即相當于P=5%),以及99%置信區間(紅色閾值線,即相當于P=1%)。
With the difference of two daughter SNP-index, calculate △ (SNP-index). The calculation process performs 1 000 displacement tests to obtain a △ (SNP index) 95% confidence interval for each site and window (blue threshold line, which is equivalent toP=5%), and a 99% confidence interval (red threshold line, That is equivalent toP=1%).
圖6 Δ(SNP index)總分布圖
Fig.6 Total distribution of Δ(SNP index)
因為兩親本遺傳背景差異較大,前期未對兩親本遺傳背景進行人為純化,故本次QTL-seq分析定位到的粒質量QTL數量較多,且本次QTL-seq分析結果比較理想。為了更有針對性的對粒質量性狀進行分析,因為調控大粒的QTL在育種中更具有研究價值,所以在本研究主要關注超過正閾值區99%置信區間的QTL位置,并進一步在這些QTL區間內篩選可能調控粒質量的基因。可以看到在水稻的2,4,5號染色體上共有5個與粒質量性狀相關的QTL區間(圖6),其中2號染色體和4號染色體的2個QTL峰值最為明顯。在正閾值區內定位到的5個QTL最小的物理區間為2.1 M(Chr2:20.9~23.0 M),最大的物理區間6.3 M(Chr4:28.9~35.2 M)(表4)。
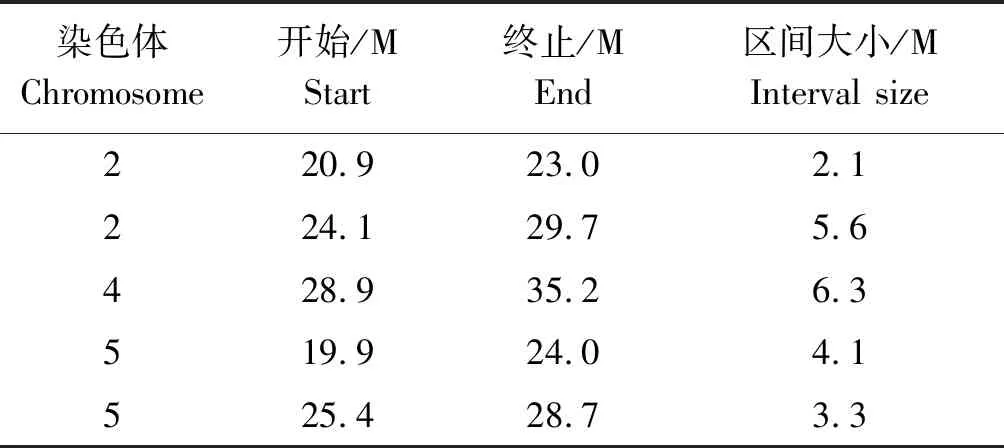
表4 水稻粒質量QTL物理位置 Tab.4 Physical location of rice grain weight QTL
2.3 正閾值區內候選基因的篩選
2.3.1 正閾值區△(SNP-index)>0.7 SNP位點和InDel位點的篩選 對正閾值區QTL位點內的基因進行△(SNP-index)分析,重點關注在子代混合池內△(SNP-index)在0.7以上的SNP位點,選出在23個基因發生非同義突變及剪接位點上的突變(表5),同時選出11個基因的Indel位點進行進一步分析(表6)。共篩選出34個候選基因,其中32個基因未報道克隆,這些位點可能對應影響粒型性狀的候選基因。
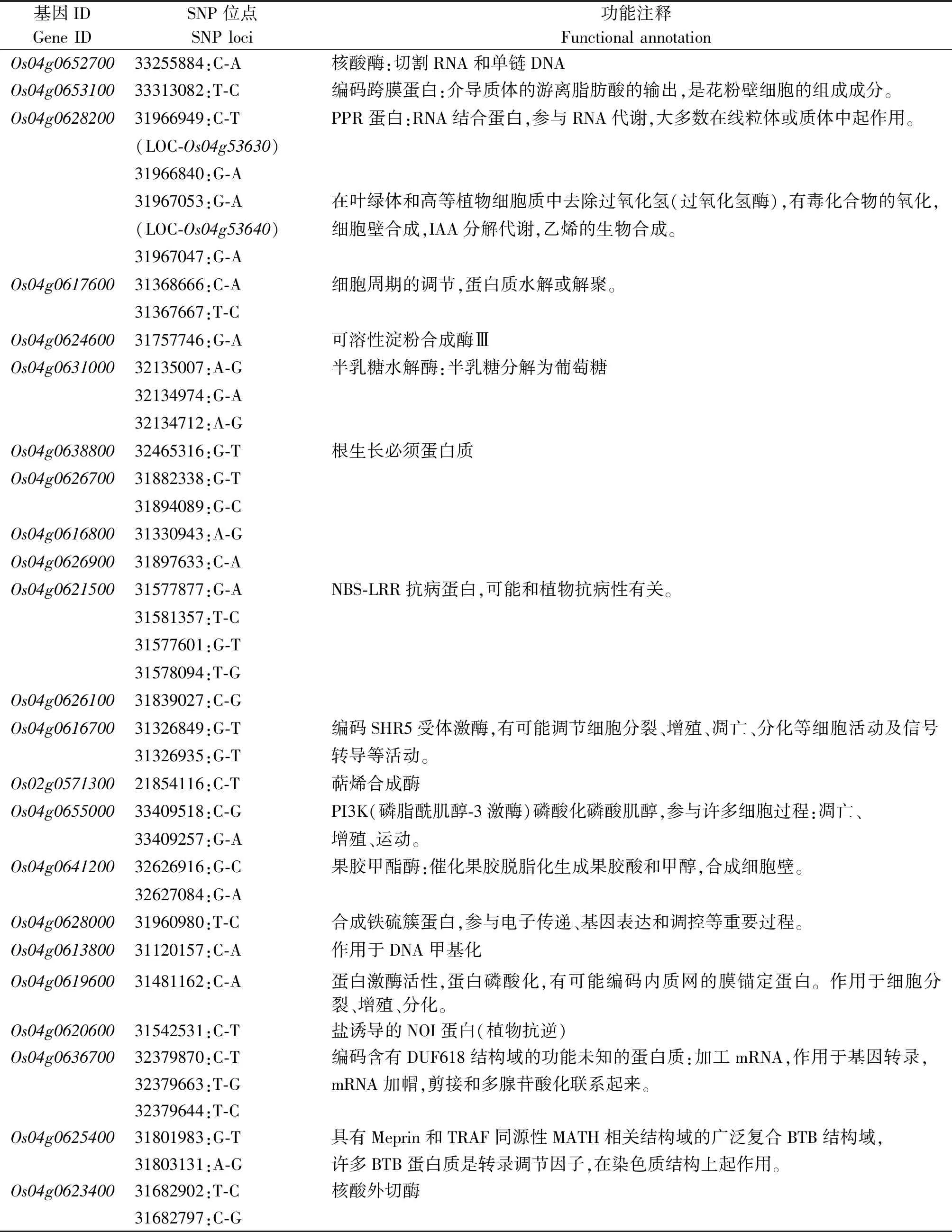
表5 正閾值區內候選基因的注釋信息Tab.5 Annotation information of candidate genes in the positive threshold region
注:SNP位點為△(SNP-index)>0.7的位點。
Note: The SNP locus is a locus with △(SNP-index)>0.7.
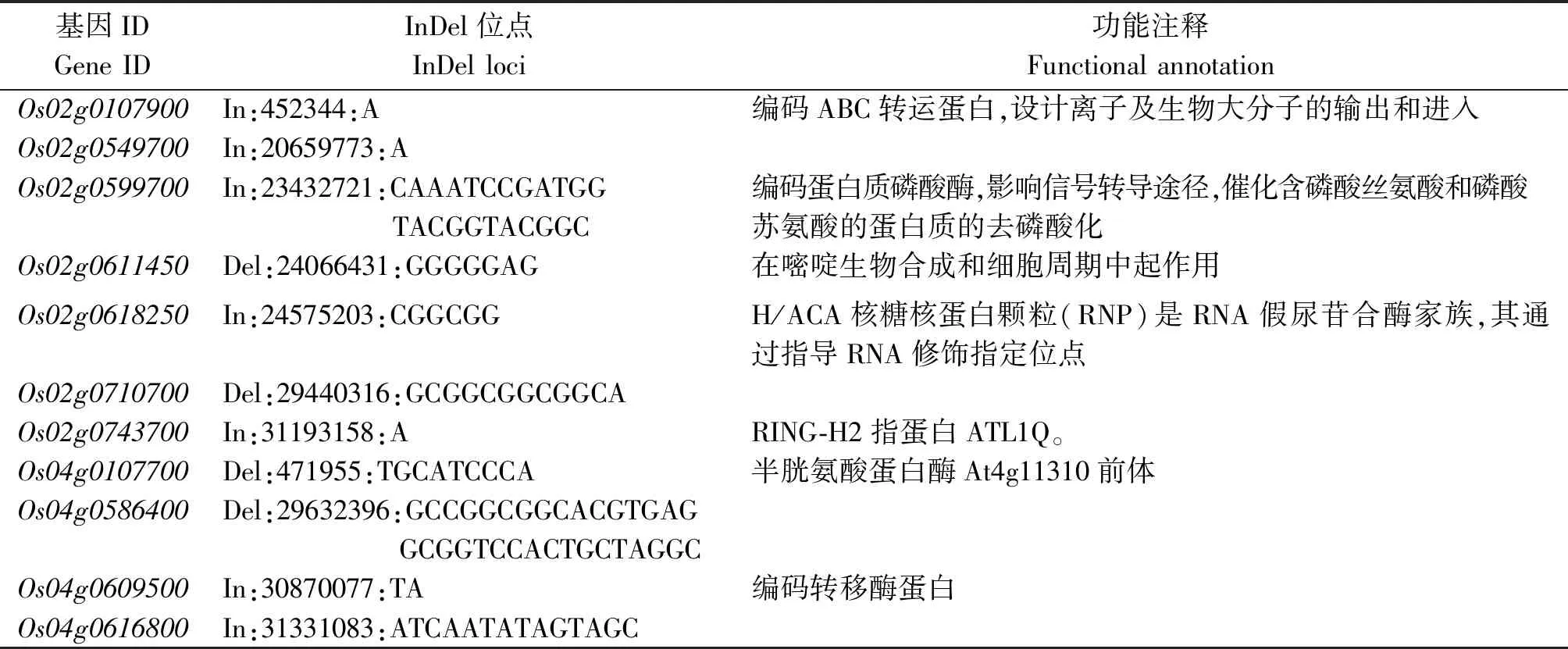
表6 Indel位點篩選Tab.6 Indel site screening
2.3.2 注釋基因的轉錄組信息篩選及預測功能分析 查詢NCBI網站注釋基因的轉錄組信息,主要篩選出在種子和花中特異表達的基因(圖7),同時根據基因的預測功能對定位到的基因進行篩選,共獲得6個可能與粒質量性狀相關的候選基因:Os04g0653100、Os04g0617600、Os04g0624600、Os04g0631000、Os04g0619600、Os02g0611450。其中,Os04g0617600、Os04g0619600編碼蛋白激酶或轉錄調節因子作用,調控細胞凋亡、分化、增殖等細胞周期和生物合成等過程;Os04g0624600、Os04g0631000與碳水化合物的合成與分解相關,可能調控稻米的粒型與品質;Os04g0653100編碼蛋白控制生物大分子的運輸,同時也是花粉壁細胞的重要組成成分;Os02g0611450編碼的蛋白質可能調控生物大分子的合成和細胞周期。
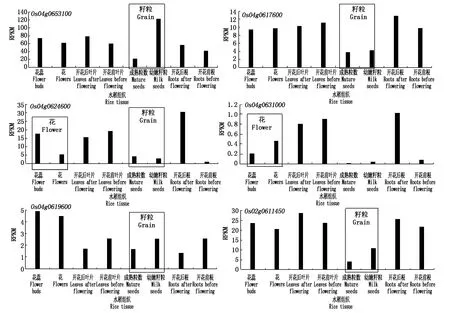
圖7 NCBI網站中注釋基因的轉錄組信息Fig.7 Transcriptome information of annotated genes in the NCBI website
3 討論與結論
3.1 粒長、粒寬、粒厚和灌漿指標是影響粒質量的關鍵生理性狀
千粒質量既是決定水稻單產的重要指標之一,也是衡量水稻品種優良與否的重要因素。本研究通過掃描電鏡觀察水稻穎殼和胚乳,旨在細胞層面解釋親本粒質量之間的差異。根據水稻穎殼掃描電鏡觀察,B233與B91粒長、粒寬、粒厚之間的差異由細胞大小和細胞數量共同決定[26]。水稻籽粒堊白的形成主要是由于水稻胚乳中存在淀粉顆粒區域性的排列松散而導致胚乳腹部存在一些空腔,而這些空腔的存在除了會影響稻米品質之外,因為灌漿不充分,也會影響到水稻籽粒質量等相關性狀[27]。通過Richards對灌漿速率曲線進行擬合,導出相關灌漿參數,B233最大灌漿速率,活躍灌漿時期等指標均大于B91,這些指標直接影響到籽粒質量。根據朱慶森等[28]的方法,因為N>1,所以(W/A)N>W/A,可以視為庫容對灌漿速率較小,所以B91和B233均屬于源限制性品種,所以受播種環境灌漿物質影響較大,邊緣效應體現的較為明顯,所以在粒質量調查中應盡量保證在同一生長條件下進行考察。因此,水稻籽粒長、寬、厚以及胚乳形態灌漿速率等是考察水稻粒質量的重要指標,對控制這些性狀遺傳位點的挖掘具有重要意義。
3.2 QTL-seq是鑒定粒質量遺傳位點的有效手段
目前,大多數QTL定位研究采用傳統的遺傳標記來定位遺傳位點,如SSR標記、RFLP標記等,但是傳統遺傳標記開發成本較高,在水稻染色體上覆蓋密度低,分布不均勻等問題制約了相關遺傳定位研究[29]。同時開發高密度遺傳圖譜的成本也較高,同時材料選擇也十分重要,構建群體的時間也較長,不適宜大規模使用[30]。本研究是基于全基因組重測序的高密度SNP標記進行QTL-seq分析,而QTL-seq技術的發展很好地解決了構建群體時間長,測序費用昂貴等問題。在本研究通過使用2個秈稻親本B91及B233構建的F2群體進行QTL-seq分析,在正閾值區共定位到了5個與粒質量相關的QTL,通過分析測序數據篩選出△(SNP-index)>0.7的位點和InDel位點,共在正閾值區篩選出34個候選基因(SNP突變基因23個,Indel突變基因11個),其中包括2個已經克隆的基因:NAL1(Chr4)[31]、OsJAZ1(Chr4)[32]。NAL1主要在葉鞘、葉片、莖稈和幼穗中表達,主要影響水稻葉片的寬窄[31]、OsJAZ1是一個茉莉酮酸酯ZIM結構域蛋白。OsJAZ1和OsCOI1b之間相互作用影響水稻小穗發育,OsJAZ1主要在幼穗和花中表達[32],這些基因在一定程度上影響水稻的產量。這些共定位結果一方面驗證了本研究的可靠性,另一方面在前人的研究中均未提及這2個基因對于水稻粒質量及相關性狀的影響,也暗示了這些基因可能存在一因多效的情況。同時通過注釋基因功能和共篩選出32個沒有報道過的基因,為后續粒質量基因的驗證及功能分析提供了基礎。
3.3 水稻粒型性狀可能受到蛋白激酶和轉錄因子相關基因的調控
目前,克隆與水稻粒型和產量相關基因很多與轉錄調節因子、泛素連接酶和蛋白激酶磷酸化相關。本研究篩選到6個可能與粒質量相關的基因中有2個基因編碼蛋白質起到蛋白激酶或轉錄調節因子作用,Os04g0617600主要編碼AAA家族的ATP酶。AAA家族的ATP酶在植物細胞中參與許多活動,包括細胞周期調節、蛋白質水解與合成、細胞內大分子轉運等,同時也充當DNA解旋酶和轉錄因子。Os04g0619600編碼的蛋白質為蛋白激酶作用,蛋白激酶按照底物的不同可分為三類,絲氨酸/蘇氨酸蛋白激酶、酪氨酸蛋白激酶及雙特異性蛋白激酶。蛋白磷酸化在大多數細胞作用中都起到重要作用,如細胞分裂分化、細胞增殖、細胞凋亡等。Os04g0624600編碼蛋白質可能調控淀粉合成與分解,起到可溶性淀粉合成酶的作用,水稻中與淀粉合成相關的基因主要分為兩類,一類主要在胚乳中特異性表達,另外一類在其他組織和早期胚乳發育中表達[33],本研究認為Os04g0624600可能是第二類群淀粉合成基因,但同樣具有進一步的研究價值。
水稻粒質量與粒長、粒寬、粒厚及籽粒飽滿度呈顯著正相關。通過灌漿指標和顯微觀察可以反映水稻籽粒質量和稻米品質。通過QTL-seq分析及分析注釋基因的預測功能和表達位置可以顯著提高候選基因的篩選效率。水稻粒質量可能受到蛋白激酶和轉錄因子相關基因控制。

