不同氛圍條件下PBT固相縮聚工藝與反應動力學研究
賴曉青,張先明,陳文興,陳世昌,王 瀅
(浙江理工大學 材料科學與工程學院,浙江 杭州 310018)
聚對苯二甲酸丁二醇酯(PBT)是一種結晶型熱塑性聚酯,一般通過酯交換反應或直接酯化法來生產,PBT中的苯環與酯基官能團之間形成的共軛結構增加了分子鏈剛性,而其4個亞甲基結構又增加了PBT分子鏈的柔順性,這兩方面共同作用使PBT材料能適應惡劣的環境,如酸堿類、油類、潮濕、高溫高壓等環境[1-4]。增強和改性過的PBT常被用于汽車工業、機械制造和家用電器、紡織等領域[5-6]。提高PBT相對分子質量是獲得其優良性能的保證,固相縮聚具有反應溫度低、工藝環保、流程簡單及產品質量高等優點。在固相縮聚中,PBT大分子鏈是靜止不動的,需要借助抽真空或通入氮氣的方法來激活聚合物末端官能團,從而加快固相縮聚反應速度,并同時移除反應體系中產生的丁二醇和水等副產物[2],使聚合反應不斷正向進行,使產物相對分子質量有效提高[7-9]。
從微觀上分析,PBT固相縮聚經歷的過程可分為:可逆化學反應、小分子產物在粒子內部的擴散、小分子產物從粒子表面擴散到體系外等過程。控制反應速度的大小往往由其中的最慢的一步或幾步決定。經過多名學者的探究,對于PBT固相縮聚,有多種反應動力學模型,如化學反應控制模型,擴散控制模型,反應與擴散共同控制模型等[10-11]。HUANG B等[12]試圖通過研究眾多變量對固相縮聚速率的影響來發現固相縮聚動力學的重要機理。CHANG Y M[13]使用擴散控制模型解釋了關于固相縮聚工藝的數據。E.SCHAFF等[14]提出了純粹的動力學模型。K.RAVINDRANATH等[15]對以前的模型進行分析提出新的模型,該模型考慮了反應過程中乙二醇的擴散和生成。作者借鑒前人研究的經驗,綜合討論了各個工藝條件對PBT固相縮聚的影響,并且結合經驗方程,得到不同反應氛圍下的動力學參數并進行比較,以此深層次地探究了PBT固相縮聚的反應機理,取得了較滿意的結果。
1 實驗
1.1 原料和試劑
PBT切片:特性黏數([η] )為1.038 dL/g,初始端羧基含量為26.3 mol/t,中國石化儀征化纖股份有限公司產;1,1,2,2-四氯乙烷、溴酚藍:分析純,上海阿拉丁生化科技股份有限公司產;苯酚、氫氧化鉀、乙醇:分析純,杭州高晶精細化工有限公司產;三氯甲烷:分析純,浙江三鷹化學試劑有限公司產;高溫導熱油:東莞克拉索潤滑油有限公司產。
1.2 主要設備與儀器
DZF-6020真空干燥箱:上海精宏實驗設備有限公司制;B-585玻璃干燥儀:瑞士Buchi公司制;VISCO 070烏氏黏度計:德國Julabo公司制;IKA C-MAG HS7加熱板:德國IKA公司制;TITRONIC 300自動滴定儀:德國Julabo公司制;FA2104分析電子天平:梅特勒-托利多國際貿易(上海)有限公司制。
1.3 實驗方法
抽真空固相縮聚:將PBT顆粒于真空烘箱中120 ℃干燥24 h待用[16],取一定量的PBT置于玻璃干燥儀中,在205 ℃下進行等溫固相縮聚,得到不同真空壓力(p)下聚合不同時間(t)的產物,并在p為50 Pa下得到不同溫度下聚合不同t的產物。
通氮氣固相縮聚:取10 g左右真空干燥的PBT顆粒置于玻璃質蛇形管反應器中,加熱裝置由內置有高溫導熱油的不銹鋼鐵杯及IKA加熱臺組成(如圖1所示),在1 L/min氮氣流速(v)下得到不同溫度下聚合不同t的產物,在205 ℃下得到不同v下聚合不同t的產物。
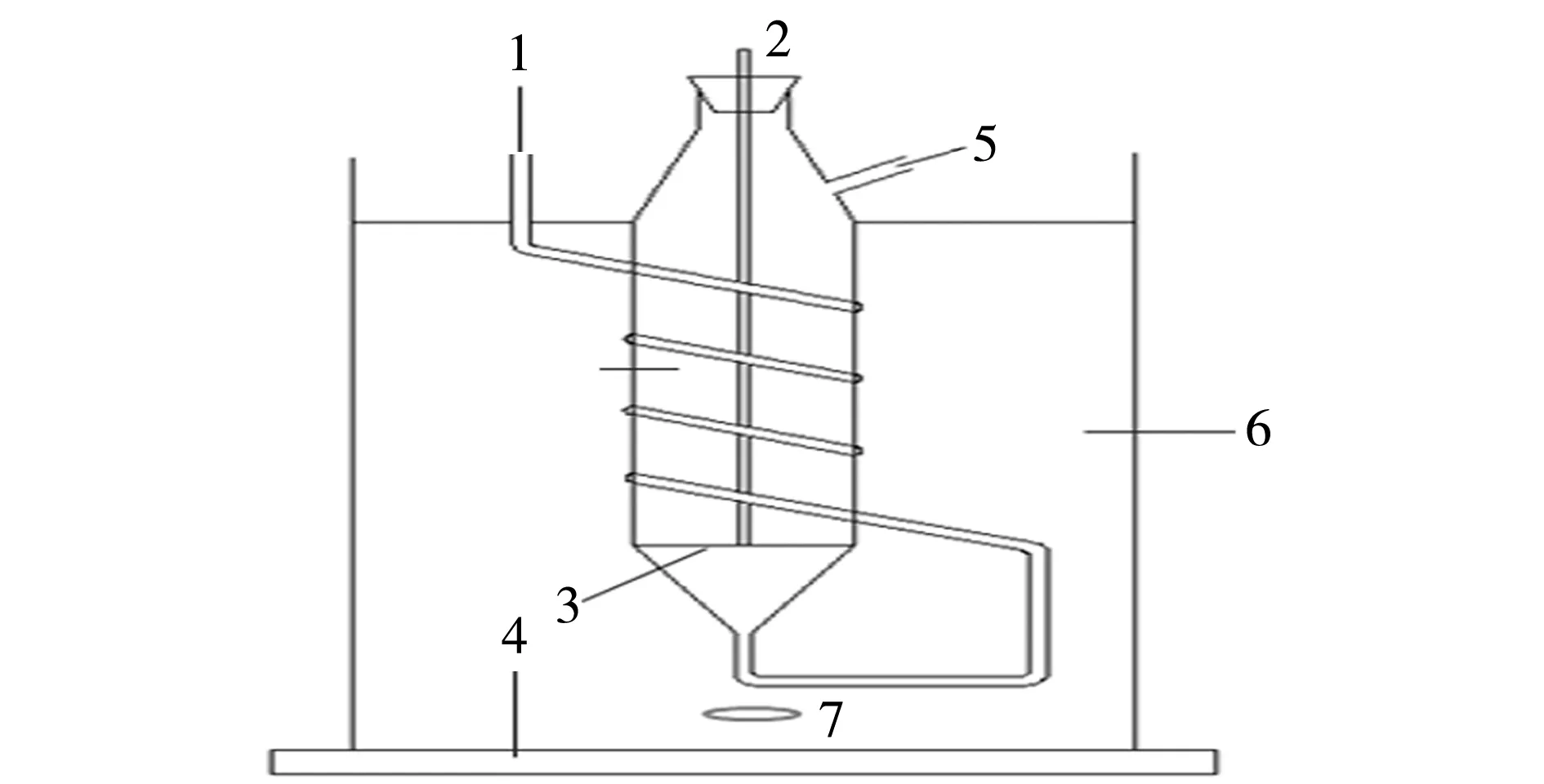
圖1 氮氣吹掃氛圍PBT固相縮聚反應裝置Fig.1 PBT solid-state polycondensation reactor in nitrogen purging atmosphere1—氮氣入口;2—溫度探頭;3—帶有小孔的玻璃板;4—加熱板;5—氮氣出口;6—高溫導熱油;7—攪拌磁子;8—蛇形管
1.4 分析測試
[η]:以苯酚-四氯乙烷(質量比1:1)為溶劑,準確稱取一定量的PBT(使溶液濃度為0.5 g/dL)置于錐形瓶中,加入溶劑,將瓶蓋密封,放入120 ℃烘箱中經過約6 h溶解,隨后冷卻移入容量瓶中定容,濃度為0.5 g/dL。利用以下公式求得[η]的大小:
ηr=t1/t0
(1)
ηsp=(t1-t0)/t0=ηr-1
(2)
(3)
式中:ηr為相對黏度;ηsp為增比黏度;t1為溶液流出烏氏黏度計的時間;t0為溶劑流出時間;c為溶液濃度。
端羧基濃度(Cs):準確稱取PBT固相縮聚產物1 g溶解于苯酚-三氯甲烷溶劑中(體積比2:3),濃度為0.05 g/mL,加入5~6滴溴酚藍指示劑,用KOH-乙醇標準滴定液(0.01 mol/L)進行滴定,當溶液由黃變綠再變藍時即為滴定終點。準確記錄標準滴定液的消耗體積,并做空白實驗,利用下列公式求得Cs:
(4)
式中:V為試樣溶液所消耗的標準溶液體積;V0為空白實驗中所記錄的標準溶液消耗量;c為標準溶液的濃度(該濃度為0.01 mol/L);m為所測試樣的質量(1 g)。
2 結果與討論
2.1 p 對PBT固相縮聚的影響
固相縮聚反應是由PBT小分子擴散速度和化學反應速度共同控制的,p降低,PBT顆粒內部待揮發的小分子與顆粒表面形成的分壓增大,改變了氣固兩相之間揮發組分的濃度梯度。圖2、圖3為205 ℃下PBT固相縮聚產物的[η]與t及p的關系。

圖2 不同p下PBT固相縮聚產物的[η]與t的關系Fig.2 Plots of [η] of PBT solid-state polycondensation products versus t under different p ■—50 Pa;●—150 Pa;▲—300 Pa;▼—600 Pa

圖3 不同t下PBT固相縮聚產物的[η] 與p的關系Fig.3 Plots of [η] of PBT solid-state polycondensation products versus p at different t■—3 h;●—6 h;▲—9 h;▼—12 h
由圖2可見,PBT固相縮聚產物的[η]在一定p下,隨著t的增加而加大,在一定t下,其[η]也隨著p的降低而升高,證明了p的降低加快了小分子副產物如丁二醇等向外擴散的速度,從而促使反應朝向鏈增長的方向進行,低壓大大加快了反應進程,能有效節約時間成本。由圖3可見,在較低壓階段,降低p顯著提升了產物的[η] ,而在極低壓階段這種對產物[η]提升的影響逐漸變小。
2.2 v對PBT固相縮聚的影響
圖4、圖5為205 ℃下,氮氣氛圍中不同v對PBT固相縮聚產物的[η]的影響。由圖4可以發現,v越高,所得到PBT固相縮聚產物的[η]越高,在v為0.2 L/min時,PBT固相縮聚產物的[η]由1.038 dL/g增長到1.311 dL/g,而在v為1 L/min時,其[η]最高增至1.59 dL/g。這是由于v的加大,增加了氣固系統中的傳質速率,降低了氣相中的副產物濃度及副產物從PBT顆粒表面擴散到氣相的阻力的緣故。圖5更加直觀地顯示了v對PBT固相縮聚產物的[η]的影響,在v較低時,v值增大會有效提高固相縮聚產物的[η],但v增加到較大值后,這種影響開始變小,尤其在較長時間下這種現象更為明顯。這是由于當v足夠大之后,氣相中小分子濃度已接近一個極低值,氣固相之間濃度差受到v的影響愈來愈小,揮發分擴散作用趨于極限,因此在實際生產中,應適當提高v以增大反應速率,但過高的v一方面對反應促進作用有限而造成資源浪費,另一方面會加快反應體系散熱,使得PBT切片不能得到充分有效地加熱。

圖4 不同v下固相縮聚產物的[η]與t的關系Fig.4 Plots of [η] of PBT solid-state polycondensation products versus t at different v■—0.2 L/min;●—0.4 L/min;▲—0.6 L/min;▼—0.8 L/min;?—1.0 L/min

圖5 不同t下固相縮聚產物的[η]與v的關系Fig.5 Plots of [η] of PBT solid-state polycondensation products versus v at different t■—3 h;●—6 h;▲—9 h;▼—12 h
2.3 反應氣氛對PBT固相縮聚的影響
圖6為PBT分別在50 Pa真空和1 L/min氮氣氛圍下反應得到的產物[η]與t的關系曲線。由圖6可以看出,反應溫度較低時,隨著t的增加PBT固相縮聚產物的[η]呈現線性上升趨勢;反應溫度較高時,隨著t的增加PBT固相縮聚產物的[η]的上升速率先快后慢,最后趨于平緩;在真空下,需要在215 ℃下反應12 h得到的產物[η]最高為2.087 dL/g,并且在反應12 h之前曲線趨近于水平,證明反應所得的產物[η]已經接近閾值,反應程度很深。在氮氣吹掃條件下215 ℃反應12 h得到的產物[η]最高為1.851 dL/g,而且曲線還有較大的上升趨勢,反應程度較淺。這是由于施加真空能導致小分子副產物過飽和,增強了小分子從聚合物基質中的擴散脫揮發作用。在氮氣吹掃下進行縮聚,在PBT切片表面形成惰性氣體保護層,防止其發生氧化降解反應,并且導致氣相中小分子副產物濃度降低,形成氣固相之間濃度梯度差,促使固相內小分子向外擴散。與氮氣吹掃下的PBT固相縮聚相比,真空條件下的固相縮聚反應更快,主要原因:一方面是由于在同等溫度下,氮氣吹掃過程會帶走PBT顆粒內部熱量,導致切片散熱更快,反應體系實際溫度要低于設定溫度;另一方面則是由于真空體系下形成的氣固相之間壓差更大,使鏈增長反應更劇烈。

圖6 不同反應氛圍下PBT固相縮聚產物的[η]與t的關系Fig.6 Plots of [η] of PBT solid-state polycondensation products versus t under different atmosphere■—185 ℃;●—195 ℃;▲—205 ℃;▼—215 ℃
由圖7可見,在真空和氮氣氛圍下,反應溫度隨著t的增加,PBT固相縮聚產物的Cs下降的速率與[η]的增長速率類似,相比于氮氣氛圍,真空氛圍下Cs下降速率更快。真空下Cs最低降至9.3 mol/t,而氮氣吹掃下Cs最低為11.5 mol/t,且在真空下Cs初期下降迅速,隨后趨于平緩,而氮氣氛圍下這種現象并不十分明顯,側面證明真空下發生的酯化反應等鏈增長反應的程度比氮氣氛圍下的更深。

圖7 不同反應氛圍下PBT固相縮聚產物的Cs與t的關系Fig.7 Plots of Cs of PBT solid-state polycondensation products versus t under different atmosphere■—185 ℃;●—195 ℃;▲—205 ℃;▼—215 ℃
3 PBT固相縮聚反應動力學
固相縮聚是一個由化學反應與小分子擴散共同控制的復雜過程。本研究在G.CHALLA[17]和B.DUH[18]研究的基礎上開發出一個能夠描述PBT固相縮聚行為的簡單動力學模型,該模型將PBT分子鏈分成兩種端基,即參與化學反應的活性端基和被晶體結構固定以及失去化學活性的非活性端基。該模型假設固相縮聚僅由與端羥基濃度([OH])有關的酯交換反應引起,且固相縮聚是由化學反應控制,在足夠高的v或真空度下沒有發生逆反應。通過以上假設和簡化措施,固相縮聚反應是一個關于活性端基的二階化學反應:
(5)
式中:C為總端基濃度;Ci為非活性端基濃度;k為速率常數。
對公式(5)進行積分得到:
(6)
式中:C0為初始聚合物總端基濃度。
將公式(6)重新排列整合得到:
(7)
對于1 t PBT試樣,其所含有的分子數(n):
(8)
(9)
式中:Mn為數均相對分子質量。
所以1 t PBT試樣中所含有的C為:
(10)
如果實驗數值與修改后的二階動力學方程相符,那么(C0-C)/t對C曲線應該是一條直線。根據公式(9),(10)可計算出PBT在各組實驗條件下的C,再結合公式(7)繪制得到(C0-C)/t與C的曲線,對其進行線性擬合得到圖8。

圖8 不同反應氛圍下PBT固相縮聚產物的(C0-C)/t與C的實驗值及其擬合曲線Fig.8 Experimental value and fitting curves of (C0-C)/t versus C of PBT solid-state polycondensation products under different atmosphere■—185 ℃;●—195 ℃;▲—205 ℃;▼—215 ℃
由圖8可見,實驗值與模型相吻合,即PBT固相縮聚符合二階反應動力學模型。再由擬合曲線的斜率計算得到k。
結合Arrhenius方程:
(11)
式中:A為指前因子;Ea為反應活化能;T為絕對溫度;R為氣體常數,數值為8.314 J/(mol·K)。
由lnk與1/T的關系作圖(見圖9)計算可得Ea數值。

圖9 PBT在真空和氮氣氛圍下固相縮聚的lnk與1/T關系Fig.9 Plots of lnk versus 1/T of PBT solid-state polycondensation under vacuum and nitrogen atmosphere■—真空(50 Pa);●—氮氣氛圍(v為1 L/min)
由表1,表2可看出,兩種氛圍下得到的k都隨著溫度的增加而升高,其中真空氛圍下得到的k明顯要高于氮氣環境下所得的值。

表1 真空(50 Pa)下PBT固相縮聚后的k與A及Ea Tab.1 k,A and Ea of PBT after solid-state polycondensation under vacuum(50 Pa)

表2 氮氣(1 L/min)下PBT固相縮聚后的k與A及Ea Tab.2 k,A and Ea of PBT after solid-state polycondensation at nitrogen atmosphere(1 L/min)
在抽真空環境下得到的Ea(169.50 kJ/mol)及A(1.42×1013kg/(mol·h))相比于氮氣氛圍下(Ea為102.36 kJ/mol,A為2.12×105kg/(mol·h))要明顯高得多。
高的Ea證明反應對溫度高的敏感性,在高真空氛圍下,溫度不僅嚴重影響化學反應進程,還極大影響副產物小分子的擴散速率。A反映了活性基團相互接觸的頻率,A越高,有效碰撞幾率越高。可見高真空體系下的活性分子有效碰撞的概率是相當高的,其活性基團有效碰撞總次數遠高于氮氣體系。
4 結論
a.PBT固相縮聚結果表明,反應溫度較低時,隨著t的增加PBT固相縮聚產物的[η]呈現線性上升趨勢;反應溫度較高時,隨著t的增加PBT固相縮聚產物的[η]的上升速率先快后慢,最后趨于平緩,表示升高溫度和t能極大地加深反應程度,使反應趨近極限。
b.PBT固相縮聚過程中,在一定溫度和t下,[η]的增長速率隨著p的降低和v的提高而增大,但p和v在達到一定值后對[η]的影響逐漸變小,且真空氛圍下[η]的增長速率高于氮氣氛圍。
c.反應動力學研究表明,PBT固相縮聚符合二階反應動力學模型,真空比氮氣下反應的A要高得多,表示真空下參與反應的活性基團之間相互有效碰撞的頻率和總次數更高。真空下所得的Ea遠遠高于氮氣環境,表示高度真空體系下的固相縮聚反應對溫度的依賴性高于氮氣體系;在真空下控制反應溫度是調節反應速率的關鍵一步。

