CRIM1通過激活ERK1/2-VEGF信號通路促進子宮頸鱗狀細胞癌微血管生成
張雨婷,汪亦君,夏 沛,張文輝,宋恩霖
富含半胱氨酸運動神經元蛋白1(cysteine-rich motor neuron 1, CRIM1)屬于腱蛋白樣富含半胱氨酸重復序列蛋白家族成員之一,其生理功能主要通過影響VEGFA的活性[1]調節器官發育過程中血管生成。目前已發現CRIM1與多種腫瘤發生、發展有關,如在肺癌[2]和膠質母細胞瘤[3]中均存在CRIM1的高表達,在前列腺癌PC細胞中CRIM1的高表達促進其浸潤侵襲能力[4],但CRIM1與腫瘤微血管生成的關系目前尚未見報道。本文通過檢測子宮頸鱗狀細胞癌組織中CRIM1蛋白表達,分析其與腫瘤微血管密度(microvascular density, MVD)的關系,并進一步觀察CRIM1對子宮頸鱗狀細胞癌細胞VEGF表達的影響,探討CRIM1與子宮頸癌微血管生成的關系及其分子機制。
1 材料與方法
1.1 臨床資料收集中山大學附屬第一醫院確診的浸潤性子宮頸鱗狀細胞癌石蠟包埋標本50例,患者平均年齡42歲;其中14例腫瘤直徑大于4 cm,29例伴淋巴結轉移,18例伴子宮旁浸潤,高分化16例,中分化22例,低分化12例。所有患者術前均未行放、化療。另取10例慢性子宮頸炎上皮標本作為對照組。
1.2 方法
1.2.1免疫組化 采用免疫組化MaxVision法染色,3~5 μm厚切片,65 ℃烘箱烤片2 h,常規二甲苯脫蠟,梯度乙醇水化,自來水沖洗,檸檬酸鈉抗原熱修復,3%H2O2處理,PBS漂洗。一抗CRIM1工作液50 μL,4 ℃過夜,PBS洗滌后,50 μL MaxVision二抗工作液(KIT-5010,福州邁新公司)室溫下孵育30 min,洗滌后DAB顯色,蘇木精復染,中性樹膠封固。以PBS代替一抗作陰性對照。測量累積光密度(integral optic density, IOD)進行蛋白表達半定量結果判定。在光鏡下(×400)選取腫瘤組織中陽性最強的3個高倍視野,數碼拍照,應用圖像分析軟件Image Pro Plus 6.0準確分割陽性區域,測量IOD值。相同條件下,每張圖片測量3次,每張切片選取3張視野測量,以9次測量的IOD均值作為該視野中蛋白的表達強度。
1.2.2MVD檢測 采用Weinner計數法檢測子宮頸鱗狀細胞癌組織中MVD。CD34免疫組化染色后(鼠抗人CD34單克隆抗體:Kit-004,福州邁新公司)以黃色顆粒狀標記的血管內皮為標準。MVD計數采用Weinner等[5]計數法:切片在光鏡下(×100)挑選MVD分布最高區域,在光鏡下(×200)計數5個不同視野中被CD34染成陽性的微血管數量,取其平均值作為MVD值。每個與鄰近微血管分離明顯的陽性染色單個血管內皮細胞或血管內皮細胞簇均視為1個獨立的微血管,結構不相連的分支血管結構也計為1個微血管。直徑≥8個紅細胞的血管,帶有厚的平滑肌血管或者硬化壞死區血管不在計數范圍內。
1.2.3子宮頸鱗狀細胞癌SiHa細胞CRIM1基因瞬時轉染 子宮頸鱗狀細胞癌細胞SiHa(TCHu113,中國科學院上海細胞庫),應用含10%胎牛血清及雙抗的DMEM培養基常規培養于37 ℃、5%CO2的細胞培養箱中。按每毫升3×105個細胞接種2 mL細胞懸液于6孔板,24 h后更換為無血清、無雙抗的基礎培養基。實驗分為3組:Control、Vector(空載質粒)、pCMV3-CRIM1組,分別用無血清、無雙抗的DMEM 500 μL稀釋6 μg的pCMV3-CRIM1過表達質粒(HG11666-UT,北京義翹神州生物公司)、6 μg的pCMV/hygro-Negative空載質粒(CV001,北京義翹神州生物公司)和兩支10 μL脂質體Sinofection(STFO2,北京義翹神州生物公司),室溫孵育5 min,各自將質粒和轉染試劑混合形成轉染復合物,室溫孵育20~25 min,加入對應孔板中。Control組加入正常培養細胞的完全培養基,轉染后培養6 h,更換培養基為新鮮含10%血清不含雙抗的培養基,繼續培養至48 h,通過Western blot檢測轉染效果及相關蛋白變化。
1.2.4Western blot法 RIPA裂解液加入蛋白酶和磷酸酶抑制劑配成細胞裂解液提取細胞總蛋白,用以檢測CRIM1(兔抗人多克隆抗體:H00051232-M01,臺灣Abnova公司)、p-ERK(兔抗人多克隆抗體:AF1015,美國Affinity公司)、total-ERK(兔抗人多克隆抗體:16443-1-AP,美國Proteintech公司)和VEGF(兔抗人多克隆抗體:19003-1-AP,美國Proteintech公司)蛋白表達;蛋白濃度測定后,按每孔20 μL上樣量用Loading Buffer和RIPA液配平,沸水加熱后冷卻離心上樣,行十二烷基磺酸鈉聚丙烯酰胺(SDS-PAGE)凝膠電泳,轉至PVDF膜上。5%脫脂奶粉封閉,加入一抗(工作濃度1 ∶500,內參β-actin為1 ∶4 000)4 ℃過夜;TBST洗滌后加入二抗(工作濃度1 ∶5 000)常溫搖床孵育;洗滌膜后,利用ECL化學發光試劑盒孵育發光,顯影。利用Image Pro Plus 6.0軟件測量目的蛋白條帶和內參條帶的灰度值,以目的條帶灰度值與內參灰度值的比值作為蛋白的相對表達水平。
1.2.5細胞上清液中VEGF含量ELISA檢測 收集各組癌細胞的上清液,離心后去沉淀取上清備用。按照ELISA試劑盒(EHC108.96.2,深圳欣博盛公司)說明書進行操作,檢測標準品及各組待測樣品的OD值,根據標準曲線計算各組待測樣品中VEGF的含量。
1.2.6CCK-8實驗 留取上述兩組的癌細胞上清液,取對數生長期的HUVEC(HF1121,上海富衡生物公司)制成細胞懸液,按每孔100 μL含2 000個細胞的濃度接種于96孔板,分為Control、Vector、pCMV3-CRIM1和DMEM組,每組5個復孔。細胞貼壁后將留取的癌細胞上清液分別作用于2組的HUVEC,Control組HUVEC加入完全培養基,培養24 h后棄去上清,加入10%的CCK-8工作液(CK04,北京沃比森科技公司),在培養箱繼續培養3 h,于酶標儀450 nm處測OD值,計算各組細胞增殖活力值。
1.2.7Matrigel膠管腔形成實驗 實驗根據In Vitro Angiogenesis Assay內管腔形成試劑盒(ECM625,美國Merck Millipore公司)說明書進行,槍頭、EP管、96孔板置于-20 ℃預冷過夜,Matrigel膠置于4 ℃預冷過夜;次日,吸取Matrigel膠每孔50 μL加入96孔板,放入4 ℃冰箱10 min(可使Matrigel膠鋪板更加均勻沒有氣泡),放入37 ℃培養箱,放置1 h待Matrigel膠聚合成凝膠。PBS清洗3次,胰蛋白酶消化HUVEC,1 000 r/min離心5 min。HUVEC細胞用DMEM培養基制備成細胞懸液(每孔約1×105個細胞),取上述轉染后的癌細胞上清100 μL和HUVEC細胞懸液100 μL以1 ∶1混合,合計200 μL加入96孔板中,記作0 h,放入5%CO2、37 ℃細胞培養箱中培養,培養10 h后取出,倒置顯微鏡下觀察并計數拍照小管形成情況。
1.2.8人重組蛋白作用SiHa 將SiHa細胞消化離心制成細胞懸液,調整濃度接種于6孔板中,實驗分為5組:0、12.5、25、50、100 ng/mL,24 h后將人重組CRIM1蛋白(H00051232-Q01,臺灣Abnova公司)稀釋加入腫瘤細胞繼續培養24 h,提取細胞蛋白及細胞上清,分別用Western blot法和ELISA法檢測細胞蛋白中VEGF表達和上清中VEGF的含量變化。
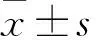
2 結果
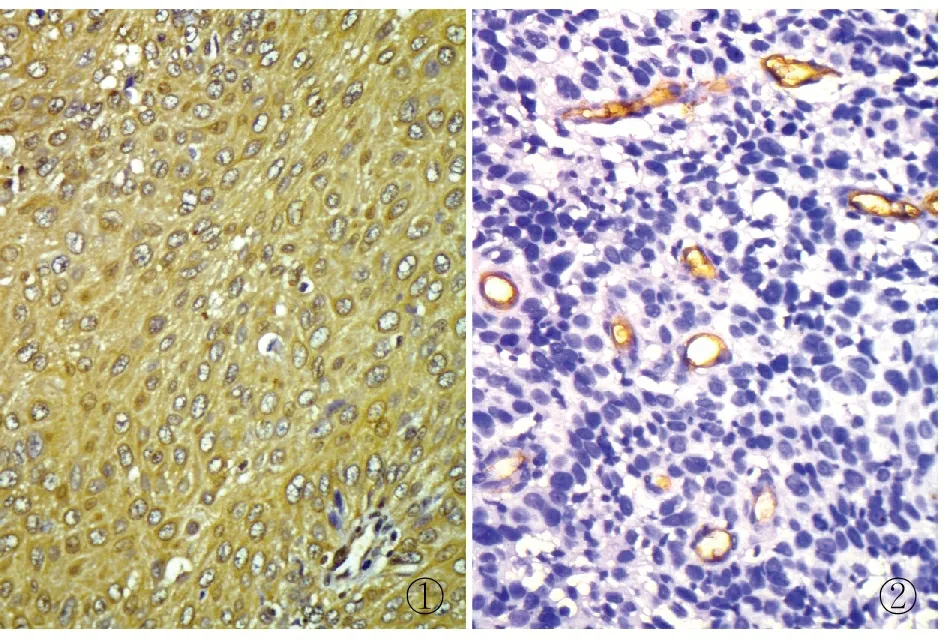
2.1 子宮頸鱗狀細胞癌中CRIM1的表達CRIM1在正常子宮頸上皮中呈弱陽性甚至陰性;而在子宮頸鱗狀細胞癌組織中均呈彌漫陽性,且主要表達于子宮頸鱗狀細胞癌的細胞質和(或)細胞核(圖1)。光密度檢測分析:CRIM1在子宮頸鱗狀細胞癌中的表達顯著高于其在正常子宮頸上皮中的表達(P<0.001,表1)。
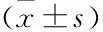
表1 子宮頸鱗狀細胞癌和正常子宮頸組織中CIRM1的表達
2.2 子宮頸鱗狀細胞癌中CRIM1的表達與MVD的關系子宮頸鱗狀細胞癌中CD34標記的微血管分布于癌巢之間和癌巢內瘤細胞之間(圖2),平均MVD值為31。相關性分析顯示:在子宮頸鱗狀細胞癌中,CRIM1的表達與MVD呈正相關(r=0.546,P<0.01)。
①②
圖1子宮頸鱗狀細胞癌組織中CRIM1的表達,胞質和(或)胞核陽性,MaxVision法圖2子宮頸鱗狀細胞癌組織中CD34內皮標記的微血管,MaxVision法
2.3 CRIM1與SiHa細胞血管誘生能力的關系
2.3.1過表達CRIM1的SiHa細胞上清液促進內皮細胞增殖 CCK-8細胞增殖實驗結果顯示,pCMV3-CRIM1質粒轉染組癌細胞上清液刺激下的內皮增殖活力(1.02±0.024)顯著高于Control組(0.93±0.030,P<0.01)和Vector組(0.93±0.028,P<0.01)。
2.3.2SiHa細胞中CRIM1過表達增強內皮細胞管腔形成能力 管腔形成實驗結果顯示,pCMV3-CRIM1質粒轉染組癌細胞上清液作用下內皮細胞的管腔形成能力(1.20±0.137)顯著高于Control組(1.0±0.088)和Vector轉染組(0.89±0.120)(P均<0.05)。
2.4 CRIM1活化ERK信號上調VEGF表達促進SiHa細胞血管誘生能力
2.4.1CRIM1的高表達上調SiHa細胞中VEGF蛋白表達 CRIM1基因轉染組SiHa細胞中CRIM1和VEGF的表達水平分別為0.819±0.086和0.404±0.039,顯著高于Control組(0.092±0.021,P<0.001;0.059±0.008,P<0.001)和Vector轉染組(0.122±0.019,P<0.001;0.056±0.008,P<0.001);Vector轉染組和Control組蛋白表達差異無顯著性(圖3),且ELISA檢測結果顯示,陽性轉染組細胞上清液中VEGF含量為(763.751±25.816) pg,顯著高于Control組[(653.501±25.487) pg,P<0.01]和Vector轉染組[(649.006±36.539) pg,P<0.01)],提示CRIM1基因轉染成功,且CRIM1高表達可上調SiHa細胞VEGF的表達水平。
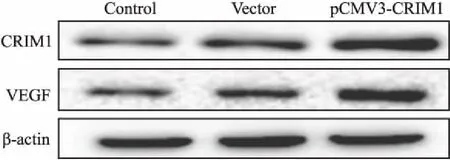
圖3 CRIM1基因轉染上調SiHa細胞中VEGF的表達:Control.空白對照組;Vector.陰性轉染組;pCMV3-CRIM1.陽性轉染組
2.4.2CRIM1上調VEGF表達依賴于ERK信號的活化 pCMV3-CRIM1質粒轉染組SiHa細胞中p-ERK和VEGF的表達水平(0.417±0.016,0.244±0.014)顯著高于Control組(0.134±0.007,P<0.001;0.066±0.004,P=0.01)。ERK抑制劑U0126與pCMV3-CRIM1轉染質粒聯合處理的SiHa細胞中p-ERK的表達水平(0.218±0.008)顯著低于pCMV3-CRIM1質粒轉染組(P<0.001),且該組細胞中VEGF的表達水平(0.061±0.009)也顯著低于pCMV3-CRIM1質粒轉染組(0.244±0.014,P<0.001),SiHa細胞中CRIM1的表達在兩組間差異無顯著性(圖4)。
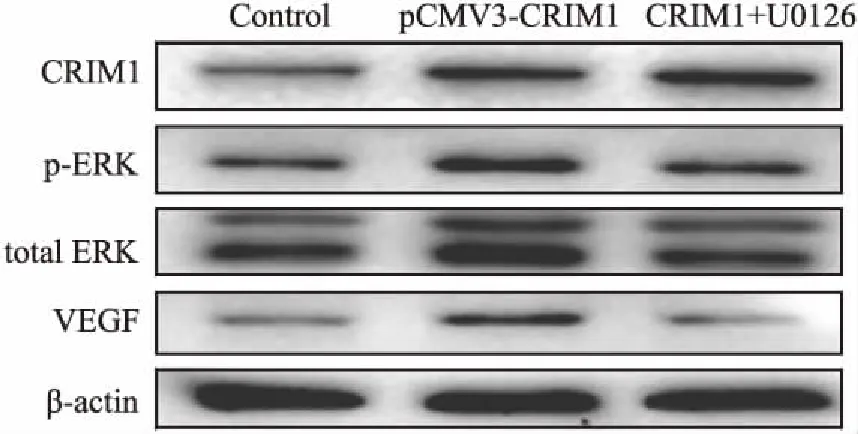
圖4 ERK信號的活化對CRIM1上調SiHa細胞VEGF表達的影響:Control.空白對照組;pCMV3-CRIM1.質粒陽性轉染組;CRIM1+U0126.ERK抑制與pCMV3-CRIM1表達質粒聯合處理組
2.5 外源性CRIM1對SiHa細胞中VEGF蛋白表達的影響不同濃度的外源性CRIM1對SiHa細胞中VEGF蛋白表達水平無明顯影響(P>0.05),且ELISA檢測結果亦顯示,不同濃度外源性CRIM1蛋白刺激下的各組SiHa細胞上清中VEGF的表達水平差異無顯著性(P>0.05)。
3 討論
實體腫瘤新形成的微血管在結構上缺乏完整性[5],易于腫瘤細胞浸潤轉移。有文獻報道許多促血管生成因子提高子宮頸癌的浸潤轉移能力,與子宮頸癌預后不良顯著相關[6-8]。故研究新的微血管生成調節因子對子宮頸癌血管生成的機制和生物治療具有重大意義。
CRIM1屬于腱蛋白樣富含半胱氨酸重復序列蛋白家族成員之一。Pennisi等[9]通過構建CRIM1等位基因敲除的小鼠模型,發現CRIM1非正常表達使小鼠出現諸如死亡、并指、大腦血腫、眼睛缺陷和皮膚血泡等表現,提示CRIM1屬于重要的器官發育調節因子。在腎小球血管發生過程中CRIM1調節VEGFA的活性及其細胞表面的遞呈[1],且通過促進內皮VEGFR2的磷酸化調節VEGFA自分泌以維持血管穩定性[10]。CRIM1可高表達于有復發潛能的胃腸間質瘤[11]、膠質母細胞瘤[3],影響肺癌A549細胞黏附和遷移行為[2],且與髓性白血病及卵巢癌耐藥有關[12-13],提示CRIM1是潛在血管生成調節因子,且與多種腫瘤的發生、發展有關,但關于它與腫瘤血管生成的研究卻鮮有報道。CD34內皮標記對腫瘤組織中新生的微血管和不完整的血管較為敏感[14]。本實驗通過內皮CD34標記檢測子宮頸鱗狀細胞癌 MVD,免疫組化檢測子宮頸鱗狀細胞癌組織中CRIM1的表達,分析CRIM1與子宮頸鱗狀細胞癌細胞血管誘生能力的關系。
CRIM1在子宮頸鱗狀細胞癌組織中的表達顯著高于正常子宮頸上皮組織,且與MVD呈正相關,提示CRIM1可能參與子宮頸鱗狀細胞癌的發生、發展,且與子宮頸鱗狀細胞癌微血管生成有關。對子宮頸鱗狀細胞癌SiHa細胞進行CRIM1基因瞬時轉染后癌細胞上清液刺激下的內皮細胞的增殖能力和管腔形成能力顯著升高,表明CRIM1能增強子宮頸鱗狀細胞癌細胞的血管誘生能力。腫瘤微血管生成是一個復雜的多因素參與的過程,包括腫瘤組織中的瘤細胞、內皮細胞和其他一些基質細胞之間的相互作用。目前較為熟知的調節途徑是瘤細胞通過表達分泌某些血管生成因子誘導內皮細胞的血管生成,稱之為旁分泌調節途徑[15]。本實驗結果顯示CRIM1可能通過某種信號途徑上調血管生成因子的表達,從而旁分泌性促進內皮的血管生成。本課題組發現CRIM1轉染后癌細胞中VEGF的表達明顯上調,且此時癌細胞上清液中VEGF含量的升高;該結果與有關CRIM1調節器官生長發育過程中的血管新生的實驗結果基本一致,說明CRIM1調節腫瘤的血管生成機制是通過介導VEGF表達變化而實現的。據報道,CRIM1對VEGF的調節作用與其分子結構上RGD模序結合integrin β1從而活化ERK信號有關[16]。本課題利用ERK特異性抑制劑U0126預處理癌細胞后再進行CRIM1基因轉染,發現正常轉染的癌細胞中VEGF表達升高的同時,p-ERK表達水平也顯著高于正常轉染組,當U0126抑制ERK信號的活化時,癌細胞中VEGF的水平顯著低于正常轉染組,但兩組間CRIM1的表達差異無顯著性,表明CRIM1通過活化下游ERK信號上調子宮頸鱗狀細胞癌VEGF的表達。ERK信號的活化與多種腫瘤微血管生成有關[17-18],其受多種上游調節因子的激活。CRIM1激活子宮頸鱗狀細胞癌細胞ERK信號是否也與CRIM1和integrin β1的相互作用尚需進一步分析。利用人工重組CRIM1蛋白直接刺激子宮頸癌細胞,其癌細胞及上清液中VEGF的表達水平均無顯著變化,說明CRIM1自身并不能作為一種分泌性蛋白發揮作用。此外,本課題組織學研究發現CRIM1表達于子宮頸鱗狀細胞癌的細胞質和(或)細胞核,CRIM1促進子宮頸鱗狀細胞癌微血管生成的功能是否與它在癌細胞中的表達定位有關,值得我們深入探討。
綜上所述,本實驗首次證實CRIM1在子宮頸鱗狀細胞癌中高表達,CRIM1能通過活化ERK信號上調癌細胞VEGF的表達,促進子宮頸癌微血管生成。