受激輻射損耗超分辨顯微成像系統研究的新進展*
王佳林 嚴偉 張佳 王璐瑋 楊志剛 屈軍樂
(深圳大學物理與光電工程學院, 光電子器件與系統教育部/廣東省重點實驗室, 深圳 518060)(2020年2月2日收到; 2020年3月11日收到修改稿)
由于受到衍射極限的影響, 傳統光學顯微鏡的分辨率被限制在半個波長左右. 近二十年來出現了許多通過不同方法繞過光學衍射極限的超分辨成像技術, 其中, 受激輻射損耗顯微(stimulated emission depletion microscopy, STED)通過引入一束環形損耗光來抑制熒光光斑外圍熒光分子的發光, 以達到減小點擴散函數的目的, 實現超分辨成像. 經過近些年的發展, STED 系統無論從光束的產生、校準和掃描, 還是最后的成像,都有了很大的發展. 本文將簡要介紹STED 成像技術的基本原理, 詳述STED 超分辨成像技術出現至今在光源、掃描及成像系統等方面的進展, 以及在三維成像和多色成像方面的發展現狀, STED 技術與其他顯微技術的結合. 最后, 本文對STED 技術近幾年的研究新進展進行了系統的論述, 對STED 技術未來的發展趨勢進行了探討.
1 引 言
早在1665年, 英國科學家羅伯特·胡克(R.Hooke)首次利用自制的顯微鏡觀察到植物細胞并提出“cell”的概念, 自此以來顯微鏡與生物學之間形成了密不可分的關系. 隨著科學的進步與技術的發展, 生物醫學領域對于生物體結構的觀察已經從微米尺度提高到了納米尺度, 這對顯微鏡的顯微性能提出了更高的要求. 縱觀顯微技術的發展歷史,在十九世紀末, 德國物理學家恩斯特·阿貝(Ernst K. Abbe)提出了光學衍射極限的概念, 認為成像系統的橫向與軸向分辨率均受到衍射極限的限制.即使光學顯微鏡經過了幾百年的發展, 顯微鏡的成像性能已經有了巨大的飛躍, 但依然受到光學衍射極限的限制, 橫向分辨率一般被限制在200 nm 左右, 軸向分辨率被限制在500 nm 左右, 該極限分辨率已然無法滿足日益發展的生物科學研究的需求. 直到二十世紀九十年代, 科研人員才陸續提出各種可以突破衍射極限的顯微技術, 這些顯微技術統稱為超分辨顯微技術. 超分辨顯微技術的發明,對于生物醫學、材料學等領域有著非常重要的意義. 在眾多超分辨顯微技術中, 由德國科學家Hell和Wichmann 于1994年提出的STED 超分辨顯微技術[1], 經過近幾年來的發展已經十分成熟, 應用范圍也非常廣泛.
本文將介紹STED 的基本原理及系統的主要組成部分, 重點介紹近年來STED 技術各方面性能提升的實現方式以及STED 與其他技術相結合的情況.
2 STED 顯微技術的基本原理及其系統的主要組成部分
2.1 STED 顯微技術的基本原理
傳統光學顯微技術即使在很大程度上消除了像差和提高了放大倍率, 但其分辨率始終無法實現突破, 主要是受到光學系統衍射效應的限制, 即一個理想的物點在經過光學系統成像后, 在成像面上形成具有一定尺寸的衍射斑. 觀測物可以被視為由多個物點組成, 在像面上則會形成多個衍射光斑,當衍射光斑之間的距離近到一定程度時就無法區分開, 稱為衍射極限. 在熒光顯微鏡中, 被衍射光斑照射的區域發出熒光, 形成一個熒光光斑.STED 技術針對熒光光斑受衍射影響而擴大的情況, 對光束進行空域上的調制, 有效地壓縮了光斑的點擴散函數(point spread function, PSF), 實現超分辨成像. 具體原理是: 利用兩束激光來進行顯微成像, 其中一束為激發光, 用于激發熒光分子;另一束是中心強度為零的中空形圓環狀STED 光(也稱為損耗光), 其與激發光共軸且波長與熒光分子發射波長匹配. 激發光使基態能級S0上的電子躍遷到激發態能級S1, 在沒有外界干擾的情況下這些激發態的電子將會以自發輻射熒光的形式回落到基態, 如果處在激發態的電子在環形STED 光照射下將會發生受激輻射效應, 導致STED 光照射區域產生光子的波長有別于自發輻射區域的光子波長, 相較于自發輻射區域,STED 光照射區域分子處于暗態, 視為不發熒光(如圖1(a)). 由于兩束光重疊區域產生受激輻射,只有中心區域發出熒光, 因此減小了激發光斑的有效面積, 即減小了PSF, 實現了空間分辨率的提高(如圖1(b)). STED 系統的橫向空間分辨率, 可用公式表示為

其中l為激發光的波長,NA是物鏡的數值孔徑,ISTED和Is分別對應STED 光的光強和飽和受激輻射光強. 飽和光強Is= 1/(tfls)由具體染料的熒光壽命tfl和STED 光的吸收截面s共同決定. 由此可知, 可以通過增加STED 光強度的方法提高成像的分辨率, 理論上STED 系統的分辨率可以提高到無限高, 但是在實際應用時要考慮到熒光材料的光漂白性, 特別是生物樣品的光毒性等, 因此在實際應用時要根據目標樣品的不同采取不同的STED 光強度.
2.2 STED 系統的基本組成
典型的點掃描式STED 系統一般由光源(圖2紅色虛線框)、光束耦合單元(圖2 綠色虛線框)、掃描單元(圖2 橙色虛線框)與成像單元(圖2 藍色虛線框)等四個部分組成.

圖1 STED 的原理圖 (a)能級輻射示意圖; (b)光束重合示意圖Fig. 1. The concept of STED: (a)The concept of stimulated emission; (b)the overlapping of beams.
一般的單色STED 超分辨成像系統需要兩個單波長輸出的激光器作為光源, 第一個激光器產生激發光束, 其波長處于熒光分子激發譜的波峰附近. 第二個激光器產生STED 光束, 其波長處于熒光分子發射譜的拖尾附近, 避免對熒光分子產生二次激發. 此外, 脈沖光在時間上具有可分離性, 為了保證激發光與STED 光到達樣品時的先后順序,激發光與STED 光一般都是脈沖光. 在光源的強度上, 為了保證一定的擦除效果以獲得高的分辨率, STED 系統中的STED 光強度一般為10—103mW量級.
要實現對PSF 的調制, 關鍵是需要對STED光進行調制, 并保證激發光束與STED 光束高度重合. 一般使用渦旋相位板(vortex phase plate,VPP)或空間光調制器(spatial light modulator,SLM)來對STED 光的波前進行調制以產生環形光, 其中心強度趨近于零的區域必須小于激發光的光斑大小. 利用二向色鏡對STED 光與激發光的反射率和透射率的不同來實現激發光與STED 光的重合, 不僅要實現橫截面上兩個光斑的重合, 也要保證在Z軸上高度重合. 此外, 二向色鏡還需要對樣品返回的熒光有透射作用.
激發光與STED 光重合之后, 通過掃描單元如掃描振鏡, 實現光斑在樣品上的掃描, 從而實現二維面陣成像. 在點掃描STED 成像系統中, 掃描單元的掃描速度直接決定了系統的成像速度.

圖2 STED 系統圖Fig. 2. The setup of STED system.
3 STED 系統的發展
3.1 STED 系統光源部分的改進
為了實現更高的空間分辨率, STED 系統通常需要具有很高功率的STED 光, 因此, 在早期的STED 系統中, 激發光多為皮秒激光器, 而STED光通常是對具有很高功率的飛秒激光器進行展寬而得到的高能寬脈沖激光, 所達到的最高分辨率為2.4 nm[2]. 雖然用飛秒激光器作為STED 光能夠獲得超高的分辨率, 但是飛秒激光器成本高, 難以普及. 對于早期的STED 系統, 最常用的光源是脈沖寬度80 ps 的激發光與脈沖寬度200 fs 的STED光. 其中, STED 光需要進行約1000 倍的脈沖展寬. 此外, 還需要將激發光與STED 光進行時間同步, 確保STED 光脈沖在樣品已經被激發到激發態但是還沒有發生自發輻射的這個時間段到達樣品, 這使得脈沖型STED 系統較為復雜. 脈沖光在帶來更高峰值功率的同時, 也更容易對生物活體樣品造成損傷.
2007年, Willig 等[3]發現可以利用連續光(continuous wave, CW)進行STED 成像. 若CW激發光以Kexc的速率進行激發時, 認為S1被電子填充的概率為N1:
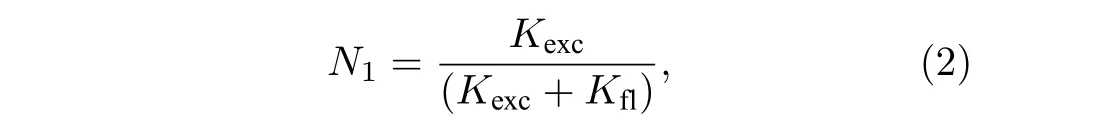
其中熒光衰減率Kfl= 1/tfl為熒光壽命tfl的倒數,且N1< 1. 當加入強度為ISTED, 受激輻射分子截面為s的CW-STED 光時, 則引入了一個額外的衰減率KSTED=sISTED, 此時S1被填充的概率變為
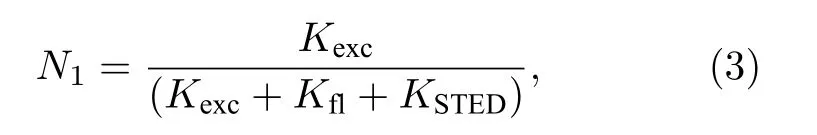
當STED 光束強度ISTED滿足
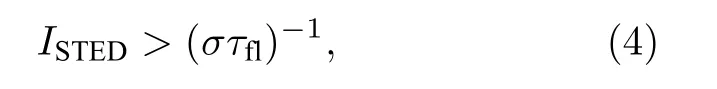
則有KSTED>Kexc>Kfl, 此時STED 占主導地位. 進一步加強STED 光束的強度, 就能夠使KSTED?Kexc, 在這種情況下N1?1, 意味著無論激發光與STED 光的時間順序如何, S1能級上的電子都會由于受激輻射迅速回到S0能級. 也就是說, 當激發光束的激發速率遠遠小于STED 光的受激輻射速率時, 激發光束與STED 光束時間順序的同步變得不再重要. 最終, Willig 等[3]在實驗中實現了CW-STED 系統的超分辨成像, 達到了29 nm 的分辨率. 使用CW 光作為STED 系統的光源, 不僅可以在相同平均功率下保證較小的峰值功率, 而且使得STED 系統更加簡化.
3.1.1 使用超連續脈沖激光器作為光源
2008年Wildanger 等報道了一種基于光子晶體光纖的超連續譜STED 顯微鏡[4], 這種STED顯微鏡使用單一的超連續譜激光器作為光源, 利用偏振分束器(polarization beam splitter, PBS)得到了用于激發和損耗的兩束光. 對于激發光, 使用干涉濾波片(interference filter, EF)分離出所需要的激發波長. 對于STED 光, 使用布儒斯特棱鏡構建的波長選擇器(wavelength selector, WS)來篩選波長. 該波長選擇器的出口設置了一個位置與寬度可變的狹縫, 通過改變狹縫的位置與寬度可以選擇STED 光的中心波長與光譜寬度, 以輸出所需STED 光(圖3).

圖3 基于超連續譜光源的STED 系統[4]Fig. 3. STED system based on supercontinuum laser source[4].
該系統在保證超分辨效果的前提下, 簡化了光源, 降低了STED 系統的成本, 同時提高了STED 光的可調諧性. 理論上, 該系統通過移動狹縫位置可以實現多色成像, 然而實際操作上受到雙色鏡透過率的限制, 實現多色成像的難度較大.
3.1.2 使用多色受激拉曼散射光作為光源
優化系統光源是改進STED 系統的重點方向之一, 使用連續光作為STED 的光源, 不僅可降低系統成本, 而且使多色成像成為可能. Rankin 等[5]在2008年嘗試了使用多色受激拉曼散射(stimulated Raman scattering, SRS)光 源 作 為STED 系統的STED 光(圖4(a)).
受激拉曼散射效應是指當入射到工作介質(如石英光纖)的激光足夠強時, 會在光纖中產生具有較高強度的拉曼散射光(頻率在激發光頻率到分子簡正振動頻率范圍內), 當入射光強度超越一定閾值時, 對應的散射光也足以成為單獨的輻射光源, 從而激發另一頻率范圍的拉曼散射光. 如此反復, 便能產生一系列頻率的拉曼散射光. 該系統中, 利用脈沖長度為1 ns, 光譜帶寬為0.3 nm的532 nm的激光作為初始光源, 通過SRS 光纖發生受激拉曼散射效應, 產生了一系列波長的散射光(圖4(b)), 利用帶通濾波器可選擇出合適波長的STED 光進行超分辨成像. 使用受激拉曼散射光作為STED光, 具有系統緊湊和STED 光波長可選的特點, 是多色STED 超分辨成像的基礎, 但是該系統的主要缺點是需要功率較高的脈沖光源,對光源的要求仍然較高, 對于活體成像也有一定的限制.
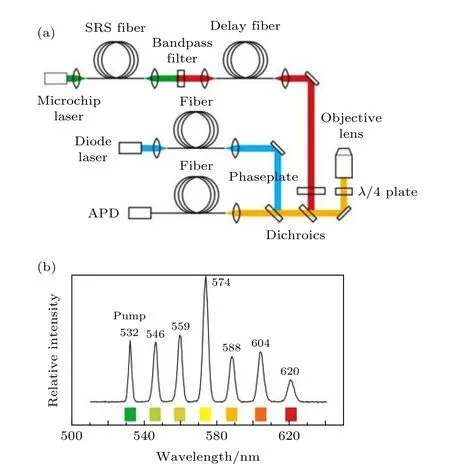
圖4 基于受激拉曼散射光源的STED 系統示意圖[5](a)基于受激拉曼散射光源的多色STED 系統; (b)激光器在光纖中的SRS 輸出光譜Fig. 4. Simplified schematic of a STED system with a stimulated Raman-scattering light source[5]: (a) Multicolor STED system with stimulated Raman-scattering laser source; (b) output spectrum from the SRS fiber.
3.1.3 使用高斯-拉蓋爾矢量光束作為STED光源
環形STED 光的產生, 對實現STED 超分辨成像非常重要. 傳統的STED 系統一般是采用VPP或SLM 進行波前調制產生環形光, T?r?k 等[6]報道了利用高斯-拉蓋爾(Gauss-Laguerre)矢量光束作為環形STED 光, 在不同深度的焦面上均能保證較好的零強度.
傳統的高斯環形光在沒有畸變的條件下能夠在聚焦位置產生較好的零強度(圖5 點劃線), 然而當聚焦深度增加且出現像差時, 其能量分布將發生移動, 并且聚焦位置的強度不再為零(圖5 實線).相反地, 高斯-拉蓋爾環形光則可以不受像差畸變的影響, 在光軸上保持穩定的零強度(圖5 虛線),能夠保證STED 光束在不同焦面深度的受激輻射效率.
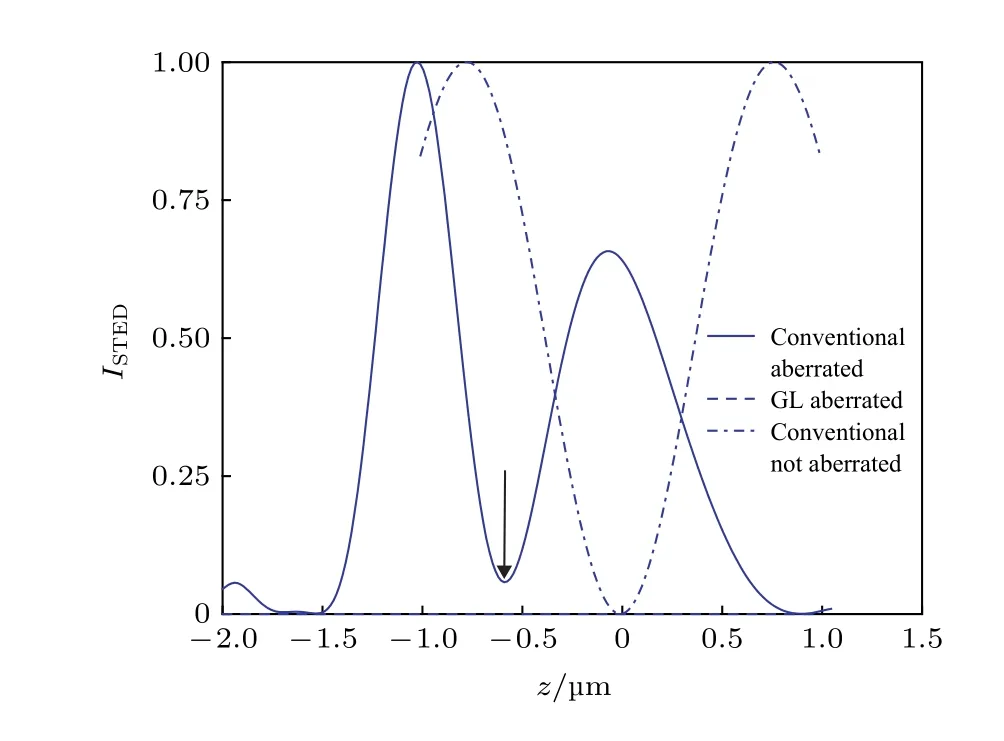
圖5 TED 光強度的分布曲線[6]Fig. 5. The intensity distributions of depletion beam[6].
3.1.4 使用貝塞爾光作為STED 光源
使用高斯光形成的STED 光進行STED 成像, 由于球面像差、散射畸變和損耗等因素, 當焦點從樣品表面移到樣品深處時, 通常無法保持一致的分辨率. 2016年北京大學Yu 等[7]利用貝塞爾光束(Bessel-beam)無畸變的特性, 將環形貝塞爾光束作為STED 光進行STED 成像(GB-STED),在固體瓊脂糖樣品和類腦組織灰質中分別達到了155 μm (圖6 左) 和100 μm (圖6 右)深度的超分辨成像.
由于貝塞爾光束在不同成像深度上能保持高的空間分辨率, Zhang 等[8]在其深度成像的基礎上, 將點掃描改為線掃描, 搭建了貝塞爾STED 光片成像系統, 有效地提升了STED 系統的成像速度, 降低了光損傷. 在系統實現上, 將零級貝塞爾光作為系統的激發光(圖7(a)), 比二階貝塞爾光效率更高的一階貝塞爾光作為STED 光(圖7(c)),通過高階貝塞爾光束來耗盡貝塞爾激發光周圍的自發輻射, 可以將光片的厚度減小到衍射極限. 與傳統的點掃描STED 顯微鏡相比, 線掃描貝塞爾光束STED(BB-STED)顯微鏡具有更快的成像速度, 能夠對大體積樣品實現快速成像. 此外,由于BB-STED 使用平面照明光限制樣品的薄層,從而顯著減少了焦平面上方和下方的光漂白和光損傷.
與高斯光束相比, 貝塞爾光束的光斑會不可避免地出現旁瓣, 使用相消干涉的方法來使邊帶最小化可以在一定程度上減少貝塞爾光束的旁瓣強度.

圖6 共聚焦、傳統STED與貝塞爾STED成像的分辨率隨成像深度的變化曲線[7] (a) 40 nm 熒光珠在固體瓊脂糖樣品不同深度成像的分辨率; (b) 40 nm 熒光珠在類腦組織灰質不同深度成像的分辨率Fig. 6. Imaging curves of Confocal、traditional STED and Bessel-STED[7]: (a) Resolution of 40 nm fluorescent beads at different depths of solid agarose samples; (b) resolution of 40 nm fluorescent beads at different depths of like-gray matter in brain tissue.

圖7 零階貝塞爾激發光與高階貝塞爾STED 光[8] (a)零階貝塞爾激發光在XY 平面的光強分布; (b)零階貝塞爾激發光的光強曲線; (c)一階貝塞爾STED 光在XY 平面的光強分布; (d)一階(黑色)與二階(紅色)貝塞爾STED 光的光強曲線Fig. 7. The zero-order Bessel beam for excitation and the higher-order Bessel beam for depletion[8]: (a) The intensity distribution of zero-order Bessel excitation beam in the XY plane.; (b) the intensity curve of zero-order Bessel excitation beam; (c) the intensity distribution of first-order Bessel depletion beam in the XY plane; (d) the intensity curve of first-order (black) and second-order(red)Bessel depletion beam.
3.2 STED 系統的光束校準
STED 系統利用STED 光來抑制激發光外圍區域的熒光發射, 前提是需要對光路進行精密準確的校準, 使STED 光與激發光完全重合, 這對于系統操作提出了非常高的要求. 在傳統STED 系統中, 光束重合的精確度決定了STED 系統的成像質量, 因此要想獲得高質量的STED 圖像, 必須保證兩束光的高度重合.
3.2.1 自適應光學自動校準
常規的STED 系統一般利用電荷耦合器(charge coupled device, CCD)等探測器成像對光束進行粗略的調節, 然后再使用金納米顆粒的散射成像進行細微調節, 直至兩束光的PSF 完全對準.這種光束重合的調節方式, 一方面需要進行手動調節, 另一方面需要切換反射成像模式, 不僅操作繁瑣, 而且反射和熒光成像模式之間的不匹配也可能引起其他問題. 針對這一問題, Gould 等[9]提出了使用自適應光學實現光束自動對準的方法, 可以實現4.3 ± 2.3 nm 的對準精度. 具體地, 通過在STED光束的路徑中放置空間光調制器(SLM), 在SLM 上輸入STED 相位掩模產生環形光束, 并施加在X和Y方向上的已知傾斜量來獲取STED圖像. 對獲取的STED 圖像的圖像亮度和清晰度進行分析計算, 當STED 光焦點的零強度位置對準激發光焦點的中心時, STED 圖像最亮, 且清晰度最高; 當STED 光束與激發光束重疊不好時, 得到的STED 圖像與重疊比較好的STED 圖像對比, 圖像的亮度和清晰度都會降低. 利用亮度與清晰度兩個指標, 能夠對光束的對準效果提供可靠的判斷標準.
利用自適應光學, 可以對熒光樣品進行程序對準操作來代替手動調節(圖8(a)—圖8(f)), 從而極大簡化STED 光與激發光的對準.
3.2.2 雙折射裝置實現光束校準
Reuss 等[10]提出了利用雙折射裝置進行光束對準的方法, 稱為easy-STED, 提高了光束的穩定性和操作的簡易性. 常規的VPP 不能在同一位置對不同波長的光束進行有效區分, 利用雙折射晶體作為光束整形裝置, 當激發光與STED 光通過該整形裝置后, 只有STED 光的波前被調制成為中空環形分布, 而激發光則不受影響. 具體來說, 該光束整形裝置的中心部分是具有四個快軸方向的組合波片, 該組合波片由一個較大的波片切割成四個部分并以一定的快軸方向夾角重新黏合到共同的基底上得到(如圖9(a)左側). 不同的快軸方向對光束偏振產生不同的效果, 因而產生方位角偏振光束. 以波長532 nm 的激發光及對應647 nm 的STED 光為例, 相應波片對激發光產生的延遲約是3l, 對STED 光產生的延遲是2.5l. 因此, STED光會產生一個半波延遲, 導致偏振面旋轉, 而激發光則不受影響. 另外, 結合消色差半波片, 可以實現針對STED 光束的環形聚焦, 而激發光則聚焦成標準的衍射光斑.
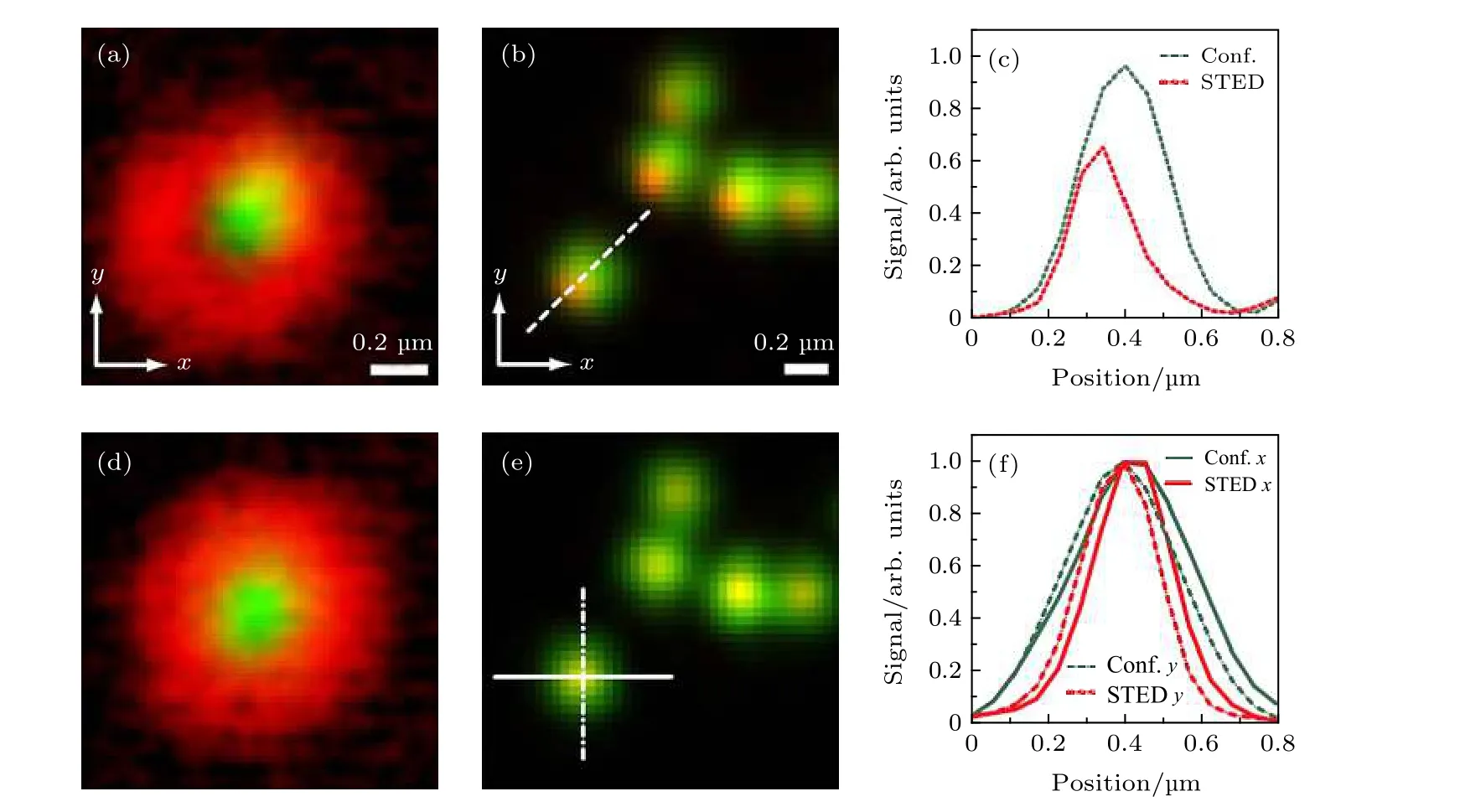
圖8 STED 光束與激發光束的對準結果[9] (a)激發光與STED 光未對準時的金納米顆粒圖像; (b) (a)中激發光與STED 光未對準時所得到的熒光珠的共聚焦(綠色)與STED(紅色)圖像的合并; (c)沿圖(b)中所示虛線的信號強度曲線: 共聚焦(綠色)和STED(紅色); (d)激發光與STED 光對準情況下的金納米顆粒圖像; (e) (d)中激發光與STED 光對準時所得到的熒光珠的共聚焦(綠色)與STED(紅色)圖像的合并; (f)沿圖(e)中所示直線和點劃線的信號強度曲線: 共聚焦(綠色)和STED(紅色)Fig. 8. Alignment results of depletion and excitation beams[9]: (a) Merged result of the excitation focus (green) and a poorly aligned depletion focus(red) using gold nanoparticles; (b) merged result of corresponding confocal (green) and STED(red) images of fluorescent beads imaged with the focus shown in (a); (c) line profiles across the dotted line in (b): confocal (green) and STED (red);(d) merged image of the excitation focus (green) and a well aligned depletion focus (red); (e) merged result of corresponding confocal (green) and STED (red) images of fluorescent beads imaged with the focus shown in (d); (f) line profiles across the solid and dashed lines in (e): confocal (green) and STED (red).
圖9(a)右側表示在光束整形裝置不同階段和周期的兩個代表點處激發光束和STED 光束的偏振狀態. 由于分段波片的波長性質, 兩個光束會受到不同的影響. 首先, 兩個線偏振光束由消色差四分之一波片(quarter-wave plate, QWP)變為圓偏振光. 然后, 通過分段波片對STED 光束選擇性地旋轉偏振. 最后, 二分之一波片選擇性地反轉兩個光束的水平偏振分量, 反轉激發光束的圓偏振并將STED 光束轉換成環形光. 對于激發光, 則形成正常聚焦的光斑. 由于組合波片是四個波片拼合而成的, 形成的環形光束不是完全規則的圓形環, 如圖9(b)所示.
3.2.3 簡易的空間光調制器校準
與easy-STED 類似, 2018年G?rlitz 等[11]研究人員提出將激發光與STED 光耦合到光纖中進行重合, 然后利用SLM 對激發光和STED 光分別進行光束整合, 稱為easySLM-STED, 進一步簡化了光束重合的復雜度, 提高了光束重合的穩定性.如圖10 所示, 利用SLM 相位調制只能作用于一個線性偏振的特性, 結合偏振方向正交的激發光與STED 光, 再利用QWP 旋轉偏振的特性, 就可以對重合的激發光與STED 光分別進行獨立的調制,使得只有STED 光被調制為環形光.
盡管能在空間上實現對準, 但是STED 光束具有軌道角動量, 因此, STED 系統的性能通常容易受到熱變化和振動的影響, 穩定性較差, 使用Qplate 可以解決這個問題[12].
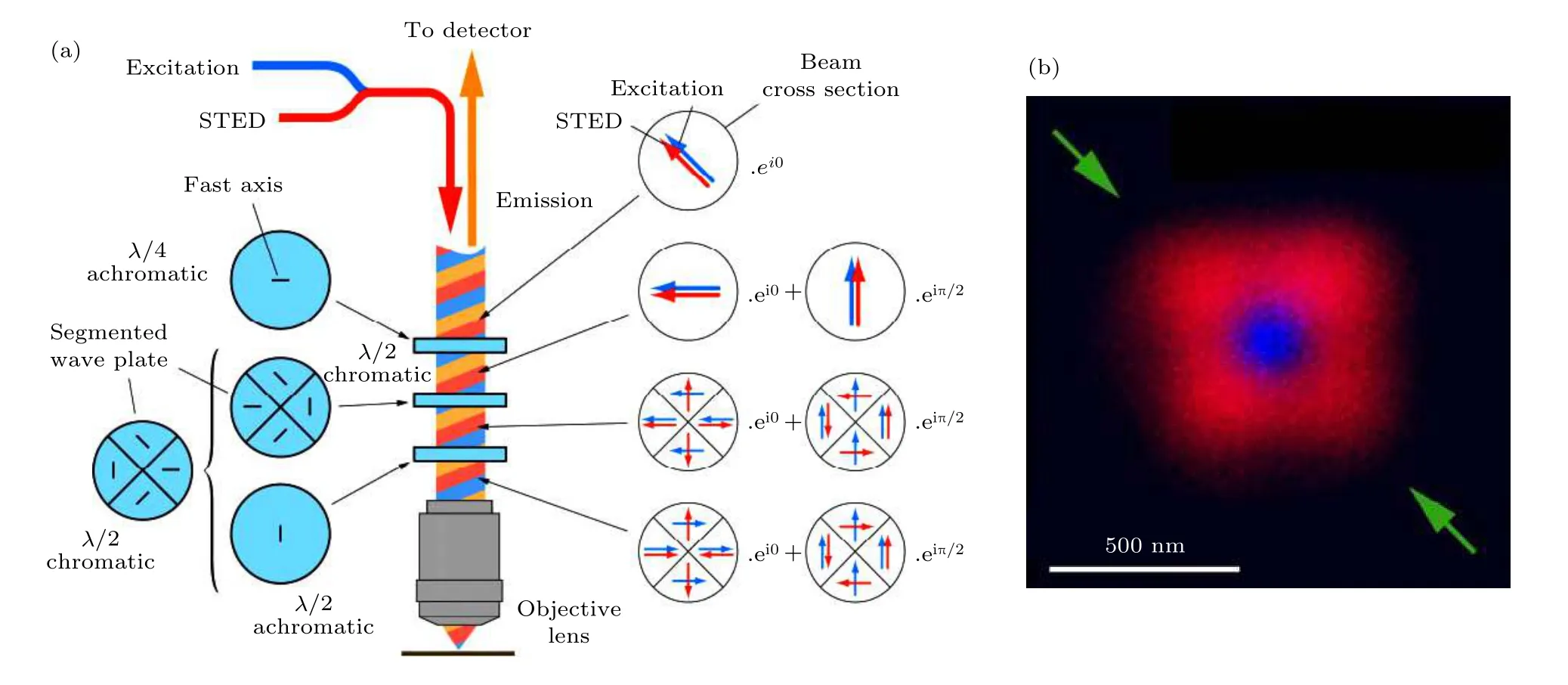
圖9 雙折射光束整形示意圖[10] (a) easy-STED 雙折射光束整形裝置示意圖; (b)光斑重合效果Fig. 9. Schematic of birefringent beam shaping[10]: (a) Schematic of an easy-STED microscope using a birefringent beam shaping device; (b) merged image of the excitation beam and a depletion beam.
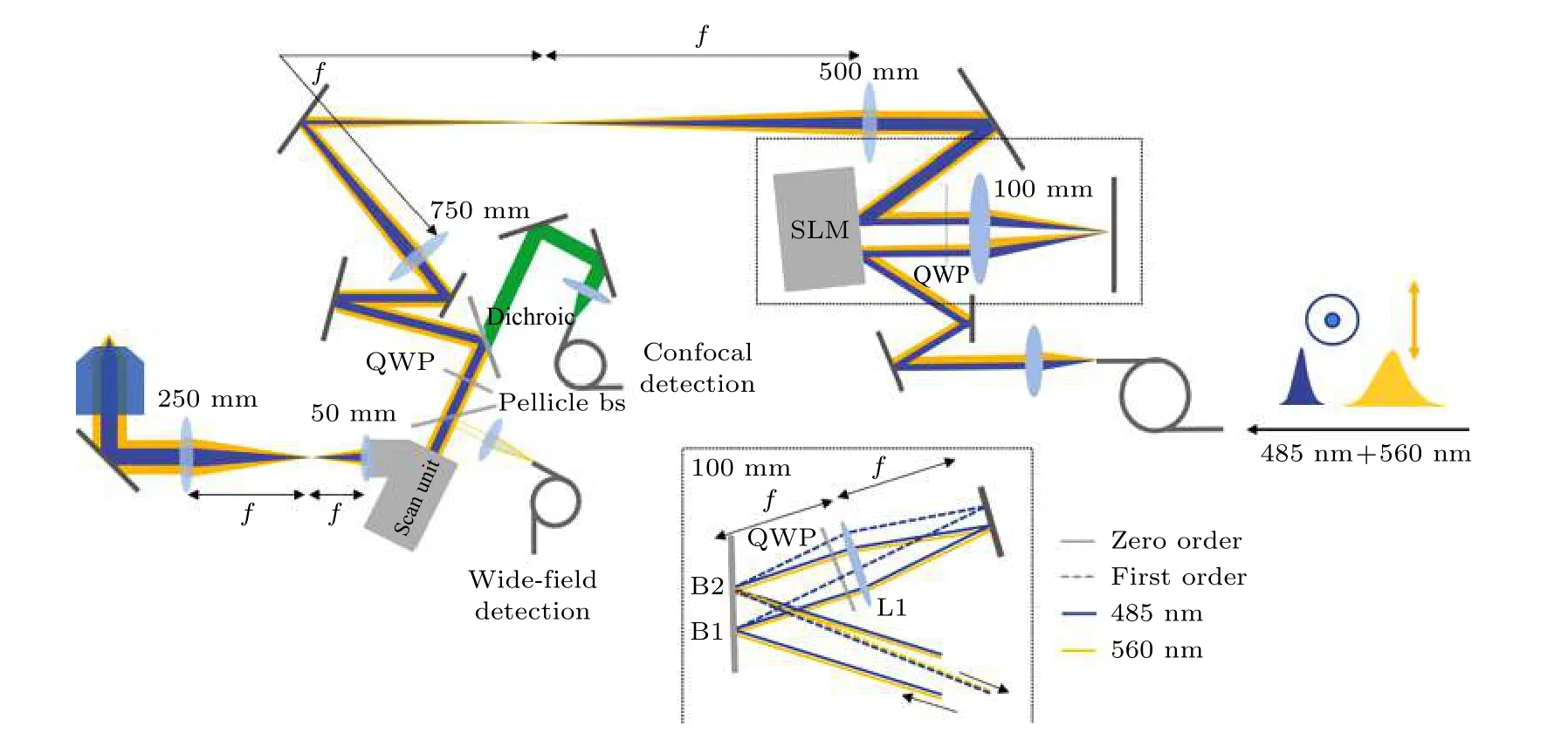
圖10 asySLM-STED 系統示意圖[11]Fig. 10. Schematic diagram of easySLM-STED system[11].
3.3 STED 系統的掃描單元
熒光成像, 包括STED 成像的質量在很大程度上取決于信號的強度, 在一定閾值內熒光信號的強度與激發光強呈正相關, 超過一定閾值后光吸收將趨于飽和并永久性地破壞熒光分子的激發態, 發生光漂白. 光漂白是STED 系統成像質量提高的一個重要的限制條件, 減少光漂白的一個有效途徑是提高掃描速度, 從而減少光斑在樣品上的停留時間. 由于STED 是基于點掃描成像的, 所以掃描速度對于光漂白有著直接的影響. 目前顯微鏡常用的掃描裝置有掃描振鏡和聲光偏轉器. 掃描振鏡主要是利用伺服電機控制鏡片擺動來達到掃描的效果.這種光束掃描不需要移動樣品, 僅靠鏡片的擺動就可以達到每秒上千行的逐行掃描, 共振振鏡掃描更是可以達到每秒上萬行的掃描速度, 振鏡是STED系統使用最廣泛的掃描裝置[13]. 聲光偏轉器是基于聲光效應, 通過控制施加在聲光晶體兩端超聲波的頻率來改變光束角度的一種掃描裝置, 有部分STED 系統使用聲光偏轉器進行掃描[14]. 與機械式偏轉的掃描振鏡相比, 聲光偏轉器在掃描速度上有一定的差距, 但卻具有無振動的優勢, 也有較好的穩定性.
3.3.1 大視場共振掃描STED
提高STED 系統的掃描速度和掃描角度, 對樣品進行大視場快速掃描, 能在有效減少光漂白的同時得到高分辨率的圖像. 目前主要通過快速共振掃描器件來實現大視場快速掃描, 減少曝光時間和光漂白. 但是, 提升掃描速度及掃描視場之后, 還必須具備相應的快速光子計數系統, 否則快速共振掃描得到的光子信息無法被及時捕獲, 也無法提升圖像的采集速率.
加州大學Wu 等[15,16]針對這種限制構建了一個基于高速光子計數圖像采集系統的共振掃描CW-STED 顯微鏡, 具有超快的讀出速率, 優異的計數線性度, 可實現在線時間門控檢測. 利用現場可 編 程 門 陣 列(fieldprogrammable gate array,FPGA)實時記錄每個光子脈沖, 讀出速率最高可達450 MHz, 搭配8 KHz 的掃描振鏡, 與共振掃描時間選通CW-STED 顯微鏡相結合, 可以在較大視場(50 μm × 50 μm)下獲得具有較小光漂白的高分辨率圖像.
3.3.2 并行掃描STED
與提高掃描速度的方法不同, 并行掃描[17,18]STED 通過提高每次掃描的效率, 來增大掃描視場, 減少光漂白. Wagner 等[17]提出了使用多波長全息術[19]來生成激發和STED 光圖案: 設計一個由兩個平面組成的全息圖, 其中一個平面編碼生成激發圖案, 另一個平面編碼生成擦除圖案, 然后將全息圖編程到SLM 上. 通過選擇投影全息圖的位置和兩個圖像平面之間的距離, 可以確保激發光束和STED 光束圖案在一個平面上對齊. 使用這種方法, 可以同時將激發光束和STED 光束分成N個光束對(圖11(a),N= 8), 使視場增加N倍,極大地提高了掃描效率.
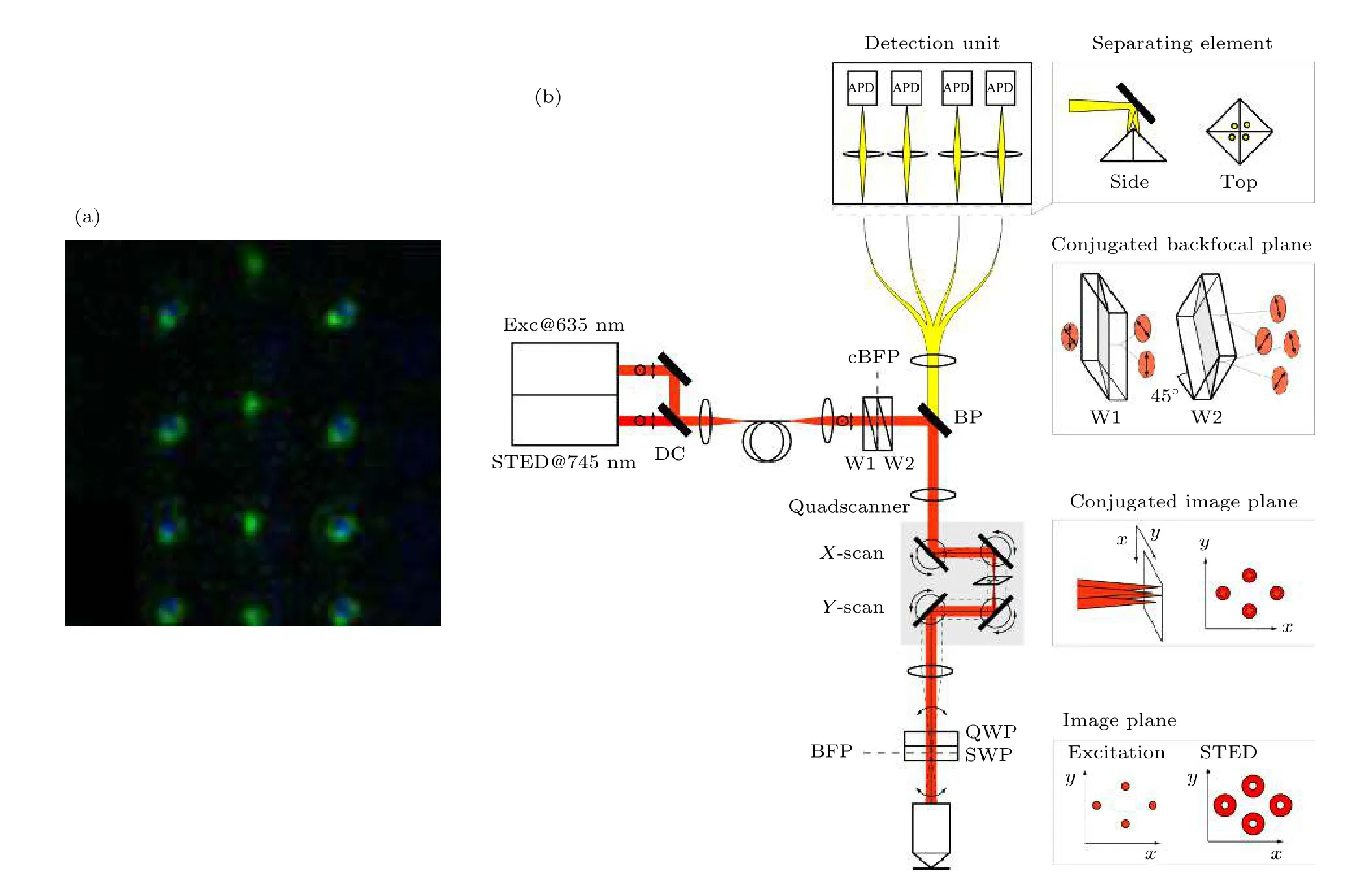
圖11 并行掃描STED 示意圖[17,18] (a)擴展STED 光束對的結果; (b)多點掃描STED 光路示意圖Fig. 11. Schematic diagram of parallel scanning STED[17,18]: (a) Results of extended STED beam pairs; (b) optical path of the multipoint scanning STED.
然而, 這種并行掃描的缺點是, 使用相同的全息圖來產生激發光以及STED 光圖案, 意味著只有一半的功率用于成像, 能量利用率較低.Bingen 等[18]提出了另外一種產生多光束的方法,將非偏振的激發光與STED 光耦合進光纖, 利用渥拉斯頓棱鏡(圖11(b)中的W1 與W2)將光束分為四個偏振的子光束. 經過掃描電鏡后, 使用雙折射裝置(詳見3.2.2)對所有子光束進行處理. 樣品發出的熒光被收集后聚焦到金字塔棱鏡上, 金字塔棱鏡將四個焦點的熒光分開并分別聚焦在四個探測器上. 這種方法可以根據激光能量以及實際需求, 分出更多的子光束來提升掃描速度, 但是這種提高掃描效率的方法也極大地增加了系統的成本和操作的復雜性.
3.4 STED 系統的成像單元
STED 系統的成像單元包括接收信號的探測器以及對信號的處理. 對STED 系統探測器得到的信號進行處理, 可進一步提高成像的空間分辨率. 由于STED 光對所激發熒光的損耗, 使探測器接收到的有效熒光信號變得很弱, 因此必須使用高靈敏度的弱信號探測器, 如光電倍增管(photomultiplier tube, PMT)、雪崩光電二極管(avalanche photo diode, APD)或單光子雪崩光電二極管[20](single-photon avalanche photo diode,SPAD)、 多 像 素 光 子 計 數 器[21](multi-pixel photon counter, MPPC)和混合探測器等. 得益于二次發射倍增系統, 光電倍增管具有較大的探測范圍以及較快的響應速度, 但是其在可見光范圍的量子效率偏低, 所以對于微弱熒光信號的探測能力較差. 雪崩光電二極管基于二極管的雪崩倍增效應,具有極高的量子效率, 但是其動態響應范圍不如光電倍增管. 多像素光子計數器則是在雪崩光電二極管的基礎上, 將APD 以像素的方式集成到1 mm2的基底上, 進一步提升了弱光探測能力. 混合光探測器則是結合了PMT 與APD 的優點, 不僅具有高的量子效率, 較大的動態范圍, 低的背景噪聲和快速的時間響應, 而且還具有較大的探測范圍, 是目前STED 商用系統最常用的探測器. 探測器接收到熒光信號之后, 需要利用數據采集卡(data acquisition card, DAQ)來對熒光信號進行收集和處理.
另外, STED 系統通常還會配置一個并行探測系統, 如CCD 或互補金屬氧化物半導體(complementary metal oxide semiconductor, CMOS)等對光路進行重合和校準.
3.5 STED 成像系統
最常見的STED 成像系統一般為單光子激發、單色STED 系統, 這種系統由一個激發光和一個STED 光組成, 下面將介紹近年來在單色STED系統基礎上發展起來的其他STED 成像系統.
3.5.1 雙光子激發STED 系統
與單光子激發相比, 雙光子激發(two-photon excitation, TPE)具有多個優點: 1)雙光子激發使用近紅外波長的激光作為光源, 對樣品的穿透深度比短波長的光更深; 2)長波長的近紅外光對細胞毒性較低; 3)雙光子只在物鏡的焦點處激發, 因此雙光子顯微不需要共焦針孔, 提高了熒光的檢測效率; 4)雙光子激發只在焦平面上有光漂白, 適合用來觀察厚樣本和活細胞, 或用來進行定點光漂白實驗[22,23].
將TPE 和STED 結合(圖12), 使用1060 nm的脈沖激發光源對熒光團進行雙光子激發, 使用676 nm 的連續光作為STED 光, 充分發揮了TPE和STED 的優勢[24].
Bianchini 等[25]報道了基于單個光源的雙光子STED 成像方案(SW2PE-STED), 該系統利用770 nm 的飛秒激光同時實現了激發與受激輻射.需要注意的是, 雙光子激發光與STED 光的脈沖寬度必須相差大約三個數量級, 并且強度必須相差兩個數量級以上. 因此, 需要通過PBS 實現對單色光源的能量分配, 并對STED 光束的脈沖寬度進行擴展(圖13). 該系統能夠在2PE 成像的基礎上將空間分辨率提升4—5 倍. 目前該系統方案僅對于ATTO647 N 這種常見的熒光染料進行了驗證,其他種類的熒光染料尚未得到驗證.
3.5.2 雙色STED 系統
生物樣品的結構和功能非常豐富, 對多種結構同時成像的需求日益迫切, 通過增加一路激發光與一路STED 光, 可以實現雙色STED 成像系統. 最早的雙色STED 系統利用四個單波長的激光器來實現雙色STED 成像[26], 這種方法雖然直接有效,但是系統復雜, 成本很高.
對于激發波長相近的兩種熒光染料, 可以考慮使用同一個波長的STED 光進行擦除. 2013年,G?ttfert 等針對ATTO594 和KK114 兩種染料,搭建了一套簡易的雙色STED 系統[27]. 分別用595 和640 nm 兩個通道的激發光進行激發, 并使用20 MHz, 脈沖帶寬1.2 ns 的775 nm 脈沖光對兩個通道同時擦除. 由于兩種染料的發射波長分別為620 和670 nm, 因此利用雙色鏡可以很容易地將熒光信號分離到兩個通道進行探測. 這種雙色STED 系統不僅結構簡單, 而且具有較好的共定位效果, 但是在染料類型的選擇上仍受到限制.
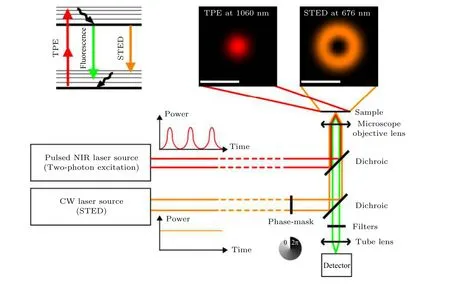
圖12 雙光子STED 系統示意圖[24]Fig. 12. Schematic diagram of two-photon STED system[24].
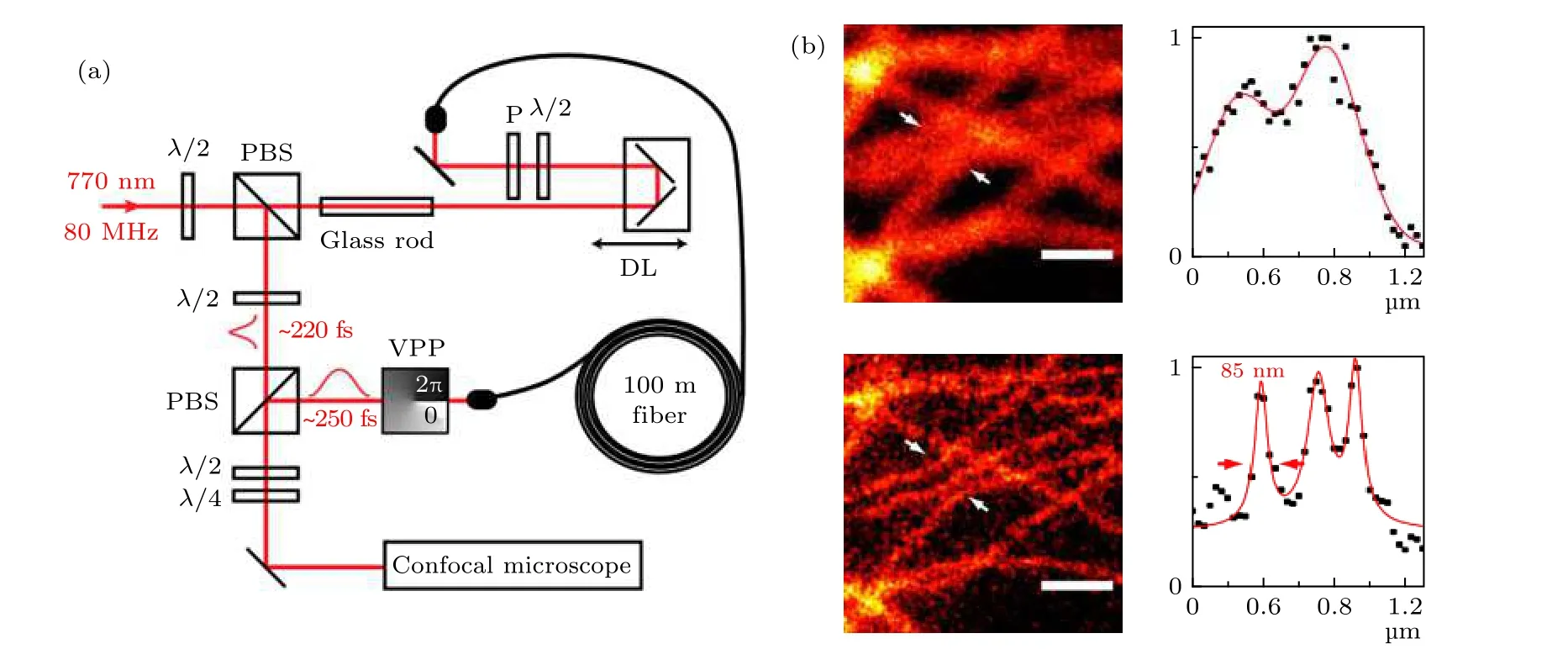
圖13 雙光子STED 系統及成像結果[25] (a) SW2PE-STED 系統示意圖; (b) 2PE 與2PE-STED 成像對比Fig. 13. Schematic of two-photon STED and imaging results[25]: (a) Schematic of SW2PE-STED system; (b) 2PE and 2PE-STED imaging.
相比于在系統中采用四個或者三個激光器來實現雙色STED 成像, 通過選取同一激發波長, 不同發射波長, 且可用同一個STED 光進行擦除的兩種染料如黃色熒光蛋白(yellow fluorescent protein, YFP)和綠色熒光蛋白(green fluorescent protein, GFP), 利用熒光發射波長的不同, 使用雙色鏡把兩路熒光信號區分開, 從而達到只用一個激發光和一個STED 光, 實現雙色成像的目的[28].T?nnesen 等[28]在2011年提出的這種雙色STED成像方法(圖14(a))利用了兩種具有不同發射波長的染料(圖14(b)), 該方法大大簡化了雙色STED 系統的復雜性, 實現了橫向分辨率為80 nm 的雙色活體突觸成像. 但是, 這種方法只對特殊的染料有作用, 所以其應用受到很大限制.
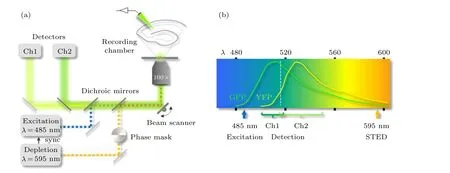
圖14 雙光源雙色STED 系統示意圖[28] (a)雙光源雙色STED 系統示意圖; (b) YFP 與GFP 的熒光發射光譜Fig. 14. Schematic diagram of two laser source dual-color STED system[28]: (a) Dual-color STED system with two laser sources;(b) emission spectra of GFP and YFP.
3.5.3 多壽命多色STED 系統
Bückers 等[29]于2011年提出了一種四光源多壽命多色STED 成像方法. 與雙光源雙色STED系統類似, 這種方法使用具有幾乎相同的吸收和發射光譜但熒光壽命不同的兩種熒光染料, 用共同的激發光和STED 光來對兩種熒光染料進行STED成像, 并通過它們熒光壽命的不同來進行信號的分離. 第三個通道則用另外的激發光與STED 光進行成像, 通過熒光發射波長來進行區分. 由于第一、第二通道不需要第二個STED 光, 壽命分離對漂移不敏感, 因此比較適合共定位分析. 這種基于壽命分離的方法雖然使多色系統得到簡化, 但卻同樣在熒光染料上受到限制.
3.5.4 三維STED 成像
隨著生物醫學的不斷發展, 對樣品的三維觀察越發重要. 目前實現3D-STED 超分辨成像的方法主要有波前非相干調節、4π 法以及結構光照明法.
通過圖15 所示的0/π(左下PM1)和0—2 π螺旋相位板(左下PM2)對兩束光進行空間調制時, 可以產生橫向及縱向的中空環形光束. 將所產生的兩束非相干光重合, 可以得到三維中空的STED 光, 在橫向及縱向壓縮激發光斑的有效點擴散函數(PSF). 利用三維光斑在樣品上進行三維掃描, 就可以通過后期重構得到樣品的三維STED圖像[30]. 這種實現3D-STED 成像的方法比較簡單, 但缺點是橫向與軸向分辨率通常相差50 nm以上, 3D 成像質量較差.
除了以上對兩束STED 光的波前進行調制外,第二種方法是基于4π 顯微鏡實現三維超分辨成像. 4π 顯微鏡是通過增加物鏡的接收角(等效于增加物鏡NA)來使空間立體角達到4π, 從而大幅度減小PSF, 提高軸向分辨率[31]. 利用4π 方法實現3D-STED 超分辨成像, 需要在樣品兩端放置兩個相同的物鏡, 在樣品兩端同時照明并接收熒光信號, 系統中的兩束STED 光只有一束通過相位板調制成環形光. 通過調節兩束STED 光以相同或相差180°的偏振方向分別從兩個物鏡入射, 在樣品上發生相長干涉(橫向環形斑)或相消干涉(縱向環形斑), 兩種光斑通過光強非相干疊加就可以產生三維的空心球形光斑, 從而實現3D-STED 成像(圖16)[32]. 利用這種方法, 可以成倍地提升光學系統的軸向分辨率, 將軸向分辨率從500 nm 提升到約40 nm, 在三維成像上有明顯的優勢. 但是,4π 方法需要用到兩個物鏡, 而且對光路的對準要求非常嚴苛, 使其應用受到了很大的限制. 2016年北京大學Yang 等[33]通過在樣品后方放置一面介質反射鏡來使入射光與反射光在樣品焦面發生干涉, 能夠在一定程度上降低系統的復雜性.
Gustafsson 等[34,35]和Xue 等[36]提出使用結構光照明可以實現三維成像. 具體方法是, 利用線性相位光柵產生–1, 0, +1 三級衍射光, 衍射光經過物鏡聚焦后在樣品的焦平面處發生干涉, 并產生具有橫向和軸向結構的強度分布(圖17(a)).

圖15 基于非相干波前調制的3D-STED 成像系統示意圖[30]. 插圖: 用于實現橫向超分辨(HR)或3D 超分辨率(3D)的相位板及對應的STED PSFFig. 15. Schematic diagram of 3D-STED system with non-coherent wavefront modulation[30]. Inset: combinations of phase plates and resulting STED PSFs used to achieve either ultimate lateral resolution (HR) or 3D superresolution.
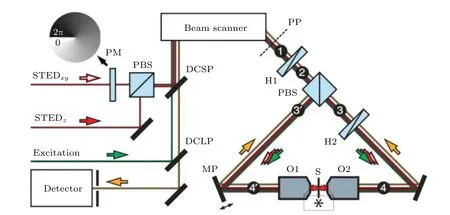
圖16 利用4π 法實現3D-STED 成像的系統示意圖[32]Fig. 16. Schematic diagram of 4π3D-STED system[32].
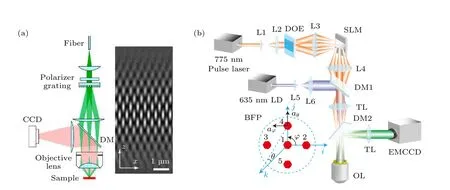
圖17 基于結構光照明的系統圖[35,36] (a)結構光照明系統圖及空間強度分布; (b)結構光照明3D-STED 系統示意圖Fig. 17. Structured illumination system[35,36]: (a) Simplified diagram of the structured illumination apparatus and spatial intensity distribution; (b) structured illumination 3D-STED system.
利用這種結構光照明的原理, Xue 和So[36]進一步利用衍射光學元件(diffractive optical elements, DOE)將衍射光擴展到五束(圖17(b)),搭建了基于結構光的3D-STED 系統. 在DOE 的傅里葉面, 每個光束的相位由SLM 調制, 可以使圖像平面中的干涉圖案發生位移. 改變中心光束和周邊光束之間的相對強度可以改變干涉圖案的對比度. 利用五束衍射光干涉來產生3D 網格, 能夠獲得對稱的徑向超分辨成像. 此外, Xue 等[37]在2011年也提出了對徑向偏振光或切向偏振光進行相位調制, 實現相干與非相干疊加的方法來產生三維空心光斑.
4 低功率STED 超分辨成像技術
對STED 成像系統所做的各種改進, 需要實現的一個非常重要的目標是對活體生物樣品成像.在STED 系統的實際應用中, 主要受限于STED光帶來的光損傷. STED 系統的分辨率與STED光的強度成正比, 理論上通過提高STED 光的功率可以使熒光光斑的面積無限小. 然而當STED光的強度增強時, 一方面會加劇熒光染料的光漂白, 另一方面也會對樣品產生光損傷. 所以, STED系統目前一個重要的發展方向, 就是在保持分辨率優勢的前提下, 降低STED 光的能量, 減小對樣品的光損傷. 另一方面, STED 光學系統一般都存在像差, 而厚的生物樣品通常會產生更復雜的像差[38],從而使STED 光的波前發生畸變, 降低擦除效率.在光路中使用一個或多個自適應光學元件如SLM,可以有效補償系統和樣品引起的像差, 在相同的STED 光功率下提高成像質量和系統的空間分辨率[39,40].
4.1時間門控STED 技術
熒光分子被激光激發, 吸收能量躍遷到激發態, 再從激發態自發輻射熒光回到基態, 這個過程稱為自發輻射. 在自發輻射熒光的過程中, 熒光強度降低到初始強度的1/e時所需要的時間, 稱為熒光壽命, 常用tfl表示. 也可以理解為熒光壽命是熒光分子被激發后回到基態之前在激發態平均停留的時間. 前文提到, 熒光衰減率Kfl= 1/tfl, 相反地,tfl也可以由Kfl表示:
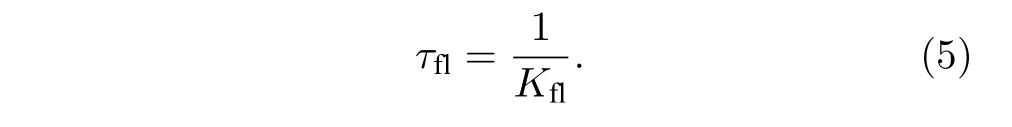
由于STED 系統中的STED 光能夠使處于激發態的分子發生受激輻射躍遷回到基態, 相當于縮短了受到STED 光照射的熒光分子的熒光壽命, 即

式中KSTED為受激輻射速率.
(6)式表明, 由于受激輻射的存在, 使得熒光分子的熒光壽命變短, 這為利用壽命信息提高系統分辨率提供了可能.
STED 成像時, 激發光照射的區域產生了熒光壽命較長的光子, 而激發光與STED 光重疊的區域由于發生了受激輻射效應, 所以該區域所發射熒光的壽命會明顯減少.時間門控STED 技術[41,42]利用不同區域熒光壽命不同的特性, 在激發光照射到樣品一定時間Tg后才開始收集光子, 過濾掉短壽命的光子, 只接收來自激發中心的長壽命光子,能夠有效提升STED 系統的空間分辨率(圖18(a)).利用時間門控來進行篩選, 需要將光源與探測單元進行時間同步調節, 并且搭配可以快速開啟和關閉的光子探測器(如SPAD).
理論上通過延遲門控SPAD 的開啟時間能夠持續提升系統的空間分辨率. 然而, 由于STED 系統的STED 光通常無法實現中心的絕對零強度,所以即使是處于激發光中心的光子也有可能受到STED 光的影響而縮短壽命, 延遲門控SPAD 的開啟時間在濾除受激輻射區域光子的同時也會濾除一部分自發輻射區域的光子, 使接收到的長壽命的光子數減少. 因此, 延遲門控SPAD 開啟時間在提升分辨率的同時也會使系統的信噪比(signalnoise ratio, SNR)降低, 需要根據系統的實際情況來調節門控的開啟時間. 此外, 可通過多圖像反卷積來減少時間門控STED 系統對SNR 的影響[43].Diaspro 等[41]選擇在激發光到達樣品2 ns 后開啟時間門,時間門長度為7 ns, 可以排除反斯托克斯光, 最終在50 mW 的STED 光功率下實現75 nm的分辨率, 而Giuseppe 等[42]則在250 mW 的功率下實現35 nm 的分辨率.
4.2 離線門控STED 技術
使用時間門控來控制探測器接收信號的時間,雖然能夠在一定程度上提升STED 成像的分辨率,然而對于不同的系統和實驗對象, 在分辨率和峰值信 噪 比(peak signal-to-noise ratios, PSNR)上,Tg的選擇則沒有一個明確的標準.
浙江大學Wang 等[44]提出了離線時間選通來實現時間門控STED 的方法, 將STED 系統的分辨 率 從75 nm 提 高 到38 nm, 同時 降 低 了 所 需STED 光的功率(圖19). 這種方法采用時間相關單光子計數(time-correlated single-photon counting,TCSPC)技術, 記錄所有激發脈沖和相應的熒光光子之間的時間間隔并統計為直方圖. 這種離線時間門控方法允許實驗人員在后期自由選擇合適的時間門, 以保證獲得分辨率與PSNR 之間最佳的平衡.


圖19 離線時間門控STED[44] (a)共聚焦、STED 與off-line gated-STED 分辨率結果; (b) Tg、分辨率與PSNR 關系曲線Fig. 19. Off-line gated-STED[44]: (a) Spatial resolutions of confocal, STED and off-line gated-STED; (b)the relationship between Tg,resolution and PSNR.
4.3 STED-FLIM 相圖分析技術
時間門控STED 方法通過選擇性接受長壽命的光子來排除STED 光區域的光子, 雖然能一定程度提升系統的空間分辨率, 但同時也會排除掉許多激發光中心區域的光子, 丟失了部分信息. 將所有光子的壽命信息記錄下來, 采用相圖分析法進行分離, 能在更大程度上利用所采集到的光子信息.2018年Wang 等[45]在STED 系統上加入了脈沖同步單元和TCSPC 數據采集卡, 將STED 系統與熒光壽命成像(fluorescence lifetime imaging,FLIM)技術相結合, 建立了STED-FLIM 系統.對STED-FLIM 系統所采集的圖像進行相圖(phasor plot)分析, 實現了在低功率下的STED超分辨成像(圖20), 利用這種STED-FLIM 的相位圖分析法, 在不增加STED 光能量的前提下成功地將不同壽命的光子進行分離, 分辨率從150 nm提高到80 nm.
4.4 pSTED-SPLIT 技術
在不提高STED 光功率的前提下, 光子數分離是基于相量分析法[46]的一種有效提高STED 系統空間分辨率的方法. 對于相位圖中壽命變化與有效熒光光子之間的關系, 目前還沒有統一的標準.Tortarolo 等[47]提出了區域分割法(圖21(a))與pSTED-SPLIT 方法(圖21(b)), 提高了系統的空間分辨率, 同時降低了光漂白.

圖20 STED-FLIM 成像及相圖分析結果[45] (a)彩色相位圖; (b)熒光珠的共聚焦圖像; (c)熒光珠的STED 圖像(10 mW);(d)時間門STED 圖像; (e)相圖分析后的圖像Fig. 20. STED-FLIM and Phasor-plot analysis[45]: (a) Phasor color map of the STED-FLIM image; (b) Confocal, (c) STED·(10 mW), (d) time gate STED and (e) Phasor-plot images of fluorescent beads.

圖21 區域分割法與pSTED-SPLIT 方法所得到的熒光珠的成像結果[47] (a)區域分割法示意圖; (b) pSTED-SPLIT 方法示意圖;(c)從左到右依次為熒光珠的共聚焦、常規STED、區域分割法STED 和pSTED-SPLIT 的成像結果Fig. 21. Imaging results of fluorescent beads using segmentation and pSTED-SPLIT methods[47]: (a) Schematic diagram of segmentation method; (b) schematic diagram of pSTED-SPLIT method; (c) from left to right: Confocal, conventional STED, segmentation STED, and pSTED-SPLIT imaging results of fluorescence beads.
4.5 利用量子點作為熒光探針實現STED超分辨成像
在STED 成像中, 使用量子點作為探針可以提高探針的抗漂白和光穩定性. 2017年北京大學Liu 等[48]首次利用上轉換納米粒子(upconversion nanoparticle, UCNP)實現了STED 超分辨成像,通過在UCNP 上摻雜高濃度的銩離子(Tm3+), 用980 nm 波長激發UCNP 可以很容易地在其中間亞穩態3H4能級上建立粒子數反轉, 使用808 nm激光照射, 匹配3H4→3H6躍遷的上轉換帶, 可以觸發放大的受激輻射以釋放3H4中間能級, 從而可以抑制上轉換路徑(圖22). 利用上轉換發光, 用980 nm 激光激發熒光, 808 nm 激光作為STED光可以有效提高受激輻射效率, 降低STED 光強度, 減少對生物樣品的光損傷. 利用這種方法,可以將STED 光飽和強度降低兩個數量級(0.19 mW/cm2), 實現橫向28 nm 的分辨率(圖22(b)).幾乎同時, 華南師范大學Zhan 等[49]利用UCNP在生物樣品上實現了STED 超分辨成像.

圖22 上轉換示意圖及利用上轉換納米顆粒的成像結果[48] (a)上轉換能級關系圖; (b)上轉換納米顆粒成像結果Fig. 22. Schematic diagram of upconversion and imaging results[48]: (a) Diagram of energy levels of upconversion nanoparticles;(b) imaging results of UCNPs.
除了UCNP 外, 還有很多其他量子點可以作為STED 探針. 2017年浙江大學Li 等[50]首次利用AIE 納米顆粒實現了STED 超分辨成像;2018年Ye 等[51]首次利用鈣鈦礦量子點作為STED探針實現了20.6 nm 的超高分辨率; 2019年Li 等[52]利用對生物體無害的碳點作為STED 探針, 實現了細胞內超分辨成像; 2020年, Liang 等[53]利用靶向性較好的有機硅量子點作為探針, 實現了活體STED 超分辨成像.
4.6 熒光發射差分超分辨成像
2013年浙江大學Kuang 等[54]提出了一種與STED 思想類似的可在低功率下實現超分辨成像的熒光發射差分(fluorescence emission difference,FED)法. 即利用同一波長的兩束激發光對樣品激發, 其中一束為常規的高斯光斑, 另一束為經過相位板調制波前的環形光斑. 高斯激發光斑(圖23(a))在探測器上的最終PSFc為高斯激發光斑與小孔PSF 卷積的結果(圖23(c)), 此時得到的是共聚焦圖像; 環形激發光斑(圖23(b))在探測器上的最終PSFn為環形激發光斑與小孔PSF 卷積的結果(圖23(d)), 此時得到的是負共聚焦圖像.
用共聚焦圖像減去負共聚焦圖像就可以得到超分辨的FED 圖像, 最終的PFSFED為
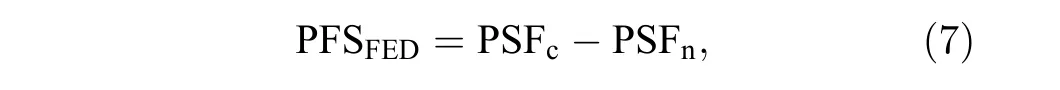
成像結果為
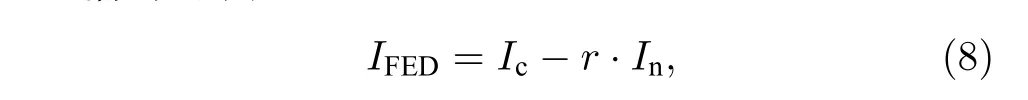
式中Ic,In和IFED分別為共聚焦、負共聚焦和FED 圖像的歸一化強度分布, 而r是減法因子.
FED 方法可以避開STED 需要高強度STED 光的劣勢, 僅在激發光功率水平, 就能夠實現對相距105 nm 的熒光珠的超分辨成像. 在熒光飽和的情況下, 通過調整減法因子r, 可以獲得高質量的超分辨圖像.
4.7 數字增強型STED 超分辨成像
受FED 超分辨成像方法的啟發, 最近我們課題組, 開發了一種新型STED 圖像處理方法, 即數字增強型STED(DE-STED), 該方法可大大降低STED 光所需功率, 使活細胞長時間超分辨成像成為可能[55]. 圖24 為DE-STED 的基本原理, 用共聚焦強度圖減去STED 強度圖, 即可得到STED光由于受激輻射效應擦除掉的光子強度圖(圖24(c)中的Donut 圖), 由于受激輻射效率在低STED 光功率情況下是很低的, 用STED 強度圖減去N倍的Donut 圖, 即可實現重疊區域的受激輻射效率100%(理想STED 成像是STED 光與激發光重疊區域的受激輻射效率為100%), 在傳統的STED超分辨成像中需要非常高的STED 光才可以實現100%的受激輻射效率. 因此, DE-STED 可以在較低的STED 光功率下實現非常高的分辨率.

圖23 FED 成像原理[53]Fig. 23. Illustration of FED theory[53].
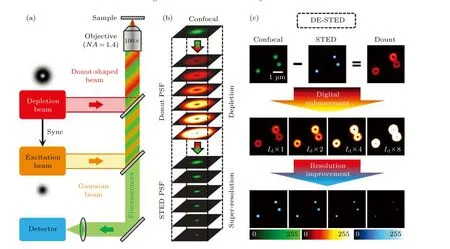
圖24 DE-STED 原理圖[55]Fig. 24. Schematic principle of DE-STED[55].
4.8 基于自適應光學的STED 超分辨成像
在進行深層生物樣品STED 超分辨成像時,常會由于樣品內部的折射率分布不均勻引入嚴重的像差, 導致STED 成像效果較差, 即便是很強的STED 光都很難實現超分辨成像. 最有效的解決辦法是引入自適應光像差校正技術, 常用的像差校正算法為澤尼克多項式[39]. 2017年Yan 等[38]首次將 相 干 自 適 應 光 學(coherent optical adaptive techniques, COAT)技術引入STED, 極大地提高了STED 的成像深度以及樣品成像的空間分辨率.2019年, Wang 等[40]發展了基于遺傳算法的STED(GA-STED)成像技術, 提高了成像速度和精度,實現了快速實時像差校正的STED 成像. 引入自適應光學技術后和之前相比, 在保持相同分辨率的情況下, 有效地降低了STED 光能量.
5 STED 系統與其他技術的組合
將STED 與其他成像系統結合, 可以提高或者擴展系統的成像能力.
5.1 STED 與FCS 的結合
熒 光 相 關 光 譜 (fluorescence correlation spectroscopy, FCS)技術是一種能夠通過檢測熒光強度的變化來獲取溶液的濃度、粒子擴散系數等信息的單分子水平檢測技術, 對于探究活細胞內的生物過程具有重要的意義[56?58]. Lanzanò等[58]最早于2005年提出將STED 與FCS 相結合. 2011年Gould 等[59]為了在宏觀分子尺度上對細胞膜的結構和功能進行成像和光譜分析, 將全內反射熒光(total internal reflection fluorescence, TIRF)顯微與STED 結合進行熒光光譜分析圖25. 一方面,由于TIRF 可以減小測量體積的軸向范圍, 另一方面, STED 又能提升系統的成像能力, 所以將TRIF與STED 結合可以克服STED 系統受到離焦信號影響及全內發射顯微系統分辨力低的缺點. TIRFSTED-FCS 系統的關鍵是要調節激發光與STED光的偏振態, 確保激發光為切向偏振態, STED 光為圓偏振態, 以獲得激發焦點的偏振和STED 焦點之間的最佳匹配[60].

圖25 TIRF-STED-FCS 系統示意圖[59]Fig. 25. Schematic of TIRF-STED-FCS system[59].
2014年Honigmann 等[61]把掃描STED 技術與FCS 相 結 合(scanning STED-FCS, sSTEDFCS), 能夠利用STED 技術提供的超高空間分辨率和FCS 技術帶來的快速時間分辨對細胞內分子的納米級活動進行檢測(圖26), 對于解決真核質膜中脂質與蛋白質之間的相互作用具有重要意義.

圖26 脂膜上sSTED-FCS 的成像結果[61]Fig. 26. sSTED-FCS results of the lipid membrane[61].
5.2 STED 與細胞膨脹技術的結合
膨脹顯微[62](expansion microscopy, ExM)通過在樣品內直接合成可溶脹的聚電解質凝膠網絡, 然后在水中透析樣品, 可以使樣品發生各向同性的膨脹, 相當于物理上將樣品結構進行擴大(約4.5 倍), 從而可以用普通顯微鏡觀察到小于衍射極限的結構. 原則上膨脹顯微技術可以和現有的超分辨成像技術進行結合, 然而由于成像體積的增大要求深度的聚焦, 且單分子定位顯微等技術需要的特殊緩沖液可能會干擾凝膠的擴增, 而STED 基于共聚焦原理, 對樣品的深度成像相對簡單, 而且無需任何特殊緩沖液, 所以將ExM 與STED 相結合是比較合理的方案. 將ExM 與STED 相結合形成ExSTED, 在樣品膨脹四倍后進行STED 成像, 能夠實現2 D 成像的有效空間分辨率小于10 nm,3D 成像的有效空間分辨率小于50—70 nm[63].
5.3 STED 與掃描離子電導顯微鏡的結合
掃描離子電導顯微鏡(scanning ion-conductance microscope, SICM)是掃描電鏡中少數可以對活細胞進行成像的顯微鏡, 通過對樣品表面電解質的局部離子電流進行采樣, 可以獲得樣品的表面輪廓[64]. 早在2002年就已實現了將SICM 和Confocal的結合[65], 因此, 理論上將SICM 與STED 結合是可行的. Hagemann 等[66]對同一樣品進行了SICM 與STED 成像, 兩種成像結果將微管蛋白網絡的變化與細胞形狀和細胞形貌的變化聯系起來,對于研究細胞膜粗糙度、細胞形狀和高度與細胞肌動蛋白結構之間的聯系有重要意義.
5.4 STED 與PALM/STROM 的結合
MINFLUX 方法是2018年提出的一種結合了光束波前調制與單分子定位[67,68]的新的超分辨成像技術, 實現了約1.5 nm 的單分子定位精度[69,70].具體來說, MINFLUX 技術通過相位掩模版對激光波前進行調制, 使光束在物鏡處產生環形激發光.與STED 技術不同的是, 該環形光束是用來激發而不是抑制熒光的產生. 然后, 與單分子定位顯微技術, 如光激活定位顯微 (photo-activated localization microscopy, PALM)或隨機光學重構顯微(stochastic optical reconstruction microscopy,STROM)技術類似, 通過控制隨機地開啟或關閉單個分子, 當目標分子位于光斑的圓環上時, 分子將發射熒光; 當目標分子位于光斑的圓環中心即暗點時則不會發射熒光. 通過探測目標分子發出的光子, 控制光束偏轉器使目標分子始終位于環形光的中心. 利用這種方法, 就可以精確地定位出光子的位置. MINFLUX 顯微方法與STED 相比, 避免了光學元器件對于光斑的影響, 通過光子狀態來實現超分辨成像. 與PALM/STROM 方法相比, 分子定位不再依賴于分子自身的熒光光子, 而是利用環形激發光束提供大量的光子來實現定位. 這樣一來, 可以提高對光子的利用率, 能夠對分子進行快速追蹤, 同時也提高了定位精度.
此外, STED 與其他技術如X 射線掃描衍射[71]、原 子 力 顯 微 鏡[72,73](atomic force microscope,AFM)等相結合, 可以提升成像性能, 對于探究生物樣品內不同結構間的聯系具有重要的意義.
6 STED 在生物醫學中的應用
STED 技術發展的早期多用于對納米熒光珠、熒光標記的生物樣品等進行成像. 但是隨著STED 技術的不斷發展, 實現超分辨成像所需的光功率大大降低, 使得STED 也能實現對活體生物樣品如小鼠大腦組織和細胞[74,75]、樹突棘細胞[76]等進行超分辨成像, 從而在神經生物學等領域有了廣泛的應用. 另外, STED 也與FCS 技術結合實現了對活細胞內分子運動的研究, 為STED 技術探究細胞動力學提供了可能[61].
7 總結與討論
STED 是近年來最有發展潛力的超分辨成像方法之一, 在分辨率及成像速率上有很大的優勢.然而, STED 技術仍然存在許多限制, 如系統比較復雜, 特別對于雙色或多色STED 系統而言, 系統價格昂貴也限制了其應用; 另一方面, STED 系統的STED 光功率通常會較高, 會造成熒光探針的光漂白和光淬滅, 對于生物樣品也會產生光損傷.這些因素都限制了STED 技術在生物醫學領域的推廣和應用. 針對這些問題, 本文介紹了通過提高掃描成像速度來降低STED 光能量, 利用量子點作為探針來降低STED 光功率所造成的光漂白與光損傷. 還介紹了可以將STED 與其他顯微技術相結合, 從而在一個系統中利用多種技術的優勢,提高系統的成像性能. 此外, 還介紹了雙色及多色STED、三維STED 成像的發展.
目前STED 最主要的問題依然是STED 光功率過高. 因此, 未來STED 技術發展的一個重要方向是在保證STED 成像速度和空間分辨率優勢的前提下, 進一步降低STED 光的功率, 實現低光照功率STED 超分辨成像; 同時, 發展低毒性甚至無毒性、靶向性好和光穩定性強的熒光探針. 此外,光毒性與成像深度和光波長都有著密切關系, 因此未來應傾向于用紅外光及其相應的探針而非可見光來進行活細胞成像.
總的來說, STED 技術發展非常迅速, 前面所提到的一些問題都在逐漸被解決, STED 超分辨成像未來有著巨大的發展潛力與空間.

