依帕司他聯合甲鈷胺治療糖尿病周圍神經病變的療效
李潔超,胡亞芬,張赟鋒,薛長春
(首都醫科大學大興教學醫院內分泌科,北京 102600)
糖尿病是多病因引起的胰島素絕對或相對不足所致的糖、脂肪、蛋白質等代謝異常的慢性疾病[1],糖尿病具有遺傳性[2]。糖尿病周圍神經病變(diabetic peripheral neuropathy,DPN)是常見的糖尿病并發癥,2型糖尿病患者DPN的發生率高達30%,與糖尿病病程呈正相關[3]。目前,DPN的病因尚不清楚,普遍認為與神經營養因子缺乏、氧化應激等對機體的影響有關[4]。流行病學資料顯示,DPN是糖尿病致殘的最主要原因[5]。現階段,改善循環狀態、營養神經等是臨床常采用的DPN治療方法,以維生素B12為輔基的甲鈷胺屬于營養神經藥物,臨床應用廣泛,主要用于治療神經痛和神經炎。單純甲鈷胺治療可在一定程度上改善DPN患者的臨床癥狀,但治療效果欠佳。糖尿病患者異常代謝導致體內山梨醇的異常蓄積,進而引發外周神經支配區域的感覺運動障礙,而依帕司他是醛糖還原酶抑制藥物,可減少體內山梨醇的蓄積,從而緩解DPN患者的癥狀。依帕司他聯合甲鈷胺能改善DPN患者周圍神經病變癥狀,促進周圍神經傳導速度加快和氧化應激水平降低,且不引起嚴重不良反應。本研究主要探討依帕司他聯合甲鈷胺治療DPN的療效,以尋找治療DPN的有效方法,改善DPN患者的預后,促進患者早日康復。
1 資料與方法
1.1一般資料 選取2011年7月1日至2012年6月30日在首都醫科大學大興教學醫院內分泌科就診的DPN患者103例為研究對象,納入標準:①根據2009年美國糖尿病學會診斷標準[6]診斷為DPN;②空腹血糖<7.8 mmol/L,餐后2 h血糖<10 mmol/L者;③無其他內分泌腺疾病者。排除標準:①有神經肌肉疾病史;②有嚴重心臟疾病;③其他嚴重系統性疾病;④糖耐量異常,但未達到診斷標準者;⑤血糖、血脂經治療無法改善者。上述患者依據隨機數字法分為試驗組(n=57)和對照組(n=46)。兩組患者性別、年齡、體質指數等一般資料比較差異無統計學意義(P>0.05),見表1。所有患者均簽署知情同意書。
1.2診斷標準 DPN診斷標準:①四肢運動、感覺神經功能障礙,表現為感覺敏感、感覺減退、疼痛等;②肌電圖檢測顯示腓總神經、正中神經的運動神經傳導速度(motor nerve conduction velocity,MNCV) 、感覺神經傳導速度(sensory nerve conduction velocity,SNCV)均減慢;③排除其他可能引發周圍神經病變的疾病。
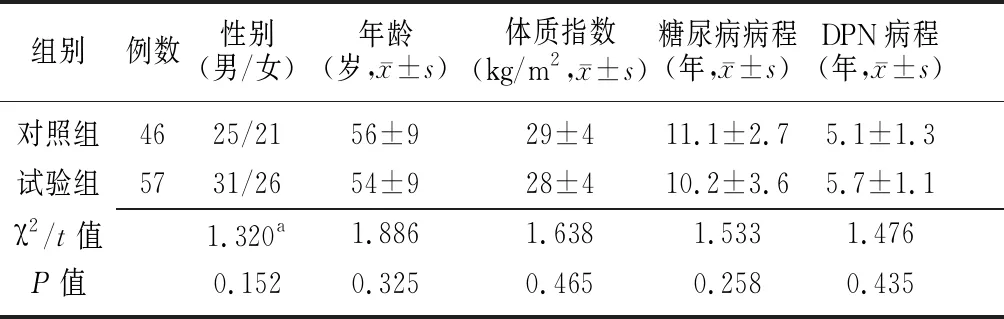
表1 兩組DPN患者一般資料比較
DPN:糖尿病周圍神經病變;對照組:單純甲鈷胺治療;試驗組:依帕司他聯合甲鈷胺治療;a為χ2值,余為t值
1.3方法 所有研究對象經治療血糖、血脂水平等基本達標。對照組口服甲鈷胺(日本偉才公司生產,批號:20070137)治療,每次500 μg,每日1次。試驗組采用甲鈷胺聯合依帕司他(揚子江藥業集團南京海陵藥業有限公司,批號:H20040840)口服治療,每次50 mg,每日3次。兩組患者均治療4周。
1.4觀察指標 ①比較兩組患者治療前和治療4周后的MNCV和SNCV,由專業技師運用丹麥維迪肌電圖儀進行測定[7]。②依據患者的肌電圖測定結果進行療效判定。與治療前相比,感覺敏感、感覺減退等臨床癥狀明顯改善者為顯效,輕微改善者為有效,無改善者為無效,加重者為惡化[8]。總有效率=(顯效例數+有效例數)/總例數×100%。
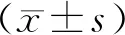
2 結 果
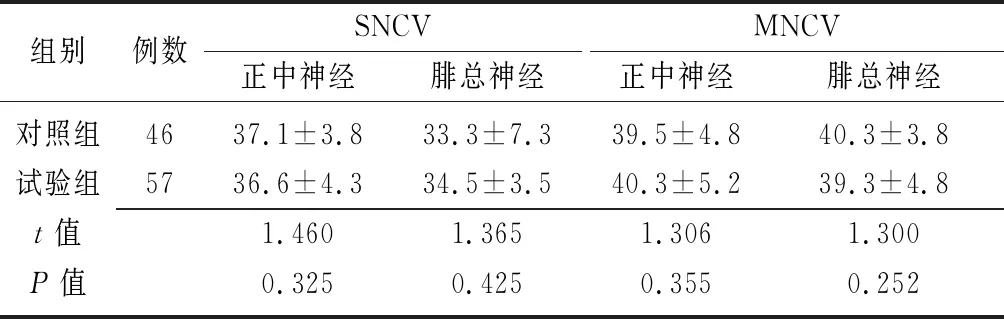
2.1兩組治療前正中神經和腓總神經SNCV和MNCV比較 治療前,兩組正中神經和腓總神經SNCV和MNCV比較差異無統計學意義(P>0.05),見表2。
2.2兩組治療后正中神經和腓總神經SNCV及MNCV比較 治療4周后,試驗組正中神經及腓總神經SNCV和MNCV均高于對照組(P<0.01)。見表3。
2.3兩組臨床療效比較 治療4周后,試驗組治療總有效率高于對照組[82.46%(47/57)比56.52%(26/46)](χ2=8.294,P=0.004),見表4。
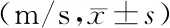
組別例數SNCV正中神經腓總神經MNCV正中神經腓總神經對照組4637.1±3.833.3±7.339.5±4.840.3±3.8試驗組5736.6±4.334.5±3.540.3±5.239.3±4.8t值1.4601.3651.3061.300P值0.3250.4250.3550.252
DPN:糖尿病周圍神經病變;SNCV:感覺神經傳導速度;MNCV:運動神經傳導速度;對照組:單純甲鈷胺治療;試驗組:依帕司他聯合甲鈷胺治療
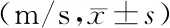
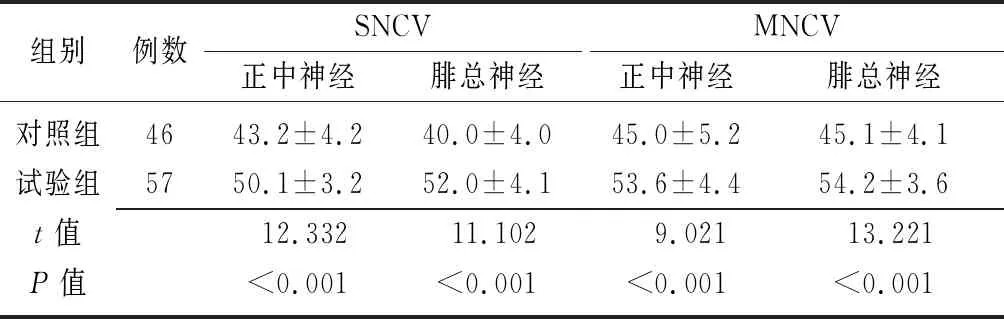
組別例數SNCV正中神經腓總神經MNCV正中神經腓總神經對照組4643.2±4.240.0±4.045.0±5.245.1±4.1試驗組5750.1±3.252.0±4.153.6±4.454.2±3.6t值12.33211.1029.02113.221P值<0.001<0.001<0.001<0.001
DPN:糖尿病周圍神經病變;SNCV:感覺神經傳導速度;MNCV:運動神經傳導速度;對照組:單純甲鈷胺治療;試驗組:依帕司他聯合甲鈷胺治療
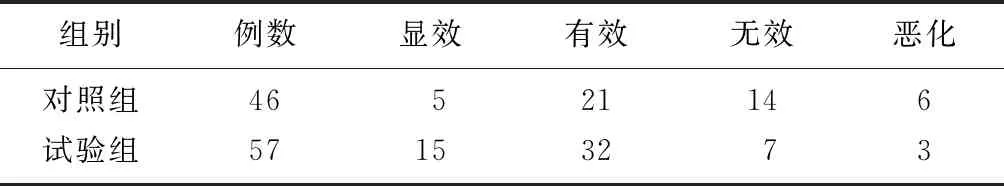
表4 兩組DPN患者臨床療效比較 (例)
DPN:糖尿病周圍神經病變;對照組:單純甲鈷胺治療;試驗組:依帕司他聯合甲鈷胺治療
3 討 論
DPN是糖尿病的常見并發癥,主要病理變化是軸突變性及脫髓鞘等[9]。DPN的主要臨床表現為自主神經、周圍神經損傷,如疼痛、肢體麻木等,嚴重者還會合并肢體潰瘍,甚至導致截肢,是糖尿病致殘的主要原因之一。研究表明,DPN發病率高達50%[10]。目前DPN的發病機制尚不完全明確,血管損傷學說認為,在長期高血糖的作用下,微血管發生病變,導致相應神經的血供缺乏[11];氧化應激學說則認為,體內氧化與抗氧化系統失衡導致細胞中各種氧自由基產生,損傷細胞及生物大分子;此外,關于DPN的學說還包括神經生長因子缺乏、多元醇通路代謝異常、脂質代謝紊亂等。隨著代謝綜合征概念的提出,對肥胖、高血壓、血脂異常、糖尿病和冠心病之間相互聯系的研究亦逐漸深入。
DPN病變過程較長,因此DPN的早預防、早治療十分關鍵。目前DPN病因發病機制尚不清楚,與代謝異常的關系密切。目前,治療DPN的藥物種類較多,主要用于改善患者癥狀,但均無法改變DPN的病程進展。針對DPN患者的神經疼痛,美國神經病學會推薦將依帕司他、甲鈷胺作為最主要的治療藥物[12-13]。此外,高壓氧、紅外激光及中醫中藥治療以及處于探索階段的基因治療和干細胞技術亦可用于DPN的治療。依帕司他是臨床治療老年DPN的常用藥物,主要通過可逆性抑制醛糖還原酶活性減少體內山梨醇、果糖的蓄積,從而恢復細胞內Na+,K+-ATP酶活性,逆轉神經變性和水腫,加快周圍神經傳導速度。同時,依帕司他還能促進老年DPN患者血清丙二醛水平降低,并提升超氧化物歧化酶水平,從而增強機體抗氧化應激能力、減輕細胞損傷。此外,依帕司他還可能參與同型半胱氨酸代謝的調節,在一定程度上降低血漿同型半胱氨酸水平,減輕高同型半胱氨酸引發的氧化應激,降低一氧化氮水平,改善老年DPN患者的病情。在蛋白激酶C激活時,亦可發生老年DPN,而依帕司他能夠抑制高血糖引發的蛋白激酶C信號通路的激活,從而發揮積極的治療作用。在形態學上,依帕司他能夠促進軸突面積增加,提高神經纖維密度,加快神經傳導速度。
甲鈷胺是維生素B12的衍生物,參與DNA合成、蛋白質、脂肪代謝,促進核酸、蛋白質的合成,可為軸突再生和神經組織修復提供良好的前提條件。多項研究認為[14-16],胰島素抵抗是代謝綜合征的發病基礎,進一步加深了臨床工作者對糖尿病及其并發癥的認識。研究表明,與單純甲鈷胺治療相比,依帕司他聯合甲鈷胺治療DPN患者的臨床癥狀顯著改善,且患者正中神經與腓總神經傳導速度也更快,表明依帕司他聯合甲鈷胺治療可明顯改善DPN患者周圍神經傳導速度、減輕神經細胞損傷,有效延緩患者病情進展[17-19]。另有研究顯示,依帕司他聯合甲鈷胺能夠改善DPN患者周圍神經病變癥狀,促進周圍神經傳導速度的加快和氧化應激水平的降低,且不引起嚴重不良反應[20]。本研究結果顯示,治療4周后,試驗組正中神經和腓總神經MNCV、SNCV的改善明顯優于對照組,且試驗組治療總有效率高于對照組,與文獻研究結果[20]一致,表明聯合應用甲鈷胺和依帕司他治療DPN效果明顯優于單用甲鈷胺治療,甲鈷胺主要起營養神經的作用,依帕司他改善多元醇通路代謝異常。但目前針對以上兩種藥物聯合治療DPN效果的機制尚不確定,本研究仍存在不足之處,研究樣本數量較少、治療時間較短,未追蹤遠期療效,可能導致研究結果的偏差,仍需大樣本、長時間隨訪的深入研究。
綜上所述,依帕司他聯合甲鈷胺治療DPN的療效顯著,可明顯改善DPN患者正中神經和腓總神經SNCV、MNCV。

