菱形二氧化鈰的水熱合成及發光機理研究
李向果,郭 淼,姚會敏,呂 靜
(1.河南質量工程職業學院食品與化工系,河南平頂山467000;2.廣西師范大學化學化工學院)
隨著家居市場需求的不斷擴大, 發光材料在智能照明系統領域的應用需求也在逐年增加。 二氧化鈰(CeO2)是一種重要的稀土氧化物發光材料,在LED 照明系統、光電子器件、智能傳感器、紫外屏蔽劑、燃料電池、催化劑、拋光材料等領域具有廣泛的應用[1-6]。 尤其是CeO2中的Ce 離子同時存在+4 和+3 兩種價態,當兩種價態相互轉換時,該材料具有很強的儲氧功能[7],這一功能將導致CeO2具有高效的發光性能。不同的制備方法導致CeO2發光材料的微結構、表面形貌、缺陷態等不同,從而影響材料的光學性質和其他物理化學性質[8]。 因此,制備高儲氧功能的CeO2稀土氧化物發光材料成為了一大挑戰。
目前,合成CeO2發光材料的方法較多,包括溶劑熱法[9]、陽極氧化鋁模板法[10]、草酸 沉淀法[11]、蛋清蛋白輔助水熱法[12]、沉淀滴定法[13]、真空熱蒸鍍法[8]、表面活性劑輔助水熱法[14]、絡合劑輔助水熱法[15]、反相微乳液法[16]等。 在上述合成方法中,水熱法是一種優異的制備方法, 尤其在制備不同形貌如八面體狀、棒狀、花狀、蝴蝶狀、空心球狀等方面具有很大的優勢,僅需引入礦化劑、表面活性劑、絡合劑等原材料即可改善CeO2發光材料的形貌[14-15]。 然而,這些方法在前驅體溶液中引入了其他試劑,對CeO2發光材料的相純度和性能都會產生不同程度的影響。 但是,不使用任何礦化劑、絡合劑以及表面活性劑合成CeO2發光材料的簡單水熱合成法尚未見報道。 因此,采用簡單一步水熱合成法合成CeO2發光材料并研究它的光學、發光性能具有重要意義。
筆者采用簡單的一步水熱法合成CeO2發光材料,基于X 射線衍射儀(XRD)和X 射線光電子能譜儀(XPS)研究它的氧空位濃度以及吸附氧,建立晶胞結構。 通過掃描電鏡觀察制備的發光材料的形貌,研究掃描電鏡(SEM)觀察結果與XRD 計算結果的一致性。 采用紫外可見分光光度計和熒光分光光度計研究CeO2發光材料的光學和發光性質。 根據熒光發射譜,利用色度軟件分析其色度坐標。基于實驗結果和理論分析,研究CeO2發光材料的發光機理。
1 實驗部分
1.1 材料的合成
采用一種簡單的水熱合成法制備菱形CeO2發光材料。 按照一定的化學劑量比稱取六水合硝酸鈰配制成水溶液,在充分溶解后除去不溶物,得到無色透明的Ce(NO3)3·6H2O 溶液。 用硝酸或氨水調節溶液的酸堿度為6。 量取上述溶液80 mL 置于聚四氟乙烯內襯的反應釜中, 將反應釜移入干燥箱中,在250 ℃保溫12 h。 升溫、降溫速率均為10 ℃/min。 待冷卻至室溫后,將反應產物轉移至燒杯中靜置24 h,去除上層清液,用適量硝酸清洗數次,再用高純酒精清洗兩次,然后置于干燥箱中在135 ℃干燥12 h,獲得菱形CeO2發光材料。
1.2 材料表征
采用DX-2700 型X 射線衍射儀對菱形CeO2發光材料的物相結構進行分析;采用Materials Studio 4.0 軟件構建CeO2晶胞;采用JSM-7600F 型掃描電鏡觀察菱形CeO2發光材料的表面形貌;采用XSAM 800 型X 射線光電子能譜儀測量CeO2發光材料的光電子能譜;采用UV-2500 型紫外可見分光光度計測試CeO2發光材料的紫外可見漫反射光譜;采用RF-5301PC 型熒光分光光度計記錄菱形CeO2發光材料的激發光譜和發射光譜,測量范圍為200~800 nm,光源為200 W 氙燈。
2 結果與討論
2.1 相結構分析
圖1 為水熱法合成CeO2的XRD 譜圖。 從圖1看出,在2θ 為28.915、33.106、47.489、56.718、59.109°處可以觀察到5 個明顯的衍射峰, 對應的晶面指數分別為(111)(200)(220)(311)(222)。全部的衍射峰屬于立方相CeO2,空間群為Fm-3m(225),標準卡號為JCPDS No.34-0394。 利用MDI Jade 6 軟件對其進行結構精修,R=13.45%,表明模擬結果可信,實驗結果與擬合的結果基本一致。 根據謝樂公式(1),挑選XRD 譜線中的4 個強峰, 相關參數見表1, 計算CeO2平均晶粒尺寸為10.962 nm。

式中:D為晶粒尺寸;k為謝樂常數;λ 為入射X 射線波長;β 為衍射角半高寬;θ 為衍射角。
通過公式(2),可計算出CeO2晶胞參數a。 經計算,其晶胞參數為0.536 76 nm,結果見表1。

式中:d為晶面間距;(h、k、l) 為晶面指數;a為晶胞參數。
為研究樣品中的氧空位濃度,通過公式(3)[17]和(4)[17]可計算出CeO2的氧空位濃度,見表1。
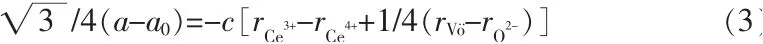
式中:a為CeO2樣品的晶胞參數;a0為塊體CeO2樣品的晶胞參數,0.541 134 nm;c為氧空位濃度系數;rCe3+為Ce3+的離子半徑,取值0.128 3 nm;rCe4+為Ce4+的離子半徑,取值0.109 8 nm;根據文獻[17],為氧空位半徑, 取值0.138 nm,rO2-為O2-離子半徑, 取值0.124 nm。

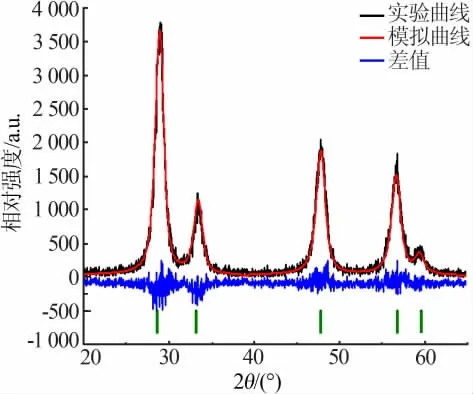
圖1 水熱法合成CeO2 的XRD 譜圖
Zhou 等[18]合成了納米尺寸的CeO2單晶,其氧空位濃度為4×1020cm-3。Choudhury 等[17]采用濕化學法合成了CeO2納米顆粒,經不同溫度燒結,其氧空位濃度隨著燒結溫度的升高而減少, 其最佳氧空位濃度接近5×1020cm-3。 Gao 等[19]采用輻照輔助聚丙烯酰胺凝膠法合成了CeO2納米顆粒,觀察到了一個相反的現象, 即氧空位濃度隨著燒結溫度的升高而增加,其氧空位濃度介于(1.27~3.96)×1020cm-3。 在本實驗中,采用水熱法合成的CeO2樣品的平均氧空位濃度為1.723 7×1020cm-3。 根據Choudhury 等[17]和Gao等[19]的結論可知,高的氧空位濃度可能導致高的光催化活性;氧空位濃度相對較低,其發光性能較強。本實驗中,CeO2樣品的氧空位濃度居于兩篇文獻獲得的最佳氧空位濃度之間,可能展示極好的發光性能。
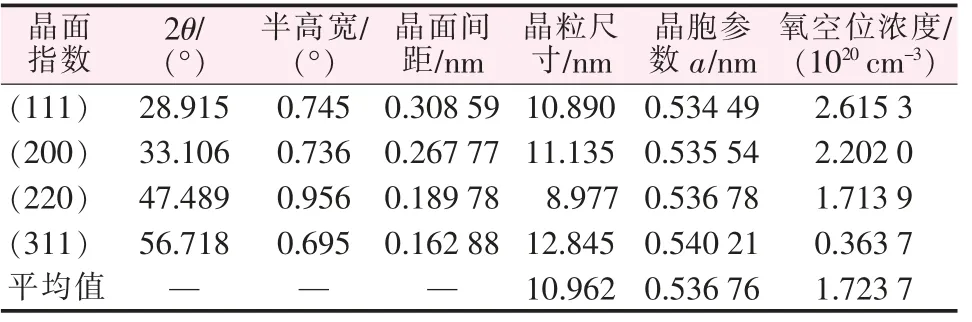
表1 XRD 譜圖分析獲得的晶粒尺寸、晶胞參數和氧空位濃度
基于MDI Jade 6 軟件結構精修和理論計算的結果, 利用Materials Studio 4.0 軟件可獲得CeO2晶體結構圖。 CeO2是一種具有螢石結構的立方相晶體, 該結構的晶體主要由面心立方晶胞的陽離子和占據八面體空間的陰離子組成,見圖2。 從圖2 看出,每個Ce 離子與O 離子的8 個最近鄰位置配位,每個O 離子與最近的4 個Ce 離子配位。

圖2 水熱法合成CeO2 晶體結構圖
2.2 表面形貌和電子衍射分析
圖3 為水熱法合成CeO2的SEM 照片。從圖3 看出, 該樣品主要由菱形的大顆粒和一些晶粒尚未長大的小顆粒組成。 大的菱形顆粒的直徑超過200 nm,這一結果與XRD 計算的結果有所不同。 盡管如此,卻與XRD 獲得的結果不矛盾。 其一,XRD 計算的是晶粒,而SEM 觀察到的是顆粒,而顆粒是由許多小晶粒組成;其二,在采用謝樂公式對晶粒進行計算的過程中,是將所獲得樣品近似為球形顆粒計算的,故結果出現較大偏差。

圖3 水熱法合成CeO2 的SEM 照片
由于結晶度會對CeO2衍射峰半峰寬產生影響,因此通過選區電子衍射(SAED)檢驗了CeO2結晶度。圖4 為水熱法合成CeO2的SAED 圖。 從圖4 看出,電子衍射圖包含5 個明顯的衍射環。 經Digital Micrograph 軟件作圖可知, 晶面間距為0.311 99、0.270 49、0.192 01、0.162 98、0.119 99、0.103 98 nm,對應的晶面指數分別為(111)(200)(220)(311)(420)(511)。經分析表明,采用水熱法合成的CeO2具有較好的結晶度。
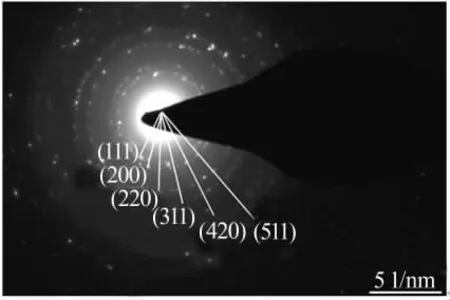
圖4 水熱法合成CeO2 的SAED 圖
2.3 XPS 表征
為研究CeO2的化學組分、電子能級、分子結構和表面缺陷, 采用X 射線光電子能譜儀獲得了其XPS 圖。圖5a 為CeO2的Ce 分譜。用U 和V 分別表示3d5/2和3d3/2的自旋軌道耦合。 4 個主要3d5/2特征峰 在885.3、888.9、891.4、901.3 eV 分 別 對 應 于V、V′、V′′、V′′′組分;在902.5、905.3、908.6、918.5 eV 的3d3/2特 征 峰 分 別 對 應 于U、U′、U′′、U′′′組 分。Watanabe 等[20]研究認為,V、V′、V′′、V′′′4 個峰分別可分配給CeⅣ(3d94f2)O(2p4)、CeⅢ(3d94f1)O(2p6)、CeⅣ(3d94f1)O(2p5)、CeⅣ(3d94f0)O(2p6);相應的U結構的4 個峰與V 結構的峰對應。 圖5b 為CeO2的O 分譜。 通過分峰處理可將譜線分為兩個特征峰,分別為528.98 eV 和530.52 eV。 其中,528.98 eV 的峰對應于Ce—O 峰, 而530.52 eV 的峰對應于吸附氧的峰[21]。 吸附氧的峰越強,表明其熒光發射性能越好。結合XRD 結果的氧空位計算和XPS 氧分譜的分析可知,采用水熱法合成的菱形CeO2具有較強的發光性能。
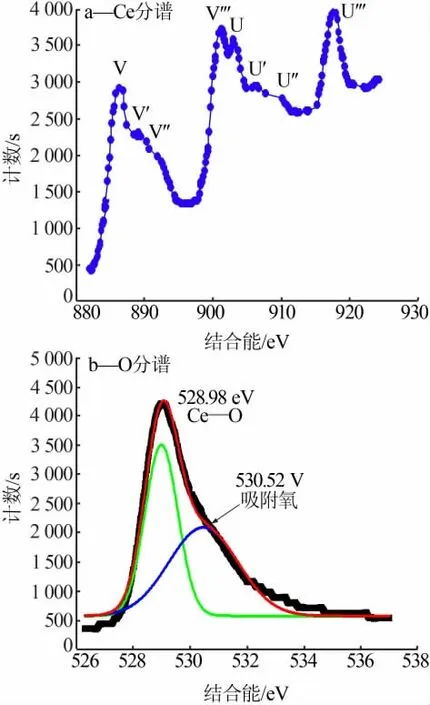
圖5 水熱法合成CeO2 的XPS 圖
2.4 光學性質
紫外可見漫反射光譜可用于分析制備材料的光學性質, 圖6a 為水熱法合成CeO2的紫外可見漫反射光譜圖。 從圖6a 看出, 在200~220 nm 波長范圍內,反射率隨著波長的增加而逐漸減小;在220~350 nm 波長范圍內,反射率隨著波長的增加略有增加;在350~550 nm 波長范圍內,反射率隨著波長的增加而急劇增加;隨后,波長繼續增加,反射率基本保持不變。 根據K-M 公式(5),可獲得CeO2的紫外可見吸收光譜圖,見圖6b。
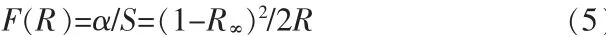
式中:R為反射率;α 為吸收系數;S為散射系數。 從圖6b 看出,兩個明顯的吸收峰在285 nm 和330 nm能被觀察到。 該結果表明,CeO2具有很強的紫外吸收能力。 而且吸收一直延伸到500 nm 左右,表明其還具有一定的可見光吸收能力。可見,該樣品具有較強的光催化活性。基于紫外可見吸收光譜,可通過公式(6)計算出CeO2樣品的光學帶隙(Eg)值。

式中:α 為吸收系數;h為普朗克常數;n為頻率;A為一個常數;n取1/2。 圖6c 為(αhν)1/2與hν 的關系曲線圖。將曲線斜率最陡處外延至與橫坐標的交點,其交點值即為樣品的Eg值。 由圖6c 可知,水熱法合成的CeO2樣品的Eg為3.19 eV。 Ramasamy 等[22]采用化學沉淀法合成了CeO2納米顆粒, 其Eg值比本實驗獲得的Eg值大,約為3.5 eV。Selvi 等[23]發現,采用共沉淀法合成的CeO2納米顆粒的Eg值比采用化學沉 淀 法 合 成 的Eg值 更 大。 Hosseini 等[24]采 用 微 波輔助燃燒法合成了CeO2納米顆粒,其Eg值約為3.26 eV。 由此可知,采用不同的方法合成同一種物質其Eg值均不同,表明CeO2樣品的Eg值強烈依賴于合成路徑。
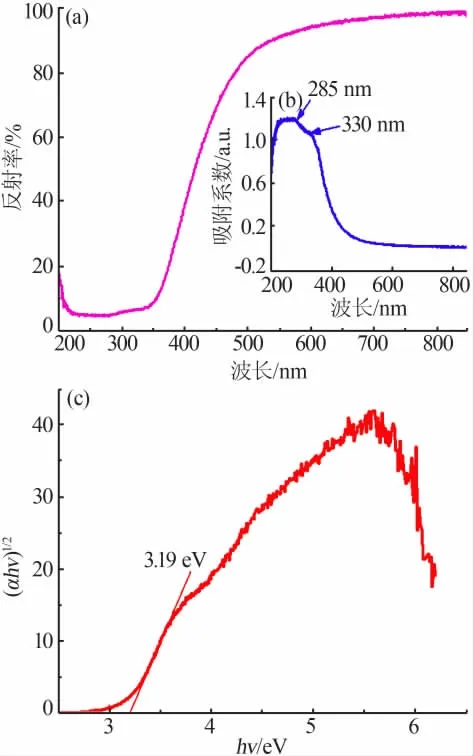
圖6 水熱法合成CeO2 的紫外可見漫反射光譜(a)、紫外可見吸收譜(b)、(αhν)1/2 與hν 的關系(c)圖
2.5 發光性質
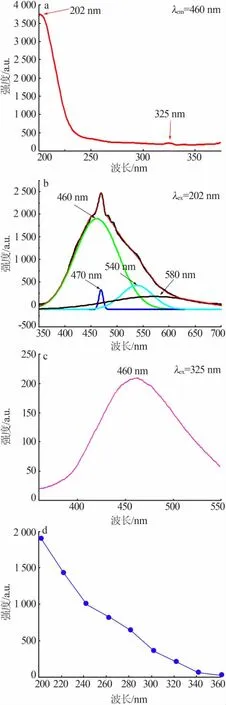
圖7 水熱法合成CeO2 的激發譜(a)、發射譜(b、c)、激發波長隨發射強度的變化曲線(d)
為研究水熱法合成CeO2的發光性質, 圖7a 給出了CeO2的激發光譜圖(發射波長為460 nm)。 從圖7a 看到兩個明顯的激發峰在202 nm 和325 nm。 圖7b 顯示了CeO2的發射光譜圖(激發波長為202 nm)。在350~700 nm 波長范圍內,CeO2展示了一個寬的發射帶。基于高斯擬合可將其分為4 個發射峰,分別位于460、470、540、580 nm。 在325 nm 波長激發下,其發射峰為460 nm,見圖7c。與圖7b 相比,圖7c 發射峰的強度較弱, 這一結果與激發譜中觀察到的現象一致。為研究不同激發波長對樣品發射強度、峰位置等的影響, 采用不同激發波長激發獲得了樣品的發射峰。發射峰的位置幾乎沒有變化,然而其發射強度發生了明顯變化,結果見圖7d。 從圖7d 看出,隨著激發波長的增加,其發射強度不斷減小,表明樣品最佳的激發波長為202 nm。 除了光學性質強烈依賴于合成路徑, 發光性質也表現出強烈依賴于制備方法和材料的維度。Gong 等[25]合成了一維桿狀和三維蓮花狀CeO2氧化物, 其發射帶分布在380~650 nm的寬范圍內。 當采用溫和的水熱法合成立方相的CeO2時,其在452 nm 和470 nm 展示了兩個明顯的發射峰[26]。 另外,Meng 等[27]采用水熱法合成了微結構的CeO2,展現了468 nm 和562 nm 兩個明顯的發射峰。 Phokha 等[28]采用一個簡單的濕化學法合成了CeO2納米顆粒,由于表面缺陷的作用,其在483 nm出現了一個弱的藍綠光發射。 Choudhury 等[17]采用簡單的溶液法合成了CeO2納米顆粒,從紫外到可見展示了一個寬的發射帶。 Kumar 等[29]采用一步水熱法合成了CeO2納米顆粒,出現了藍色、綠色和黃色3個強的發射帶。 Murugan 等[30]采用射頻濺射法制備了CeO2薄膜,觀察到了兩個紫外發射峰、一個淡紫色發射峰和兩個綠色發射峰。一般地,380~500 nm發射帶可歸因于不同缺陷能級到CeO2價帶間的轉變,500 ~675 nm 發射帶能被歸因于晶體中的氧空位[25]。為進一步闡述各發射峰產生的原因,將在發光機理部分對其進行詳細分析。
基于GoCIE 色度軟件,可研究水熱法合成CeO2的顯色性和色度坐標。 將獲得的發射譜調入GoCIE色度軟件, 獲得相應的色度坐標, 其色度坐標值為(0.188,0.243),結果見圖8。 由此可見,樣品的發光顏色趨向于藍綠色, 可將其作為一種藍綠色發光材料的候選材料。
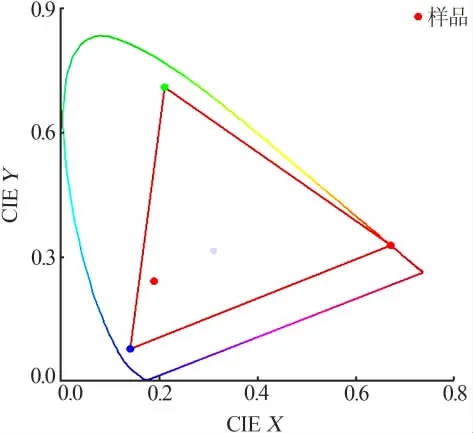
圖8 水熱法合成CeO2 的色度圖
2.6 發光機理
為進一步理解水熱法合成CeO2的發光機理,圖9 提出了一個可能的解釋機理。O2p和Ce4f分別組成了CeO2的價帶和導帶, 當激發光照射到CeO2發光材料上,電子在價帶被激發躍遷到導帶上,在價帶留下空穴。 由于激發光能量大于Eg值,因此躍遷到導帶的電子會通過振動馳豫下降到更低的能級。 在CeO2發光材料中,由于F++心的存在,通過振動馳豫下降到更低能級的電子會繼續下降, 與Ce4f上的空穴發生復合,并產生發光現象。對于CeO2發光材料,其發射峰能量需大于2.6 eV 才能產生這一現象[30]。 因此,低波長的兩個發射峰在460 nm 和470 nm 應歸因于這一發射。 由于樣品中存在大量的氧空位,電子可繼續下降到氧空位所占據的能級,進一步下降到價帶與空穴進行復合, 從而產生發光現象,發射峰的能量介于2.2~2.6 eV 之間[31],540 nm的熒光發射即由氧空位所引起。 同時,由于F0*心的存在,電子會在該能級短暫停留,并繼續下降到F0心能級與空穴復合,釋放的能量以光的形式發出,其發射峰能量位于2.1~2.2 eV之間[30],本實驗中580 nm 的熒光發射即屬于這一發射。
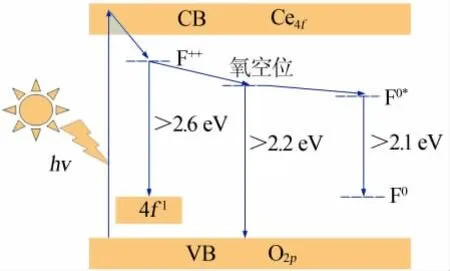
圖9 水熱法合成CeO2 的發光機理
3 結論
通過水熱法制備了存在大量氧空位或吸附氧的CeO2發光材料, 經計算其晶胞參數為0.536 76 nm,氧空位濃度為1.723 7×1020cm-3。 紫外可見吸收光譜顯示其在400 nm 以下具有強的光吸收能力,計算其Eg值為3.19 eV, 是一種強的紫外光光催化候選材料。 經202 nm 的光激發,熒光發射光譜出現了460、470、540、580 nm 4 個熒光發射峰, 色度坐標值為(0.188,0.243)。 經發光機理分析,CeO2發光材料中存在的F++心、 氧空位和F0*心在發光方面扮演了重要角色。

