光電化學催化中的富勒烯基材料:機理及應用
程源晟 蔡號東 凌 敏 宋 超 魏先文*,
(1安徽工業大學化學與化工學院,材料科學與工程研究院,煤清潔轉化與高值化利用安徽省重點實驗室,馬鞍山 243002)
(2安徽師范大學化學與材料科學學院,功能分子固體教育部重點實驗室,蕪湖 241000)
(3廣西科學院廣西紅樹林研究中心,北海 536000)
0 引 言
為克服能源危機和環境污染問題帶來的不利影響,近幾十年來,光催化和電化學催化等新型催化方式,因其具有的清潔、綠色且反應條件溫和等優勢而備受關注,并得到了飛速發展。經過科學家們的不斷努力,一大批性能優良的光電催化劑,特別是貴金屬催化劑已經被廣泛開發并投入使用,但發展廉價高效的新型光電催化劑以滿足實際應用需要,仍是當前相關研究的主要目標[1-3]。眾所周知,碳材料具有種類豐富、價格低廉、性質穩定、環境友好且易于改性等多種優勢,其自身不僅可以用作非金屬催化劑,還可以作為載體與其他材料進行復合,所以被認為是傳統催化劑的優良替代品[4-5]。在巨大的“碳家族”中,存在著如石墨、金剛石、無定形碳、富勒烯、碳納米管、石墨烯以及石墨炔等一大批不同結構不同維度的碳材料,并還處在不斷擴充之中,它們之間既有共性也有差異性。其中,富勒烯作為第3種被發現的碳的同素異型體,也是目前已知的唯一可溶解且具有明確分子結構的碳材料,從發現之初便引起了人們的極大興趣[6-7]。作為富勒烯家族中最具代表性的一員,C60最早被發現且實現了宏量制備,因此大量與富勒烯相關的工作都是圍繞C60開展[8-9]。
C60是由60個碳原子組成的高度對稱全碳分子籠,含有12個五邊形面和20個六邊形面,面排布遵循五元環分離規則(IPR,isolated-pentagon rule),即任意2個五邊形面均不相鄰,這樣可以有效避免因分子間張力過大造成結構的不穩定[10]。C60屬于Ih點群,分子直徑為0.71 nm,分子中60個碳原子都是等價的,均以近似sp2雜化的方式形成3根不共平面的σ鍵,余下的1個p軌道電子互相重疊形成閉殼層電子結構,π電子云分布在C60分子籠的內外層表面上。由于C60的π電子并不能在分子間自由移動,故C60固體導電性較差[9]。此外,C60分子能級高度簡并,能極差較小(1.6~1.9 eV),最高占據軌道HOMO能級五重簡并,最低空軌道LUMO能級三重簡并,且能量較低,因此具有較高的電子親和能(~3.0 eV)[9]。循環伏安測試表明,C60在溶液中可以逐步可逆地接受6個電子形成負離子,卻很難失去電子變為陽離子,所以C60常作為電子受體應用于催化領域[11-13]。經過30多年的研究,富勒烯及其衍生物的化學及物理性質研究得到迅速發展,已經發現富勒烯具有優良的超導和磁性能、非線性光學效應及光學限幅效應等一系列奇異的光電磁等物理性質,在光調制、光開關、光電轉換等光電器件和通訊、太陽能電池、生物應用、光電催化等領域有著潛在的應用前景[14]。我們主要以[60]富勒烯(C60)及其衍生物的結構與性質為基礎,總結了C60、C60籠外衍生物、C60基復合材料以及C60衍生碳材料在光催化和電化學催化中的機理、作用和應用(圖1),并對目前所存在的一些問題以及未來可能的發展方向進行了展望。
圖1 C60材料在光電催化化學中的應用Fig.1 Applications of C60-based materials in photo-and electro-catalysis
1 富勒烯基材料的合成
1.1 富勒烯衍生物
C60具有典型的缺電子性質,其分子中含有大量不飽和雙鍵,因此具有較好的反應活性。通過向C60分子中引入官能團,以改變C60的溶解性、電子結構和表面能等性質,對拓展C60的應用具有重要意義。如圖2所示,C60的反應類型涵蓋了如:親核加成、環加成、氫化、氧化、聚合和鹵化等諸多反應[15-21]。受C60分子籠中角錐張力的影響,加成反應主要發生在[6,6]雙鍵位置,相關的合成方法也從傳統的有機合成,拓展到如今的電化學合成、光化學合成等新型合成方法[22-23]。以C60為基礎的富勒烯合成化學儼然成為了一個獨立的研究領域,不論在原理方法還是新結構合成上都有了長足發展,在此不做贅述。
1.2 富勒烯基復合材料

圖2 C60的常見反應類型Fig.2 General reactions known to occur on C60
出于材料成本、催化活性和穩定性等多方面考慮,目前人們所研究的富勒烯基光催化劑和電催化劑主要是以多組分的復合材料為主。針對不同材料各自特點,按需組合并選擇合適的制備方法以使材料達到最佳的催化活性,成為當下研究者們所要面對的主要問題。不同的制備方法會直接影響C60在復合材料中的分布比例以及聚集狀態等特性,從而導致催化性能的顯著差異。
目前常見的制備方法主要包括:球磨法[24-26]、吸附法[27-30]、溶膠凝膠法[31-32]、水熱法和溶劑熱法等[33-36]。其中,球磨法較為簡單,常被使用于C60與二維材料如C3N4[25]、黑磷[26]和石墨烯[37]等的復合之中。如圖3所示,利用球磨法制備黑磷/C60復合材料[26],球磨過程中C60會在黑磷表面及邊緣形成共價鍵而牢固結合,高分辨透射電鏡圖中能清楚地看出單個C60分子有序地排列在黑磷邊緣。然而,球磨法中為了共價鍵的形成,通常會添加足量的C60以增加球磨時不同組分的接觸機率,隨后通過CS2等溶劑洗去游離的C60,這樣使得球磨法制備的復合材料中,C60的精確計量不易控制。相反的,吸附法通常是將溶有一定量C60的溶液與另一組分混合均勻,通過分子間作用力使C60吸附在材料表面,隨后溶劑揮干形成復合材料,有時還會將固體進一步加熱以增強組分之間的相互作用。吸附法操作簡單,計量可控,且由于存在Langmuir吸附,易形成單分子層[28]。但最大的問題是易受C60負載量的影響,會出現結晶分布和尺寸不均的現象,且由于是范德華力作用,不同組分之間相互作用力也不強。溶膠凝膠法、水熱法以及溶劑熱法都是類似“一鍋煮”的方法,即將C60作為原料之一參與材料合成中,并且通常還會采用酸化等方法提高C60的溶解性[30,33]。盡管這些方法目前使用較多,但在這些涉及復雜反應條件甚至高溫煅燒的方法中[29,31],C60能否維持自身穩定,是否會發生氧化、籠坍塌形成量子點或者碳摻雜等現象[38-40],往往因為表征難度大而被忽略。總之,就目前復合材料的制備合成方法而言,發展簡單、有效且能精確地控制C60負載甚至組裝形成單分子層的方法仍是一項富有意義但充滿挑戰的課題。
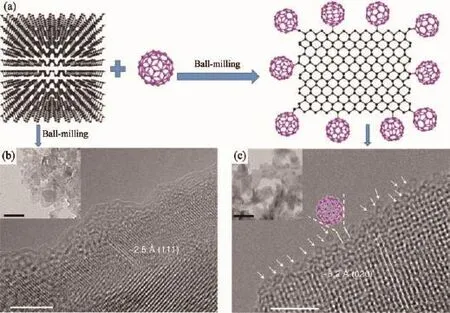
圖3 (a)黑磷/C60材料制備示意圖;黑磷 (b)和黑磷/C60材料 (c)的高分辨透射電鏡圖,插圖為低倍透射電鏡圖[26]Fig.3 (a)Scheme of the preparation process and structure of black phosphorus/C60 hybrid;High resolution transmission electron microscopy images of black phosphorus(b)and black phosphorus/C60(c),where insets are low-magnification TEM images[26]
1.3 富勒烯衍生碳材料
富勒烯衍生碳材料主要是指C60球形結構受到外界因素影響使之籠狀結構坍塌,繼而破碎或重構所形成的碳材料[39,41]。通過這種方法制備出的衍生碳材料中仍保留了大量C60碳五元環結構,具有豐富的本征缺陷,能提供大量的潛在活性位點,展現出更為優異的催化性能[42]。譬如C60在濃硫酸、高錳酸鉀的強氧化氛圍中長時間攪拌后,C60分子籠破裂,形成氧化石墨烯量子點,這種量子點具有很好的熒光性質和催化性能[39]。如圖4(a)所示,Tan等[41]采用高溫KOH輔助活化的方法,以C60為原料制得富缺陷的多孔碳,當改用氨氣氣氛后,則會得到高氮含量的氮摻雜多孔碳。從透射電鏡圖(圖4(b~d))中可以觀察到,由于熱重構和KOH高溫刻蝕作用,所得到的碳材料具有海綿狀三維多孔結構,選區衍射圖表明高溫熱處理使C60晶體結構被破壞轉而成為無定形碳結構。豐富的孔結構以及缺陷結構,使得該衍生材料具有良好的電化學性質。
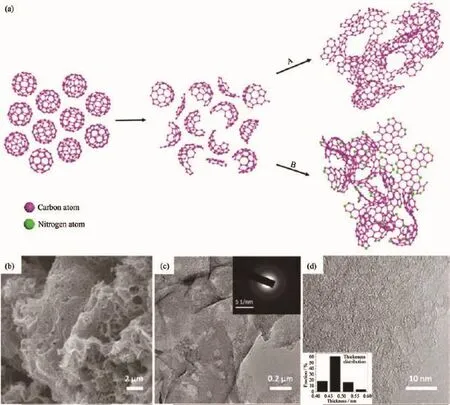
圖4 (a)KOH活化C60制備示意圖;(b~d)為活化后C60的SEM和TEM圖,插圖為電子衍射圖(c)和層間距分布比例 (d)[41]Fig.4 (a)Scheme of the preparation process for KOH action of C60;(b~d)SEM and TEM images of active C60,insets are electron diffraction pattern(c)and the distribution of the interlayer spacings(d)[41]
2 光催化中的應用
因C60具有高度對稱的共軛大π鍵體系,使C60具有很強的吸電子能力、較快的電子遷移率和較小的重組能,并且直接帶隙的存在,也使得C60具有光敏化能力,因此C60既可以作為一種優良的電子受體,也可以作為敏化劑、電子供體等用于光能轉化領域之中。
2.1 單線態氧發生
單線態氧(1O2)是氧分子的一種較穩定激發態形式,具有較高的反應活性,極易與不飽和化合物發生氧化還原反應,因此在催化、醫療和環境保護等領域廣受關注[43-44]。以基態3O2為原料,利用光能生產1O2是一種理想清潔的合成途徑,但由于躍遷高度禁阻,3O2并不能通過光照直接產生1O2,需要額外添加光敏劑以吸收光能,傳遞能量幫助激發3O2。
早在1991年Arbogast等[45]就發現可以通過光照激發C60獲得高產率的1O2,其反應機理如圖5所示。基態 (S0)的C60受到光照后躍遷為激發intersystem crossing)轉變為長壽命的激發三重態(T1)的3C60*(>40 μs)。 當有氧存在時,3C60*會以三重態-三重態淬滅(TTET,triplet-triplet energy transfer)的方式將能量傳遞到基態氧3O2(3∑),改變3O2中未成對電子的自旋方向,以產生不同自旋方向的2個電子占據同一軌道的第一激發態1O2(1Δ)和占據不同軌道的第二激發態1O2(1∑,能量較高,穩定性較差)。值得注意的是,相較于基態C60,3C60*由于具有更強的接受電子能力(E(C60/C60-)≈-0.2 V,E(3C60*/C60-)≈+1.1 V,V vs NHE)[46],因此容易從胺、醇及抗氧化劑等電子供體(ED)中得到電子成為C60·-負離子自由基,并能將電子傳遞給電子受體(EA)返回C60基態[47]。不同于能量傳輸過程,在這種電子傳輸路徑中,O2是作為電子受體,先接受電子成為,再通過的歧化反應或氧化反應產生1O2[44,48]。由于C60的ISC過程的效率近乎100%且三重態穩定,非常適合能量轉換,所以C60又被稱作“單線態氧發生器”[49]。
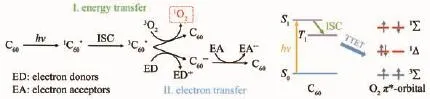
圖5 C60敏化生成1O2機理圖Fig.5 Illustration of C60as photosensitizer for the1O2 generation
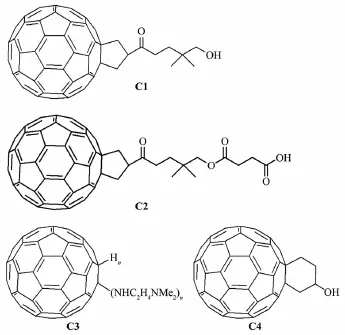
圖6 幾種具有良好溶解性的C60衍生物敏化劑(C1~C3[50],C4[56])Fig.6 Several C60 derivatives based photosensitizers with high solubility(C1~C3[50],C4[56])
基于C60光照產生1O2這一現象,化學家便嘗試將C60作為光敏劑引入到已知的1O2特征氧化反應中測試其催化活性。Tokuyama等[50]首先選取了1O2催化烯烴加成這一典型反應作為模型,利用C60、C70及3種具有很好溶解性的C60衍生物(C1、C2和C3)(圖6)充當敏化劑,定性分析了不同底物在光照下的催化反應速率及產率,并與常規敏化劑(玫瑰紅和血卟啉)催化結果做了對比。結果表明,所選擇的幾種富勒烯基催化劑在甲苯體系中均能使Schenck Ene反應(Ene反應)和Diels-Alder反應(D-A反應)有效發生,證實了光照下游離1O2的產生。其中,C70具有最高的催化活性(相同催化劑濃度下,100 W鎢燈光照激發,反應速率約為C60的5倍),最低僅需0.01%(n/n)即可催化反應完全。C60展現出與常規敏化劑相近的催化活性,并且羧基修飾的C60衍生物C1和C2可以在多種溶劑中產生與C60接近的催化活性,但缺少6個雙鍵的水溶性氨基富勒烯C3催化性能卻遠不如C60,該現象的成因在報道中并未給出解釋。隨后,以富勒烯類材料作為敏化劑,用于如圖7所示的烯類、酚類和雜原子化合物等各類底物的1O2特征氧化反應也相繼被報道[51-55]。
盡管富勒烯被證明具有較高1O2產率,并可以在甲苯以及氯仿等溶劑中催化諸多1O2特征反應,但若將其直接作為敏化劑來使用,仍存在許多問題。首先,C60的三維芳香結構導致其在多數溶劑中都難以溶解,這極大地限制了C60催化體系的拓展。當然,通過向C60中引入適當的官能團以增加其溶解性并改善富勒烯性能的方法已被廣泛使用于C60相關研究中,并被證明在1O2催化體系中同樣有效。如Anderson等[56]設計合成了一種具有良好溶解性的富勒烯衍生物C4(圖6),該衍生物不僅光學性質與C60相近, 都可以有效產生1O2(C4:ΦΔ=0.84±0.05;C60:ΦΔ=0.96;四苯基卟啉(TPP):ΦΔ=0.55(C6D6中 532 nm光激發)),而且官能團的引入還可以促進衍生物對近紅外光的吸收,具有較高的潛在應用價值。但從前文所述Tokuyama[50]的實驗中可以看出,并不是所有具有良好溶解性的衍生物都具有高活性,選擇合適取代基以及取代基的數目和位置是十分重要的。Prat等[57]通過比較一系列不同位置和取代基數目(0~6)的富勒烯衍生物的化學性質(圖8(a)),發現以犧牲[6,6]雙鍵數目換取的取代基數目的增多,導致了C60中共軛結構面積的減小,造成三重態能量升高,三重態量子產率(ΦT)降低,從而引起1O2量子產率(ΦΔ)隨之降低(圖8(b~c))。這個結論對后續設計富勒烯基敏化劑起到了指導作用,并且也能很好地解釋如前文所述的缺少6個雙鍵的氨基富勒烯C3等類似衍生物性能降低的原因。
不同于引入官能團提高溶解性,Peris等[58]提供了另一種有趣的方法,他們利用主客體包合的原理,設計了一種具有良好溶解性的Pd金屬籠并將C60及C70成功包入其中充當活性中心,實現了在乙腈溶劑中的1O2高效催化反應(圖9)。類似的包合方法,如γ-環糊精[59]和非離子型表面活性劑(聚乙烯吡咯烷酮PVP、聚乙二醇PEG)等[60-61]也常被用來制備具有光敏活性的水溶性C60材料并廣泛用于生物體系之中。但值得注意的是,C60在水溶液中能否產生1O2與其在溶液中的聚集狀態有很大關系。有研究表明[62],盡管通過長時間攪拌或超聲也能使C60進入水中,形成低濃度的C60水溶膠,但這種分散在水溶液中的C60晶體并不具備1O2生產能力。然而當溶液中存在一定濃度的非離子型表面活性劑使C60晶體分散細化后,卻能恢復C60的光敏活性[63]。對于這種現象,目前的原因尚無定論,可能是由于C60晶體表面形成的3C60*容易被周圍基態C60分子快速猝滅,從而阻礙能量的傳遞過程,造成活性的缺失。
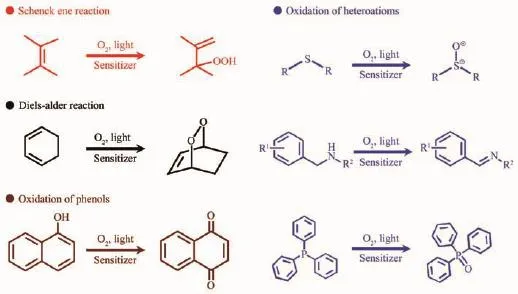
圖7 C60作為敏化劑的常見1O2反應類型Fig.7 Ordinary types of1O2 reactions catalysed by C60 photosensitizer
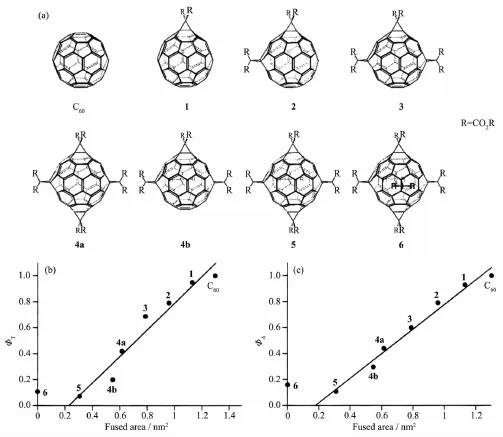
圖8 (a)富勒烯衍生物結構示意圖;三重態 (b)和單線態氧 (c)量子產率與C60核共軛面積的關系圖[57]Fig.8 (a)Structures of C60 derivatives;Correlations of the triplet(a)and singlet oxygen(b)quantum yields with the fused area of the C60 core[57]
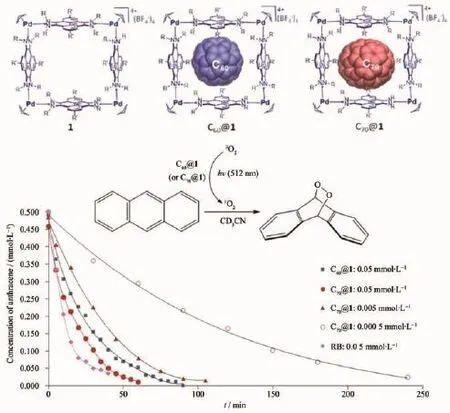
圖9 Pd金屬立方體包覆C60用于生成單線態氧的實例[58]Fig.9 Example of a Palladium metallosquare with encapsulated C60 via singlet oxygen generation[58]
盡管均相的C60及其衍生物具有較好的催化活性,但考慮到C60衍生物的合成、提純通常較為復雜,并且均相催化反應結束后催化劑與產物也不易分離,所以將C60固載,實現非均相催化也是研究思路之一。比如利用C60易與胺類加成的性質,將其固載在氨基化的SiO2[54-55]、聚乙烯球[64]和分子篩[65]等非均相載體上,不僅可以實現其在多種溶劑體系中的敏化催化,還能通過離心、過濾甚至磁力等簡單方法實現催化劑的快速分離、回收[66]。基于這種思路,Blacha-Grzechnik等[67]巧妙地利用電化學聚合的方法,將三噻吩-C60衍生物單體固定在ITO導電玻璃上,形成聚噻吩鏈錨定的C60光敏催化層。通過原子力顯微鏡(AFM)可以觀察到,聚噻吩-C60衍生物在ITO表面以直徑100~150 nm,十幾納米厚的片狀均勻分布,并且該聚合層保留了光敏特性,可以在532 nm波長的綠光下激發產生1O2。這種聚合在ITO基底上的獨特體相催化劑可以直接放入溶液體系中進行催化反應,具有很好的實用性。但這類方法的不足是,非均相的C60催化劑不論是催化速率還是1O2產率都要明顯低于均相催化劑。
C60及其衍生物直接作為敏化劑的另一個顯著缺點是,C60本身在可見光區的吸收很弱,不能充分地利用光能。所以,化學家們參照染料敏化太陽能電池工作原理,首先利用有機發色基團作為光吸收“天線”分子以增強催化劑在可見光區的吸收,隨后通過能量共振的方式將吸收的能量傳遞至C60,再借由C60高效的ISC過程最終達到激發三重態,實現更高效的1O2產生。如圖10(a)所示,Huang等[68]選取在可見光區具有強吸收但無ISC能力的苯乙烯氟硼吡咯衍生物(Styryl-Bodipy,Dyad-1)作為“天線”分子與C60結合。從圖10(b)的UV-Vis圖中可以清楚的看到,“天線”分子極大地改善了C60對可見光的吸收。將其作為敏化劑用于1O2反應中,結果如圖10(c~e)所示,得益于二元組分的高效協同作用,該敏化劑在1,5-二羥基萘(DHN)的1O2反應中展現出超越常規Ir(Ⅲ)配合物敏化劑近20倍的超高催化效率。說明這種修飾“天線”分子的方法是行之有效的,除了Bodipy類衍生物外,如卟啉[69]、酞菁[70]以及苝酰亞胺(PBI)[71]等衍生物也常被用來作為天線分子增強光吸收。
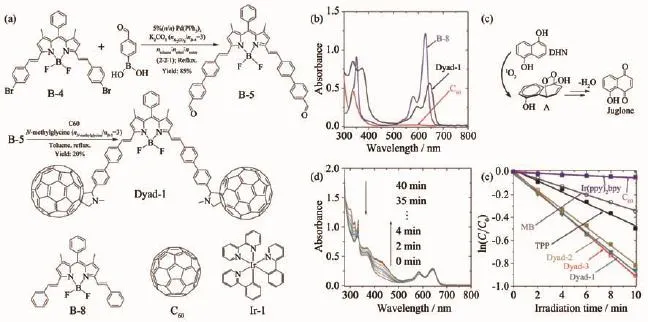
圖10 (a)Dyad-1合成路徑;(b)UV-Vis吸收光譜;(c)DHN1O2氧化反應;(d)Dyad-1光氧化DHN吸收變化圖;(e)ln(C/C0)與光照時間關系圖[68]Fig.10 (a)Scheme for synthesis of Dyad-1;(b)UV-Vis absorption spectra;(c)Photooxidation of DHN by1O2;(d)Absorption change in the photooxidation of DHN by Dyad-1;(e)Plots of ln(C/C0)vs irradiation time[68]
2.2 水中污染物降解
近年來,利用半導體受光激發后產生的如空穴(h+)、·O2-及·OH等活性物質來降解水體中的偶氮染料[72-73]、除草劑[74]和重金屬離子[75-76]等環境污染物,被認為是一種綠色經濟的治污新方式。如圖11(a)所示,當光照能量大于半導體禁帶寬度(Eg)時,電子會從半導體的價帶(CB)躍遷到導帶(VB),產生光生電子(e-)和h+,隨后光生載流子會遷移到半導體表面催化反應發生。然而,由于光生電子-空穴對復合速率要遠比自由基的捕獲速率快得多,導致許多光催化劑的量子產率和降解速率普遍較低。所以需要通過合理構筑復合材料來有效分離光生電子和空穴,優化自由基生產過程從而提高太陽光的利用率。
C60獨特的π-電子共軛體系,使其可以作為電子受體,捕獲電子,減小半導體中電子-空穴復合機率,能顯著提高半導體催化活性(圖11(a))。Kamat等[77-78]首先通過激光光解實驗發現ZnO和TiO2等半導體膠體溶液中的C60會在紫外光照射下發生單電子還原生成C60-,并且C60-負離子容易被O2猝滅回到基態。他們認為紫外光照會激發半導體產生電子和空穴對,光生電子很容易被C60所捕獲,發生轉移,證明了C60具有促進半導體電子空穴對分離的潛力。Zhang等[27]使用TiO2吸附甲苯中的C60制成復合材料,高分辨電鏡觀察表明C60在TiO2表面吸附呈一種近似單分子層的狀態,最佳質量百分含量為2.5%時復合材料展現出最佳的催化活性,紫外光下對水楊酸降解速率是純TiO2的4倍。紫外可見漫反射譜(DRS)表明C60的修飾增加了復合材料在可見光區的吸收,熒光光譜(PL)、電子自旋共振(EPR)以及自由基捕獲實驗都說明,電子由TiO2導帶傳遞到C60后,有效抑制了電子與空穴對的復合,并且C60上的電子更容易被O2捕捉形成活性自由基。Fu等[28]采用相同的方法制備了C60/ZnO復合材料,其在紫外光下降解亞甲基藍(MB)速率明顯優于未修飾ZnO,并且他們發現C60的修飾不僅可以提高光催化活性,還能有效減緩光腐蝕現象的發生。通過對比光照前后形貌以及物相的變化,推測C60通過與ZnO表面不飽和配位的O原子成鍵,降低了表面氧的反應活性,疏水層也有利于阻止表面氧的逸出,從而有效抑制了光腐蝕。類似的保護作用在如黑磷[26]、CdS[79]、CdSe[80]以及Ag3PO4[81-82]等易發生光腐蝕現象的窄帶隙半導體中尤為突出。
為了能更好地利用光能,各類帶隙適中的半導體包括異質體系如 C3N4[83-84]、Bi2TiO4F2[34]、ZnFe2O4[85]、BiOCl[86]、Bi2WO6[87]、Bi2MoO6[88]、LDH/AgCl[89]、WO3/TiO2[31]以及BiVO4/g-C3N4[90]等,在與C60及其衍生物復合之后都展現出了或多或少的性能提升。由此可見,C60作為良好的電子受體具有很好的普適性,能有效抑制光生電子-空穴對的復合以及提高材料光穩定性。
此外,由于帶隙的存在,C60及其衍生物除了可以充當電子受體,在某些時候還可以充當電子供體,用于與TiO2、SnO2這類寬禁帶半導體復合,增強對可見光的利用率。Kamat等[91]用532 nm波長激光激發表面載有C60的TiO2,通過時間分辨瞬態吸收光譜捕捉到了C60+陽離子信號,相關實驗證明在這種情況下,C60會吸收雙光子進行激發,通過二次躍遷將電子轉移到TiO2導帶,隨后被TiO2表面氧氧化,說明C60具有充當電子供體的能力(圖11(b)中typeⅠ)。類似的,Ding等[92]通過第一原理模擬計算認為,適量C60耦合的SnO2(101)晶面會形成具有間接帶隙的Ⅱ型異質結構,窄帶隙的C60能受到可見光的激發,發生電子躍遷隨后傳遞到SnO2導帶,促進了電子空穴對的分離,從理論層面說明C60可作為電子供體。
在實際應用中,Long等[33]發現酸化后C60修飾的TiO2棒具有可見光下降解羅丹明B(RhB)的能力,其降解速度是未修飾C60的TiO2棒的3.3倍,是商業TiO2(P25)的2.7倍。Zhang等[93]采用超聲法制備了聚羧酸C60衍生物/TiO2復合材料并同樣運用于可見光下RhB的降解實驗中,結果與Long等[33]的類似,C60衍生物的引入有效提升了TiO2在可見光下的降解速率。通過自由基捕捉實驗,他們發現空穴h+捕獲劑乙二胺四乙酸(EDTA)和捕獲劑 1,4-對苯醌(BQ)的加入都會降低降解速率,證明 h+和同是活性物質。Liu 等[94]使用 C60衍生物 6,6-苯基-C61-丁酸甲酯(PCBM)修飾TiO2并用于可見光下降解MB,性能顯著優于未修飾的TiO2。此外還有大量研究都表明,C60及其衍生物的修飾能顯著提高寬禁帶半導體在可見光下對染料的催化效率。但由于染料本身的光敏性,所以有觀點認為可見光下寬禁帶半導體/C60復合材料對染料的降解作用,主要源自于染料敏化[33]。即染料自身吸光敏化產生電子注入復合材料,再與O2進一步生成活性氧自由基促進降解,缺乏直接證據證明C60在這種情況下可以充當電子供體。有趣的是,在Lim等[95]的報道中,僅使用富勒醇與RhB,就可以實現染料降解、氯酚氧化等很多光氧化反應。如圖12所示,在光照下富勒醇主要是通過RhB敏化得到電子,EPR譜中光照下RhB+富勒醇產生的各類氧活性自由基要顯著高于單一組分,一定程度上佐證了染料敏化的觀點。
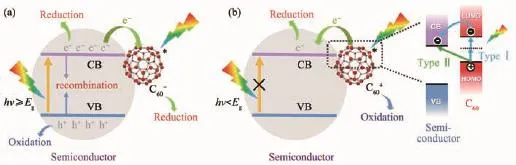
圖11 C60在光催化劑中的主要作用機制:(a)電子受體;(b)電子供體Fig.11 Representative mechanisms of C60based photocatalysts:(a)electron acceptor;(b)electron donor
為了驗證C60或C60衍生物能否作為電子供體應用于可見光催化。Park等[96]通過使用富勒醇(C60(OH)x)修飾的TiO2作為催化劑,不僅實現了包括4-氯酚和CrⅥ在內的非染料底物可見光還原,甚至當復合材料進一步負載Pt作助催劑后還能用作可見光下產氫,證明富勒醇修飾的TiO2確實具有可見光光催化能力。有趣的是,在他們的實驗中,C60與TiO2(C60/TiO2)以及C60(OH)x與氟化的 F-TiO2(C60(OH)x/FTiO2,表面氟化會抑制C60(OH)x與TiO2表面氫鍵的形成)形成的復合材料幾乎都沒有可見光活性。根據這個現象,他們認為C60(OH)x/TiO2復合材料的可見光激發應該是類似于鄰苯二酚修飾TiO2的配體金屬電荷轉移(LMCT)機制[97],即利用配體與半導體金屬原子形成的表面配合物吸收低能光子,促使電子從富勒醇的HOMO軌道直接躍遷到TiO2導帶 (圖11(b)中typeⅡ)。相關理論計算也同樣證明(圖13(a~b)),只有TiO2表面具有耦合的富勒醇時,可見光區才出現吸收,并且當富勒醇羥基與TiO2表面成鍵后,可見光區吸收會顯著增強。此外,532 nm波長激發下的時間分辨瞬態吸收光譜也捕捉到了980 nm處的C60+陽離子特征信號,證明電子是由富勒醇提供(圖13(c))。Long等[98]通過理論計算證明,盡管C60可以在TiO2(110)面形成Ⅱ型異質結,但由于二者之間作用力很弱,導致電子-空穴分離效率往往十分低下。當C60與TiO2以共價鍵方式連接時,施主-受體耦合作用得到極大的增強,優化了能帶對接,有利于電子在二者之間的轉移。由此可以看出,與寬禁帶半導體之間以共價鍵方式連接,對C60及其衍生物作為電子供體十分必要。Qi等[99]首先通過制備不同比例的酸化C60修飾的銳鈦礦型TiO2驗證了其可見光催化能力。隨后如圖13(c~d)所示,他們通過計算TiO2(101)表面和羧基化C60-TiO2(101)表面的偏態密度(PDOS)表明,未修飾的TiO2(101)表面價帶最大值(VBM)主要由O2p軌道構成,而導帶最小值(CBM)則是由Ti3d貢獻,帶隙能量為1.9 eV。當修飾羧基化C60后,由于C60-COOH與TiO2之間形成共價鍵,會形成較強的施主-受體電子耦合,TiO2受 C60-COOH2p軌道的影響會在原VBM與CBM之間形成一個新的中間價帶,使帶隙能量減小為0.8 eV。表明C60-COOH與TiO2中間配合物的LMCT過程有利于減小帶隙,擴展光吸收范圍。這些例子都很好地說明了C60衍生物可以作為電子供體,用于發展新的C60衍生物/半導體緊密異質結體系。
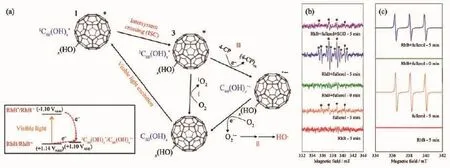
圖12 (a)光敏化氧化途徑和富勒醇的相對能態圖;EPR譜添加(b)DMPO和(c)TEMP作為捕獲劑[95]Fig.12 (a)Photosensitized oxidation pathways and the relative energy states for fullerol;EPR spectra of(b)DMPO(5,5-dimethyl-1-pyrroline-N-oxide)and(c)TEMP(2,2,6,6-tetramethyl-4-piperidone)as radical scavenger[95]
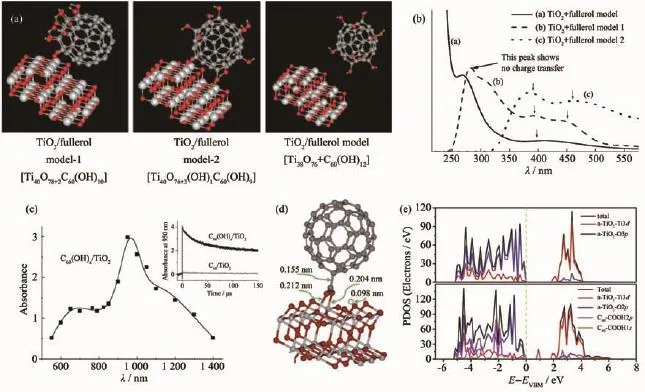
圖13 (a)TiO2/富勒醇模型;(b)3種模型的理論吸收譜;(c)時間分辨漫反射光譜[96];(d)C60-COOH@a-TiO2(101)的密度泛函理論模型;(e)(上)表面潔凈a-TiO2(101)和(下)C60-COOH@a-TiO2(101)的DOS譜[99]Fig.13 (a)Model systems of TiO2/fullerol;(b)Calculated absorption spectra for 3 models;(c)Time-resolved diffuse reflectance(TDR)spectrum[96];(d)DFT optimized structures of C60-COOH@a-TiO2(101);(e)DOS of(above)clean a-TiO2(101)and(blew)C60-COOH@a-TiO2(101)[99]
那么在一個復合體系中,C60究竟是作為電子受體,還是作為電子供體?結合目前報道,我們認為在大多數時候,C60都是起電子受體作用(圖11(a)),當復合材料中各組分都可被激發時,C60吸收光躍遷為3C60*,很容易捕捉半導體產生的光電子變為,從而促使電子-空穴對有效分離。但當C60與半導體緊密結合,存在很強的相互作用,且在光照時,體系中僅有C60可以激發,C60及其衍生物則有可能作為電子供體為導帶位置合適的半導體提供電子。如圖11(b)所示,C60可能是以異質結的typeⅠ方式傳遞電子,C60衍生物則可能以typeⅡ的LMCT方式傳遞電子。此外,也有觀點認為C60可能是通過形成中間價帶來促使寬禁帶半導體在可見光下的躍遷[73]。總之,C60與半導體之間的電子傳遞仍有許多不明之處,在實際情況中除了根據能帶位置,還需結合其他表征結果 (包括原位光譜以及時間分辨光譜等),來判斷實際電子流向。
盡管利用C60及其衍生物修飾的半導體復合材料在污染物降解應用中取得了較大的進展,但仍存在不少問題。由于缺乏統一標準(輻照強度、溫度以及催化劑用量等條件不統一),使得不同種催化劑的催化活性很難準確衡量。此外,目前對染料以及其他的一些有機污染物的光催化降解實驗多采用紫外吸收峰值變化進行衡量,該方法無法有效判斷污染物降解為脂肪烴、脂肪醇還是徹底礦化,所以有必要采用其他方法如化學需氧量(COD)[33]、氣相色譜或液相色譜等分析底物殘留[100],建立健全污染物降解的測試標準。
2.3 光活化加氫
通常斷開氫氣和氮氣這類物質的穩定化學鍵需要很高的能量以及合適的過渡金屬作為催化劑。有研究表明,在光照輔助下的C60具有作為非金屬催化劑的潛力,可以在較為溫和的條件下活化某些化學鍵(如氫氫鍵、碳氫鍵、和氮氮鍵等)并能有效催化氫轉移。
如Li等[101]發現C60在紫外光照下可以使用氫氣作為氫源,高效、高選擇地催化芳香性硝基化合物還原成芳香胺。C60和C60-存在協同效應,且C60與C60-之比為2∶1時最優。Guo等[102]利用C60作為催化劑,在紫外光下使用NaBH4作為氫源,催化偶氮化合物中氮氮雙鍵斷裂加氫還原生成伯胺。理論計算表明,C60可以利用空軌道接受偶氮染料中成鍵軌道中的電子,活化N=N雙鍵。Nishibayashi等[103]利用水溶性的γ環糊精/C60((γ-CD)2/C60)包合物在含有Na2S2O4的水溶液中,60℃、氮氣氛圍和可見光照1 h后,發現該C60包合物可以催化氮氣中氮氮三鍵斷裂,產生產率33%的氨。改用紫外-可見光照射后,產率會進一步提升至45%。作者推測N2的還原主要歸因于C60還原產生的C60-/C602-負離子具有很強的還原性。盡管C60在光照下加氫以及固氮的本質原因尚不明確,但現有報道已經證明了C60在惰性鍵活化加氫上具有巨大的應用前景,值得繼續深入研究。
2.4 光(電)解水制氫
自從1972年,人們首次以TiO2作為催化劑,通過光電催化水分解,將太陽能轉化為氫能以來,光解水制氫這項技術就一直被認為是最理想的未來能源生產方式而受到熱捧[104]。與光催化降解污染物原理類似,無論是通過直接光催化,還是外加電場的光電催化,其核心都在于半導體對光的吸收以及電子-空穴對的有效分離。如圖14所示,從熱力學角度看,理論上只要半導體能帶大于1.23 eV,并且導帶和價帶電位分別滿足氫析出(HER)電位(相對標準氫電極電勢為0 V)和氧析出(OER)電位(相對標準氫電極電勢為1.23 V)就能實現水的分解。但實際中受過電勢的影響,光解水的半導體帶隙往往需要達到1.7 eV以上。從動力學角度看,光解水的過程較為緩慢,這要求光生電子和空穴必須能保持很長一段時間的有效分離才能實現水分解,并且為了降低析氫過電勢,提高反應速率,光催化劑往往還需要額外修飾如Pt、Ru等助催化劑。C60因能有效抑制光生電子-空穴對的復合,并對H存在一定活化作用,故可以作為一類潛在的非金屬助催化劑應用于光解水制氫。值得注意的是,為了篩選出性能優異的光解水制氫催化劑,目前大多數光解水制氫實驗都會采用犧牲劑(圖14中ED-ED+過程)提供電子,屏蔽OER反應,獨立研究析氫半反應。這種方式雖然可以獲得更高的氫產率,但并不適用于實際生產。
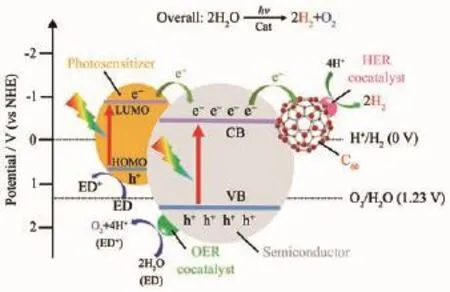
圖14 理想全解水C60基光催化劑設計圖:C60促進電子空穴分離;光敏劑提高量子產率;助催劑提高反應速率Fig.14 Design of ideal C60 based photocatalysts for water splitting:C60 can eectively separate light-induced charges;Photosensitizer to enhance quantum yield;Cocatalyst helps expediting the reaction rates
表1中列舉了目前報道的典型C60材料的光催化產氫結果[25,79,105-112]。 以最為經典的 TiO2為例,C60修飾后的商業P25在300 W氙燈光照下 (無濾光片),以三乙醇胺為犧牲劑,產氫速率可達597.2 μmol·h-1·g-1,是未修飾 P25的 31倍[105]。 Cai等[79]通過水熱法制備了C60均勻包覆的C60/CdS復合材料,在可見光下實現了2.3倍的產氫速率提升。實驗發現C60的引入極大地提高了材料穩定性,阻抗和熒光測試結果證實了C60的存在能加速電子傳遞,有效抑制光生電子-空穴的復合。Lian等[106]將酸化后的C60嵌入CdS/TiO2介孔材料中,在可見光下產氫速率達到了6.03 μmol·h-1,是不含 C60材料的8.5倍。有2個很有趣的例子值得關注,在2個C60與二維材料(MoS2[112]、C3N4[25])雜化體系中,都在未使用貴金屬助劑的情況下,實現了氫的高效產出,證明C60也可作為一種潛在的析氫助催化劑。此外,這2個體系都使用了曙紅(EY)染料作為敏化劑,以提高可見光的吸收,為光解水制氫與污水降解聯用提供了很好的實驗依據[113]。利用污水中的染料氧化代替緩慢的水氧化過程提供電子產生氫能源,同時滿足環境與能源的雙重需求,具有很好的發展前景。
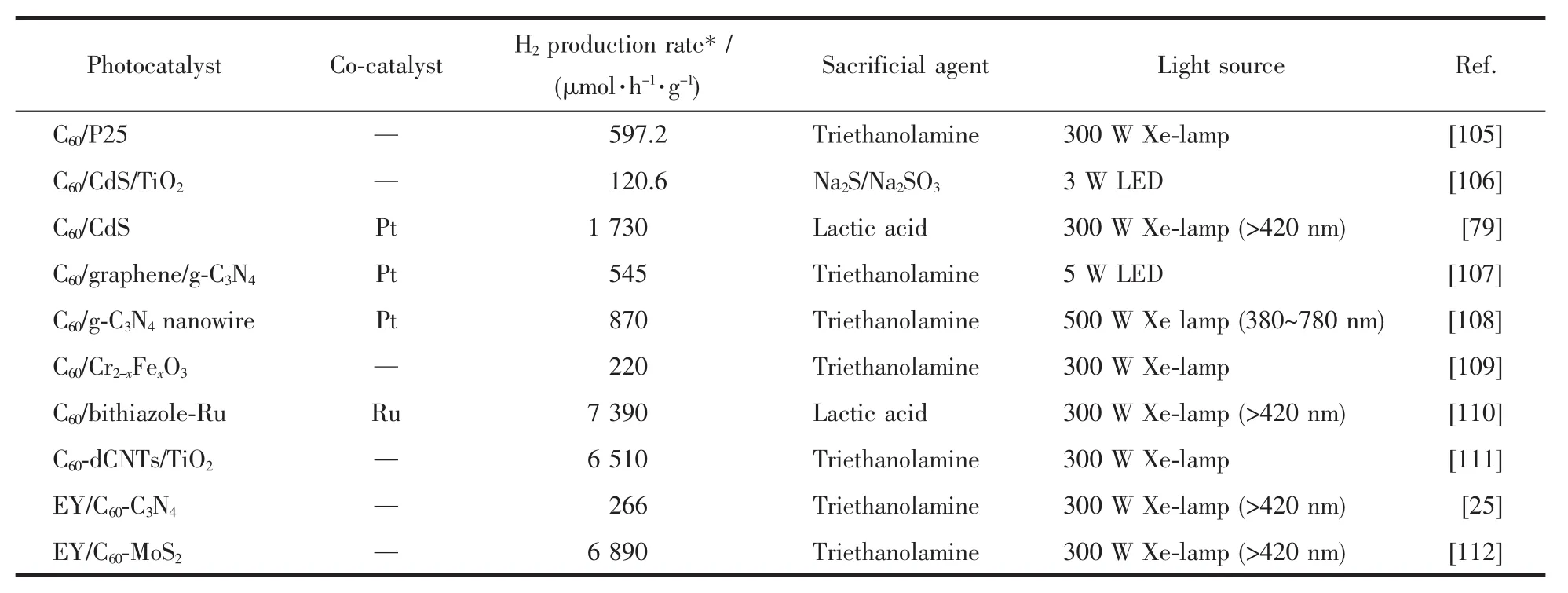
表1 C60基光催化劑光產氫性能Table 1 Hydrogen production activity of C60based photocatalysts
將光能轉化為氫能源的另一種思路是使用光電催化技術。盡管都是利用光激發產生電子,但光電催化因為有外加電場的作用,不僅可以使光生電子-空穴對更有效地分離,而且氧化反應和還原反應分別發生在陰陽兩極,使產物分離更加方便。作為太陽能電池中應用最多的材料之一,利用C60高電子遷移率、低重組能等優勢,與其他材料構筑p-n結后能使電子快速遷移到電極表面,使得C60在光電催化中也有很好的應用。Abe等[114]發現酞菁與C60構筑的有機p-n結可以吸收750 nm波長以內的光而產生光電壓,在修飾少許Pt作為共催化劑后可以有效產氫(圖 15(a,b)),量子效率達到了 11%(525 nm 下)和5%(625 nm下)。如圖15(c)所示,原位光譜揭示了反應過程中C602-負離子的生成,C602-可作為活性物質促使氫質子在Pt表面被還原為氫氣。后續實驗表明,使用吸光性能更好的金屬酞菁[115]以及采用TiO2光陽極[116]都能進一步提高光電催化效率(圖15(d))。此外,一些利用C60構筑的其他光電催化體系也都展現出很好的催化結果[117-118]。總之,不論是在光催化還是光電催化中,C60都能很好促進光生載流子分離,并抑制光生電子和空穴的復合,C60接受電子后形成的高活性的C60-/C602-負離子也有助于氫的還原。
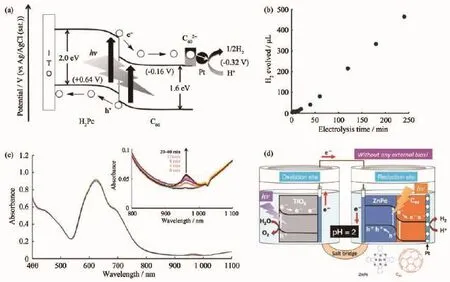
圖15 (a)產氫原理圖;(b)產氫速率;(c)吸收光譜隨時間變化圖[114];(d)雙光電極光解水示意圖[116]Fig.15 (a)Schematic diagram of H2 production;(b)H2-production rate;(c)Time course of absorption spectrum[114];(d)Schematic diagram of water splitting by using photoelectron-catalysis[116]
2.5 CO2還原等其他催化體系
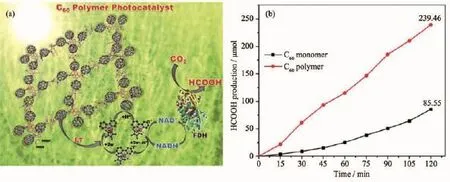
圖16 C60/酶用于CO2還原反應的實例[119]Fig.16 Example of C60/enzyme using for CO2 reduction reaction[119]
C60及其衍生物因具有的優良光學性質,在其他一些光催化體系中也具有很高的研究價值。譬如,Yadav等[119]巧妙地將C60聚合物膜運用到生物酶催化體系中實現了對CO2的光催化還原(圖16)。C60聚合物薄膜作為良好的可見光吸收單元,能將可見光的能量傳遞到Rh配合物上,隨后利用Rh配合物將輔酶Ⅰ(NAD+)高效還原(91.07%),為甲酸氫酶(FDH)還原CO2提供質子與能量,實現了5.506×106μmol·h-1·gcat-1的甲酸產率。除了還原反應外,C60及其衍生物在如苯甲醇氧化等[39]有機氧化反應中也有很好的表現。但總體上來說,目前基于C60及其衍生物材料的光催化反應還處在發展初級階段,有很多未知的應用值得進一步探索。
3 電化學催化中的應用
如前文所述,不同于其他碳材料,C60本身導電性差,這點限制了C60材料在電催化領域中的應用。然而C60獨特的孔結構以及多變的衍生結構,使其具有潛在的性能調控手段,在為數不多的電化學催化例子中展現出有趣的催化性質。
3.1 甲醇氧化
作為甲醇燃料電池(DMFC)中重要的陽極反應,甲醇電化學氧化由于涉及了6電子轉移的復雜過程,速率通常較慢,所以需要Pt、Pd等貴金屬催化劑加快反應速率。如何降低貴金屬負載量,實現最大催化活性成為甲醇氧化中的主要問題之一[120]。C60作為典型的“零維”材料,具有巨大的比表面積,并且擁有與過渡金屬配位的能力,可以實現貴金屬的高度分散,是一種良好的碳載體。
Vinodgopal等[121]通過電泳的方法在導電玻璃表面沉積了一層均勻的C60團簇薄膜,由于C60本身化學性質穩定,很難失去電子,所以C60薄膜在氧化電位下十分穩定,電沉積Pt顆粒后展現出顯著的電催化活性提升,明顯優于不含C60的Pt修飾電極。然而,單一的C60薄膜并未顯示出對甲醇的催化活性,證明C60在修飾電極中只起到了載體的作用。Lee等[122]發現在貴金屬納米顆粒合成過程中加入不同量的C60可以有效調控粒徑尺寸,得到最小約為2.5 nm左右的尺寸均勻的Pt和PtRu納米顆粒。使用導電碳黑(Vc)負載所得到的貴金屬Pt/C60、PtRu/C60顆粒展現出超越商業催化劑 (E-TEK Pt和E-TEK PtRu)的催化活性,其原因可能來自于C60與貴金屬之間的強電子耦合效應。因為在很多貴金屬/C60體系中都可以觀察到貴金屬XPS價電子結合能發生移動,說明其與C60載體之間存在電子轉移[123-124]。
除了C60之外,一些C60衍生物也被用于甲醇電化學氧化中。Yang等[125]利用富勒醇負載Pd作為催化活性位點,用碳納米管(CNTs)提升導電性,復合材料的電流密度是未添加富勒醇的Pd/CNTs的1.72倍。Zhang等[126]發現吡啶功能化的富勒烯吡咯烷衍生物納米片可以作為有效載體,大幅提升Pt納米片的催化活性。富勒烯吡咯烷衍生物不僅可以增加材料電化學活性比表面積,還能顯著提升催化劑的穩定性。另外,一些富勒烯納米晶以及衍生碳材料也被用于作為載體提升貴金屬催化活性[127-128],并且在其他類似物如乙醇[129]、甲酸[130]、肼[131]以及葡萄糖[132]等物質的氧化中也擁有很高的電催化活性。
3.2 氧氣還原
氧氣還原反應(ORR)不僅是燃料電池和金屬-空氣電池中的陰極反應[133],也是制備綠色氧化劑H2O2的重要反應[134],在電催化反應中占有重要地位。近年來,非金屬催化劑在ORR領域有了長足的發展,大有取代貴金屬催化劑的趨勢。C60具有很多其他碳材料不具備的獨特性質,因此在ORR研究中具有潛在應用價值。
Guan等[37]采用球磨法制備了C60-石墨烯共價化合物,通過在球磨過程中添加LiOH促使C60形成自由基,與石墨烯邊緣基團形成共價鍵。該非金屬碳雜化材料展現出較好的ORR活性,其極限電流值為3.4 mA·cm-2,是天然石墨的2倍,達到了商業Pt/C催化劑的76%。C60因其獨特的缺電子結構,會使石墨烯基面碳原子的電子向C60偏移,石墨烯基面帶微正電荷成為O2的吸附活化的活性位點。Hasanzadeh等[135]通過Birch反應將4-氯苯甲酸修飾的C60衍生物共價橋聯到碳納米管上形成雜化材料。該材料在氧還原反應中,由于受C60衍生物的影響,能以兩電子還原的方式與氧氣作用,其H2O2生成速率為 792.6 mmol·h-1·gcat-1, 法拉第效率達到82.6%,是一種性能優越的合成H2O2催化劑。如圖17所示,Gao等[136]采用單壁碳納米管(SWCNT)吸附C60,C1s XPS譜清晰的表明,隨著C60含量的增高,電子由碳納米管向C60偏移的程度也越大,從而產生局部Lewis堿位點,表現出了優越的全pH ORR性能,并且可以用作析氫和析氧反應催化劑,是一種高效的非金屬多功能催化劑。
除了與其它碳材料雜化作為催化劑外,C60衍生碳材料因為富含五元環C5本征缺陷同樣也展現出良好的ORR活性[42]。如圖18(a~c)所示,在高溫KOH輔助刻蝕的作用下,C60結構遭到破壞,發生開籠重構現象,轉化為富五元環的網狀結構(PD-C)。通過理論計算,發現C5結構能帶隙要比六圓環C6結構小很多,更有利于電子傳遞過程,此外C5結構上的C原子還展現出更大的電荷密度以及更高的O2吸附能(圖18(d)),都證明C5上的碳原子更有可能作為ORR活性位點。ORR性能對比如圖18(e,f)所示,相比于石墨烯衍生的C6結構碳材料,C60衍生的C5結構不論是在起始電位、半波電位還是極限電流密度都遠超C6結構。并且對該材料進一步氮摻雜增加活性位點后,其ORR性能足以媲美商業Pt/C。
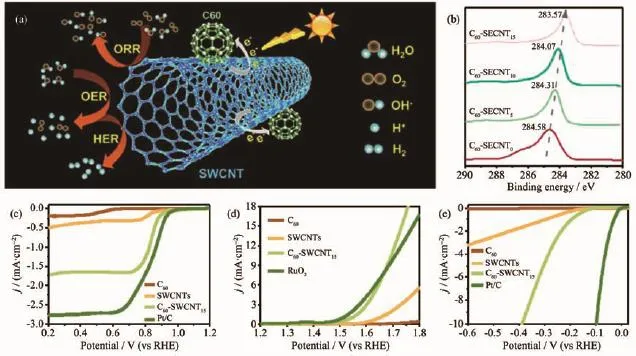
圖17 (a)C60-SWCNT上電子傳遞以及ORR/OER/HER過程示意圖;(b)C1s XPS譜;0.1 mol·L-1KOH 中 ORR(c)、OER(d)以及 HER(e)的線性掃描伏安法(LSV)圖[136]Fig.17 (a)Illustration of charge-transfer process and ORR/OER/HER on C60-SWCNT;(b)C1s XPS spectra;LSV of ORR(c),OER(d)and HER(e)in 0.1 mol·L-1KOH[136]
3.3 電解水
C60在電解水催化劑中主要起到作用有二,一方面C60及其衍生物本身可以作為有效的非金屬催化劑,另一方面也可以通過強電子耦合效應提高C60基復合材料的催化活性。
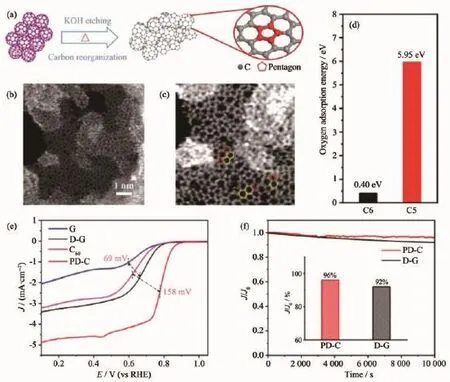
圖18 (a)PD-C合成示意圖;(b,c)PD-C掃描透射電鏡圖;(d)C6和C5結構理論氧氣吸附能;(e,f)氧氣還原反應性能圖[42]Fig.18 (a)Schematic illustration of the synthetic method of PD-C;(b,c)Scanning transmission electron microscope images of PD-C;(d)Calculated oxygen adsorption energies of C6 and C5;(e,f)ORR activities[42]
從前文中我們知道,C60及其衍生物可以在溶液中可逆地接受1~6個電子形成負離子。根據這個性質,Zhuo等[137]通過電化學方法將可溶性的富勒烯醇(C60(OH)8)還原為富勒醇一價負離子,并與支持電解質中的K+或Na+形成穩定的富勒醇負離子鹽沉積在電極表面。利用全氟磺酸樹脂(Nafion)覆蓋沉積了負離子鹽的修飾電極進行HER測試時,他們驚奇地發現,Nafion/C60(OH)8鹽展現出相當高的HER活性,析氫起始電位僅有-0.11 V(vs RHE),Tafel斜率為78 mV·dec-1,活性與MoS2接近。他們認為由于C60(OH)8鹽帶負電,很容易因為靜電作用吸附H+,并且富勒醇表面豐富的羥基也能與H形成氫鍵,可以充當活性位點。此外,C60(OH)8鹽與玻碳電極表面高效的電耦合加快了電子傳遞過程,有利于HER動力學過程。不僅是C60(OH)8鹽,單壁碳管表面吸附的C60分子[136],也能加速C60/CNT界面的電子傳遞速率,表現出了類似的高HER活性,并且還同時具備OER活性,其全解水性能甚至超越了商業Pt/RuO2催化劑(圖 17)。
通過電子耦合加速HER過程也同樣適用于C60與其他材料的組合。譬如,Choi等[138]通過浸漬法將C60團簇沉積到MoS2表面后,發現C60團簇的引入能大幅降低MoS2析氫過電勢,電流密度達到10 mA·cm-2(η10)的過電位從 245 mV降低到了 172 mV(vs RHE),Tafel斜率也 81 mV·dec-1降至 60 mV·dec-1,表明復合材料具有更快的析氫動力學過程。研究發現,C60與MoS2接觸后可以形成p-n結,加速界面電子傳遞速率,改善了原有MoS2基面導電性差的問題。如圖19所示,Du等[139]采用C60分子耦合Ni-Co-P催化劑用作高效HER催化劑,在3.93%(w/w)C60最佳負載量下,起始電位僅有23.8 mV,Tafel斜率為48 mV·dec-1,此外該催化劑還展現出極佳的電化學穩定性。電化學阻抗測試表明同其他碳材料一樣,C60耦合能顯著提高析氫時的電子傳遞過程[140]。這種利用C60耦合增強電化學活性的方法,可以作為一種普適策略應用到其他相關材料的設計之中。
3.4 其他反應
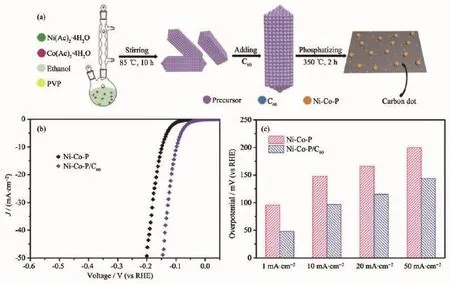
圖19 (a)Ni-Co-P/C60合成示意圖;(b,c)HER性能圖[139]Fig.19 (a)Scheme for synthesis of Ni-Co-P;(b,c)HER performance[139]
在其他電催化新興領域如CO2還原(CO2RR)[141-142]、氮氣還原(NRR)等[143]反應中,關于C60材料的報道寥寥無幾,但從為數不多的例子中卻依然可以看出C60材料所擁有的巨大發展空間。從前文可知,C60自身是性能良好的HER非金屬催化劑,這使得純C60材料在CO2還原反應中以析氫競爭占據主導,CO2還原效率較低,這可能也是未見純C60報道的主要原因。通過引入雜原子或其他金屬對C60材料進行改性是提高CO2還原選擇性的可行途徑。Chen等[144]將尿素與C60衍生物PC61BM混合物置于不同溫度的惰性氣氛中熱處理,制備了一系列具有不同含氮類型的氮摻雜C60材料。其中,800℃熱處理的氮摻雜的PC61BM催化活性最佳,能在較低過電位下保持很高的甲酸產率,其法拉第效率達到了91.2%。這是一個很有趣的結果,我們知道,大部分氮摻雜碳材料在低電位下都是以CO為主產物[145],但氮摻雜的PC61BM卻生成了高附加值的甲酸。對于這種現象,文章中并未給出具體原因,我們猜測可能是與N摻雜后形成的N-C結構與氧的強相互作用有關[146-147]。
電催化合成氨的報道來自于對C60光催化合成氨材料的延伸實驗[148],以γ環糊精/C60((γ-CD)2/C60)包合物作為均相催化劑,用電化學方式提供能量,同樣檢測到NH4+離子生成,再次證明(γ-CD)2/C60體系是一個有效的非金屬催化合成氨體系。令人遺憾的是,無論是CO2RR還是NRR都沒有更多的報道可供我們參考,相關研究有待進一步發掘。
4 總結與展望
發展光催化和電化學催化這2種環境友好的能源轉化新技術,對人類未來能源結構的調整轉變有非常重要的戰略意義。不論是在光催化還是電化學催化中,C60、C60衍生物及其衍生碳材料都因其獨有的性質而展現出非凡的應用前景。我們對C60的結構以及主要材料的合成方法進行了簡單的回顧,并著重對C60及其衍生物材料在光電催化領域中的功能及應用進行了總結。
在光催化中,首先,窄帶隙半導體C60由于具有近乎100%的ISC效率,因此被認為是一種有效的1O2敏化劑,可以在諸多1O2催化的特征反應中用作光催化劑。其次,由于C60獨特的缺電子性質,使其可以作為很好的電子受體和媒介,能有效促進電子和空穴對的分離,并且在接受電子后形成高活性的C60負離子,既能將電子用于氧活性物的生成,也能將電子用作如H+、N2等的還原。此外,C60還能作為電子供體,用作增強寬禁帶半導體對可見光的吸收,以及驅動生物酶體系運轉。C60對許多惰性鍵也有一定的活化作用,是性能良好的非金屬加氫催化劑。
在電化學催化中,盡管C60導電性較差,但依然可以作為有效載體抑制金屬團聚,并且由于C60所具有的強電子耦合效應,能加速復合材料界面電子傳輸速率,提高催化活性。不僅在金屬催化劑中如此,在非金屬催化劑也同樣適用,利用C60與其他碳材料作用,不僅能有效改善C60導電性差的缺點,界面引發的電子偏移,產生Lewis堿位點,用作有效的非金屬活性位點。
盡管C60在光電化學催化中有許多應用,但仍有許多性質需要進一步探索,C60在其中的相關機理研究還不夠深入,許多問題有待解決:
(1)不論是在光催化,還是在電化學催化中,構筑C60界面都能很好地促進電子-空穴對分離、電子傳遞。但目前高效界面的構筑,仍存在較大難度,C60在界面處的分布狀態對催化活性的影響尚不明確,電子在C60單分子層、C60團簇乃至于C60晶體的傳輸過程存在顯著差異,但缺乏系統的實驗以及理論依據。發展新的合成方法與手段,優化C60界面構筑,對提高催化活性,研究電子傳輸路徑都有著巨大意義。
(2)C60相較于其他種類的碳材料最大的優勢就在于它有著海量的衍生物種類。龐大的富勒烯合成化學能夠支撐C60各種性質不同的衍生物的合成,通過改變官能團,對C60衍生物的性質進行調整,從而改變復合材料界面性質、影響底物吸附以及中間產物的選擇,最終實現催化活性和選擇性的調控,具有非常高的研究價值。
(3)目前C60在光電催化中的應用很多都還處于剛剛起步或停滯狀態,如CO2RR、NRR以及有機反應催化等等,需要進一步對相關應用進行深入的挖掘。
- 無機化學學報的其它文章
- 《無機化學學報》投稿須知(NOTICE TO AUTHORS)
- An N-Alkylated 2-(5-Bromo-4-methylthiophen-2-yl)-imidazo[4,5-f]-[1,10]-phenanthroline Rhenium(Ⅰ)Tricarbonyl Compound Showing Aggregation-Induced Emission Enhancement
- Syntheses,Structures and Magnetic Properties of Manganese Phosphonates
- Two Zn(Ⅱ) and Cd(Ⅱ) Metal-Organic Frameworks with Mixed Ligands:Synthesis,Structure,Sorption and Luminescent Properties
- Syntheses and Crystal Structures of Two Copper Complexes Based on Quinolyl and Pyridyl Substituted Triaryltriazoles
- Plasma-Assisted Fabrication of Ferroelectric Flakes with Single-Unit-Cell Thickness and Characterization of Ferroelectricity

