利用血管內超聲結果驗證定量血流分數對冠狀動脈造影臨界病變診斷價值的研究
李夢寰,柳楊,何源,廖深根,姚文明,王驍智,宋雯,王暉
冠狀動脈(冠脈)臨界病變通常指冠脈造影發現血管狹窄40%~70%。這種病變是否引起心肌缺血及是否需要冠脈血運重建治療,仍是臨床面臨的一大困境[1]。目前,冠脈血流儲備分數(FFR)被認為是評估冠脈臨界病變功能學的金標準。數個大規模、多中心、臨床隨機對照研究均顯示:FFR<0.8時冠脈血運重建治療是安全的,FFR指導的經皮冠脈介入治療(PCI)近、遠期主要不良心血管事件發生率均較低[2-6]。但FFR要求術中使用壓力導絲及冠脈內注入血管擴張藥物,且醫療費用高、手術時間長、冠脈內注藥存在風險,其臨床應用受到一定的限制。血管內超聲(IVUS)能提供詳細的冠脈解剖結構、準確的冠脈狹窄程度等信息。有研究顯示,在非左主干病變中,IVUS測得的最小管腔面積(MLA)>4 mm2時,病變相關的主要不良心血管事件發生率低,可行延遲PCI[7-10]。Ben-Dor等[11]發現,IVUS測得的MLA及面積狹窄率(AS)與FFR呈中等程度相關,其對冠脈臨界病變功能學診斷有一定參考意義。
定量血流分數(QFR)是一種無創的、體外評估冠脈功能學的方法,通過兩個不同角度的冠脈造影(CAG)圖像,構建成三維立體的目標冠脈,經血流速度校正得出QFR數值[12]。國內外數項前瞻性、多中心、臨床隨機對照研究證明,QFR與FFR一致性極好,以FFR為心肌缺血評估金標準時,QFR診斷的敏感度及特異度均很高[12-14]。QFR與IVUS參數之間的關系尚不明確。本文旨在使用無創的QFR系統來分析血管功能學意義,并探究其對血管管腔形態學狹窄程度的診斷價值。
1 資料與方法
研究對象:連續篩選2014年1月至2015年1月于南京醫科大學第一附屬醫院心血管內科住院行CAG、目測冠脈病變狹窄為40%~70%且行IVUS檢查的患者。所有CAG及IVUS結果均由兩名冠心病介入技師判斷得出。排除標準:CAG圖像質量不佳,QFR平臺無法自動獲取血管輪廓;目標血管少于2個投照體位,或2個投照方向<25°;選取的2個投照體位血管暴露不充分,重疊過多;左主干病變、分叉病變、慢血流。
資料收集:患者的基本臨床資料及IVUS測量參數(IVUS-MLA、IVUS-AS)均通過回顧住院電子病歷系統獲得;采用QFR測量系統獲得QFR數值及三維CAG定量分析(3D-QCA)參數(包括直徑狹窄率、病變長度、MLA、AS等)。
IVUS操作和測量:所有患者IVUS測定均參照美國心臟病學會制定的IVUS測定技術標準[15],具體過程:(1)采用波士頓公司生產的iLab超聲診斷儀及冠脈超聲成像導管(Atlantis SR),頻率40 Hz,2.9 F血管內超聲探頭;(2)冠脈內注入200 μg硝酸甘油,靜脈予以普通肝素5 000 U,排空超聲成像,導管保護鞘內空氣,經0.014 F導絲將超聲導管送至血管遠端,以0.5~1.0 mm/s速度自動撤回,同時記錄超聲圖像。(3)血管段分析均在心臟舒張期時選擇最狹窄血管橫截面進行。(4)記錄MLA及AS。AS=(參考管腔橫截面積-MLA)/參考管腔橫截面積×100%。
QFR測定方法:執行QFR測量的分析人員已通過QFR分析規范化培訓。納入的病變血管均采用離線QFR測量平臺[版本AngioPlus1.0.1.1,博動醫學影像科技(上海)有限公司,中國],具體操作過程如下[12]:(1)選取兩個投照體位(角度>25°)的目標血管造影圖像;(2)排除過度重疊、短縮的目標血管圖像;(3)分別選取一幀舒張末期且目標血管內對比劑充盈良好的造影圖像;(4)標記兩個圖像中同一處解剖位置,推薦分叉處作為解剖標志;(5)選取需要測量目標血管段,系統將自動描繪出二維血管輪廓(圖1A、1B),且生成目標血管三維圖像(圖1C);(6)獲取對比劑通過目標血管段的幀數以計算通過時間(造影采集速度15楨/s);(7)基于血管三維模型及流體動力學原理,系統計算出病變QFR值(圖1E)。除了QFR數值外,系統還將給出三維QCA數據,如直徑狹窄率、病變長度、MLA、AS等數據,并記錄。以QFR≤0.8作為評估冠脈臨界病變存在心肌缺血的標準[12],并將病變分為QFR≤0.8組及QFR>0.8組。
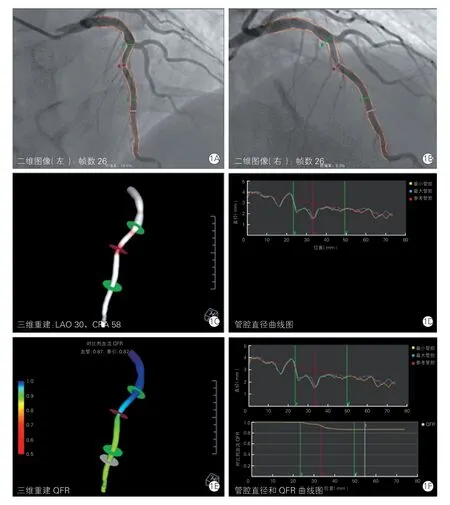
圖1 定量血流分數操作過程
統計學方法:使用SPSS 19.0統計軟件進行數據分析。符合正態分布的計量資料用均數±標準差表示,組間比較采用Studentt檢驗。計數資料用例數和百分比表示,采用卡方檢驗或Fisher確切概率法。通過Pearson及Spearman相關分析分別評估QFR與IVUS參數之間、冠脈病變目測狹窄程度評估及IVUS參數的關系及變異性,計算Cohen's Kappa系數對IVUS參數及QFR的診斷價值進行一致性評價。采用ROC曲線來分析QFR≤0.8對血管顯著狹窄病變的預測價值。P<0.05為差異有統計學意義。
2 結果
符合研究標準的冠脈病變篩選流程:150處冠脈病變符合臨界病變且行IVUS檢查,其中57處病變目標血管兩個投照體位重疊嚴重,21處病變兩個投照方向<25°,9處病變圖像質量不佳,最終共納入57例患者、共62處病變,并完成QFR測定。
57例患者的一般資料和冠脈病變特點(表1):平均年齡為(62.8±9.5)歲,男性占77.2%。4例(7.0%)患者既往行PCI,38例(66.7%)患者診斷為不穩定性心絞痛。50處(80.6%)冠脈病變位于左前降支,13處(21.0%)病變QFR≤0.8。
QFR與IVUS參數相關性分析結果:線性回歸分析(圖2)顯示,QFR與IVUS-MLA(R=0.477,P<0.001)之間存在中等程度正相關,QFR與IVUSAS之間呈較強負相關(R=-0.604,P<0.001);散點圖(圖3)顯示,IVUS-MLA>4 mm2的冠脈病變QFR值均>0.8;在IVUS-MLA≤4 mm2的病變中,52.7%的病變QFR>0.8;在IVUS-MLA<3 mm2的病變中,40%的病變QFR≤0.8;在IVUSAS<70%的病變中,2處(5.1%)病變QFR≤0.8;在IVUS-AS>70%的病變中,11處(47.8%)病變QFR≤0.8。
QFR≤0.8組和QFR>0.8組患者一般臨床資料和冠脈病變特征比較(表2、3):兩組間患者的一般臨床資料差異均無統計學意義。QFR≤0.8組的靶病變IVUS-MLA小于QFR>0.8組[(3.04±0.52)mm2vs.(4.15±1.16)mm2],前者IVUSAS[(76.03%±5.65%) vs.(60.19%±10.79%)]更高(P均<0.001)。3D-QCA分析顯示,QFR≤0.8組的病變血管AS(68.60%±9.71% vs.50.33%±12.44%,P<0.001)、直徑狹窄率(55.92%±8.05% vs.37.74%±7.95%,P<0.001)均高于QFR>0.8組(P均<0.001),但兩組的病變長度無明顯差異[(34.16±23.76)mm vs.(20.45±9.82)mm,P=0.063]。
冠脈病變目測狹窄程度與IVUS-AS相關性散點圖(圖4):冠脈病變目測狹窄程度與IVUS-AS存在一定相關關系,但相關程度較低(rs=0.453,P<0.001)。
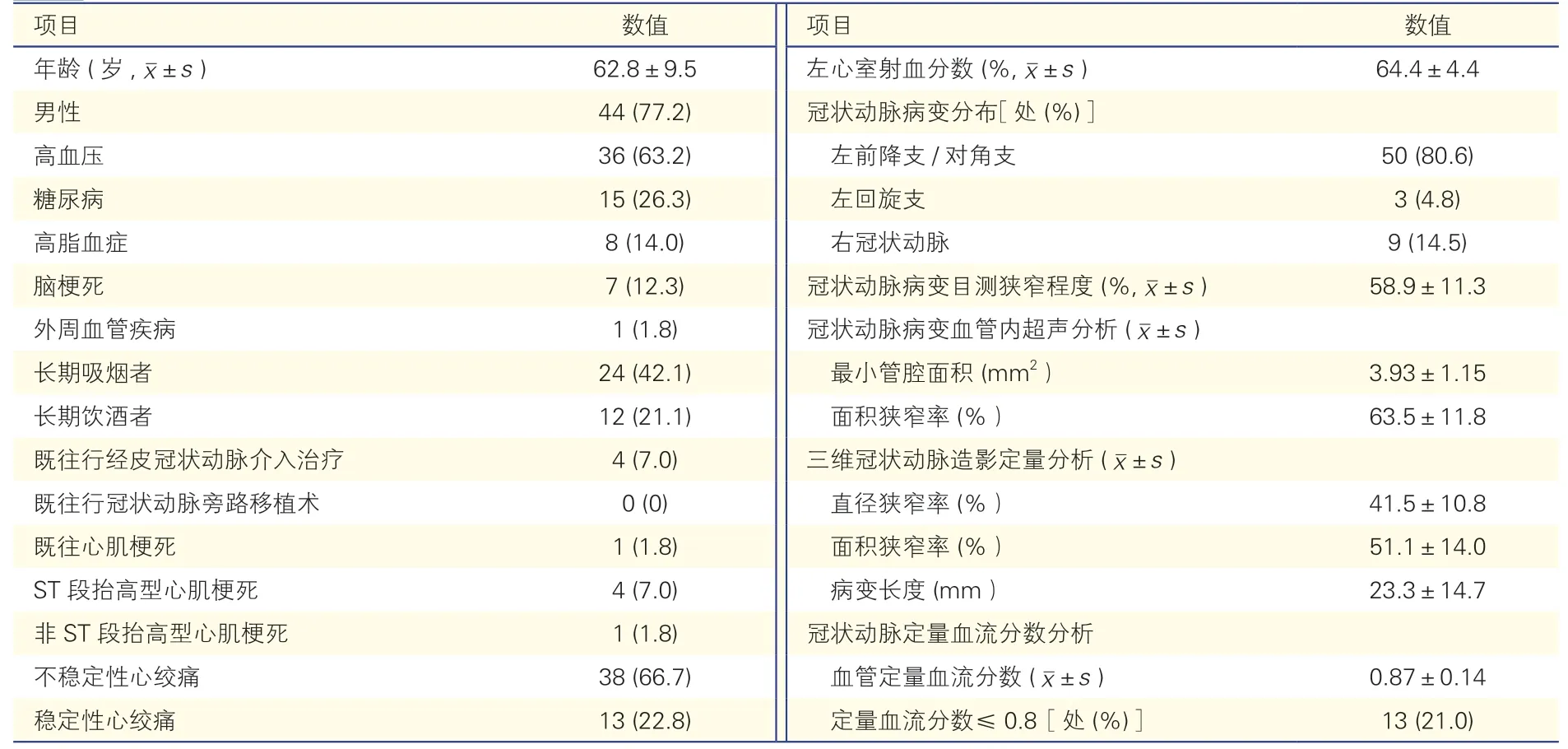
表1 57例患者的一般資料及冠狀動脈病變特點[例(%)]

圖2 IVUS-MLA、IVUS-AS與QFR之間的線性回歸分析圖

圖3 IVUS-MLA(3A)、IVUS-AS(3B) 與QFR之間的散點圖

表2 QFR≤0.8組和QFR>0.8組患者一般臨床資料比較[例(%)]*

表3 QFR≤0.8組和QFR>0.8組患者冠狀動脈病變特征比較

圖4 冠狀動脈病變目測狹窄程度及IVUS-AS相關性散點圖
以IVUS-MLA<4 mm2或IVUS-AS>70%作為血管顯著狹窄診斷標準時,QFR≤0.8作為診斷界值的ROC曲線分析結果(圖5):QFR值預測IVUSMLA<4 mm2的曲線下面積(AUC)為0.822(95%CI:0.717~0.926,P<0.001),QFR≤0.8對應的敏感度為32.4%,特異度為96.0%,陽性預測值為92.3%,陰性預測值為49.0%;QFR值預測IVUS-AS>70%的AUC為0.746(95%CI:0.617~0.876,P=0.001),QFR≤0.8對應的敏感度為47.8%,特異度94.9%,陽性預測值為84.6%,陰性預測值為75.5%。
以IVUS-MLA<4 mm2或IVUS-AS>70%作為冠脈顯著狹窄病變診斷標準時,QFR≤0.8作為診斷界值的一致性分析結果:QFR與IVUS-MLA判斷結果的Cohen's Kappa系數為0.246(95%CI:0.085~0.407,P=0.007),具有一般強度一致性;而QFR與IVUS-AS判斷結果的Cohen's Kappa系數為0.469(95%CI:0.246~0.692,P<0.001),具有中等強度一致性。

圖5 以IVUS-MLA<4 mm2(5A)或IVUS-AS>70%(5B)作為血管顯著狹窄診斷標準時QFR≤0.8作為診斷界值的ROC曲線
3 討論
近年來,用無創方法來識別冠脈狹窄性病變是否存在心肌缺血越來越受到關注。FAVOR ⅡChina研究顯示,QFR與基于壓力導絲的FFR測定結果一致性達92.7%[12],該研究也在國外其他多個中心得到了驗證[14,16-17]。本研究比較了QFR與IVUS參數之間的關系,我們發現QFR與IVUSMLA(R=0.477,P<0.001)存在中等程度相關,與IVUS-AS相關性更強(R=-0.604,P<0.001)。當QFR≤0.8時,IVUS-MLA更小,IVUS-AS更高。Ben-Dor等[11]比較了FFR與IVUS參數的關系,發現FFR與MLA呈正相關,與AS呈負相關,并具有中等程度相關;因FFR與QFR極好的一致性,本研究結果在一定程度上為上述研究結果提供了證據支持。我們的研究結果顯示,QFR≤0.8組中的冠脈病變長于QFR>0.8組,但差異并無統計學意義(P=0.067),也許增加樣本量,兩組間的冠脈病變長度差異可能會達到統計學意義。
在臨床實踐中,血管狹窄程度越嚴重往往提示心肌缺血越重。多項回顧性研究比較了IVUS參數與FFR之間的關系,均提示血管狹窄越嚴重,FFR值越低[11,18]。因QFR具有無創的優點,我們嘗試分析QFR對血管顯著狹窄病變的診斷價值。一致性檢驗分析顯示,以IVUS-MLA及IVUS-AS作為診斷血管顯著狹窄病變標準時,QFR≤0.8與IVUS的診斷一致性較好。QFR≤0.8對IVUS-MLA<4 mm2診斷血管顯著狹窄病變的敏感度為32.4%,特異度為96.0%,陽性預測值為92.3%,陰性預測值為49.0%;QFR≤0.8對IVUS-AS>70%診斷血管顯著狹窄病變的敏感度為47.8%,特異度為94.9%,陽性預測值為84.6%,陰性預測值為75.5%。該研究結果顯示,QFR對血管顯著狹窄病變具有較高的診斷價值。
我們希望通過使用無創的方法,除了獲取靶血管功能學信息,還可以了解靶血管形態學特征,推測靶血管病變的狹窄程度,為術者術中決策的制定提供更多信息。本研究的局限性在于,研究結果由單中心樣本得出,樣本量偏少,仍需多中心數據進一步驗證。

