MALDI-TOF-MS和RT-qPCR對于SLCO1B1和ApoE多態性檢測的比較
葉阿里,鄒雨桐,張海燕,吳 潔,張 睿,張曉峰,馬慶偉
(1.中國醫學科學院 北京協和醫學院 北京協和醫院 檢驗科, 北京 100730; 2.北京毅新博創生物科技有限公司, 北京 102206)
他汀類藥物(statins)是臨床常用的調脂藥物之一,也是預防心血管疾病風險的首選用藥[1]。然而,他汀類藥物的治療效果和臨床適用性存在明顯的個體差異,他汀相關性肌病(statin-associated muscle symptoms,SAMS)是最普遍的他汀藥物不良反應[2]。SLCO1B1編碼有機陰離子轉運多肽(OATP1B1),主要定位于人類肝細胞膜上,介導他汀類藥物的轉運[3],研究表明SLCO1B1單核苷酸多態性位點(single nucleotide polymorphism,SNP),rs2306283(388A>G)和rs4149056(521T>C) 與SAMS密切相關[4]。另一個與他汀藥物療效相關的基因是ApoE,其表達產物載脂蛋白E通過與LDL受體結合,調控膽固醇和其他脂質的轉運。ApoE的SNP位點rs429358(388T>C)和rs7412 (526C>T),可構成ε3(388T-526C), ε2(388T-526T)和ε4(388C-526C) 3種單倍體,及6種基因型:ε2ε2、ε2ε3、ε2ε4、ε3ε3、ε3ε4、ε4ε4。實時熒光定量PCR(RT-qPCR)是目前臨床實驗室最常用的檢測SLCO1B1和ApoE多態性的技術,然而該方法僅適用于個別SNP位點的檢測。近年來,核酸質譜技術在基因組學領域得到了飛速發展,基質輔助激光解析電離飛行時間質譜(matrix-assisted laser desorption ionization time of flight mass spectrometry, MALDI-TOF-MS)因其可同時完成多個SNP位點的檢測,準確性高、成本較低等優勢已逐漸成為SNP分析的新方法。本研究通過對MALDI-TOF-MS和RT-qPCR兩種技術進行方法學比對,評價MALDI-TOF-MS是否能應用于臨床脂質和藥物代謝相關基因的檢測,從而指導臨床他汀類藥物的使用。
1 材料與方法
1.1 材料
1.1.1 病例:選取2018年7月至2018年9月在北京協和醫院就診,臨床診斷為高脂血癥、高血壓或動脈粥樣硬化的患者71例,其中男性32例,女性39例。收取其常規檢測后剩余無污染的EDTA抗凝外周血標本,用于后續基因組DNA提取和基因多態性檢測。納入者的基本信息和生化檢測結果由北京協和醫院臨床實驗室信息管理系統獲取,整個分析過程進行隱私化處理。此研究經中國醫學科學院北京協和醫院倫理委員會批準(批準文號:S-K1108),并免除知情同意。
1.1.2 試劑及試劑盒:MALDI-TOF-MS(Clin-TOF Ⅱ)配套高血脂相關基因檢測試劑盒(微陣列芯片-飛行時間質譜法)、軟件分析系統(北京毅新博創生物科技有限公司);飛行時間質譜系統核酸樣本純化試劑(北京毅新博創生物科技有限公司,京經械備20190095號);人SLCO1B1和ApoE多態性檢測試劑盒(PCR-熒光探針法)(武漢友芝友醫療科技有限公司,國械注準20153400245);全血基因組DNA提取試劑盒(西安天隆科技有限公司)。
1.2 方法
1.2.1 基因組DNA的提取:取200 μL EDTA-K2抗凝外周血,使用NP968全自動核酸提取儀及配套天隆全血提取試劑盒,按照說明書操作提取基因組DNA,使用Thermo MultiskanGO核酸分析儀測定提取DNA的濃度和純度,取濃度在5 mg/L~200 mg/L,A260/280在1.7~2.0的樣本用于后續實驗,置-20 ℃保存。
1.2.2 MALDI-TOF-MS檢測SLCO1B1和ApoE多態性:PCR擴增:PCR擴增體系包括1 μL基因組DNA、0.2 μL PCR酶、1 μL PCR緩沖液、1 μL擴增引物和1.8 μL增效劑,擴增條件為50 ℃反應2 min;95 ℃預變性2 min;95 ℃變性30 s,56 ℃退火30 s,72 ℃延伸1 min, 45個循環后72 ℃持續5 min。SAP酶消化:將蝦堿性磷酸酶0.5 μL及其反應液1.5 μL加入上一步的PCR擴增產物中,37 ℃保溫30 min后,65 ℃保溫5 min。單堿基延伸:在SAP酶消化后的產物中加入延伸反應混合物,包括0.23 μL延伸酶、0.83 μL反應液和0.94 μL延伸引物,進行延伸反應,延伸反應條件為94 ℃預變性30 s;94 ℃變性5 s,56 ℃退火5 s,80 ℃延伸5 s,內部5個循環,持續外部40個循環;最后72 ℃延伸3 min。MALDI-TOF-MS檢測:延伸反應完畢后,向每PCR管/孔延伸產物中加入41 μL超純水和15 mg飛行時間質譜系統核酸樣本純化試劑,顛倒混勻5 min完成脫鹽,5 000 r/min離心1 min。取經過脫鹽處理的樣品點在樣品靶上使之自然結晶;而后,通過MALDI-TOF-MS(Clin-TOF II)進行檢測,MALDI-TOF-MS采用的是樣品與基質混合進樣,激光解析方式電離以及飛行時間方法進行質量分析。樣本檢測結果由配套分析軟件檢測質譜峰并判讀所檢測基因位點的基因型。
1.2.3 RT-qPCR檢測SLCO1B1和ApoE多態性:用人SLCO1B1和ApoE多態性檢測試劑盒,按照試劑盒操作說明要求配制PCR體系。簡單來說,試劑盒中包括4種反應液,分別針對SLCO1B1 rs2306283 (388A>G)、rs4149056(521T>C)和ApoE rs429358(388T>C)、rs7412(526C>T) 4個基因位點,每人份需配置4個反應體系,將4種反應液分裝到PCR管中,23 μL/管,再加入2 μL基因組DNA模板。在Roche LightCycler 480實時熒光定量PCR儀上完成這4個基因位點的檢測。PCR反應條件為:37 ℃ 10 min;95 ℃ 5 min;95 ℃ 15 s,60 ℃ 60 s,40個循環。檢測結果通過使用“Endpoint Genotyping”(終點基因分型)進行結果判讀。
1.3 統計學分析
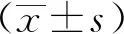
2 結果
2.1 研究對象的基因與基因型分布
71例患者包括男性32例,平均年齡為(57±13)歲,女性39例,平均年齡為(64±9)歲。分別用RT-qPCR和MALDI-TOF-MS對這71例患者的SLCO1B1 rs2306283 (388A>G)、rs4149056 (521T>C)和ApoErs429358 (388T>C)、rs7412 (526C>T) 4個基因位點進行檢測(圖1,2)。
2.2 兩種方法檢測SLCO1B1和ApoE的基因型結果的一致性(表1,2)
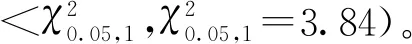
3 討論
作為治療脂代謝紊亂的一線藥物,他汀類藥物雖具有很好的降脂作用,但其所產生的包括他汀相關性肌病在內的副作用及治療效果的個體差異已成為困擾臨床用藥的難題,這種差異被證實與基因多態性密切相關[5]。SLCO1B1 rs4149056(521T>C)和rs2306283(388A>G)多態性,ApoErs429358(388T>C)和rs7412(526C>T)多態性是種族多樣化人群中普遍發生的變異,許多體外和臨床研究已經評估了這些變異對個體藥物配置和反應差異的影響[6-7]。
本研究中SLCO1B1 388A>G位點的基因型分布為AA(4.32%)
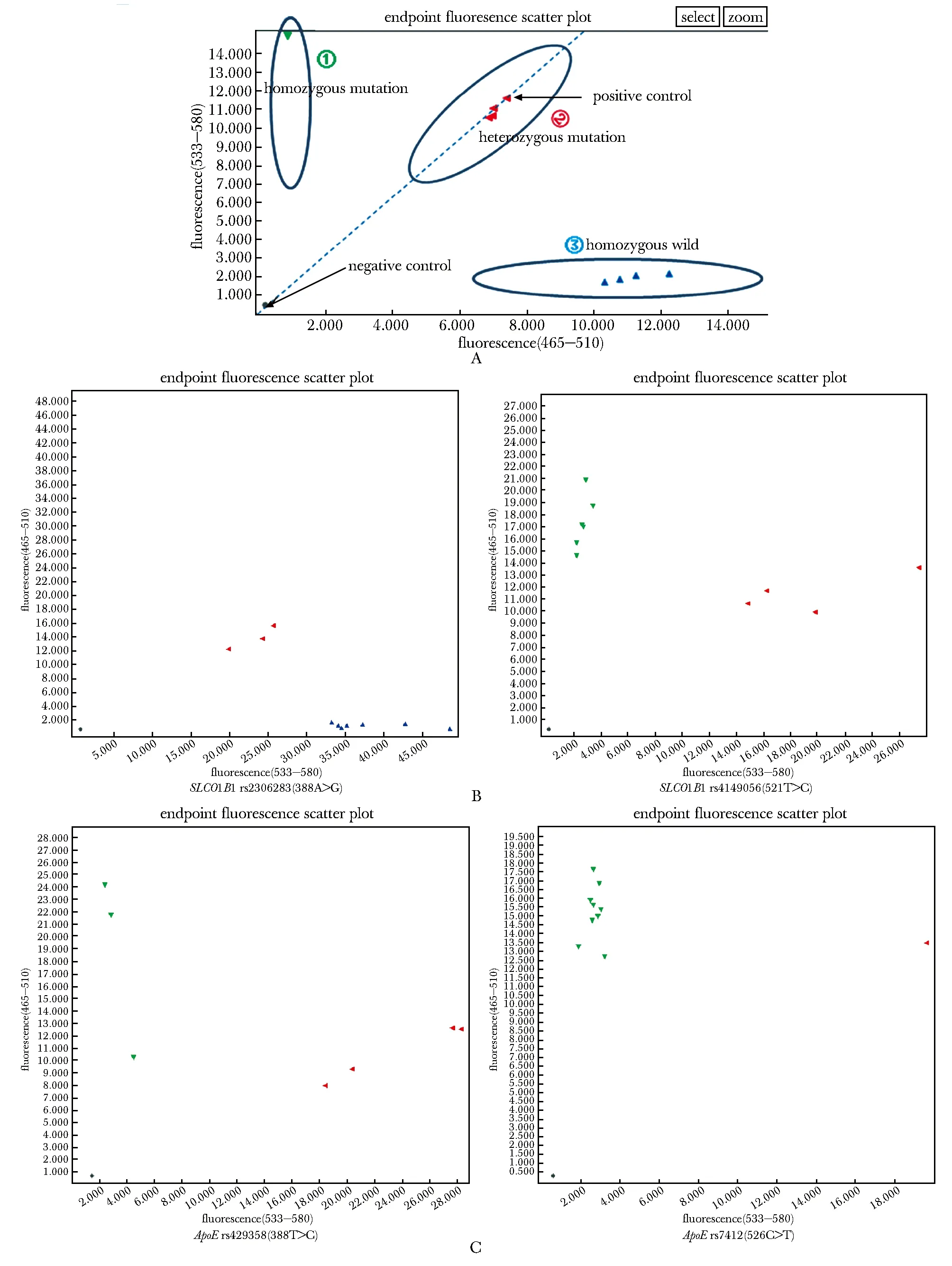
A.criteria for interpreting results by RT-qPCR; B.SLCO1B1 SNPs analysis; C.ApoE SNPs analysis
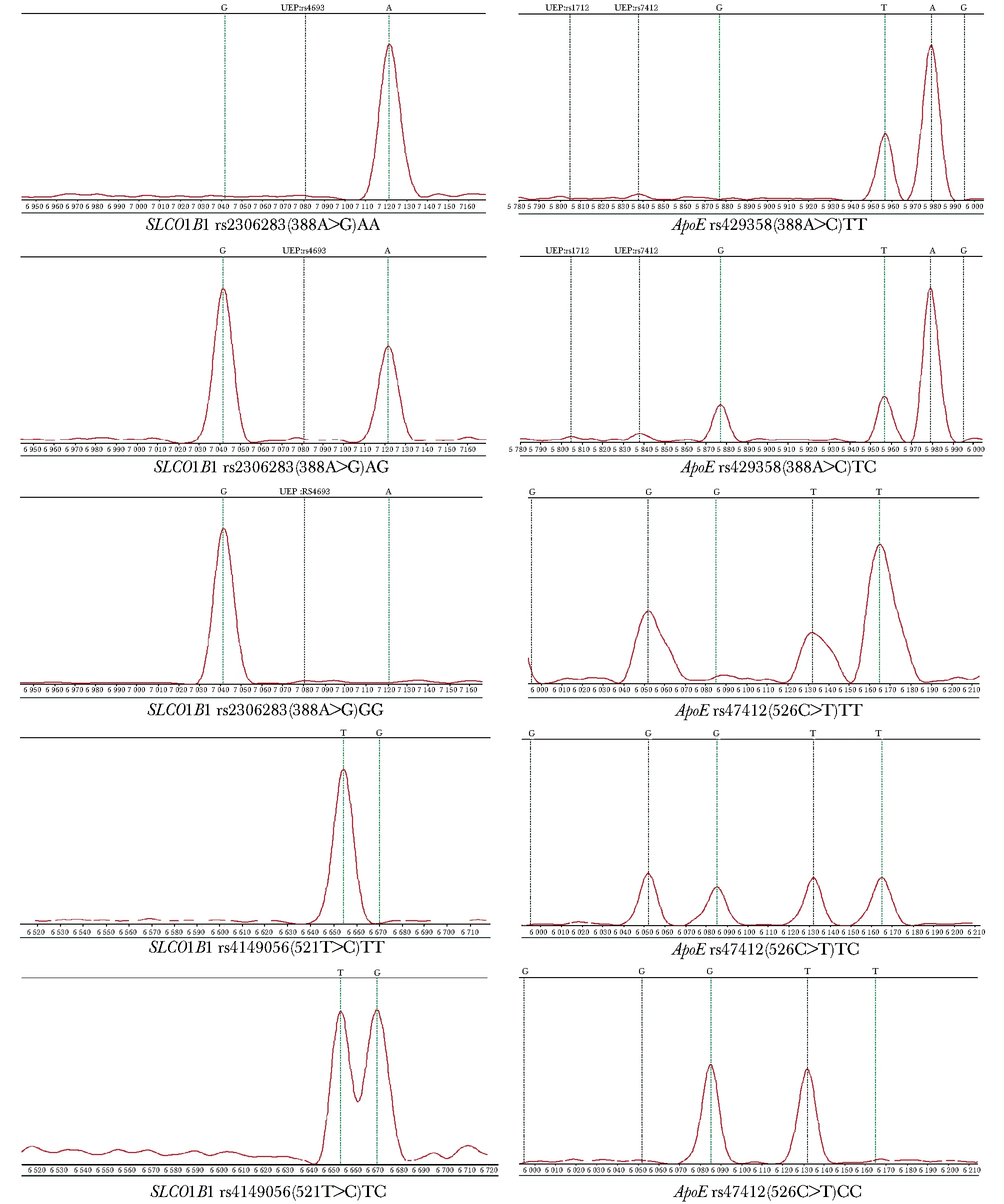
圖2 MALDI-TOF-MS檢測SLCO1B1和ApoE多態性位點
目前市場上檢測SNP的商品化試劑盒多是基于RT-qPCR或基因芯片法,這些方法基于化學(熒光)方法,依賴于核苷酸的互補性對核酸序列進行分析,對序列的長度、復雜性和反應條件等具較高的要求,易受多種化學因素的影響,從而導致檢測結果的偏差。MALDI-TOF-MS依賴于分子量這一物理參數,是根據核苷酸組成分子被電離后在真空管中的飛行時間來確定其分子量大小,最終確定核苷酸序列。此外,RT-qPCR技術只適用于對有限的基因位點進行檢測,MALDI-TOF-MS可在同一反應體系中對多個SNP位點進行多重檢測和分析,可大幅提高檢測通量和效率,是對現有RT-qPCR的重要補充。本研究發現,雖然MALDI-TOF-MS與RT-qPCR兩種方法在檢測結果上具高度一致性,但有1例樣本出現差異,MS復檢時得到與RT-qPCR一致的結果,說明重復檢測可提高MALDI-TOF-MS的準確性,建議在實際應用中針對每個樣本設立3個重復檢測。
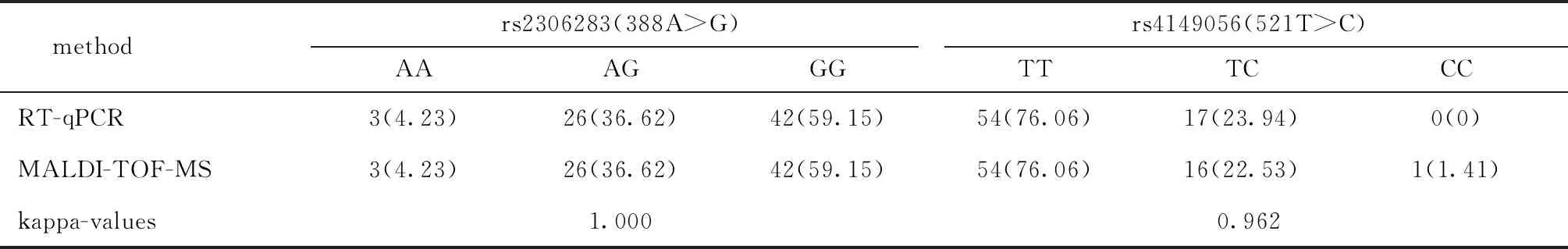
表1 研究對象SLCO1B1的基因型分布
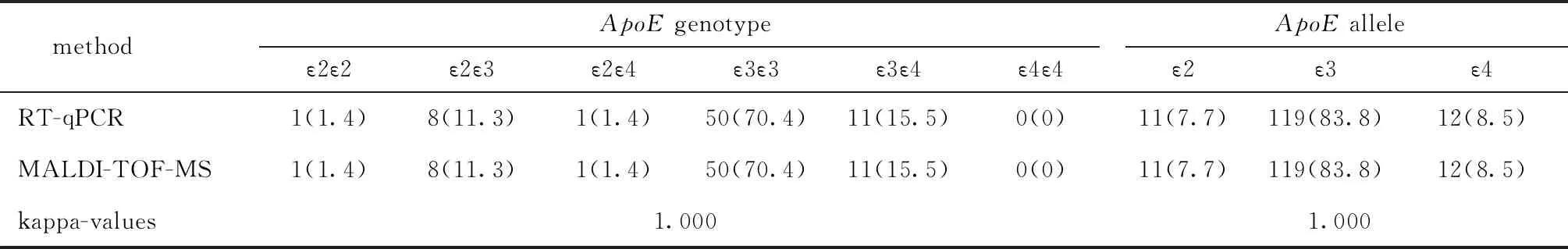
表2 研究對象ApoE基因型及等位基因的分布
本研究首次建立了MALDI-TOF-MS對于SLCO1B1和ApoE常見多態性位點的檢測方法,并與RT-qPCR技術進行比較,結果表明MALDI-TOF-MS與RT-QPCR的檢測結果有較好的一致性。綜上所述,MALDI-TOF-MS技術可應用于脂質和藥物代謝相關基因檢測,其臨床適用性仍需結合臨床具體用藥情況和個體化的反應進一步分析。

