lncRNA LEF1-AS1 通過靶向miR-612 調(diào)控皮膚鱗狀細胞癌細胞株增殖、凋亡、遷移侵襲的體外實驗研究
鄭云鵬 李旭陽 蔡丙杰 李冬芹 尹光文
鄭州大學第一附屬醫(yī)院皮膚科450052
皮膚鱗狀細胞癌(簡稱皮膚鱗癌)是一種常見的皮膚惡性腫瘤,部分患者可發(fā)生快速轉(zhuǎn)移,影響皮膚外觀和預后[1-4]。早期快速準確地控制腫瘤進展對患者具有重要意義。長鏈非編碼RNA(long noncoding RNA,lncRNA)和微小RNA(microRNA,miR)均為常見的非編碼RNA(non-coding RNA,ncRNA),其在機體癌癥中的促進功能或者抑制功能均已得到很多研究的認可[5-6]。lncRNA LEF1-AS1 在多種癌癥中均已有研究報道,但是在皮膚鱗癌中的功能及機制尚不清楚。本實驗通過生物信息學預測LncRNA LEF1-AS1 的靶向miRNA,發(fā)現(xiàn)LncRNA LEF1-AS1 與miR-612 有結(jié)合位點,且研究報道LncRNA LINC00460通過使miR-612海綿化可促進頭頸部鱗癌細胞的增殖,遷移和侵襲[7]。但miR-612在皮膚鱗癌中的功能尚不清楚。本研究以皮膚鱗癌細胞SCC13 為研究對象,檢測lncRNA LEF1-AS1、miR-612的表達,觀察干擾lncRNA LEF1-AS1、miR-612的表達對其增殖、遷移、侵襲和凋亡的影響。
材料與方法
一、實驗材料
收集鄭州大學第一附屬醫(yī)院2018 年3 月至2019 年6 月外科手術(shù)切除的20例皮膚鱗癌及對應的癌旁組織。本研究符合2013 年修訂的《赫爾辛基 宣 言》(https://www.wma.net/policies-post/wmadeclaration-of-helsinki-ethical-principles-for-medicalresearch-involving-human-subjects/)的要求,所有受試者均簽署知情同意書。
SCC13細胞(編號:CVCL_4029)購自美國模式培養(yǎng)物集存庫。實時熒光定量逆轉(zhuǎn)錄PCR(qRTPCR)檢測試劑盒、反轉(zhuǎn)錄試劑盒(日本Takara 公司);LipofectamineTM2000 脂質(zhì)體轉(zhuǎn)染試劑盒(美國Invitrogen 公司,規(guī)格:1.5 ml);CCK8 細胞計數(shù)試劑盒(日本同仁化學研究所);膜聯(lián)蛋白V-異硫氰酸熒光素和碘化丙錠(Annexin V-FITC/PI)雙染細胞凋亡檢測試劑盒(南京諾唯贊生物科技有限公司);遷移實驗(Transwell)小室(美國Corning 公司);雙熒光素酶報告基因檢測試劑盒(美國Promega 公司)。 流 式 細 胞 儀(Cytomics FC 500,美 國BECKMANCOULTER公司)。
二、qRT-PCR法檢測組織中皮膚鱗癌及癌旁組織中LEF1-AS1、miR-612的表達
將充分研磨的組織用RNA提取試劑盒抽提總RNA,再用反轉(zhuǎn)錄試劑盒將其合成cDNA,采用qRT-PCR 檢測試劑盒檢測lncRNA LEF1-AS1、miR-612的表達,以GAPDH、U6為內(nèi)參,引物由南京科佰生物科技有限公司合成,序列見表1,以2-△△Ct法分析lncRNA LEF1-AS1、miR-612的相對表達量。
三、SCC13細胞的培養(yǎng)與分組
使用含10%胎牛血清的DMEM 培養(yǎng)基在37 ℃、5% CO2的細胞培養(yǎng)箱中常規(guī)培養(yǎng)和傳代SCC13 細胞。按脂質(zhì)體LipofectamineTM2000 試劑的說明書操作將lncRNA LEF1-AS1 的干擾無意義序列(si-NC)、lncRNA LEF1-AS1 的干擾序列(si-LEF1-AS1)、miR-612 過表達的無意義序列(miR-NC)、miR-612 過表達基因序列(miR-612)轉(zhuǎn)染至SCC13 細胞,記為si-NC 組、si-LEF1-AS1 組、miR-NC組、miR-612組;將si-LEF1-AS1分別與抑制miR-612 表達的無意義序列(anti-miR-NC)、抑制miR-612 表達基因序列(anti-miR-612)共轉(zhuǎn)染至SCC13 細胞中,記為si-LEF1-AS1+anti-miR-NC 組和si-LEF1-AS1+anti-miR-612 組;各組在轉(zhuǎn)染8 h后棄去培養(yǎng)基繼續(xù)培養(yǎng)48 h,用qRT-PCR法檢測轉(zhuǎn)染的效率,確定轉(zhuǎn)染成功后用于后續(xù)實驗研究。
四、干擾lncRNA LEF1-AS1表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響
取si-NC 組、si-LEF1-AS1 組SCC13 細胞,采用CCK8 法檢測細胞增殖,流式細胞儀分析細胞的凋亡情況,Transwell試驗檢測細胞的遷移、侵襲能力,Western印跡檢測增殖相關(guān)蛋白細胞周期蛋白依賴激酶1(cyclinD1)、細胞周期蛋白依靠性激酶抑制劑(p21),凋亡相關(guān)蛋白Bcl-2、Bcl-2 相關(guān)X 蛋白(Bax),遷移及侵襲相關(guān)蛋白基質(zhì)金屬蛋白酶2(MMP-2)、基質(zhì)金屬蛋白酶9(MMP-9)的相對水平。
1.CCK8 法檢測細胞增殖:以100 μl、5×105個細胞置于96孔板中,培養(yǎng)24、48、72 h,加入20 μl的CCK8溶液,使用酶標儀在490 nm波長檢測各組細胞的吸光度(A值)。以A值反映細胞的增殖能力。
2.流式細胞儀分析細胞凋亡:收集細胞,使用結(jié)合緩沖液重懸,按照Annexin V-FITC/PI雙染細胞凋亡檢測試劑盒說明書要求操作,避光孵育待測細胞,快速上流式細胞儀檢測分析細胞的凋亡情況。凋亡率(%)=早期凋亡率+晚期凋亡率。
3.Transwell 試驗檢測細胞的遷移、侵襲能力:收集細胞,先用不含血清的培養(yǎng)基培養(yǎng)24 h,取1×105/ml 細胞100 μl 均勻鋪在上室表面,下室內(nèi)加入700 μl含有血清的培養(yǎng)基,將小室置于恒溫培養(yǎng)箱中培養(yǎng)24 h,取出小室后,進行甲醇固定、結(jié)晶紫染色,顯微鏡下觀察穿膜細胞數(shù),取5個視野拍照,計算平均值。選用含有基質(zhì)膠的小室檢測細胞的侵襲能力,不含基質(zhì)膠的小室檢測細胞的遷移能力。

表1 實時熒光定量逆轉(zhuǎn)錄PCR引物信息
4.Western印跡試驗:收集細胞,裂解后提取總蛋白,使用BCA 法對蛋白進行定量。目的蛋白沸水浴變性處理,取上清液上樣電泳,經(jīng)轉(zhuǎn)膜、封閉后,將膜轉(zhuǎn)移至一抗溶液(1∶500)中,4 ℃下孵育過夜。將膜轉(zhuǎn)移至相應的二抗稀釋液(1∶1 000)中,室溫孵育2 h,通過超敏ECL 發(fā)光試劑盒顯影、定影、曝光。使用Quantity One 4.6軟件分析條帶灰度值,以GAPDH 為參照,以目的條帶灰度值與GAPDH 條帶的比值為cyclinD1、p21、Bax、Bcl-2、MMP-2、MMP-9的相對表達水平。
五、過表達miR-612對SCC13細胞增殖、凋亡、遷移及侵襲的影響
取miR-NC 組、miR-612 組SCC13 細胞,采用CCK8 法檢測細胞增殖,流式細胞儀分析細胞的凋亡情況,Transwell 試驗檢測細胞的遷移、侵襲能力,Western 印跡檢測cyclinD1、p21、Bax、Bcl-2、MMP-2、MMP-9的相對水平。
六、lncRNA LEF1-AS1 與miR-612 的結(jié)合能力檢測
用LncBase Predicted v.2 在線預測網(wǎng)站(http://carolina.imis.athena - innovation.gr/diana_tools/web/index.php?r=lncbasev2%2Findex-predicted)預 測lncRNA LEF1-AS1 與miR-612 之間的互補序列,根據(jù)互補序列設計合成有互補結(jié)合位點的WT-LEF1-AS1序列和無互補結(jié)合位點的MUT-LEF1-AS1序列(圖1),并將其克隆至熒光載體上,構(gòu)建熒光素酶報告基因質(zhì)粒,分別與miR-NC、miR-612 共轉(zhuǎn)染至SCC13細胞,轉(zhuǎn)染48 h后按照雙熒光素酶報告基因檢測試劑盒要求操作,檢測細胞的螢火蟲熒光素酶活性和海腎熒光素酶活性,以二者的比值表示報告基因的表達水平。
將LEF1-AS1過表達的無意義序列(LEF1-AS1-NC)、LEF1-AS1 過表達基因序列(LEF1-AS1)、si-NC、si-LEF1-AS1 轉(zhuǎn)染至SCC13 細胞中,采用qRT-PCR 法檢測各組細胞miR-612 的相對表達水平,以檢測lncRNA LEF1-AS1 對miR-612 的調(diào)控作用。

圖1 根據(jù)長鏈非編碼RNA LEF1-AS1與微小RNA-612(miR-612)之間的互補序列設計的互補和不互補序列WT-LEF1-AS1:有互補結(jié)合位點的序列;MUT-LEF1-AS1:無互補結(jié)合位點的序列
七、干擾lncRNA LEF1-AS1 及抑制miR-612 表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響
取si-NC 組、si-LEF1-AS1 組、si-LEF1-AS1 +anti-miR-NC 組、si-LEF1-AS1 + anti-miR-612 組細胞,采用qRT-PCR法檢測各組細胞miR-612的相對表達,CCK8法檢測細胞增殖,流式細胞儀分析細胞的凋亡情況,Transwell 試驗檢測細胞的遷移、侵襲能力,Western 印跡檢測cyclinD1、p21、Bax、Bcl-2、MMP-2、MMP-9的相對水平。
八、統(tǒng)計學處理
結(jié) 果
一、lncRNA LEF1-AS1 和miR-612 在皮膚鱗癌組織中的表達
皮膚鱗癌組織中的lncRNA LEF1-AS1 相對表達(2.93±0.29)高于癌旁皮膚組織(1.00±0.08,t=28.69,P <0.001),miR-612 的相對表達(0.52 ±0.05)低于癌旁皮膚組織(1.01±0.09,t=21.28,P <0.001)。
二、干擾lncRNA LEF1-AS1 表達對SCC13 增殖、凋亡、遷移及侵襲的影響
見圖2、表2。si-LEF1-AS1 組細胞lncRNA LEF1-AS1 相對表達低于si-NC 組(P <0.05);24、48、72 h 時細胞增殖能力低于si-NC 組(均P <0.05),細胞凋亡率高于si-NC 組(P <0.05),遷移、侵襲細胞數(shù)均低于si-NC組(均P <0.05)。
Western 印跡顯示,si-LEF1-AS1組細胞增殖相關(guān)蛋白cyclinD1相對水平低于si-NC 組(P <0.05),p21 相對水平高于si-NC 組(P <0.05);凋亡相關(guān)蛋白Bcl-2相對水平低于si-NC組(P <0.05),Bax相對水平高于si-NC 組(P <0.05);遷移、侵襲相關(guān)蛋白MMP-2、MMP-9 相對水平均低于si-NC 組(均P <0.05)。見圖3、表3。
三、miR-612 過表達對SCC13 細胞增殖、凋亡、遷移及侵襲的影響
miR-612 組細胞miR-612 相對表達高于miRNC 組(P <0.05);24、48、72 h 時miR-612 組細胞增殖能力低于miR-NC 組(均P <0.05);miR-612組細胞凋亡率高于miR-NC 組(P <0.05);miR-612 組遷移、侵襲細胞數(shù)均低于miR-NC組(均P <0.05)。見圖4、表4。
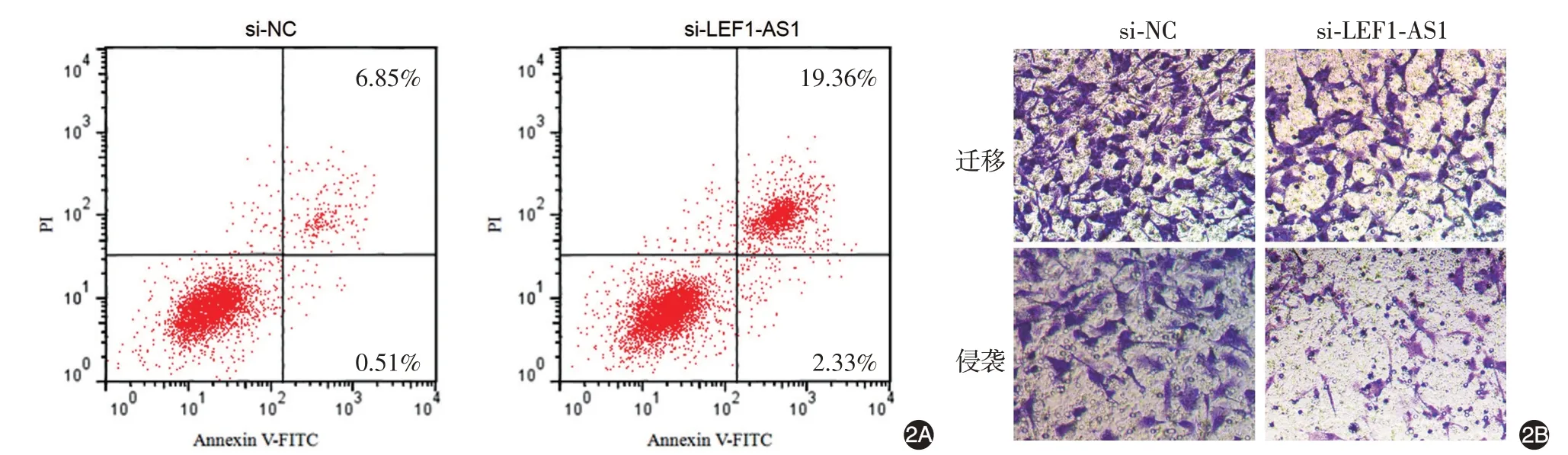
圖2 干擾長鏈非編碼RNA(lncRNA)LEF1-AS1表達后SCC13細胞的凋亡、遷移、侵襲能力 2A:流式細胞儀檢測,si-LEF1-AS1組細胞凋亡率高于si-NC組;2B:Transwell試驗檢測,si-LEF1-AS1組遷移、侵襲細胞數(shù)均低于si-NC組。si-NC,轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1,轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列
表2 干擾長鏈非編碼RNA(lncRNA)LEF1-AS1表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響(±s)
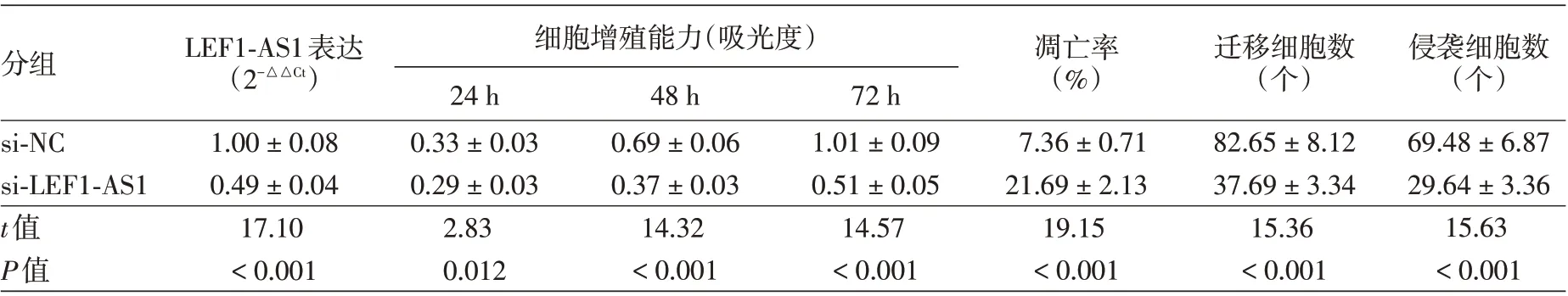
表2 干擾長鏈非編碼RNA(lncRNA)LEF1-AS1表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響(±s)
注:n=9。si-NC:轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1:轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列
分組LEF1-AS1表達(2-△△Ct)細胞增殖能力(吸光度)24 h 0.33±0.03 0.29±0.03 2.83 0.012 48 h 0.69±0.06 0.37±0.03 14.32<0.001 72 h 1.01±0.09 0.51±0.05 14.57<0.001凋亡率(%)遷移細胞數(shù)(個)侵襲細胞數(shù)(個)si-NC si-LEF1-AS1 t值P值1.00±0.08 0.49±0.04 17.10<0.001 7.36±0.71 21.69±2.13 19.15<0.001 82.65±8.12 37.69±3.34 15.36<0.001 69.48±6.87 29.64±3.36 15.63<0.001
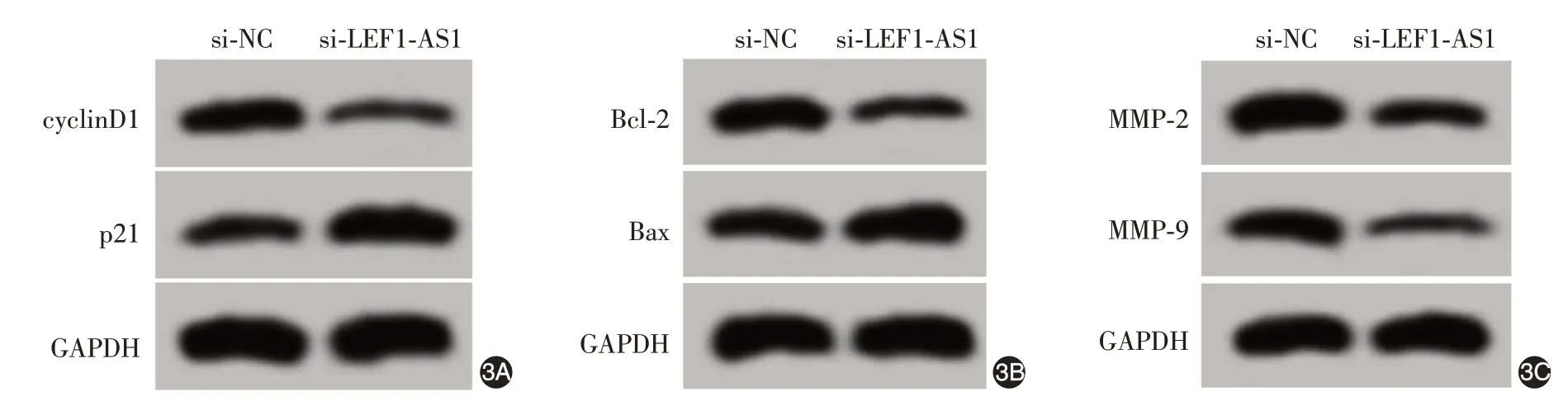
圖3 Western 印跡檢測干擾長鏈非編碼RNA(lncRNA)LEF1-AS1 表達后SCC13 細胞增殖、凋亡、遷移和侵襲相關(guān)蛋白的表達 3A:si-LEF1-AS1 組cyclinD1 相對水平低于si-NC 組,p21 相對水平高于si-NC 組;3B:Bcl-2 相對水平低于si-NC 組,Bax 相對水平高于si-NC 組;3C:MMP-2、MMP-9相對水平均低于si-NC組。si-NC,轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1,轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列
表3 Western印跡檢測干擾lncRNA LEF1-AS1表達后SCC13細胞增殖、凋亡、遷移和侵襲相關(guān)蛋白的表達(±s)
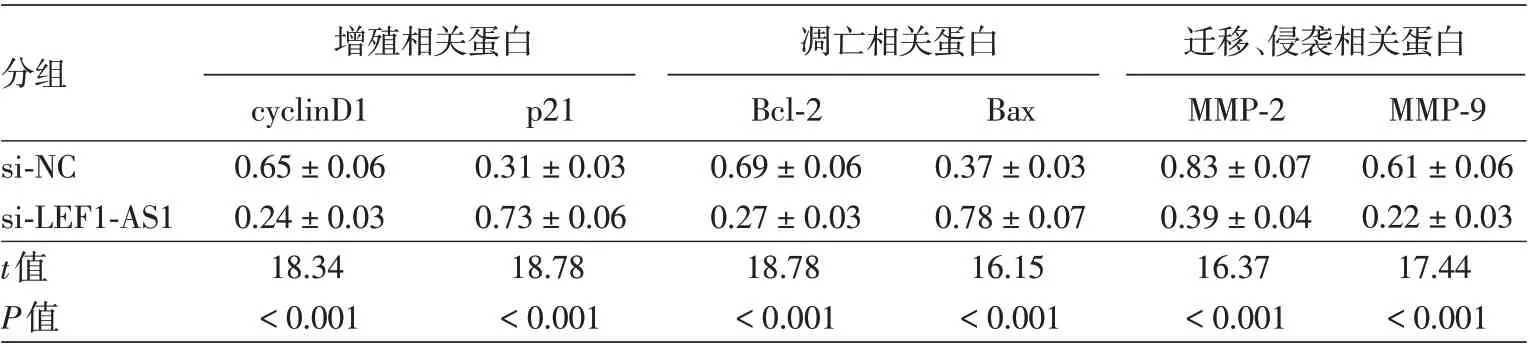
表3 Western印跡檢測干擾lncRNA LEF1-AS1表達后SCC13細胞增殖、凋亡、遷移和侵襲相關(guān)蛋白的表達(±s)
注:n=9。si-NC:轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1:轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列
分組 增殖相關(guān)蛋白cyclinD1 0.65±0.06 0.24±0.03 18.34<0.001 p21 0.31±0.03 0.73±0.06 18.78<0.001凋亡相關(guān)蛋白Bcl-2 0.69±0.06 0.27±0.03 18.78<0.001 Bax 0.37±0.03 0.78±0.07 16.15<0.001遷移、侵襲相關(guān)蛋白MMP-2 0.83±0.07 0.39±0.04 16.37<0.001 MMP-9 0.61±0.06 0.22±0.03 17.44<0.001 si-NC si-LEF1-AS1 t值P值
Western印跡顯示,miR-612組細胞增殖相關(guān)蛋白cyclinD1 相對水平低于miR-NC 組(P <0.05),p21 相對水平高于miR-NC 組(P <0.05);凋亡相關(guān)蛋白Bcl-2相對水平低于miR-NC組(P <0.05),Bax相對水平高于miR-NC 組(P <0.05);遷移、侵襲相關(guān)蛋白MMP-2、MMP-9相對水平均低于miR-NC 組(均P <0.05)。見圖5、表5。
四、lncRNA LEF1-AS1 靶向調(diào)控SCC13 細胞miR-612的表達
共轉(zhuǎn)染W(wǎng)T-LEF1-AS1后,miR-612組細胞熒光活性(0.33 ± 0.03)低于miR-NC 組(1.00 ± 0.09,t =21.19,P <0.001);而共轉(zhuǎn)染MUT-LEF1-AS1 后,miR-612 組細胞熒光活性(0.97 ± 0.07)與miR-NC組(0.98 ± 0.08)差異無統(tǒng)計學意義(t = 0.28,P =0.78)。
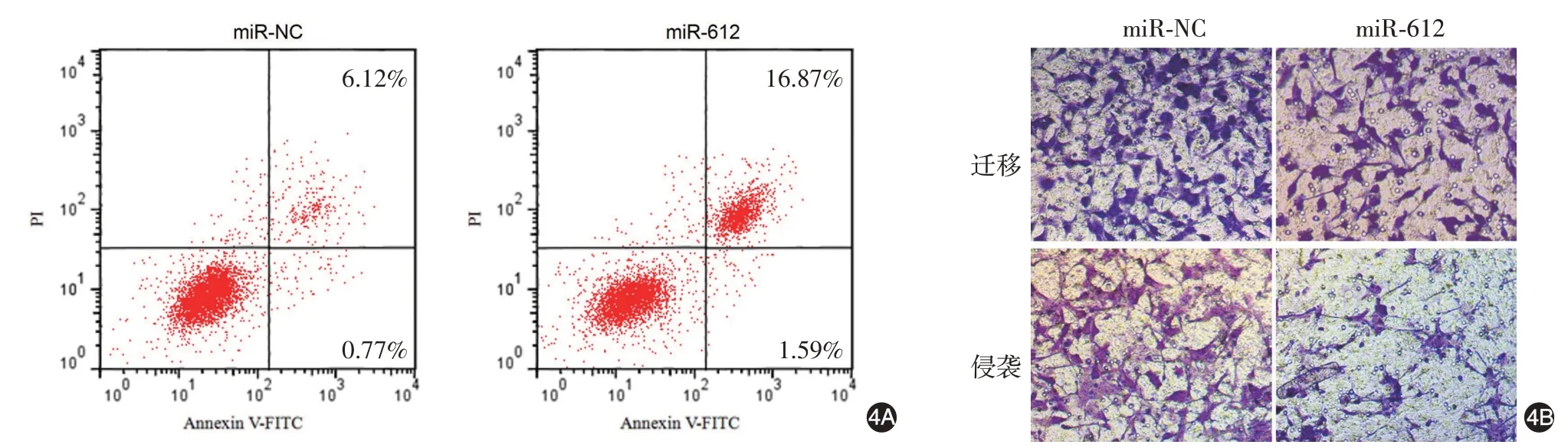
圖4 miR-612 過表達對SCC13 細胞的凋亡、遷移、侵襲能力的影響 4A:流式細胞儀檢測,miR-612 組細胞凋亡率高于miR-NC 組;4B:Transwell試驗檢測,miR-612組遷移、侵襲細胞數(shù)均低于miR-NC組。miR-NC組,轉(zhuǎn)染miR-612過表達的無意義序列;miR-612組,轉(zhuǎn)染miR-612過表達基因
表4 miR-612過表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響(±s)
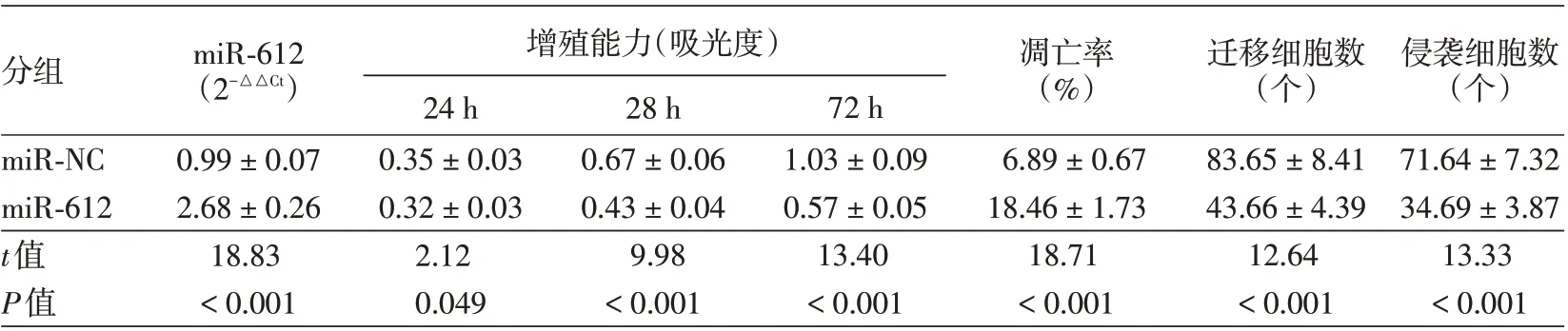
表4 miR-612過表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響(±s)
注:n=9。miR-NC組:轉(zhuǎn)染miR-612過表達的無意義序列;miR-612組:轉(zhuǎn)染miR-612過表達基因
分組miR-612(2-△△Ct)凋亡率(%)遷移細胞數(shù)(個)miR-NC miR-612 t值P值0.99±0.07 2.68±0.26 18.83<0.001增殖能力(吸光度)24 h 0.35±0.03 0.32±0.03 2.12 0.049 28 h 0.67±0.06 0.43±0.04 9.98<0.001 72 h 1.03±0.09 0.57±0.05 13.40<0.001 6.89±0.67 18.46±1.73 18.71<0.001 83.65±8.41 43.66±4.39 12.64<0.001侵襲細胞數(shù)(個)71.64±7.32 34.69±3.87 13.33<0.001
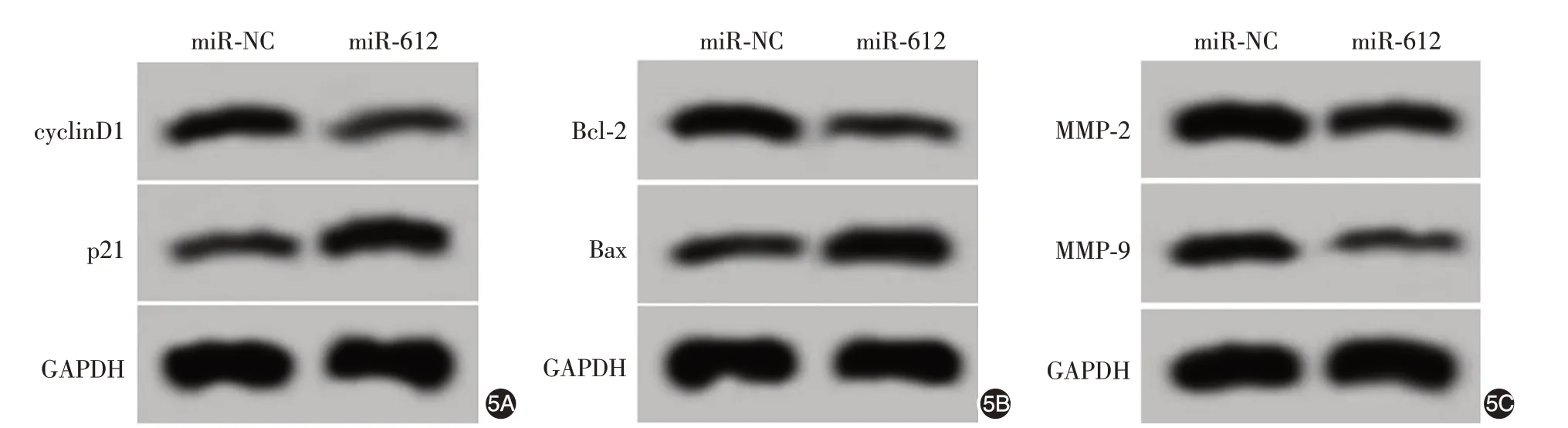
圖5 Western印跡檢測干擾miR-612過表達對SCC13細胞增殖、凋亡、遷移和侵襲相關(guān)蛋白表達的影響 5A:miR-612組cyclinD1相對水平低于miR-NC組,p21相對水平高于miR-NC組;5B:Bcl-2相對水平低于miR-NC組,Bax相對水平高于miR-NC組;5C:MMP-2、MMP-9相對水平均低于miR-NC組
表5 Western印跡檢測miR-612過表達對SCC13細胞相關(guān)蛋白的影響(±s)
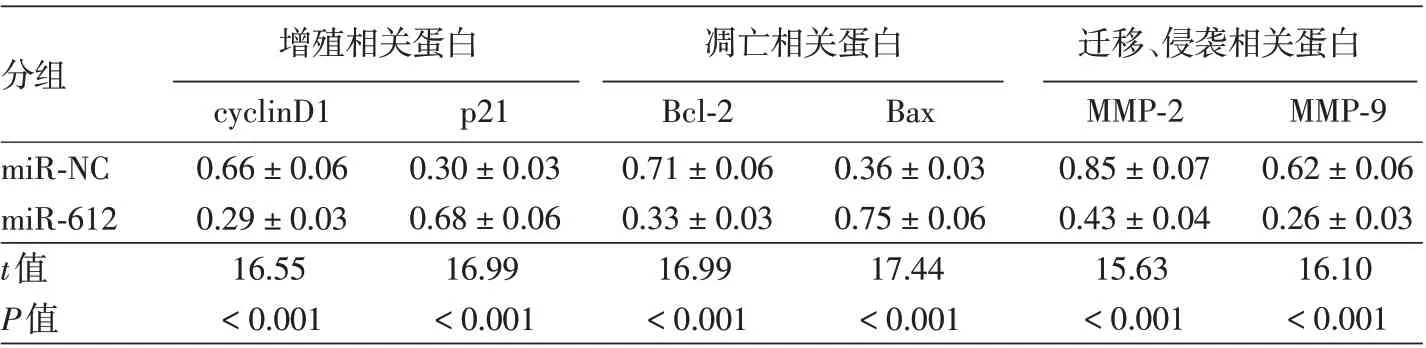
表5 Western印跡檢測miR-612過表達對SCC13細胞相關(guān)蛋白的影響(±s)
注:n=9。miR-NC組:轉(zhuǎn)染miR-612過表達的無意義序列;miR-612組:轉(zhuǎn)染miR-612過表達基因
分組 增殖相關(guān)蛋白cyclinD1 0.66±0.06 0.29±0.03 16.55<0.001 p21 0.30±0.03 0.68±0.06 16.99<0.001凋亡相關(guān)蛋白Bcl-2 0.71±0.06 0.33±0.03 16.99<0.001 Bax 0.36±0.03 0.75±0.06 17.44<0.001遷移、侵襲相關(guān)蛋白MMP-2 0.85±0.07 0.43±0.04 15.63<0.001 MMP-9 0.62±0.06 0.26±0.03 16.10<0.001 miR-NC miR-612 t值P值
LEF1-AS1-NC 組、LEF1-AS1 組、si-NC 組、si-LEF1-AS1 組細胞miR-612 的相對表達分別為1.00±0.09、0.49±0.04、1.01±0.08、2.53±0.25,差異有統(tǒng)計學意義(F=356.62,P <0.001),LEF1-AS1組低于LEF1-AS1-NC 組(LSD-t =15.54,P <0.05),si-LEF1-AS1 組高于與si-NC 組(LSD-t=17.33,P <0.05)。
五、干擾lncRNA LEF1-AS1 并抑制miR-612 的表達對SCC13細胞增殖、凋亡、遷移及侵襲的影響
si-NC 組、si-LEF1-AS1 組、si-LEF1-AS1+antimiR-NC 組、si-LEF1-AS1 + anti-miR-612 組細胞間miR-612 的相對表達差異有統(tǒng)計學意義,24、48、72 h 時的增殖能力差異有統(tǒng)計學意義,凋亡率(圖6)、遷移、侵襲細胞數(shù)(圖7)差異均有統(tǒng)計學意義(均P <0.05)。si-LEF1-AS1 組細胞中miR-612表達高于si-NC組,48、72 h細胞增殖能力低于si-NC組,細胞凋亡率高于si-NC組,遷移細胞數(shù)和侵襲細胞數(shù)低于si-NC 組(均P <0.05),而si-LEF1-AS1+anti-miR-612 組細胞中miR-612 表達低于si-LEF1-AS1+anti-miR-NC 組,48、72 h 細胞增殖能力高于si-LEF1-AS1 + anti-miR-NC 組,細胞凋亡率低于si-LEF1-AS1+anti-miR-NC 組,遷移細胞數(shù)和侵襲細胞數(shù)高于si-LEF1-AS1+anti-miR-NC 組(均P <0.05)。見表6。
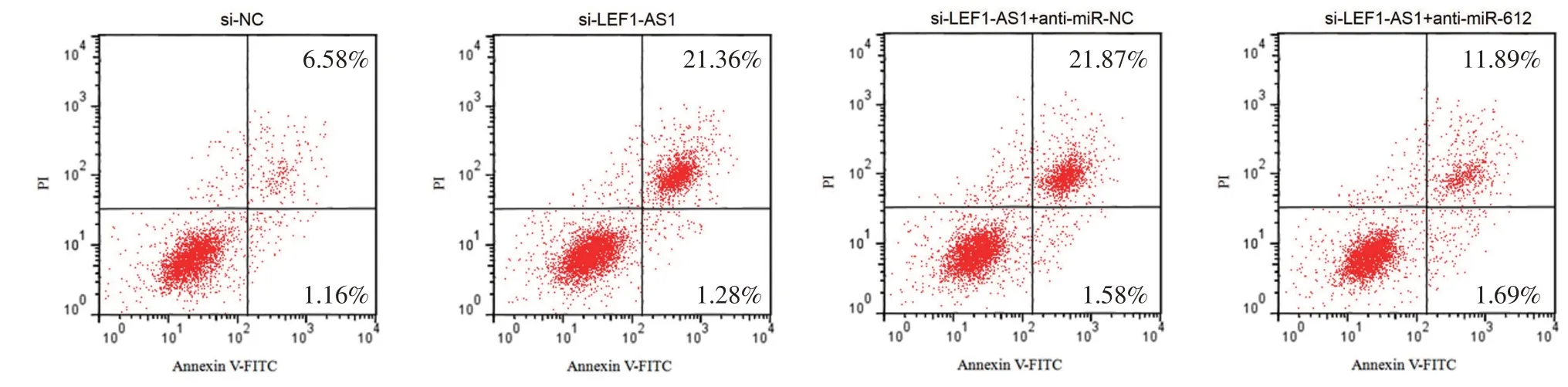
圖6 流式細胞儀檢測干擾長鏈非編碼RNA(lncRNA)LEF1-AS1并抑制miR-612的表達對SCC13細胞凋亡的影響 si-LEF1-AS1組細胞凋亡率高于si-NC組(P <0.05);si-LEF1-AS1+anti-miR-612組細胞凋亡率低于si-LEF1-AS1+anti-miR-NC組。si-NC,轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1,轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列;anti-miR-NC,轉(zhuǎn)染抑制miR-612表達的無意義序列;anti-miR-612,轉(zhuǎn)染抑制miR-612表達基因
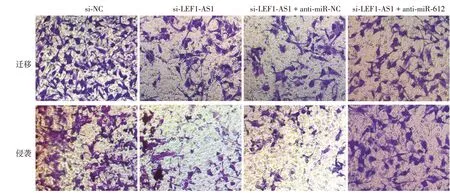
圖7 Transwell試驗檢測干擾長鏈非編碼RNA(lncRNA)LEF1-AS1并抑制miR-612的表達對SCC13細胞遷移、侵襲能力的影響 si-LEF1-AS1組遷移細胞數(shù)和侵襲細胞數(shù)低于si-NC組;si-LEF1-AS1+anti-miR-612組遷移細胞數(shù)和侵襲細胞數(shù)高于si-LEF1-AS1+anti-miR-NC組
Western 印跡顯示,4 組細胞cyclinD1、p21、Bcl-2、Bax、MMP-2、MMP-9蛋白相對水平差異均有統(tǒng)計學意義(均P <0.001),si-LEF1-AS1 組cyclinD1、Bcl-2、MMP-2、MMP-9蛋白相對水平均低于si-NC 組,p21、Bax 蛋白相對水平高于si-NC 組(均P <0.05);而si-LEF1-AS1 + anti-miR-612 組cyclinD1、Bcl-2、MMP-2、MMP-9蛋白相對水平高于si-LEF1-AS1 + anti-miR-NC 組,p21、Bax 蛋白相對水平低于si-LEF1-AS1 + anti-miR-NC 組(均P <0.05)。見圖8、表7。
討 論
Zong 等[8]報道,lncRNA LEF1-AS1 在食管鱗癌組織中的表達異常上調(diào),并與患者的淋巴轉(zhuǎn)移和臨床分期具有顯著的相關(guān)性,提示lncRNA LEF1-AS1可能是參與食管鱗癌臨床進展的lncRNA,可作為潛在的預測指標。Zhang等[9]在口腔鱗癌的研究中發(fā)現(xiàn),lncRNA LEF1-AS1在組織和細胞中的表達均顯著升高,且與患者預后不良相關(guān),下調(diào)lncRNA LEF1-AS1能夠在體外抑制癌細胞的增殖、遷移,促進凋亡并發(fā)生G0/G1期阻滯,在體內(nèi)抑制裸鼠腫瘤的生長,產(chǎn)生這種影響的作用機制與抑制Hippo信號通路活性具有明顯的相關(guān)性,提示lncRNA LEF1-AS1 通過抑制Hippo 信號通路,從而在口腔鱗癌中發(fā)揮致癌作用。由此,我們推測lncRNA LEF1-AS1可能在皮膚鱗癌中也具有致癌作用。本研究發(fā)現(xiàn),lncRNA LEF1-AS1 在皮膚鱗癌組織中的表達異常升高,干擾lncRNA LEF1-AS1 表達后,皮膚鱗癌細胞SCC13的增殖能力、遷移侵襲能力均受到明顯的抑制,細胞的凋亡明顯增強,這些試驗結(jié)果均與lncRNA LEF1-AS1 在食管鱗癌和口腔鱗癌中的功能相呼應,提示其在皮膚鱗癌中也發(fā)揮致癌的功能。
表6 干擾長鏈非編碼RNALEF1-AS1并抑制miR-612的表達對SCC13細胞增殖、凋亡、遷移侵襲的作用(±s)
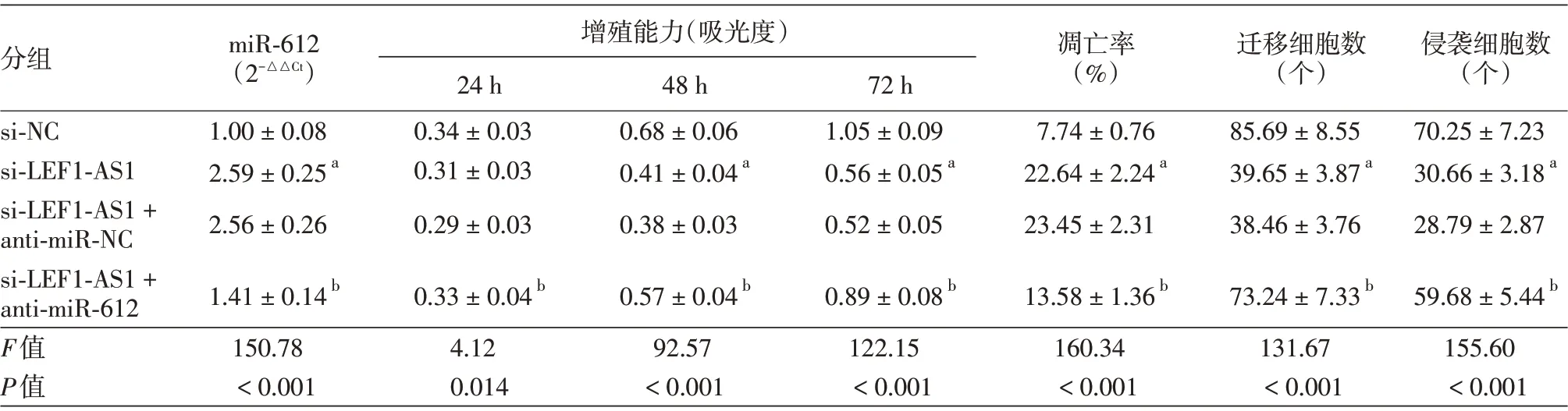
表6 干擾長鏈非編碼RNALEF1-AS1并抑制miR-612的表達對SCC13細胞增殖、凋亡、遷移侵襲的作用(±s)
注:n=9。si-NC:轉(zhuǎn)染lncRNA LEF1-AS1 的干擾無意義序列;si-LEF1-AS1:轉(zhuǎn)染lncRNA LEF1-AS1 的干擾序列;anti-miR-NC,轉(zhuǎn)染抑制miR-612 表達的無意義序列;anti-miR-612,轉(zhuǎn)染抑制miR-612表達基因。a與si-NC 組比較,P <0.05;b與si-LEF1-AS1+anti-miR-NC 組比較,P <0.05
增殖能力(吸光度)分組miR-612(2-△△Ct)si-NC si-LEF1-AS1 si-LEF1-AS1+anti-miR-NC si-LEF1-AS1+anti-miR-612 F值P值1.00±0.08 2.59±0.25a 2.56±0.26 1.41±0.14b 150.78<0.001 24 h 0.34±0.03 0.31±0.03 0.29±0.03 0.33±0.04b 4.12 0.014 48 h 0.68±0.06 0.41±0.04a 0.38±0.03 0.57±0.04b 92.57<0.001 72 h 1.05±0.09 0.56±0.05a 0.52±0.05 0.89±0.08b 122.15<0.001凋亡率(%)7.74±0.76 22.64±2.24a 23.45±2.31 13.58±1.36b 160.34<0.001遷移細胞數(shù)(個)85.69±8.55 39.65±3.87a 38.46±3.76 73.24±7.33b 131.67<0.001侵襲細胞數(shù)(個)70.25±7.23 30.66±3.18a 28.79±2.87 59.68±5.44b 155.60<0.001
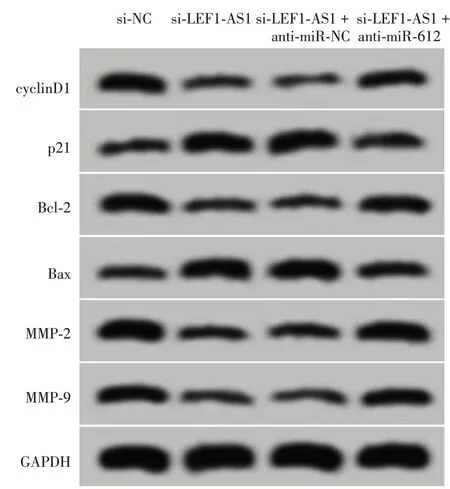
圖8 Western印跡檢測干擾長鏈非編碼RNA(lncRNA)LEF1-AS1 并抑制miR-612 的表達對SCC13 細胞增殖、凋亡、遷移和侵襲相關(guān)蛋白表達的影響 cyclinD1、Bcl-2、MMP-2、MMP-9蛋白相對水平,si-LEF1-AS1組低于si-NC 組,si-LEF1-AS1+anti-miR-612 組高于si-LEF1-AS1+anti-miR-NC組;p21、Bax蛋白相對水平,si-LEF1-AS1 組高于si-NC 組,si-LEF1-AS1+anti-miR-612 組低于si-LEF1-AS1+anti-miR-NC組
miRNA 既可作為lncRNA 的靶標,還可作為靶基因的直接上游調(diào)控因子,其在癌癥中的功能得到普遍認可[10]。miR-612在肝癌、黑素瘤中均表達異常[11-12],發(fā)揮調(diào)控癌癥進展的作用,但在皮膚鱗癌中的作用尚未十分清楚。Kang等[13]在非小細胞肺癌的研究中發(fā)現(xiàn),miR-612 的表達異常降低,且與患者的臨床病理分期和淋巴結(jié)轉(zhuǎn)移密切相關(guān)。另外,過表達miR-612能夠抑制非小細胞肺癌細胞的增殖、遷移和侵襲,促進凋亡,阻止裸鼠體內(nèi)腫瘤的生長,其機制為miR-612 靶向含溴結(jié)構(gòu)域的蛋白4(BRD4)進而抑制PI3K/Akt 信號通路的活性,揭示miR-612/BRD4/PI3K/Akt信號通路在非小細胞肺癌中的功能,提示miR-612可能成為非小細胞肺癌患者抗癌治療的潛在靶標。Sheng 等[14]在研究中發(fā)現(xiàn),miR-612在結(jié)直腸癌組織或細胞中的表達顯著降低,并且miR-612 在體外抑制結(jié)直腸癌細胞的增殖和遷移,miR-612 直接靶向抑制AKT2,進而抑制下游的上皮-間質(zhì)轉(zhuǎn)化相關(guān)的信號通路,說明miR-612 在結(jié)直腸癌的發(fā)展中起著關(guān)鍵性的作用。目前,miR-612 在皮膚鱗癌中的功能尚不清楚,我們推測其在皮膚鱗癌中也具有相似的抑癌作用。CyclinD1、p21 均是細胞周期調(diào)控因子,CyclinD1 高表達,p21 低表達,提示細胞增殖增多[15]。Bcl-2、Bax 是凋亡相關(guān)蛋白,Bcl-2 抗凋亡,Bax 促凋亡[16]。MMP-2、MMP-9是基質(zhì)金屬蛋白酶家族成員,其高表達可促進細胞外基質(zhì)的降解,促進細胞遷移、侵襲[17]。本研究發(fā)現(xiàn)干擾LncRNA LEF1-AS1 表達和miR-612 過表達后,CyclinD1、Bcl-2、MMP-2、MMP-9蛋白表達顯著降低,p21、Bax蛋白表達顯著升高。表明干擾LncRNA LEF1-AS1表達和miR-612 過表達可抑制皮膚鱗癌細胞的增殖、遷移侵襲,促進凋亡。本研究發(fā)現(xiàn),miR-612在皮膚鱗癌組織中的表達異常降低,過表達miR-612具有與干擾lncRNA LEF1-AS1 相類似的抑制皮膚鱗癌細胞增殖、遷移、侵襲和促進凋亡的作用。
表7 干擾長鏈非編碼RNALEF1-AS1并抑制miR-612的表達對SCC13細胞相關(guān)蛋白表達的影響(±s)

表7 干擾長鏈非編碼RNALEF1-AS1并抑制miR-612的表達對SCC13細胞相關(guān)蛋白表達的影響(±s)
注:n=9。注:si-NC:轉(zhuǎn)染lncRNA LEF1-AS1的干擾無意義序列;si-LEF1-AS1:轉(zhuǎn)染lncRNA LEF1-AS1的干擾序列;anti-miR-NC,轉(zhuǎn)染抑制miR-612表達的無意義序列;anti-miR-612,轉(zhuǎn)染抑制miR-612表達基因。a 與si-NC 組比較,P <0.05;b與si-LEF1-AS1+anti-miR-NC 組比較,P <0.05
分組 增殖相關(guān)蛋白cyclinD1 0.64±0.06 0.26±0.03a 0.25±0.03 0.53±0.05b p21 0.32±0.03 0.74±0.06a 0.75±0.07 0.43±0.03b凋亡相關(guān)蛋白Bcl-2 0.70±0.06 0.29±0.03a 0.28±0.03 0.59±0.05b Bax 0.35±0.03 0.79±0.06a 0.80±0.08 0.46±0.04b遷移、侵襲相關(guān)蛋白MMP-2 0.84±0.07 0.38±0.03a 0.37±0.04 0.72±0.07b MMP-9 0.59±0.06 0.23±0.03a 0.22±0.03 0.48±0.04b si-NC si-LEF1-AS1 si-LEF1-AS1+anti-miR-NC si-LEF1-AS1+anti-miR-612 174.68<0.001 166.60<0.001 206.13<0.001 151.87<0.001 167.10<0.001 175.20<0.001 F值P值
我們通過生物信息學預測、雙熒光素酶報告基因檢測實驗驗證,lncRNA LEF1-AS1 可靶向作用miR-612,猜測這可能與lncRNA LEF1-AS1在皮膚鱗癌中的功能具有聯(lián)系。本研究發(fā)現(xiàn),抑制miR-612能夠逆轉(zhuǎn)干擾lncRNA LEF1-AS1 對皮膚鱗癌細胞增殖、遷移侵襲和凋亡的調(diào)控作用。提示在皮膚鱗癌中,lncRNA LEF1-AS1 可能通過miR-612 發(fā)揮調(diào)控皮膚鱗癌細胞增殖、凋亡、遷移、侵襲的作用。
利益沖突所有作者均聲明不存在利益沖突

