空腹血糖受損患者血尿酸與腎小球濾過率的相關性分析
拾莉, 劉學奎, 龔瑩, 桑誼荃, 梁軍
(1. 徐州市醫學科學研究所, 江蘇 徐州 221006; 2. 徐州市中心醫院內分泌科, 江蘇 徐州 221009; 3. 徐州市糖尿病研究所, 江蘇 徐州 221006)
糖尿病腎病是糖尿病常見的慢性并發癥,是慢性腎臟病的重要病因。國外研究發現糖尿病前期患者慢性腎臟病的發病率高于正常人群[1]。另有研究表明,空腹血糖受損(impaired fasting glucose,IFG)患者易出現腎小球濾過率(GFR)增加、腎小球高度灌注和過度濾過及蛋白尿,但慢性腎臟病的發病率并沒有明顯增加[2]。當前關于糖尿病前期人群中慢性腎臟病的發病率亦尚有爭議,估算腎小球濾過率(eGFR)是慢性腎臟病發病的獨立危險因素,是臨床評估腎臟濾過功能的一項重要指標[3]。研究顯示高血糖、高尿酸與GFR呈相關關系[4-6],因此本研究選取徐州社區體檢人群作為研究對象,探討空腹血糖受損患者血尿酸對eGFR的影響,為防治糖尿病腎病提供依據。
1 對象和方法
1.1 對象
選擇江蘇徐州地區2016年在徐州市中心醫院體檢且資料完整者11 078例為研究對象,年齡18~80周歲,排除既往有糖尿病,心腦血管疾病,嚴重肝、腎、肺功能不全者,排除近期用過影響血尿酸或糖代謝的藥物(如非布司他、碳酸氫鈉、糖皮質激素等)。本研究經徐州市中心醫院倫理委員會批準,研究對象知情同意。
1.2 方法
1.2.1 數據測量 統一設計體檢表格,體檢醫師統一培訓后上崗,詳細詢問記錄受試者一般情況、既往史、用藥史等。測量受試者脫鞋穿單衣身高、體重。受試者靜坐至少5 min后用水銀測壓計測量右上臂收縮壓及舒張壓,手臂與心臟在同一水平,連續測量3次,期間至少間隔1 min,取平均值進行分析[7]。計算體重指數(BMI)=體重(kg)/身高2(m2)。
1.2.2 實驗室檢查 受試者晚餐后禁食8~10 h,次日清晨空腹采集靜脈血。日立7600全自動生化分析儀酶法測定空腹血糖、血尿酸、總膽固醇、三酰甘油、高密度脂蛋白膽固醇(HDL-C)、低密度脂蛋白膽固醇(LDL-C)、血清γ-谷氨酰轉肽酶(GGT)。空腹血糖受損的定義為6.1 mmol/L≤空腹血糖<7.0 mmol/L。
1.2.3 分組 先根據空腹血糖水平將受試者分為血糖正常組和空腹血糖受損組,比較兩組血壓、BMI、血脂、GGT等相關生化指標。再根據血尿酸四分位水平將空腹血糖受損患者分為4組:Q1組(女<191.30 μmol/L;男<273.60 μmol/L)302例,Q2組(女<222.90 μmol/L;男<316.10 μmol/L)264例,Q3組(女<257.60 μmol/L;男<362.73 μmol/L)259例,Q4組(女≥257.60 μmol/L;男≥362.73 μmol/L)276例。
1.2.4 eGFR計算 依據腎臟病膳食改良試驗(MDRD)簡化公式計算eGFR,血肌酐單位為mg/dL,年齡單位為歲,eGFR[mL/(min·1.73 m2)]=175×[血肌酐]-1.234×[年齡]-0.179×[女性×0.79]。eGFR<60 mL/(min·1.73 m2)定義為腎小球濾過率下降。
1.3 統計學處理
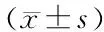
2 結果
2.1 受試者一般情況
入選研究對象共11 078例,空腹血糖正常組9 977例,空腹血糖受損組1 101例。空腹血糖受損組的BMI、血壓、總膽固醇、三酰甘油、LDL-C、GGT值較血糖正常組明顯升高,而HDL-C、eGFR值較血糖正常組明顯降低,差異均有統計學意義(表1)。
2.2 血尿酸與eGFR的相關性分析
空腹血糖受損組隨著血尿酸的增高,模型1狀態下(未校正其他因素),eGFR逐漸降低;模型2狀態下(校正了年齡、性別、BMI后),這種下降趨勢仍然存在;進一步校正血壓、血脂等5項后(模型3),eGFR仍隨著血尿酸的增高而降低;且趨勢有統計學意義(表2)。
2.3 空腹血糖受損與血尿酸的交互作用對eGFR的影響
空腹血糖正常組隨著血尿酸的升高,eGFR呈下降趨勢;空腹血糖受損與血清尿酸水平對eGFR的影響有協同作用(交互作用P= 0.035)。見圖1。

表1 不同空腹血糖水平患者一般資料比較

表2 空腹血糖受損患者血尿酸與eGFR的相關性分析 mL/(min·1.73 m2)

圖1 空腹血糖受損與血尿酸對eGFR的交互作用
3 討論
糖尿病腎病是慢性腎臟病的重要病因,據文獻報道國外約20%~40%的糖尿病患者合并糖尿病性腎病;國內尚無全國性相關流行病學調查資料,文獻顯示2型糖尿病患者糖尿病腎病的患病率為10%~40%[7]。合并糖尿病腎病的糖尿病患者較單純糖尿病患者死亡風險更高,且死因多為心血管事件。而eGFR下降與心血管疾病、死亡風險增加密切相關,輕度的eGFR下降即可增加心血管疾病風險,隨著eGFR下降,糖尿病患者心血管事件、心血管相關死亡風險顯著升高[8-10]。因此及早發現高血糖人群中早期慢性腎臟病患者并加以干預,對預防和延緩糖尿病腎病進展,降低心血管疾病和死亡風險、延長患者壽命及提高生存質量具有重要意義。
研究表明慢性腎臟病的發生與高胰島素血癥及胰島素抵抗相關,在慢性腎臟病早期甚至eGFR處于正常范圍時即可發生糖代謝紊亂,與糖代謝正常者相比,糖尿病前期患者發生慢性腎臟病的風險明顯增加[11]。在動物實驗中,連續6 d注射糖,使其血糖達到6.5~7.1 mmol/L,可以顯著增高GFR[12]。本研究中空腹血糖受損患者的eGFR較空腹血糖正常者偏低,在空腹血糖受損人群中,eGFR隨著血尿酸的升高而降低,在校正性別、年齡、BMI、血脂、血壓等指標后,eGFR仍隨著血尿酸的升高而降低,提示空腹血糖受損人群中血尿酸與eGFR呈負相關,且血尿酸是eGFR的獨立危險因素。目前血尿酸導致GFR下降的機制尚不明確,可能的機制是:高血尿酸水平可激活炎性介質導致慢性炎癥,內皮細胞、平滑肌細胞增生功能紊亂,致內皮細胞損傷,血小板黏附異常;其次血尿酸還可以改變腎小球內血流動力學,導致腎皮質血管收縮,最終導致GFR下降腎功能受損[13]。
本研究結果顯示,空腹血糖受損與血清尿酸水平對eGFR的變化有協同作用,兩者發生交互作用共同導致eGFR進一步下降。這是因為高尿酸血癥與胰島素抵抗密切相關。研究表明高尿酸可引起肝細胞線粒體氧化應激,損傷血管內皮,抑制脂肪細胞及骨骼肌細胞胰島素信號轉導,導致胰島素抵抗;同時也引起胰島細胞氧化應激導致胰島功能異常[14]。胰島素抵抗的同時,胰島素敏感性下降,血糖調節能力大大減弱,引起空腹血糖升高。在糖代謝受損的早期階段,尿酸水平的升高往往還伴隨著高胰島素血癥,內源性胰島素作用于腎近曲小管腎尿酸轉運載體(URAT1),促進腎小管對鈉鹽重吸收,同時減少腎臟對尿酸鹽排泄[15]。另一方面胰島素抵抗還可激活腎素-血管緊張素-醛固酮系統(RAAS),RASS激活后易導致腎臟毛細血管內壓力增高,腎臟細胞外基質改變,從而導致腎小球濾過腔狹窄,濾過面積減少,GFR降低[16]。
除性別、年齡外血清肌酐還受肌肉量、蛋白攝入量、藥物(西咪替丁等)影響,但本研究僅校正了年齡、性別的影響,可能對研究結果產生偏差。同時GFR異常的影響因素較復雜,有待大規模的研究進一步證實。綜上所述,本研究表明空腹血糖受損與血清尿酸水平對eGFR的變化有協同作用,兩者共同作用導致eGFR進一步降低。因此,在社區人群中應加強血尿酸和血糖水平的監測,以早期預防和控制糖尿病腎病的發生。

