3 株乳桿菌發(fā)酵秈米粉漿及其產(chǎn)酶特性
梁 言,陳 中,劉秉杰
(1.廣東省食品檢驗所,廣東 廣州 510080;2.華南理工大學(xué)食品科學(xué)與工程學(xué)院,廣東 廣州 510640;3.東莞石龍津威飲料食品有限公司,廣東 東莞 523320)
乳酸菌是一類無芽孢、革蘭氏染色陽性細菌的總稱,可利用碳源發(fā)酵產(chǎn)生乳酸。在乳酸菌中,乳桿菌是最大的一個屬。乳桿菌一般利用葡萄糖和乳糖等還原糖作為碳源,但在某些環(huán)境下也可利用非還原糖如淀粉和蔗糖,通過產(chǎn)淀粉酶與蔗糖酶等酶系,將非還原糖轉(zhuǎn)化為還原糖,以供自身利用[1],目前己有較多乳桿菌利用多糖或二糖作為碳源的文獻報道。Lee等[2]從豬腸道內(nèi)分離了20 株乳酸菌,通過觀察3 種菌株生長過程中淀粉在肉湯培養(yǎng)基中的消失情況測定淀粉的水解情況,其中3 株乳桿菌所產(chǎn)淀粉酶擁有高酶活力,3 株菌中A-4和L23菌株確定為嗜酸乳桿菌,L9菌株為發(fā)酵乳桿菌。Kocabay等[3]研究了1 株可產(chǎn)β-淀粉酶的發(fā)酵乳桿菌,探究了其淀粉酶的最適溫度及pH值。Giraud等[4]發(fā)現(xiàn),從發(fā)酵木薯中分離得到的植物乳桿菌A6可以分解未發(fā)酵的木薯原淀粉,Humblot等[5]研究了植物乳桿菌A6發(fā)酵過程中淀粉代謝相關(guān)基因的表達及其所產(chǎn)淀粉酶的活性。Chookietwattana[6]研究了其分離所得的1 株植物乳桿菌MSUL 903,證實該菌株是一種高效的木薯淀粉水解乳酸菌。Panda等[7]通過響應(yīng)面法優(yōu)化了1 株植物乳桿菌 MTCC 1407在深層發(fā)酵下淀粉酶的產(chǎn)酶條件。趙志丹等[8]從健康仔豬腸道分離篩選出1 株具較強產(chǎn)淀粉酶能力的乳桿菌G8-5,經(jīng)鑒定為羅伊氏乳桿菌。Bai Yuxiang等[9]對羅伊氏乳桿菌35-5在淀粉和蔗糖中形成的胞外多糖進行了表征,發(fā)現(xiàn)淀粉與蔗糖對羅伊氏乳桿菌35-5的胞外多糖形成有一定程度的影響。張莉力等[10]從自然發(fā)酵的甘薯酸漿中,分離篩選得到1 株能產(chǎn)淀粉酶的副干酪乳桿菌,命名為副干酪乳桿菌L1,孫竹萍等[11]進一步研究了溫度與pH值對副干酪乳桿菌 L1所產(chǎn)淀粉酶活力的影響,優(yōu)化了其產(chǎn)淀粉酶的條件。Padmavathi等[12]研究了乳桿菌sp G3_4_1TO2的產(chǎn)淀粉酶能力,與發(fā)酵乳桿菌相比其所產(chǎn)淀粉酶的活力更高,是一種潛在高產(chǎn)淀粉酶的益生菌。Hyeyeon等[13]提取并純化了植物乳桿菌ST-III所產(chǎn)淀粉酶LpMA,發(fā)現(xiàn)該酶不僅可將直鏈淀粉和支鏈淀粉作為底物生產(chǎn)麥芽糖,還可將麥芽三糖、麥芽五糖作為底物。吳鵬[14]從發(fā)酵米漿中篩選出3 株干酪乳桿菌,驗證其均可利用蔗糖作為碳源。
乳桿菌可利用淀粉作為碳源在大米淀粉體系中發(fā)酵,廣泛應(yīng)用于以淀粉為主要原料的發(fā)酵類食品中,如米發(fā)糕、米乳飲料、發(fā)酵米粉等[15-17]。乳桿菌利用淀粉的能力可在不加入或少加入其他碳源的情況下用于制作低糖型發(fā)酵食品,產(chǎn)品不僅更有利于健康,從工業(yè)化生產(chǎn)的角度還可以節(jié)省成本,簡化生產(chǎn)步驟。乳桿菌在發(fā)酵過程中所產(chǎn)的細菌素可抑制其他微生物的生長[18],通過發(fā)酵還可消減米類制品中的重金屬如鎘等[19],從而提高產(chǎn)品的安全性。此外,乳桿菌發(fā)酵后的淀粉類食品如大米的理化特性會發(fā)生改變[20],可改善口感與營養(yǎng)成分。因而研究乳桿菌降解大米淀粉的能力具有一定的應(yīng)用價值,可為制作大米發(fā)酵食品提供新的菌種和發(fā)酵工藝思路。秈米粉漿是制作傳統(tǒng)大米發(fā)酵食品的一種前體,為了使秈米粉漿經(jīng)發(fā)酵后的風(fēng)味更為多樣化,需要探究不同種類的產(chǎn)淀粉酶乳桿菌,及其在秈米粉漿中的生長狀況。本研究通過預(yù)實驗篩選3 株具有降解淀粉能力的乳桿菌為嗜酸乳桿菌14(Lactobacillus acidophilus 14,La)、干酪乳桿菌M(L. casei M,Lc)與植物乳桿菌115(L. plantarum 115,Lp),構(gòu)建嗜酸乳桿菌-秈米粉漿發(fā)酵體系(L. acidophilus-indica rice flour slurry,La-IRFS),干酪乳桿菌-秈米粉漿發(fā)酵體系(L. casei-indica rice flour slurry,Lc-IRFS)和植物乳桿菌-秈米粉漿發(fā)酵體系(L. plantarum-indica rice flour slurry,Lp-IRFS),研究3 種乳桿菌在秈米粉漿體系中的單菌發(fā)酵過程,及其所產(chǎn)淀粉酶嗜酸乳桿菌淀粉酶(L. acidophilus-amylase,La-a)、干酪乳桿菌淀粉酶(L. casei-amylase,Lc-a)和植物乳桿菌淀粉酶(L. plantarum-amylase,Lp-a)的酶學(xué)特性。分析比較3 株乳桿菌在秈米粉漿中的生長能力,降解淀粉能力,產(chǎn)淀粉酶活力。同時,研究3 株乳桿菌所產(chǎn)淀粉酶的酶學(xué)特性,包括其最適反應(yīng)溫度和pH值、耐高溫能力與pH值穩(wěn)定性,以期對大米發(fā)酵食品的發(fā)酵工藝起一定指導(dǎo)作用。
1 材料與方法
1.1 材料與試劑
秈米粉 市售;La、Lc、Lp均保存于華南理工大學(xué)食品科學(xué)與工程學(xué)院實驗室,直投式菌粉,活菌數(shù)分別為1.83×1010、6.34×1010、1.08×1011CFU/g。
直鏈淀粉、支鏈淀粉(均為標(biāo)準(zhǔn)物) 北京北方偉業(yè)計量技術(shù)研究院;可溶性淀粉 賽默飛世爾科技公司;麥芽糖、葡萄糖 上海奧博生物試劑有限公司;3,5-二硝基水楊酸(3,5-dinitrosalicylic acid,DNS)國藥集團化學(xué)試劑有限公司;碘試劑 上海銀碘化工有限公司;MRS培養(yǎng)基 廣東環(huán)凱微生物科技有限公司。所有試劑均為分析純。
1.2 儀器與設(shè)備
DGX-9243B-2干熱滅菌器 上海福瑪實驗設(shè)備有限公司;XSP-104光學(xué)顯微鏡 寧波湛京光學(xué)儀器有限公司;SW-CJ-ECU超凈工作臺 蘇州凈化設(shè)備有限公司;LRH-70恒溫生化培養(yǎng)箱 上海恒科儀器有限公司;HWS-24電熱恒溫水浴鍋 上海齊欣科學(xué)儀器有限公司;pHS-25數(shù)顯pH計 上海精密儀器有限公司;TGL-16gR高速冷凍離心機 上海安亭科學(xué)儀器廠;752N紫外-可見分光光度計 上海棱光技術(shù)有限公司。
1.3 方法
1.3.1 乳桿菌-秈米粉漿發(fā)酵體系的構(gòu)建
秈米粉鋪成薄層,于干熱滅菌器中以180 ℃干熱滅菌45 min,冷卻后與無菌水以1∶1的質(zhì)量比混合調(diào)成米漿,于超凈工作臺接入直投式乳桿菌菌粉La、Lc和Lp(接種量均為9×109CFU/mL),于恒溫培養(yǎng)箱發(fā)酵后得到乳桿菌-秈米粉漿體系La-IRFS、Lc-IRFS和Lp-IRFS,體系初始總淀粉質(zhì)量分?jǐn)?shù)為33.78%,直鏈淀粉質(zhì)量分?jǐn)?shù)為10.26%。
1.3.2 乳桿菌生長曲線測定
接種后取初始樣,之后每隔2 h取一次樣,采用GB 4789.35—2016《食品微生物學(xué)檢驗 乳酸菌檢驗》[21]方法測活菌數(shù)。
1.3.3 秈米粉滅菌前后及發(fā)酵后淀粉顆粒形態(tài)的觀察
取適量滅菌前秈米粉于載玻片上,以50%乙醇溶液分散后,滴加1 滴0.01 mol/L碘試劑進行染色,滴加香柏油,以油鏡觀察淀粉顆粒形態(tài);取適量滅菌后的秈米粉或發(fā)酵后的秈米粉漿于載玻片上,重復(fù)上述操作,對比滅菌前后及發(fā)酵前后淀粉顆粒形態(tài)的變化。
1.3.4 發(fā)酵前后體系淀粉含量變化分析
總淀粉含量的測定:采用酸水解法[22],樣品除去脂肪和可溶性糖類,淀粉酸水解為還原性單糖后按還原糖測定并折算。取9 支25 mL具塞刻度試管,分別加入質(zhì)量濃度為1 mg/mL的葡萄糖標(biāo)準(zhǔn)液0、0.2、0.4、0.6、0.8、1.0、1.2、1.4、1.6 mL,蒸餾水2、1.8、1.6、1.4、1.2、1.0、0.8、0.6 mL,再各加入1.5 mL DNS液,配成不同葡萄糖含量的反應(yīng)液,沸水浴5 min,冰浴冷卻至室溫,用蒸餾水定容至25 mL,混勻,在分光光度計上進行比色。于波長540 nm處測吸光度。以吸光度為縱坐標(biāo),葡萄糖質(zhì)量(mg)為橫坐標(biāo),繪制標(biāo)準(zhǔn)曲線:y=0.548 8x-0.009 2,R2=0.999 6。樣品按酸水解法處理后在波長540 nm處讀取吸光度,根據(jù)標(biāo)準(zhǔn)曲線計算葡萄糖含量,乘0.9折算為淀粉含量。
直鏈淀粉含量的測定:采用GB/T 15683—2008《大米直鏈淀粉含量的測定》[23]方法測定直鏈淀粉占總淀粉的比例。分別量取1 mg/mL直鏈淀粉標(biāo)準(zhǔn)溶液0、2、4、5、6、7 mL和1 mg/mL支鏈淀粉標(biāo)準(zhǔn)溶液18、16、14、13、12、11 mL于100 mL容量瓶中,各加入0.09 mol/L氫氧化鈉溶液2 mL。另取1 個100 mL容量瓶,加入0.09 mol/L氫氧化鈉溶液5 mL作空白。于各瓶中依次加入50 mL水、1 mL 1 mol/L乙酸溶液及2 mL碘試劑,用水定容后發(fā)色10 min,空白調(diào)零,在波長720 nm處讀取吸光度。以直鏈淀粉含量為橫坐標(biāo),吸光度為縱坐標(biāo),繪制標(biāo)準(zhǔn)工作曲線:y=0.021 0x+0.127 9,R2=0.999 4。待測樣品按國標(biāo)方法預(yù)處理,稀釋1 倍后在波長720 nm處讀取吸光度,根據(jù)標(biāo)準(zhǔn)曲線計算直鏈淀粉占比,乘2得樣品直鏈淀粉含量。
1.3.5 淀粉酶粗酶活力的測定
采用DNS法測定總酶活力[24]。取7 支25 mL具刻度試管,分別加入1 mg/mL麥芽糖標(biāo)準(zhǔn)液0、0.1、0.2、0.4、0.6、0.8、1.0 mL,蒸餾水1、0.9、0.8、0.6、0.4、0.2、0 mL,再各加入1 mL DNS液,搖勻后沸水浴5 min,冷卻后加蒸餾水定容至20 mL,在550 nm波長處比色測定吸光度,對應(yīng)麥芽糖含量繪制得標(biāo)準(zhǔn)曲線:y=0.916 1x-0.016 4,R2=0.999 7。
粗酶液的提取:發(fā)酵秈米粉漿8 000 r/min、4 ℃離心15 min,取上清液即為粗酶液(含麥芽糖)。
酶活力的測定:粗酶液稀釋10 倍后取1 mL與1 mL 1%淀粉標(biāo)準(zhǔn)溶液混合,加入1 mL DNS液,搖勻后沸水浴5 min,冷卻至室溫,定容至20 mL,測波長550 nm處吸光度,得麥芽糖含量A0。粗酶液稀釋10 倍后取1 mL與1 mL 1%淀粉標(biāo)準(zhǔn)溶液混合,37 ℃放置1 h后加入1 mL DNS液,搖勻后沸水浴5 min,冷卻至室溫,定容至20 mL,測波長550 nm處吸光度,得麥芽糖含量A。
酶活力定義:每1 h從1 mL 1%淀粉標(biāo)準(zhǔn)溶液中釋放出1 mg麥芽糖所需的酶量為1 個酶活力單位。計算公式如下:
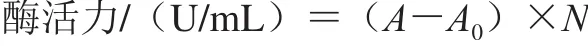
式中:A為加酶處理1 h后麥芽糖量/mg;A0為原粗酶液中麥芽糖量/mg;N為總稀釋倍數(shù)。
1.3.6 pH值與總酸的測定
pH值:使用pH計測定;總酸:采用GB 5009.239—2016《食品酸度的測定》[25]第二法測定。
1.3.7 酶學(xué)特性分析
溫度對淀粉酶的影響:用1.3.5節(jié)方法測定酶活力,水浴鍋溫度分別設(shè)為30、35、40、45、50、55、60、65、70 ℃;pH值對淀粉酶的影響:用1.3.5節(jié)方法測定酶活力,粗酶液與淀粉標(biāo)準(zhǔn)溶液混勻后,將pH值分別調(diào)為3.0、4.0、5.0、6.0、7.0、8.0、9.0后再放入水浴鍋中37 ℃放置1 h。
酶熱穩(wěn)定性:取粗酶液在50、60、70、80、90 ℃保溫30、60、120、180 min后,用1.3.5節(jié)方法測定酶活力;酶pH值穩(wěn)定性:取粗酶液分別將pH值調(diào)節(jié)為3.0、4.0、5.0、8.0、9.0后放置30、60、120、180 min,用1.3.5節(jié)方法測定酶活力。
La-a粗酶液提取于發(fā)酵6 h的La-IRFS,Lc-a粗酶液提取于發(fā)酵8 h的Lc-IRFS,Lp-a粗酶液提取于發(fā)酵8 h的Lp-IRFS,以相對酶活力作為最終結(jié)果。
1.4 數(shù)據(jù)處理
用Origin 9.0處理數(shù)據(jù)并繪制圖表。
2 結(jié)果與分析
2.1 乳桿菌發(fā)酵過程分析
2.1.1 3 株乳桿菌的生長曲線
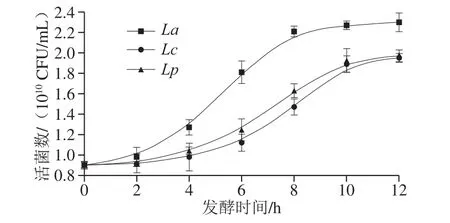
圖1 3 株乳桿菌在秈米粉漿中的生長曲線Fig. 1 Growth curves of three strains of Lactobacillus in indica rice flour slurry
由圖1可得,3 株乳桿菌在秈米粉漿中生長狀況良好,La活菌數(shù)增長速率明顯快于Lc與Lp,在2~8 h階段活菌數(shù)翻倍,在發(fā)酵8 h后生長開始趨于平緩,活菌數(shù)變化較小;Lc與Lp活菌數(shù)變化趨勢相近,在2~8 h的階段活菌數(shù)增長較快,但增長量明顯小于La,發(fā)酵10 h后生長趨于平緩。在發(fā)酵12 h后La的活菌數(shù)可達2.3×1010CFU/mL,Lc與Lp的活菌數(shù)皆達1.9×1010CFU/mL。
2.1.2 滅菌及發(fā)酵前后淀粉顆粒形態(tài)的變化
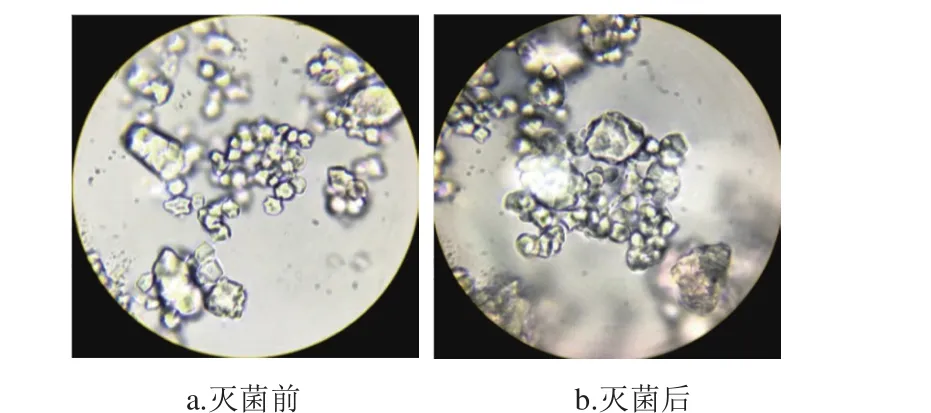
圖2 滅菌前后的淀粉顆粒形態(tài)(目鏡×16,物鏡×100)Fig. 2 Morphology of starch granules before and after sterilization(eyepiece ×16, objective lens ×100)
由圖2可看出,滅菌前后淀粉顆粒變化不大,淀粉在滅菌后仍保持完整顆粒,沒有出現(xiàn)漲破的現(xiàn)象,說明本實驗的滅菌方法不會使秈米粉中的淀粉糊化,其仍為生淀粉。
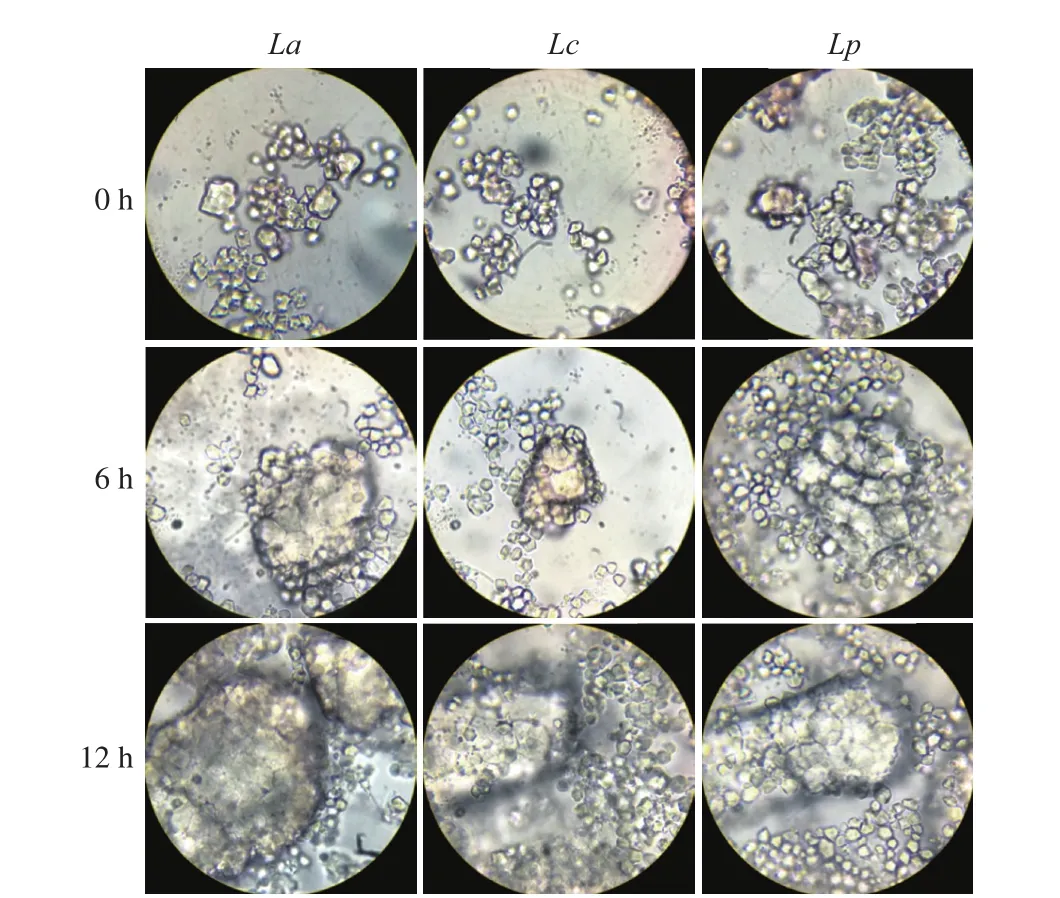
圖3 發(fā)酵前后的淀粉顆粒形態(tài)(目鏡×16,物鏡×100)Fig. 3 Morphology of starch granules before and after fermentation(eyepiece ×16, objective lens ×100)
由圖3可看出,與發(fā)酵前相比,經(jīng)3 株乳桿菌發(fā)酵后的秈米粉漿中淀粉顆粒的形態(tài)均有不同程度的破裂,這說明3 株乳桿菌都具有一定降解生淀粉的能力,可產(chǎn)淀粉酶使淀粉中的α-1,4-糖苷鍵水解生成小分子糊精,這一過程會使淀粉顆粒形態(tài)遭到破壞,因而在顯微鏡下呈現(xiàn)出許多淀粉顆粒破裂呈糊的狀態(tài)。3 株乳桿菌發(fā)酵6 h后,顯微鏡下均可觀測到小面積的淀粉顆粒破裂,發(fā)酵12 h后,均可觀測到較大面積的淀粉顆粒破裂,可見隨發(fā)酵時間的延長有更多淀粉被乳桿菌所產(chǎn)的淀粉酶酶解導(dǎo)致結(jié)構(gòu)崩壞。
2.1.3 發(fā)酵前后淀粉含量的變化
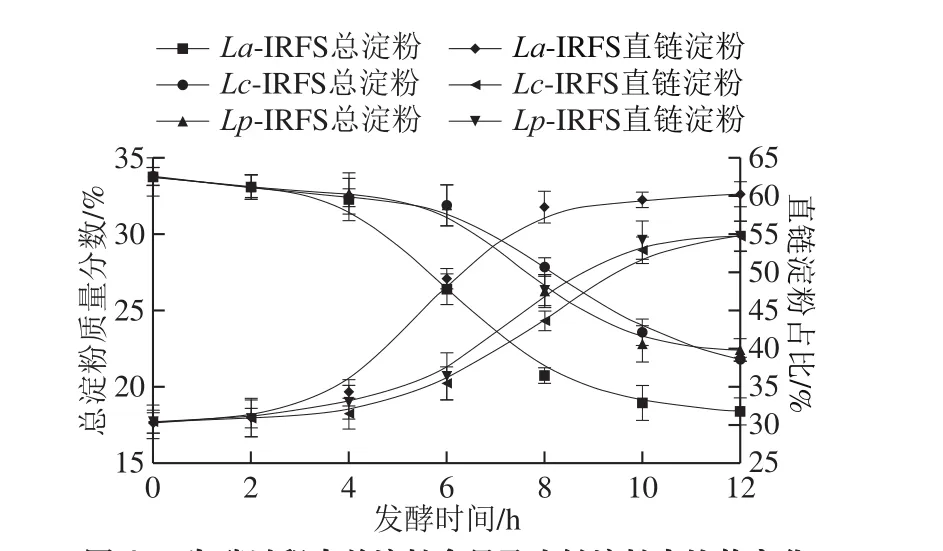
圖4 發(fā)酵過程中總淀粉含量及直鏈淀粉占比的變化Fig. 4 Changes in starch content and amylose proportion during fermentation
由圖4可得,經(jīng)3 株乳桿菌發(fā)酵過后,乳桿菌-秈米粉漿體系中的總淀粉含量均顯著降低,進一步證實3 株乳桿菌都有一定利用生淀粉作為碳源的能力。通過總淀粉含量降低的速率可知,3 株乳桿菌中La降解生淀粉的能力較強,Lc與Lp較弱。在發(fā)酵時間為4~8 h階段,La降解淀粉的速率最快,6~8 h階段,Lc與Lp降解淀粉速率最快,這是由于4~8 h期間La-a活力最大,6~10 h期間Lc-a與Lp-a活力最大。發(fā)酵12 h后,La-IRFS中直鏈淀粉在總淀粉中占比從30%增大到60%,Lc-IRFS和Lp-IRFS中直鏈淀粉在總淀粉中的占比則從30%增大到55%,隨著總淀粉含量的降低,直鏈淀粉在總淀粉中的占比增大,說明在體系中淀粉酶活力較高時,直鏈淀粉的占比迅速上升,初步推測原因為乳桿菌所產(chǎn)淀粉酶中,有一定量的異淀粉酶,該酶只水解支鏈淀粉分枝點的α-1,6-糖苷鏈,切下整個側(cè)枝,形成長短不一的直鏈淀粉,因而體系中淀粉酶活力性高時,異淀粉酶迅速將支鏈淀粉轉(zhuǎn)化為直鏈淀粉,從而導(dǎo)致發(fā)酵過后直鏈淀粉的占比增大,這與文獻報道中乳酸菌發(fā)酵淀粉的特性一致[26-27]。
2.1.4 3 株乳桿菌產(chǎn)淀粉酶的粗酶活力
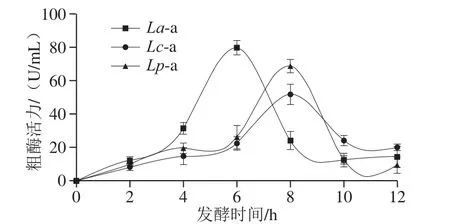
圖5 3 株乳桿菌產(chǎn)淀粉酶的粗酶活力Fig. 5 Production of amylase activity by three strains of Lactobacillus
由圖5可得,La-a活力在發(fā)酵第6小時達最大,為79.78 U/mL,整個發(fā)酵過程中4~8 h時酶活力較大,相對應(yīng)的該階段La活菌數(shù)增長速率最快,這是因為在淀粉酶的作用下La-IRFS體系內(nèi)還原糖含量顯著增大,可直接利用的碳源充足,La的生長環(huán)境最佳。而Lc-a與Lp-a活力則在8 h達最大,分別為51.89 U/mL和68.77 U/mL,同樣,6~10 h階段Lc-IRFS與Lp-IRFS中充足的還原糖使得該階段Lc與Lp活菌數(shù)增長速率最快。
2.1.5 pH值與總酸測定結(jié)果
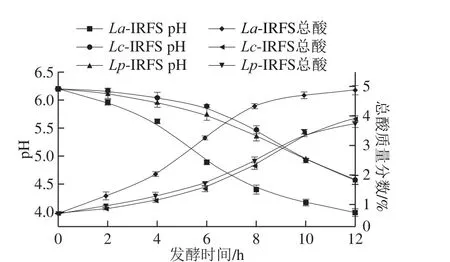
圖63 種乳桿菌-秈米粉漿體系發(fā)酵過程中pH值與總酸的變化Fig. 6 Changes in pH and total acid content during fermentation of indica rice flour slurry by three Lactobacillus strains
由圖6可得,3 種乳桿菌在秈米粉漿中均具有一定產(chǎn)酸能力,Lc的產(chǎn)酸能力與Lp相近,而La的產(chǎn)酸能力強于Lc和Lp,發(fā)酵12 h后能使La-IRFS體系的pH值降至4.0以下,而Lc-IRFS與Lp-IRFS的pH值則在4.5以上;發(fā)酵12 h后La-IRFS的總酸約為5%,Lc-IRFS與Lp-IRFS總酸皆低于4%。這是由于發(fā)酵時間在12 h內(nèi),La在秈米粉漿中的活菌數(shù)高于Lc與Lp,且其所產(chǎn)淀粉酶的最高總酶活力大于Lc與Lp,這使得La-IRFS中由淀粉轉(zhuǎn)化成的乳酸及乙酸等有機酸的含量更高,因而La-IRFS的pH值下降更快且總酸更高。其中,La-IRFS的pH值在4~8 h下降最快,總酸升高最快,這是由于6 h的La-a活力最高,淀粉大量降解為還原糖乳桿菌可利用的碳源量充足,活菌數(shù)增長較快,使更多的還原糖轉(zhuǎn)化為有機酸。Lc-IRFS與Lp-IRFS的pH值下降速率及總酸升高速率在6~10 h最快,同樣是因為Lc-a與Lp-a在8 h活力達到最高。
2.2 3 種淀粉酶的酶學(xué)特性
2.2.1 溫度與pH值對3 種淀粉酶的影響
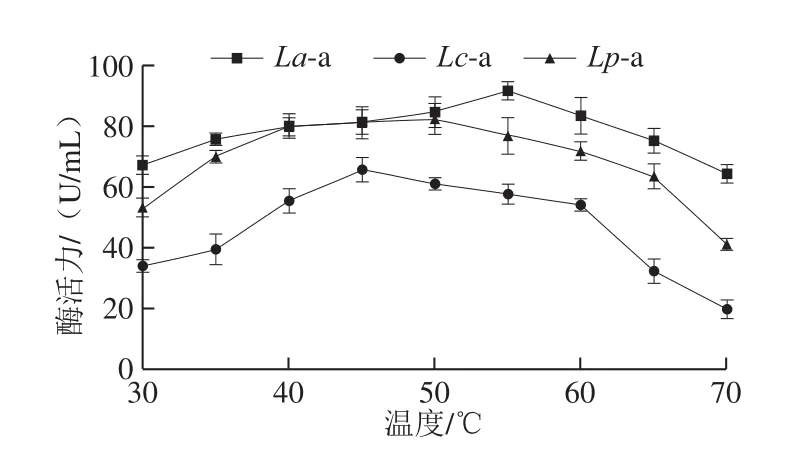
圖7 溫度對淀粉酶活力的影響Fig. 7 Effect of temperature on amylase activity
從圖7可看出,溫度為55 ℃時La-a活力最大,大于90 U/mL,30~70 ℃范圍內(nèi)La-a活力變化不大,因而La-a的較適溫度范圍為30~70 ℃;溫度為45 ℃時Lc-a活力最大,約為65 U/mL,40~60 ℃為Lc-a的較適溫度范圍;溫度為50 ℃時Lp-a活力最大,約為80 U/mL,35~65 ℃為Lp-a的較適溫度范圍。La-a在30~50 ℃與60~70 ℃活力仍保持較高,Lc-a和Lp-a在較低或較高溫度時活力較低,且在70 ℃時最低,分別低于20 U/mL和40 U/mL,說明La-a受溫度的影響較小,Lc-a和Lp-a受溫度的影響較大。

圖8 pH值對淀粉酶活力的影響Fig. 8 Effect of pH on amylase activity
從圖8可看出,La-a和Lp-a的最適pH值為6,該pH值下其酶活力分別大于85 U/mL和95 U/mL,Lc-a的最適pH值為7,該pH值下酶活力約為80 U/mL。La-a在較低與較高pH值下仍保持較高的酶活力,在pH值為3、4、9時酶活力都在65 U/mL以上;而Lc-a和Lp-a在較低或較高pH值時,酶活力明顯較低。綜上表明,La-a活力受pH值的影響較小,Lc-a和Lp-a受pH值的影響較大,三者皆為中性酶。pH值對酶活力性的影響是由于其改變了酶活性中心或與之有關(guān)的基團的解離狀態(tài),一般淀粉酶都在中性偏酸性環(huán)境下酶活力較大[28],而Lc-a則在中性偏堿性環(huán)境下酶活力較大,可能是由于Lc-a活性部位有關(guān)的基團在中性偏堿性狀態(tài)下達到最大解離狀態(tài)。此外,α-淀粉酶和異淀粉酶的最適pH值存在差異,Lc-a所產(chǎn)淀粉酶中α-淀粉酶、異淀粉酶的比例與La-a和Lp-a存在差異也可能導(dǎo)致這一現(xiàn)象。
2.2.2 3 種淀粉酶熱穩(wěn)定性

圖9 溫度和處理時間對La-a活力的影響Fig. 9 Effects of temperature and treatment time on La-a activity
如圖9所示,La-a在50~60 ℃處理180 min仍保持80%左右的相對酶活力,但當(dāng)溫度升高至70 ℃以上時,酶活力快速下降,經(jīng)70 ℃處理60 min后相對酶活力降至50%左右,180 min后相對酶活力降至30%,80 ℃以上處理60 min相對酶活力即降至20%左右,180 min后幾乎完全失活。可見La-a在50~60 ℃酶活力非常穩(wěn)定,但不可耐受70 ℃以上的高溫,80 ℃以上則失活速率極快。
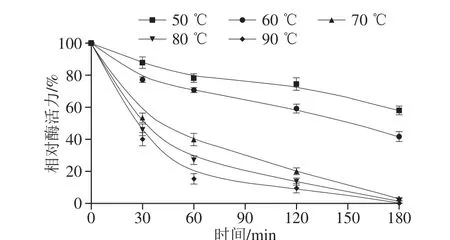
圖10 溫度和處理時間對Lc-a活力的影響Fig. 10 Effects of temperature and treatment time on Lc-a activity
如圖10所示,Lc-a在50 ℃處理180 min仍保持有60%以上的相對酶活力,在60 ℃處理180 min后降至40%,70、80、90 ℃處理60 min后相對酶活力分別降至40%、30%、20%以下,在70 ℃以上處理180 min后幾乎完全失活。即Lc-a在50~60 ℃范圍內(nèi)具有一定耐熱能力,70 ℃以上時失活速率較快。
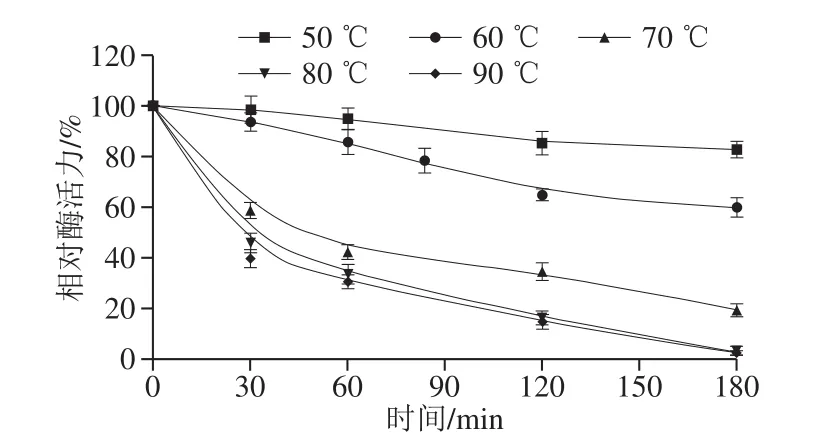
圖11 溫度和處理時間對Lp-a活力的影響Fig. 11 Effects of temperature and treatment time on Lp-a activity
如圖11所示,Lp-a在50 ℃處理180 min后仍保持90%的相對酶活力,在60℃處理180 min后仍保持有60%以上的相對酶活力,在70 ℃處理60 min后降至40%左右,80 ℃以上處理60 min后仍有超過30%的相對酶活力,處理180 min后幾乎完全失活。可見Lp-a可長時間耐受50 ℃的溫度,在60 ℃也具有一定耐熱性,不可耐受70 ℃以上的高溫,70 ℃以上時失活速率較快。
比較3 種乳桿菌所產(chǎn)的淀粉酶,Lp-a的耐熱性相對最強。
2.2.3 3 種淀粉酶pH值穩(wěn)定性
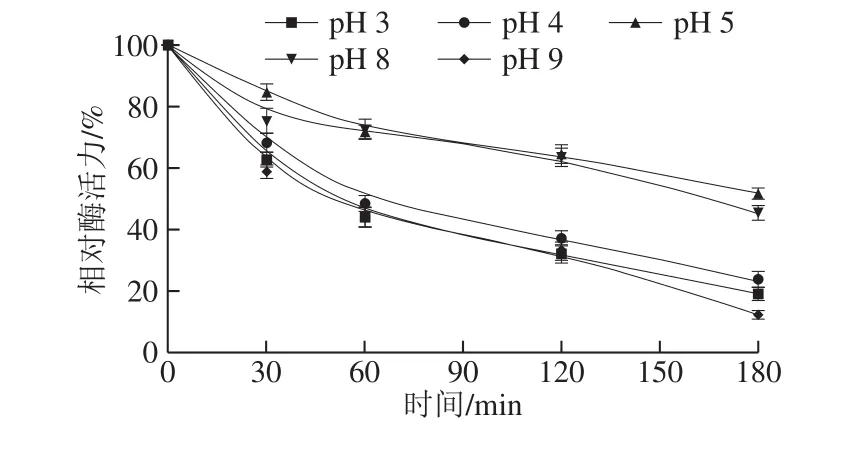
圖12 pH值和處理時間對La-a活力的影響Fig. 12 Effects of pH and treatment time on La-a activity
如圖12所示,La-a在pH值為5時的穩(wěn)定性較強,處理180 min后仍保持50%以上的相對酶活力,但pH值為4或更低時,60 min后La-a相對酶活力降至50%以下,180 min后降至30%以下;La-a在pH值為8時的耐堿能力較強,處理180 min后仍保持50%以上的相對酶活力,而當(dāng)pH值增大到9時,La-a失活速率較快,60 min后降至50%以下,180 min后相對酶活力在20%以下。可見La-a在pH 5~8范圍內(nèi)穩(wěn)定性較強。
如圖13所示,Lc-a的耐酸能力差,在pH值為5時處理60 min相對酶活力降至30%,pH值為3時處理30 min相對酶活力降至30%以下,60 min后降至10%以下,pH值為4以下處理180 min后幾乎完全失活。pH值為8時耐堿能力較好,處理120 min后仍保持50%以上相對酶活力,但pH值增大至9后耐堿能力驟降,處理60 min相對酶活力僅為10%,180 min后幾乎完全失活。可見Lc-a的pH值穩(wěn)定性很差,不可長時間處于pH 6~8以外的環(huán)境中。
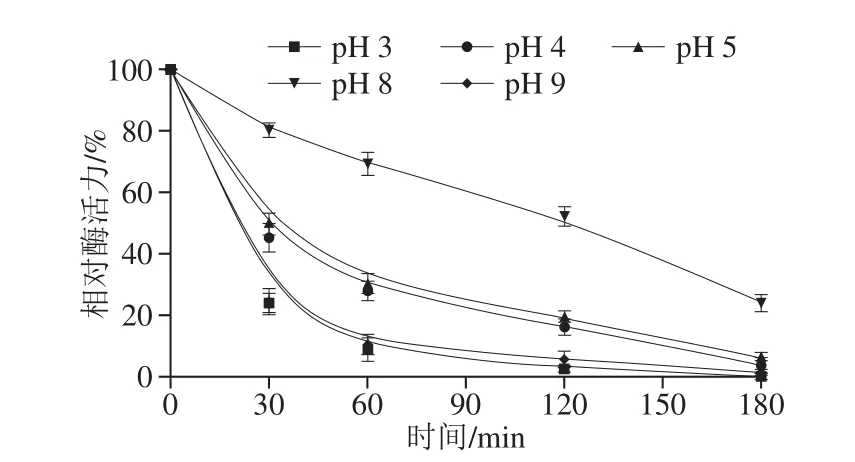
圖13 pH值和處理時間對Lc-a活力的影響Fig. 13 Effects of pH and treatment time on Lc-a activity
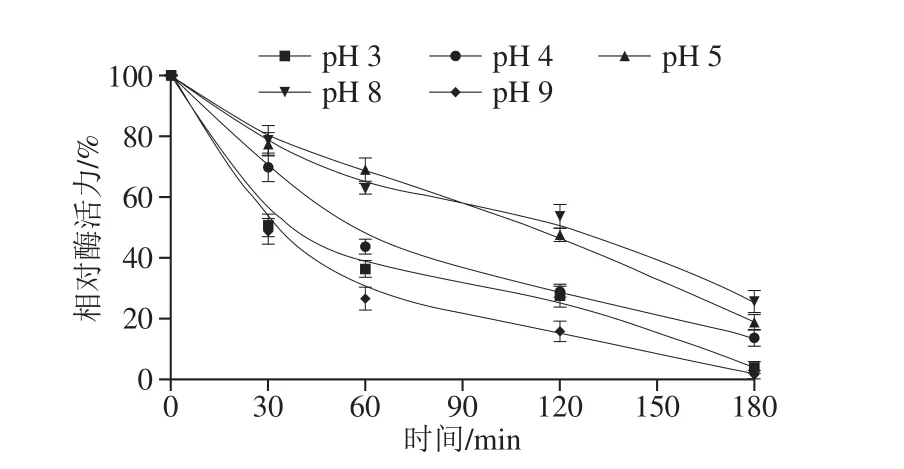
圖14 pH值和處理時間對Lp-a活力的影響Fig. 14 Effects of pH and treatment time on Lp-a activity
如圖14所示,Lp-a處于pH值為5和8的環(huán)境下120 min后相對酶活力仍有50%以上,在pH值為3、4或9的環(huán)境下處理60 min后相對酶活力即降至50%以下。在pH值為4、5、8的環(huán)境下180 min后,相對酶活力均降至30%以下,在pH值為3和9的環(huán)境中180 min后,幾乎完全失活。可見Lp-a的酸堿耐受能力較差,但略優(yōu)于Lc-a。
綜上可得,La-a在3 種乳桿菌所產(chǎn)淀粉酶中pH值穩(wěn)定性最好,Lp-a次之,Lc-a的pH值穩(wěn)定性最差。
3 結(jié) 論
本實驗通過構(gòu)建乳桿菌-秈米粉漿體系,研究3 株具有降解淀粉能力的乳桿菌La、Lc與Lp在秈米粉漿體系中單菌發(fā)酵過程,并研究其所產(chǎn)淀粉酶的酶學(xué)特性,同時也對發(fā)酵過程體系中淀粉含量,直鏈淀粉占比進行測定。結(jié)果表明,3 株乳桿菌中最適合在秈米粉漿體系中生長的為La,其在經(jīng)過12 h發(fā)酵后可使La-IRFS體系的pH值降至4.0以下,總酸達到5%,La在秈米粉漿體系中的產(chǎn)酸能力強于Lc與Lp,發(fā)酵過程中La活菌數(shù)始終大于Lc與Lp,且所產(chǎn)淀粉酶的最大酶活力亦大于Lc與Lp,能在6 h內(nèi)達到最大。在3 株乳桿菌所產(chǎn)的淀粉酶中,55 ℃時La-a活力最高,45 ℃時Lc-a活力最高,而Lp-a最適溫度為50 ℃,三者均不可耐受70 ℃以上的高溫,但其中Lp-a的耐熱性相對較強。La-a和Lp-a的最適pH值為6,Lc-a最適pH值為7,三者皆為中性酶,pH值穩(wěn)定性的排序為:La-a>Lp-a>Lc-a。發(fā)酵過后,乳桿菌-秈米粉漿體系中的總淀粉含量均顯著降低,直鏈淀粉在總淀粉中的占比增大,說明乳桿菌所產(chǎn)淀粉酶中有一定量的異淀粉酶,可將體系中的支鏈淀粉轉(zhuǎn)化為直鏈淀粉,從而導(dǎo)致發(fā)酵過后直鏈淀粉的占比增大。乳酸菌一般不產(chǎn)淀粉酶,但有些乳酸菌在碳饑餓的情況下會利用替代碳源[29],在發(fā)酵過程中某些多糖降解基因(如apu、yucG)會超量表達[30]。初步推測本實驗中的3 株乳桿菌在秈米粉漿體系中由于缺乏碳源進入碳饑餓狀態(tài),其與淀粉酶相關(guān)的基因被誘導(dǎo)表達,從而擁有生產(chǎn)淀粉酶的能力。

