高血壓早期心肌應力及細胞外間質容積的動物實驗研究
莊白燕,崔辰,何健,王學民,王欣,段雪晶,王紅月,趙世華,陸敏杰
高血壓性心臟病會引起一系列左心室(Left ventricle,LV)異常改變,包括左心室形態改變、左心室肥厚、收縮和舒張功能障礙。研究證明高血壓是發生重大心臟不良事件的主要危險因素[1],及早診斷和控制原發性高血壓患者的血壓及左心室功能改變,可以從根本上減少心血管事件的發生率和病死率。高血壓性心臟病的干預應以早期功能監測和治療為重點,常規影像學檢查很難評估高血壓心臟病早期的心臟結構及功能改變,但是射血分數等心功能參數的異常多發生在心肌疾病的晚期,因此左心室功能早期監測一直未能實現[2]。近年來,心臟磁共振特征追蹤(cardiac magnetic resonance feature tracking,CMR-FT)技術被認為是目前測量應變的有效手段,CMR-FT主要針對心臟內、外膜邊界,檢測腔-組織界面的內、外運動,可量化不同層次心肌運動的狀態[3],是心臟功能的敏感指標。另外,T1-mapping 技術可以直接定量測定心肌組織的T1值從而定量評估心肌損傷的程度和范圍,準確評價多種心肌病變的心肌組織特征[4-6]。細胞外間質容積分數(extracellular volume,ECV)基于平掃T1值、增強后T1值,同時引入了血細胞比容的值進行校對,因而可有效避免干擾因素,更加穩定、精準地反映心肌間質改變的嚴重程度及范圍。本課題組前期進行的臨床研究發現T1及ECV較釓對比劑延遲強化(late gadolinium enhancement,LGE)更敏感地發現高血壓心肌纖維化[7],但因臨床研究缺乏病理證據,也未進行心肌應力的功能學研究。本研究擬以病理為金標準,聯合應用CMR-FT及T1-mapping評估高血壓早期心臟結構、功能及心肌組織特征改變。
材料與方法
1.實驗動物
本研究前瞻性納入了19頭健康中國雄性小型豬(高血壓組13頭,對照組6頭),6~12個月,體重20~25 kg。對于高血壓組,通過結扎左腎動脈建立高血壓動物模型[8]。進行基線MRI掃描后,在麻醉后做垂直腹部切口,分離腎動脈和腎靜脈,游離長度0.5~1.0 cm。將直徑為0.25 mm的針頭置于動脈上方,將縫合線牢固地綁在針頭和血管周圍,然后取出針頭。對照組(假手術組)除未結扎左腎動脈外,其余操作均與實驗組相同。所有動物術后均接受抗細菌治療以預防感染(頭孢唑啉1.0 g,肌肉注射,每天兩次,連續3天),術后鎮痛使用丁丙諾啡(0.3 mg,每天兩次,連續3天)[9]。
2.CMR掃描方法
對實驗組和對照組中的所有動物都在基線,手術后6個月進行了CMR檢查,所有CMR檢查均在Philips 3.0T MR上進行(Ingenia,Philips Healthcare,Best,Netherland)。心臟短軸電影序列:采用穩態自由進動梯度回波(steady state free precession,SSFP)技術,從心底到心尖以進行無間距連續掃描,結合心電及呼吸屏氣采集短軸電影序列(視野321 mm×321 mm,矩陣180×200,層厚8 mm,TR 3.10 ms,TE 1.56 ms,翻轉角45°,時間分辨率43 ms,并行采集系數2)。LGE:對比劑注射后10 min,采用心電門控屏氣相位敏感反轉恢復PSIR序列,在與心臟電影圖像相同的橫截面位置掃描(視野350 mm×321 mm,矩陣192×132,層面厚度8 mm,TR 6.1 ms,TE 3.0 ms,翻轉角25°,并行采集系數2)。T1-mapping:使用改良的Look-Locker反轉序列(MOLLI),在給予對比劑之前和經耳緣靜脈高壓注射器給予對比劑(0.15 mmol/kg)15~20 min之后,在四腔,兩腔和三個左心室短軸(基底、中間和心尖平面)層面掃描。心尖短軸定義為緊鄰心尖帽的一層,心室中間短軸定義為位于乳頭肌中部的一層,基底短軸定義為在電影成像中顯示心室腔內血池的最后一層。成像參數:視野300 mm×300 mm,矩陣152×150,層厚5 mm,TR 2.30 ms,TE 1.03 ms,翻轉角20°,并行采集系數2。
3.CMR圖像分析
心功能:采用圖像后處理軟件CVI 42(Circle Cardiovascular Imaging Inc,Calgary,Canada)進行左心室心功能檢測。心內膜和心外膜的輪廓通過半自動檢測獲得并進行手動校正。心室腔包括乳頭肌和心肌小梁在內。舒張末期和收縮末期分別定義為心動周期中心室最大和最小的時期[10]。心功能參數包括左心室射血分數(left ventricular ejection fraction,LVEF)、左心室舒張末期直徑(left ventricular end-diastolic dimension,LVEDD)、左心室舒張末期容積(left ventricular end-diastolic volume,LVEDV)、左心室收縮末期容積(left ventricular end-systolic volume,LVESV)、左心室每搏量(left ventricular stroke volume,LVSV)、左心室心輸出量(left ventricular cardiac output,LVCO)和左心室舒張末期質量(left ventricular mass at end-diastole,LV mass at ED)。并將上述心功能參數根據體表面積(body surface area,BSA)標準化,得到相應的指數參數。
應力和應變率:采用QStrain軟件(QStrain 2.0,Medis BV,Leiden,Netherland)在SSFP電影圖像中分析應力和應變率,在指定模塊中打開短軸及長軸電影序列,勾勒左心室內、外膜,手動調整心內膜與心外膜邊界處的曲線,使其與室壁厚度保持一致,然后運行程序,自動計算左心室應力及應變力。參數包括徑向應力(radial strain,RS),徑向收縮期應變率和舒張早期應變率(radial systolic strain rate and early diastolic strain rate,RSRS,RSRE),周向應力(circumferential strain,CS),周向收縮期應變率和舒張早期應變率(circumferential systolic strain rate and early diastolic strain rate,CSRS,CSRE)(圖1),縱向應力(longitudinal strain,LS),縱向收縮期應變率和舒張早期應變率(longitudinal systolic strain rate and early diastolic strain rate,LSRS,LSRE)(圖2)[11]。
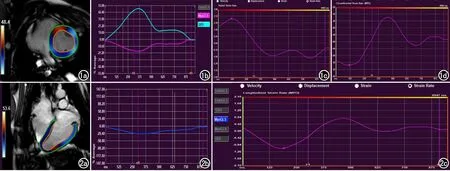
圖1 左室整體徑向、周向應力及應變率測量。a)心臟內外膜描記方法示意圖,其中橙色圓圈為內膜,綠色圓圈為外膜;b)電影圖像上測量徑向及周向應力及其變化的曲線圖,其中徑向應力為(藍線),周向應力為(紅線);c)電影圖像上徑向收縮期應變率及舒張早期應變率及其變化的曲線圖;d)電影圖像上周向收縮期應變率及舒張早期應變率及其變化的曲線圖。 圖2 左室整體縱向應力及應變率測量。a)心臟長軸內外膜描記方法示意圖,其中橙線為心內膜,綠線為心外膜;b)電影圖像上測量縱向應力及其變化的曲線圖;c)電影圖像上縱向收縮期應變率及舒張早期應變率及其變化的曲線圖。
LGE:采用盲法,使用CVI42軟件進行分析,使用全寬/半最大值方法對LGE進行半自動定量分析[12]。測量過程中手動校正排除血池或心包的部分容積偽影。
ECV:在CVI 42軟件上進行分析,心內膜和心外膜的輪廓通過半自動檢測后手動校正。根據美國心臟協會推薦的心肌17節段法,本研究測量并計算了心肌各節段的ECV值(因為無法獲得心尖值,因此刪除了心肌的第17段)。ECV的計算基于增強前和增強后T1-mapping的數據,使用以下公式:ECV(%)=(1-Hct)·(ΔR1 myo/ΔR1blood)·100%,其中ΔR1myo =(1/T1myo增強后-1/T1myo增強前),ΔR1blood=(1/T1blood增強后-1/T1blood增強前)分別是心肌和血池增強前后的差值,HCT為血細胞比容[13]。
4.病理
在最后一次MR掃描后處死動物,在麻醉下靜脈注射20 mL 15%(v/w)氯化鉀,直至動物心臟停跳。將取出的心臟浸入95%乙醇中20 min固定,預冷至-80℃,然后由經驗豐富的病理醫生從下至上將心臟切成6 mm厚的短軸切片。然后將切片浸入37℃水浴的1%的三苯基氯化四唑(TTC)溶液中10 min。根據標志點(如乳頭肌和右心室插入點等)將TTC圖像與CMR圖像進行匹配。這個過程由放射科醫生和病理科專家共同完成。然后由病理科專家進行HE、Masson和天狼星紅染色。使用半自動圖像分析軟件(ImageJ _v1.8.0),以膠原纖維面積占心肌總面積的百分比來確定膠原纖維體積分數(collagen volume fraction,CVF)。
5.統計學分析
采用 SPSS 22.0軟件進行分析,連續變量表示為平均值±標準差。使用Kolmogorov-Smirnov's檢驗連續變量是否是正態分布。采用配對t檢驗或Wilcoxon秩和檢驗(取決于數據是否正態分布)比較組與組之間的差別。以P<0.05為差異有統計學意義。使用Pearson相關和線性回歸模型分析應變與ECV之間的關系。
結 果
在19只動物中,高血壓組的一只動物在術后6天死于感染(死亡率5.0%)。因此最終共18只豬納入分析(高血壓組12只,對照組6只),對所有動物成功地進行了兩次MRI檢查并獲得了病理學染色。
1.LV形態和功能改變
對照組的血壓和心功能在基線和術后6個月之間無明顯差異。高血壓組中,,手術后6個月的收縮壓和舒張壓從102/71 mmHg增加到145/86 mmHg。高血壓組造模前后的左心室舒張末期容積指數無明顯差異(61.9±4.6 mL/m2、66.6±10.4 mL/m2,P= 0.96)。平均LVEF在基線時為(72.7±1.4)%,在手術后6個月為(69.9±3.5)%(P= 0.34)。兩組的詳細血壓和心功能參數見表1。
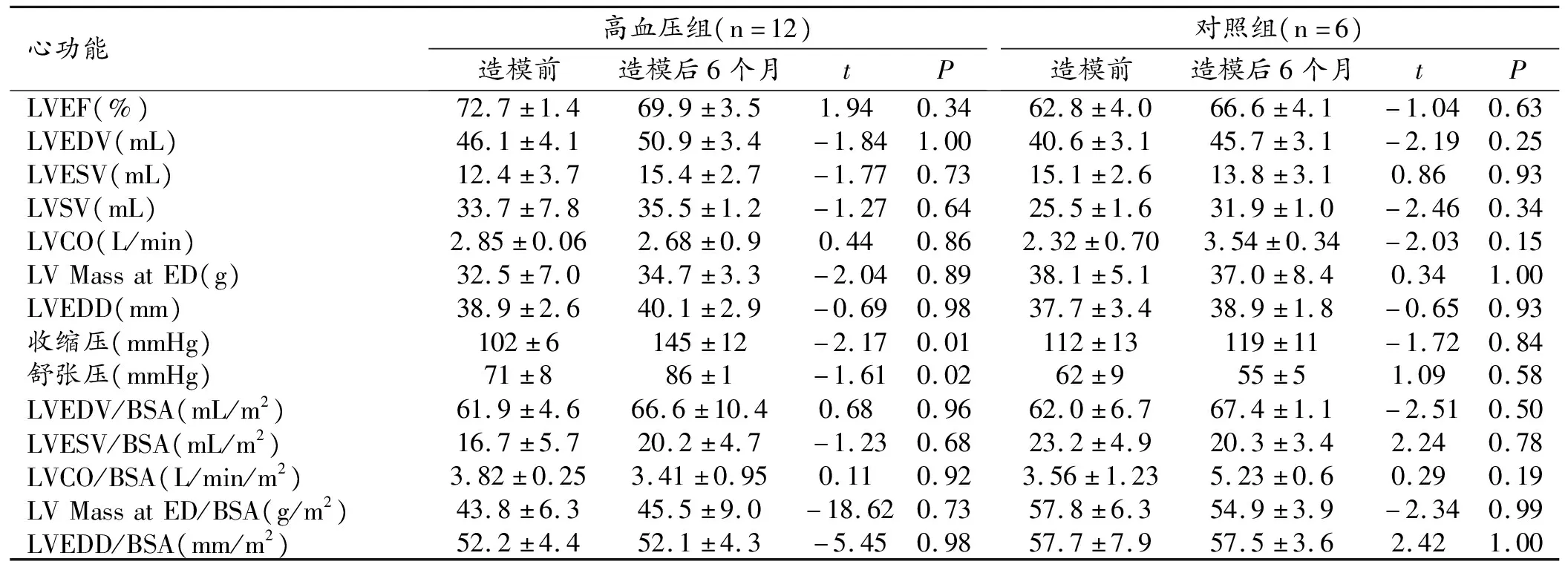
表1 高血壓組與對照組左心室心功能及血壓情況
2.LV心肌應變
左心室的整體RS、RSRS、RSRE、CS、CSRS、CSRE、LS、LSRS、LSRE見表2。高血壓組和對照組之間除RSRS、RSRE及 CSRS外,所有應力和應變率均差異均有統計學意義(P均<0.05)。術后6個月,高血壓組的RS(從46.05~30.40)、LS(從-18.06~-12.51)、CSRE(從1.52~0.92)、LSRE(從1.35~1.01)顯著降低(P<0.05,表2,圖3),而對照組沒有顯著變化。在應變與ECV的相關性分析中發現,心肌ECV與RS呈負相關(r=-0.74,P=0.01),與LSRE呈負相關(r=-0.92,P<0.001),與CSRE呈負相關(r=-0.65,P=0.02),見圖4。
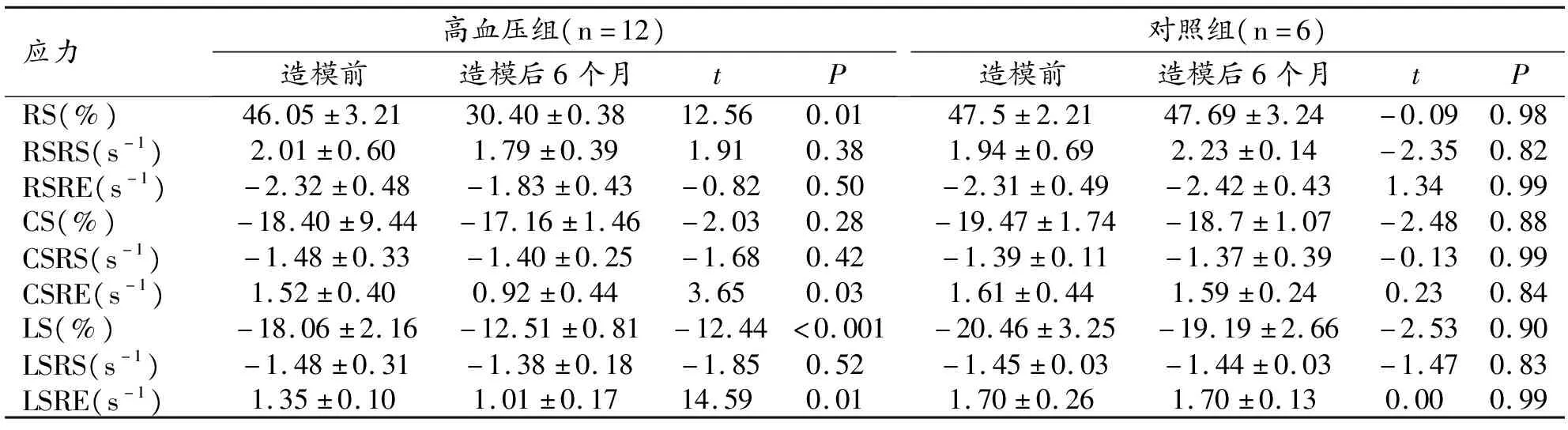
表2 高血壓組和對照組的詳細應力和應變率數值
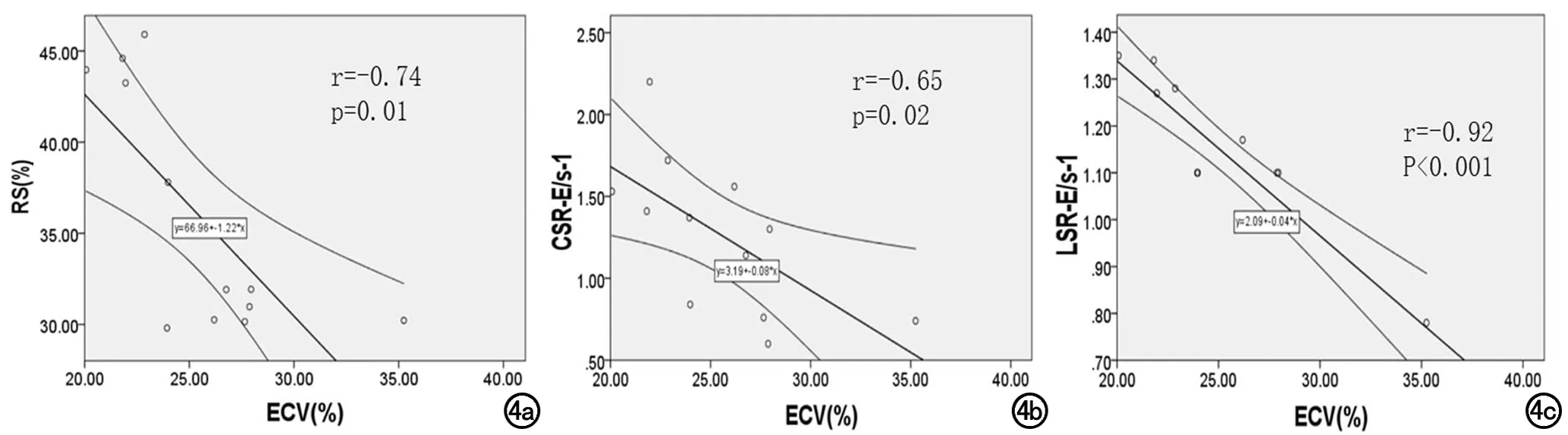
圖4 ECV與應力及應變率的相關性研究,實線條表示最佳擬合線和均值的95%置信區間。a)ECV與RS的相關性;b)ECV與CSRE的相關性;c)ECV與LSRE的相關性。
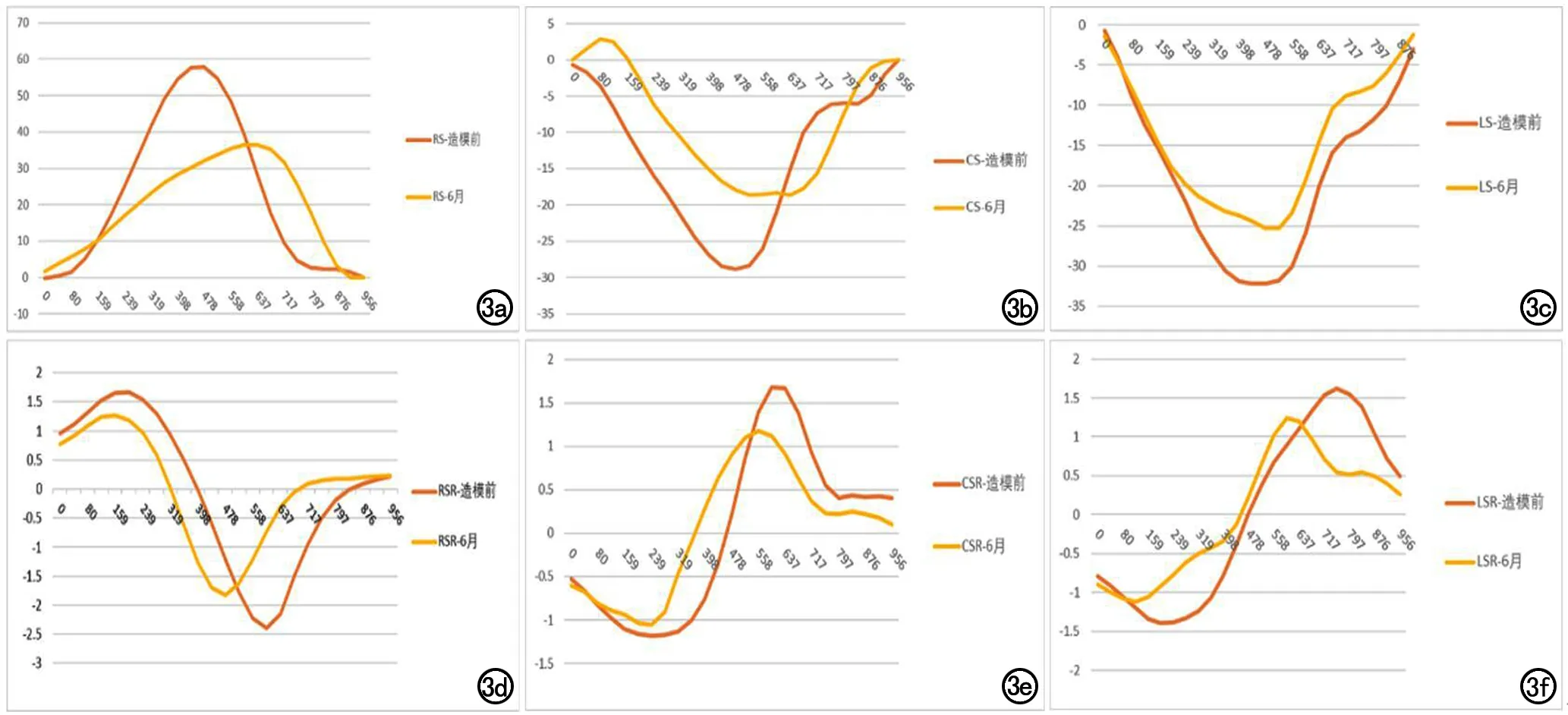
圖3 高血壓組基線和造模后6個月的一個心臟周期內的應力和應變率。造模后6個月的RS、RSRS、RSRE、CS、CSRS、CSRE、LS、LSRS和LSRE均減小。a)RS;b)CS;c)LS;d)RSR;e)CSR;f)LSR。
3.心肌組織特征
在手術前后的各個階段,對照組和高血壓組均未檢測到LGE。但是高血壓組與對照組之間的ECV值差異具有統計學意義(P=0.02)。高血壓組術前、手術后6個月的總體ECV差異具有統計學意義(21.7±1.2,29.2±4.1,P=0.03)。造模前后心臟的ECV詳細分段對比見表3。
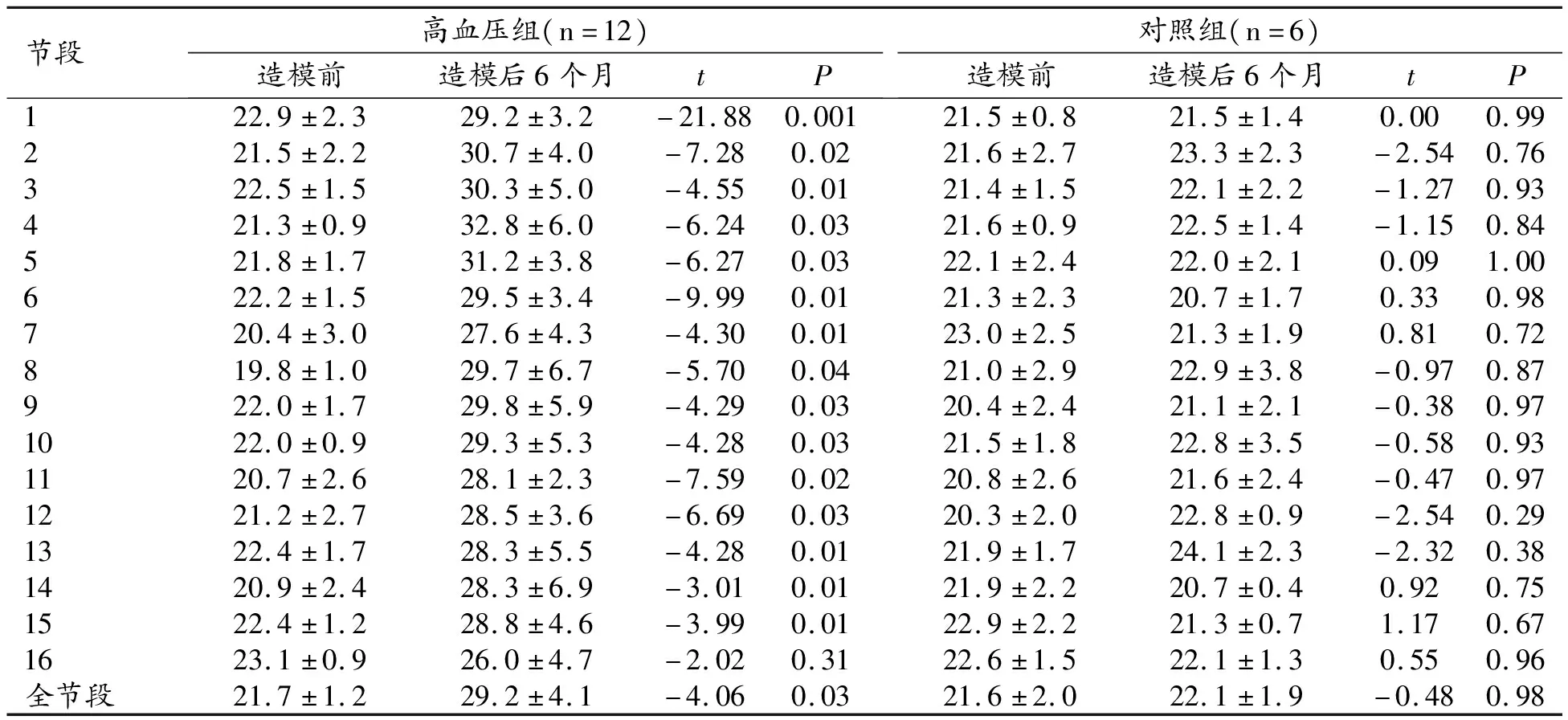
表3 高血壓組與對照組各節段造模前、造模后6個月的ECV值
4.病理
在手術后獲得的切片中,TTC大體染色均未觀察到明顯的心肌異常表現,進一步的組織學染色(HE、Masson和天狼星紅)可以看出基線無明顯異常,術后6個月左心室出現了明顯心肌間質纖維化(圖5),左心室17個節段的CVF見表4。另外,CVF與RS具有很好的相關性(r=-0.61,P=0.03,圖6)。
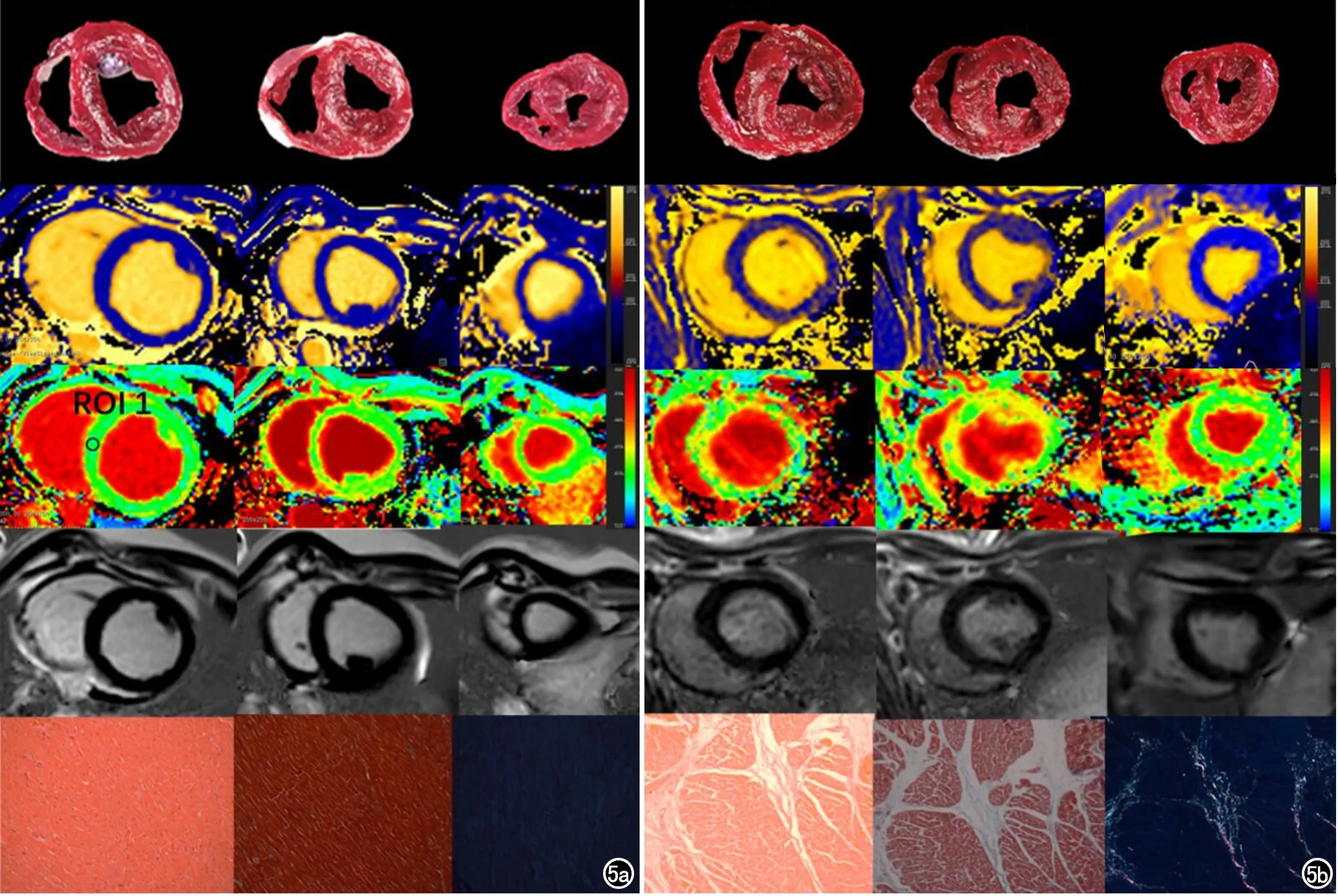
圖5 TTC染色(第一行)、ECV圖像(第二行)、native T1圖像(第三行)、LGE(第四行)和ROI 1的HE、Masson和天狼星紅染色(第五行,×200)。ECV的色階范圍為1%~60%;native T1的色階范圍為500~2000 ms;TTC染色沒有明顯的異常表現;LGE圖像中沒有明顯的信號強度增加。a)基線,ECV沒有明顯增加(ROI1 = 20.0%),HE,Masson和天狼星紅染色中沒有明顯的心肌纖維化;b)術后6個月,左心室native T1及ECV明顯增加。HE、Masson和天狼星紅色染色顯示術后6個月左室出現明顯的間質纖維化。
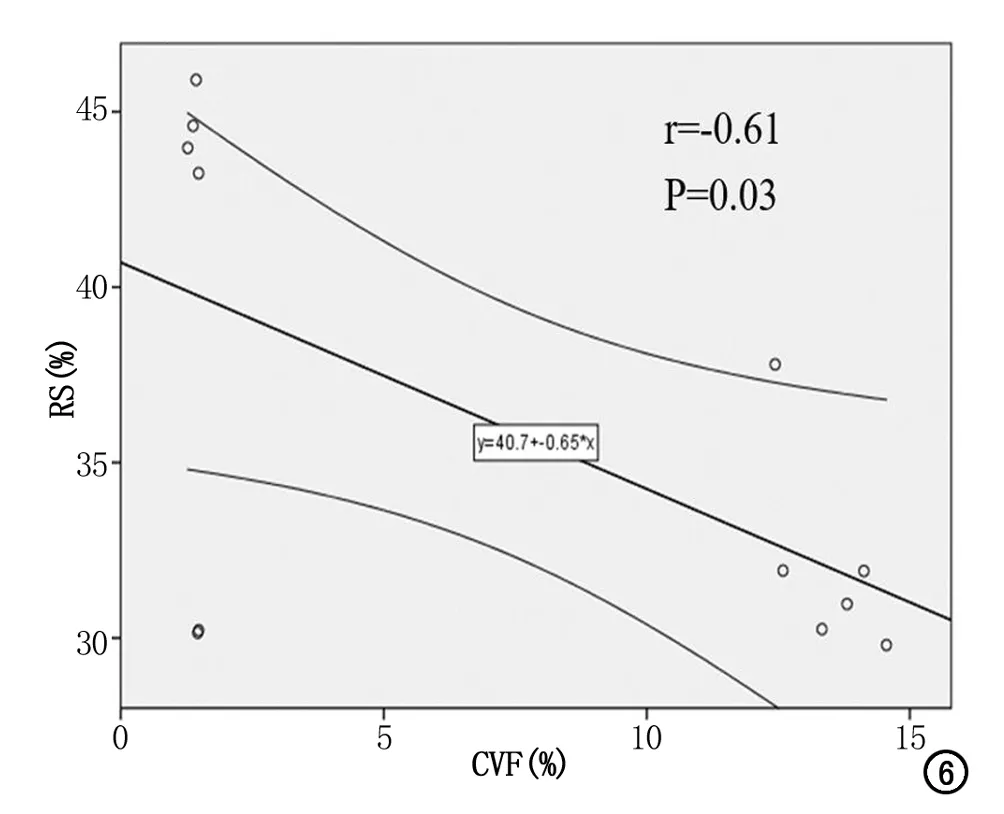
圖6 CVF與RS呈負相關,實線條表示最佳擬合線和均值的95%置信區間。
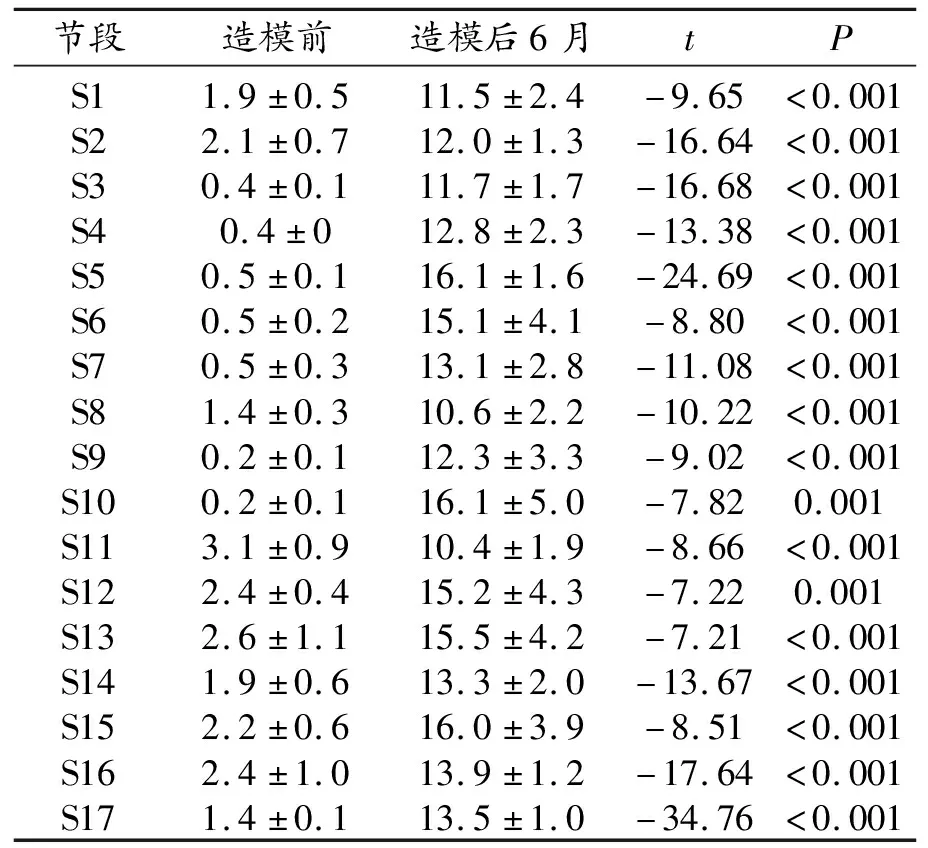
表4 高血壓組17個節段造模前、造模后6個月的CVF
討 論
本研究評估了高血壓早期的不同階段的應力和應變率特點,并在病理水平觀測左心室心肌纖維化的程度。筆者發現RS、LS、CSRE和LSRE值是隨高血壓的進展而減低的,CVF、ECV的值是明顯增加的,然而在高血壓早期左心室射血分數等心功能參數和LGE沒有明顯的變化,說明在尚未出現心功能明顯變化及心肌明顯損傷的高血壓早期,心肌應變和ECV已有明顯的改變。及時監測心肌應變的變化對高血壓早期患者的干預和心臟結構監測有重要的意義。
本課題組先前的一個臨床研究前瞻性地對連續134例高血壓患者進行了ECV測量,以確定CMR定量的ECV是否能顯示左心室結構異常[7]。結果表明,LGE陰性的高血壓早期患者的左心室結構異常可被ECV定量識別。本文進一步研究了高血壓早期心肌應變的動態變化,并且在病理上證實了ECV的動態升高與心肌細胞外間質纖維化增重的程度一致,說明ECV可以早期、敏感監測心肌細胞間質內纖維化,從而揭示高血壓早期的心肌細胞外間質增多是除心臟細胞肥大及肌小節增加的心肌肥厚的另一個重要原因。另外本研究發現RS、CSRE、LSRE的減小與ECV的增加有相關性,揭示了在高血壓早期,心臟收縮功能可能因心肌纖維化的出現而減低,心肌應變可以早期敏感地反映心臟功能的改變。
EF是一項廣泛應用于不同心臟疾病分期的指標,在判斷預后、風險分層和選擇治療方案等方面發揮作用,既往一致認為EF正常的高血壓性心臟病的心功能異常體現在舒張功能異常[14],然而EF是反應心室的容積變化,并不是心肌的實際運動特質,而且易受瓣膜反流、心率等因素的干擾。有新研究表明,如果使用足夠敏感的檢測方法,許多EF正常的高血壓患者的心肌收縮功能實際上存在可檢測到的異常[15]。CMR-FT通過追蹤心肌各節段的位置變化得到該節段心肌的各種應力和應變率,能更準確地反映心肌本身的運動并評價心肌在三維空間運動特征,從而更好地評價左心室功能。
之前有研究表明,高血壓患者縱向收縮應力的減低與膠原的更新和心肌纖維化程度的增加有關[16],在本研究中,發現應變率(代表按距離標準化后的心肌速度)也有較明顯的組間差異。這與Narayanan等[17]的研究一致,他們使用超聲斑點追蹤的方法對動脈性高血壓輕度左心室肥厚的患者進行研究,發現組織多普勒成像測量的心肌收縮速度降低,而二維斑點應力成像測量的應力值仍然在正常范圍內,說明與左心室肥厚患者的應力相比,應變率是監測心肌功能障礙的更敏感的指標。考慮到CMR相對于超聲心動圖的優勢,即不受鄰近骨骼或空氣的干擾,對操作員的依賴性較小,CMR的測量可提供更為準確的結果。目前心臟護理的重點是早期發現和早期開始治療,以減少心肌功能障礙的發生[18],應將CMR的應力和應變率參數結合起來監測心臟的收縮和舒張功能改變。
綜上所述,高血壓早期有心肌細胞外間質纖維化的出現,并且隨著高血壓的進展而加重,在常規CMR心功能檢查無明顯異常改變時,CMR-FT已經可以檢測到左心室縱向、徑向應力和周向、縱向舒張早期徑向應變率有所減低。ECV和心肌應變能敏感地反映繼發于高血壓的左心室結構變化和功能性改變,為早期發現高血壓心臟改變提供依據,從而防止疾病進程,改善遠期生存質量。

