人工髖關節置換治療股骨頸骨折合并尿毒癥的療效及安全性分析
劉 超,戴 慧
(1.南華大學附屬第一醫院創傷骨科,湖南 衡陽 421000;2.長沙市第四醫院血液凈化中心,湖南 長沙 410006)
隨著我國步入老齡化社會,骨質疏松性骨折的發生率逐年增高,其中以股骨頸骨折多見,其致殘率及病死率高,治療難度大[1]。尿毒癥是各種原因導致的慢性腎臟病的晚期,需要維持性血液透析治療。尿毒癥患者由于慢性腎功能不全,往往全身情況差,合并眾多基礎疾病,且骨質疏松發生率高,更易發生股骨頸骨折[2]。股骨頸骨折合并尿毒癥處理困難,手術麻醉風險大,圍手術期并發癥發生率高[3]。但目前對于股骨頸骨折合并尿毒癥的相關報道較少。本文擬探討人工髖關節置換手術治療股骨頸骨折合并尿毒癥的臨床療效及安全性。
1 資料與方法
1.1 一般資料
2014年1月至2018年12月南華大學附屬第一醫院骨科收治的股骨頸骨折合并尿毒癥患者13例,選取其中10例行人工髖關節置換手術作為觀察組,另3例未行手術治療,予以排除;同期行人工關節置換手術治療的無尿毒癥股骨頸骨折患者20例作為對照組。所有患者均為單側肢體骨折,均為輕微外傷導致的閉合性骨折,排除病理性骨折,并經X線片檢查確診,Garden分型Ⅲ型/Ⅳ型,排除神經、血管損傷。其中男性13例,女17例。年齡49~94歲,平均年齡(75.00±10.42)歲。兩組患者性別、合并基礎疾病、骨折類別、Garden分型、白蛋白水平、手術方式及股骨柄固定方式比較差異無統計學意義(P>0.05)。其中尿毒癥組患者的平均年齡比無尿毒癥組小,尿毒癥組血紅蛋白較無尿毒癥組更低(P<0.05)。見表1。
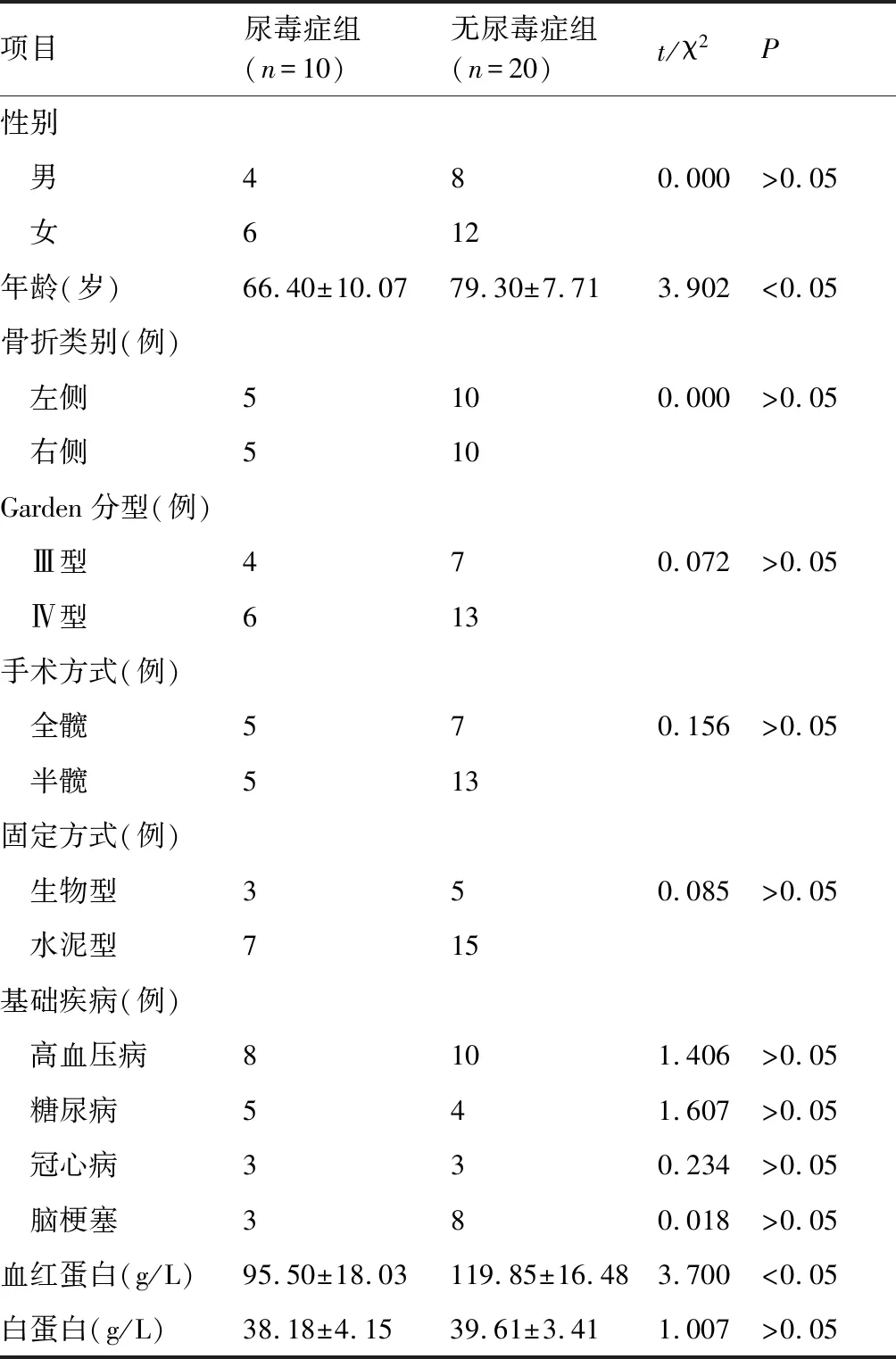
表1 兩組患者一般資料比較
1.2 術前處理
兩組患者入院后完善常規檢查。高血壓患者規律服用降血壓藥物,控制血壓至正常范圍。糖尿病患者口服降糖藥物或皮下注射胰島素降糖,監測血糖,控制血糖平穩,空腹10 mmol/L以下,餐后2 h 12 mmol/L以下。完善心臟彩超,了解心臟收縮及舒張功能,EF值小于40%認為不能耐受手術,予以排除。
指導踝泵鍛煉及股四頭肌等長收縮功能鍛煉,常規低分子肝素抗凝,術前一天查雙下肢深靜脈彩超,排除下肢深靜脈血栓。協助患者定期翻身拍背預防壓瘡及墜積性肺炎。予以鎮痛等對癥處理,糾正低白蛋白血癥,抗骨質疏松治療。加強營養支持治療,進食低脂、高蛋白食物,進食不佳時適當靜脈補充氨基酸。髖部骨折患者臥床時間長,往往都有便秘,盡早使用通便藥物,保持大便通暢。睡眠不佳時,服用改善睡眠藥物。
尿毒癥患者往往外傷前就有腎性貧血,加之骨折失血,往往貧血嚴重,給予重組人促紅素注射液(益比奧10 000 IU,皮下注射,一周一次)、補鐵治療,必要時輸注濃縮紅細胞,糾正血紅蛋白至90 g/L。患者往往伴有甲狀旁腺功能亢進,術前常規檢查甲狀旁腺激素及血鈣水平,補充鈣劑與維生素D,使用降鈣素改善骨質疏松。術前1天聯系血透室行無肝素血液透析治療。
1.3 手術操作
椎管內麻醉,中心靜脈置管,監測中心靜脈壓。側臥位,取患髖后側入路,逐層切開,止點處切斷梨狀肌、閉孔內肌等短外旋肌群,T形切開關節囊,顯露股骨頭頸結合部位及骨折端,內旋內收患肢并屈膝屈髖,于股骨小轉子上方1~1.5 cm鋸斷股骨頸,取出股骨頭。行全髖關節置換時需磨挫髖臼至軟骨下骨面少量滲血,試模后安裝生物型髖臼。股骨擴髓試模后置入骨水泥型或生物型股骨柄,保持10°~15°前傾角。半髖關節置換則直接安裝股骨柄。安裝股骨頭假體,復位,檢查穩定性。術中局部浸潤氨甲環酸,嚴密修復后方關節囊及外旋肌群,逐層縫合切口。
1.4 術后處理
術后監測中心靜脈壓,控制血壓、血糖,及時糾正貧血及低白蛋白,保持血紅蛋白高于80 g/L,白蛋白高于30 g/L,維持水、電解質及酸堿平衡。預防感染、鎮痛、抗凝對癥支持治療。繼續加強營養,保持大便通暢,改善睡眠。指導患者早期踝泵及股四頭肌等長收縮鍛煉,術后第1~3天指導患者床上翻身及坐立,情況允許的情況下可扶助行器下地行走。
尿毒癥組,術后第一天透析一次,此后繼續規律透析。控制入量,監測24 h出入水量,維持水、電解質及酸堿平衡。注射重組人促紅素注射液及補鐵糾正貧血,繼續抗骨質疏松治療。
1.5 評價指標
比較兩組患者入院至手術時間、輸血率、住院時間及并發癥等住院期間情況;記錄兩組術后髖關節功能Harris評分。髖關節功能采用Harris評分標準,從疼痛、關節功能、活動情況和關節畸形四個方面評分,90~100分為優,80~89分為良,70~79分為可,<70分為差。
1.6 統計學方法
數據應用SPSS22.0統計學軟件進行分析,計量資料采用均數±標準差表示并采用t檢驗,計數資料采用χ2檢驗,P<0.05為差異有統計學意義。
2 結 果
2.1 兩組患者住院期間情況比較
尿毒癥組在入院至手術時間、住院時間上均較無尿毒癥組長,輸血率較無尿毒癥組高(P<0.05)。住院期間無尿毒癥組2例并發癥肺部感染1例,傷口淺表感染1例;尿毒癥組2例合并并發癥:均為肺部感染。兩組并發癥發生率間比較,差異無統計學意義(P>0.05)。見表2。
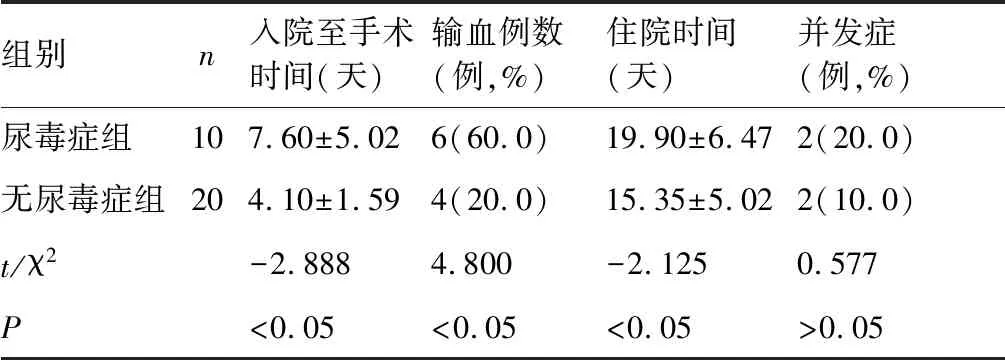
表2 兩組患者住院期間情況比較
2.2 兩組隨訪及髖關節Harris評分比較
兩組患者術后1,2,3,6,9,12個月門診定期復查,之后每年復查。24例患者最終獲得平均26.1(13~59)月隨訪,無感染、假體周圍骨折、假體松動及下沉發生。至隨訪結束時,無尿毒癥組3例死亡,其余17例獲得隨訪;尿毒癥組2例死亡,1例隨訪丟失,其余7例獲得隨訪。無尿毒癥組術后末次隨訪Harris評分為(85.29±11.95)分,尿毒癥組為(90.43±5.16)分,兩組比較,差異無顯著性(t=-1.084,P>0.05)。
3 討 論
3.1 尿毒癥患者更易發生股骨頸骨折
尿毒癥患者在骨代謝方面主要表現在骨吸收增加,骨密度下降[4]。尿毒癥導致的繼發性甲狀旁腺功能亢進,造成鈣磷代謝、骨代謝紊亂[5],使骨流失進一步加劇,骨密度下降,導致嚴重骨質疏松[6]。尿毒癥患者,通常活動量較少[7],也是骨質疏松的不利因素,加之肌肉萎縮,更易發生骨質疏松性骨折,尤其是股骨頸骨折[2]。尿毒癥患者在中老年人較多見,也是骨質疏松性骨折發生率高的不利因素[8]。本文尿毒癥組平均年齡比無尿毒癥組小,提示尿毒癥患者發生股骨頸骨折年齡較普通人群提前。
3.2 股骨頸骨折合并尿毒癥處理困難
股骨頸骨折合并尿毒癥患者,由于慢性腎功能不全,往往全身情況差,同時合并基礎疾病,如高血壓、糖尿病等。腎臟分泌的促紅細胞生成素不足,往往導致腎性貧血。腎小球濾過功能障礙,不可避免導致低白蛋白,電解質紊亂,大大增加了手術麻醉的風險,以及外科治療圍術期處理的難度,手術并發癥及病死率高[3,9]。Suh YS等[10]學者對比手術治療63例合并CKD髖部骨折及67例未合并CKD髖部骨折,CKD組17例出現并發癥,明顯高于無CKD組的8例并發癥,且證明尿毒癥是髖部骨折術后并發癥的顯著危險因素。Hsiue PP等[11]學者發現與沒有腎臟疾病患者相比,合并尿毒癥股骨頸骨折患者行半髖關節置換術輸血、再次入院及翻修手術風險增加。本文報告中,兩組患者基礎疾病及并發癥發生率相似,但尿毒癥組患者術前血紅蛋白明顯偏低。此外,股骨頸骨折合并尿毒癥患者治療期間仍需要規律透析,給患者增加痛苦,也增加護理難度。尿毒癥患者腎功能不全,限制了許多腎毒性藥物的使用及最大劑量。且尿毒癥組手術前準備時間長,入院至手術時間及住院時間均延長。本文排除3例股骨頸骨折合并尿毒癥患者,均因為一般情況差,無手術條件,從而放棄手術治療。
3.3 股骨頸骨折合并尿毒癥圍手術期處理的重點
股骨頸骨折合并尿毒癥患者,應聯系血液凈化中心,術前1天行無肝素透析。透析效果不如肝素透析,由于手術創傷,肌肉局部壞死,炎癥因子釋放等原因,毒素聚集較平常加重;且由于手術失血,圍手術期補液等因素,容易產生水鈉潴留,電解質紊亂等,因此,有必要在手術后第一天再次行透析,減輕這些因素的影響。圍手術期補液過多,容易導致急性心衰,而補液不足,可能導致休克,因此行中心靜脈置管,監測中心靜脈壓,及時抽血復查,監測紅細胞、血紅蛋白、白蛋白、電解質水平非常重要,根據監測結果精準補液、輸血和補充白蛋白。圍手術期補充促紅細胞生成素和補鐵,增強自身造血能力必不可少。正確的抗骨質疏松治療也是良好的手術療效和防止再骨折的必要措施:補充鈣劑與維生素D,使用降鈣素改善骨質疏松,因雙膦酸鹽類藥物約60%以原形從腎臟排泄,故避免使用雙膦酸鹽類藥物[12-13]。
3.4 股骨頸骨折合并尿毒癥手術注意事項
股骨頸骨折合并尿毒癥患者年齡偏大,一般情況差,不能耐受內固定治療后的長期臥床休息,故推薦行人工髖關節置換術。對于高齡、活動量不大、身體條件差、合并癥多,髖臼無明顯退變的患者推薦采用半髖置換。而身體條件相對較好,活動要求相對較高的選擇全髖置換[14]。本組報告中兩組患者半髖關節置換比例為60%。且兩組患者平均年齡相對較大、骨質疏松嚴重,故大部分患者選擇骨水泥型股骨柄假體[15]。對股骨頸骨折合并尿毒癥施行手術,術中需嚴密監測生命體征,術中保溫,嚴格液體控制。手術關鍵在于微創、精細操作,縮短手術時間,減少手術創傷[16]。術中局部應用氨甲環酸,減少術中及術后出血[17]。
綜上所述,股骨頸骨折合并尿毒癥患者往往全身情況差,合并貧血,骨質疏松等。行人工髖關節置換手術麻醉風險大,輸血率高,但通過積極的圍手術期處理仍能取得較好臨床療效。

