血管緊張素Ⅱ聯合PGA指數對酒精性肝病、食管胃底靜脈曲張及出血的預測意義
徐艷麗 鄧敏 吳一鳴


[摘要] 目的 探討血管緊張素Ⅱ(AngⅡ)聯合PGA指數無創性評估酒精性肝病患者食管胃底靜脈曲張程度及出血風險。 方法 選取2017年6月~2018年6月嘉興市第一醫院收治的82例酒精性肝病患者,用胃鏡檢查評估食管胃底靜脈曲張的程度,并測定血AngⅡ水平,計算PGA指數。比較不同食管胃底靜脈曲張程度患者的AngⅡ水平和PGA指數。隨訪6個月,對AngⅡ和PGA指數預測出血的診斷效能進行比較。 結果 胃鏡下食管胃底靜脈曲張0級組、1級組、2級組、3級組的AngⅡ分別為(2318.621±346.043)pg/mL、(2867.420±383.144)pg/mL、(3430.193±686.725) pg/mL、(4204.723±997.436) pg/mL,PGA指數分別為(2.858±0.210)、(3.848±0.265)、(5.446±0.585)、(7.944±0.891)。AngⅡ和PGA指數均與食管胃底靜脈曲張的嚴重程度相關,AngⅡ的相關系數為0.701,P=0.001;PGA指數的相關系數為0.774,P=0.013。隨訪6個月出血組的AngⅡ為(3705.471±784.323) pg/mL,PGA指數為(6.591±2.094);未出血組的AngⅡ為(3185.862±914.118)pg/mL,PGA指數為(4.851±2.234)。出血組AngⅡ(敏感度0.765,特異度0.646)和PGA指數(敏感度0.882,特異度0.523)均明顯高于未出血組,差異有統計學意義(P<0.05)。 結論 AngⅡ聯合PGA指數能良好預測酒精性肝病患者食管胃底靜脈曲張程度及出血風險,為臨床醫生及時判斷病情、采取進一步措施提供指導意見。
[關鍵詞] 血管緊張素Ⅱ;PGA指數;酒精性肝病;食管胃底靜脈曲張;出血
[中圖分類號] R575.5? ? ? ? ? [文獻標識碼] A? ? ? ? ? [文章編號] 1673-9701(2020)16-0028-04
The predictive significance of angiotensin II combined with PGA index for esophagogastric varices and bleeding in alcoholic liver disease
XU Yanli1 DENG Min1 WU Yiming2
1.Department of Infection, Jiaxing City the First Hospital in Zhejiang Province, Jiaxing? ?314000, China; 2.Institute of Hepatology, Jiaxing City the First Hospital in Zhejiang Province, Jiaxing? ?314000, China
[Abstract] Objective To explore the noninvasive evaluation of angiotensin II (Ang II) combined with PGA index for the degree of esophagogastric varices and the risk of bleeding in patients with alcoholic liver disease. Methods A total of 82 patients with alcoholic liver disease admitted to Tiaxing City First Hospital from June 2017 to June 2018 were selected for gastroscopy to evaluate the degree of esophagogastric varices. The blood Ang II level was determined, and the PGA index was calculated. The Ang II level and PGA index of patients with different esophagogastric varices were compared. The patients were followed up to 6 months. The diagnostic efficacy of Ang II and PGA index in predicting bleeding was compared. Results The Ang II of gastroscopic esophagogastric varices degree 0 group, degree 1 group, degree 2 group and degree 3 group were (2318.621±346.043)pg/mL, (2876.420±383.144)pg/mL, (3340.193±686.725) pg/mL, and (4204.723±997.436)pg/mL, and the PGA indexes were (2.858±0.210), (3.848±0.265), (5.446±0.585), and (7.944±0.891) respectively. Both Ang II and PGA index were related to the severity of esophagogastric varices. The correlation coefficient of Ang II was 0.701, P=0.001. The correlation coefficient of PGA index was 0.774, P=0.013. After 6 months of follow-up, the Ang II and the PGA index was (3705.471±784.323) pg/mL and (6.591±2.094) in the bleeding group. The Ang II of the non-bleeding group was(3185.862±914.118) pg/mL, and the PGA index was (4.851±2.234). The Ang II (sensitivity 0.765, specificity 0.646) and PGA(sensitivity 0.882, specificity 0.523) indexes in the bleeding group were significantly higher than those in the non-bleeding group, and the difference was statistically significant(P<0.05). Conclusion Ang II combined with PGA index can well predict the degree of esophagogastric varices and bleeding risk in patients with alcoholic liver disease. It can provide guidance advice for clinical doctors to timely judge the condition and take further measure.
[Key words] Angiotensin II; PGA index; Alcoholic liver disease; Esophagogastric varices; Bleeding
我國目前有數量龐大的飲酒者,飲酒時間超過5年,或2周內大量飲酒均有導致酒精性肝病的風險[1]。對于該類人群如不及時干預,病情會由初起時的輕型酒精性肝病逐漸發展為酒精性脂肪肝、酒精性肝炎,最終進展為酒精性肝硬化,并引起肝功能衰竭及各種并發癥,其中食管胃底靜脈曲張破裂出血是最嚴重的并發癥及死亡原因之一[2]。多項研究指出,肝硬化伴急性上消化道出血者,出血急性期病死率可高達30%[3]。因此,臨床醫生如能及時篩選出食管胃底靜脈曲張程度重、出血風險大的患者,并采取相應的干預措施,對降低肝病患者出血率、改善預后、提高生存率具有重要意義。目前胃鏡是診斷食管胃底靜脈曲張的金標準[4],但該項操作作為侵入性檢查,患者依從性差,且易造成醫源性再出血。現有相關研究指出,肝硬化患者腎素-血管緊素(Renin-angiotension system,RAS)系統被激活,血管緊張素Ⅱ(AngⅡ)升高,且AngⅡ水平與肝硬化程度、門脈高壓程度均呈正相關[5-7]。PGA指數,包括國際化標準比值(INR)、谷酰轉肽酶(GGT)、載脂蛋白A1,也已被證實與酒精性肝病肝纖維化程度相關[8]。本研究旨在分析非侵入性檢查AngⅡ水平及PGA指數對酒精性肝病患者食管胃底靜脈曲張程度及出血風險的評估,為臨床醫生提供可靠依據,現報道如下。
1 資料與方法
1.1一般資料
選取2017年6月~2018年6月嘉興市第一醫院收治的82例酒精性肝病患者。納入標準[9]:有長期飲酒史(一般超過5年,折合乙醇量男性≥40 g/d,女性≥20 g/d),或2周內有大量飲酒史,折合乙醇量>80 g/d;臨床癥狀為非特異性;血清AST、ALT、谷氨酸轉肽酶(GGT)、TBIL、PT、平均紅細胞容積和缺糖轉鐵蛋白等指標升高;肝臟B型超聲、CT、MRI或瞬時彈性成像檢查有酒精性肝病典型表現;取得患者知情同意并簽署知情同意書。排除標準[10]:高血壓、糖尿病、慢性呼吸系統疾病、惡性腫瘤等基礎疾病者;嗜肝病毒現癥感染、藥物和中毒性肝損傷、自身免疫性肝病者;長期使用血管緊張素轉換酶抑制劑、血管緊張素受體阻滯劑、β受體阻滯劑和鈣通道阻滯劑等藥物的患者。82例患者全部為男性,年齡34~84歲,平均(58.00±14.81)歲。所有患者均行胃鏡檢查評估食管胃底靜脈曲張的程度:無曲張13例,輕度曲張19例,中度曲張32例,重度曲張18例。隨訪6個月,出現食管胃底靜脈曲張破裂出血(包括嘔血、黑便、大便OB陽性)患者17例,未出血患者65例。本項目經嘉興市第一醫院倫理委員會審查通過。
1.2 方法
1.2.1 胃鏡檢查? 根據胃鏡下血管形態對食管胃底靜脈曲張患者進行嚴重程度分級[11],分為0級、1級、2級、3級。見表1。
1.2.2 AngⅡ檢測? 血液樣本取自各項臨床觀察指標的同期,應用EDTA抗凝管收集,隨即3000 r/min離心10 min分離血漿,置-80℃凍存待檢。采用酶聯免疫吸附法(ELISA)檢測,試劑購自美國RB公司。
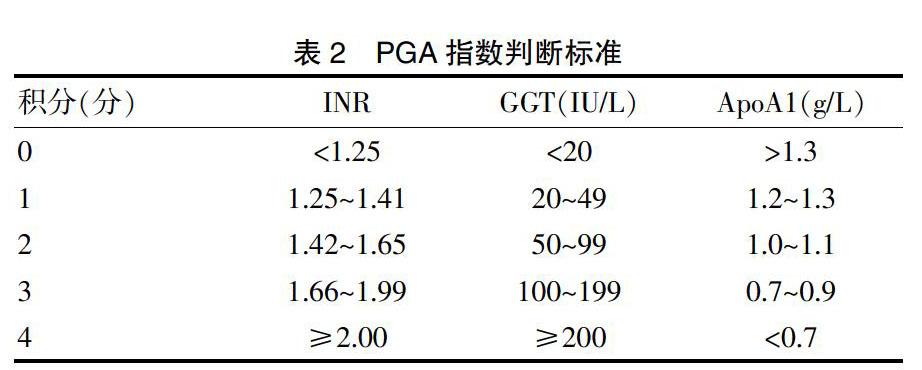
1.2.3 PGA指數測定? PGA指數診斷模型中,INR用希森美康CA7000凝血儀檢測,GGT與ApoAl用貝克曼庫爾特,AU542l用全自動生化儀檢測。PGA指數判斷標準見表2,每例患者根據三項指標的積分之和得出PGA指數,其值0~12[12]。
1.3 觀察指標
觀察食管胃底靜脈曲張0級組、1級組、2級組、3級組患者的AngⅡ和PGA指數及6個月后出血組與未出血組患者AngⅡ和PGA指數及其預測出血的敏感度和特異度。
1.4 統計學處理
采用SPSS19.0統計學軟件,計量資料以(x±s)的形式表示,方差齊性分析采用Levene檢驗,不同程度靜脈曲張分組之間比較先行Kruskal Wallis秩和檢驗,再用Mann-Whitney U檢驗行各組間兩兩比較,相關性分析采用Spearman相關分析。應用ROC曲線分析AngⅡ和PGA指數診斷酒精性肝病食管胃底靜脈曲張破裂出血的準確性,以胃鏡結果為金標準,計算診斷二者的靈敏性、特異性,本研究以靈敏性和特異性之和最大時為最佳界限值。P<0.05表示差異有統計學意義。
2 結果
2.1 不同程度食管胃底靜脈曲張分組的AngⅡ和PGA指數比較
0級組、1級組、2級組、3級組的AngⅡ分別為(2318.621±346.043)pg/mL、(2867.420±383.144)pg/mL、(3430.193±686.725)pg/mL、(4204.723±997.436)pg/mL,PGA指數分別為(2.858±0.210)、(3.848±0.265)、(5.446±0.585)、(7.944±0.891)。食管胃底靜脈曲張程度越重,AngⅡ和PGA指數均逐漸升高,且各級別組間差異均有統計學意義(P<0.05),見表3。AngⅡ和PGA指數均與食管胃底靜脈曲張的嚴重程度相關,AngⅡ的相關系數為0.701(P=0.001),PGA指數的相關系數為0.774(P=0.013)。
2.2 出血組與未出血組的AngⅡ和PGA指數比較
出現食管胃底靜脈曲張破裂出血的患者17例(包括嘔血、黑便、大便OB陽性者),未出血患者65例。出血組的AngⅡ為(3705.471±784.323)pg/mL,PGA指數為(6.591±2.094);未出血組的AngⅡ為(3185.862±914.118)pg/mL,PGA指數為(4.851±2.234)。出血組AngⅡ和PGA指數均明顯高于未出血組,差異有統計學意義(P<0.05)。見表4。
2.3 AngⅡ和PGA指數預測出血診斷效能比較
AngⅡ和PGA指數預測出血的ROC曲線下面積分別為0.709和0.734,最佳界值點分別為3203.00 pg/mL和4.50,敏感度分別為76.5%和88.2%,特異度分別為64.6%和52.3%。PGA指數預測出血的敏感度更高,AngⅡ預測出血的特異度更高。見表5、封三圖1。
3 討論
酒精性肝病(Alcoholic hepatitis)是由于長期大量飲酒導致的肝臟疾病,初期通常表現為脂肪肝,進而可發展成酒精性肝炎、肝纖維化和肝硬化,其主要臨床特征是惡心、嘔吐、黃疸,可有肝臟腫大和壓痛,或并發肝功能衰竭和上消化道出血等。嚴重酗酒時可誘發廣泛肝細胞壞死,甚至肝功能衰竭[13-14]。酒精性肝病是我國常見的肝臟疾病之一,目前在我國乙醇已成為僅次于肝炎病毒導致肝損害的第二大病因,嚴重危害人民健康。酒精性肝病治療難度大,最終引起肝硬化及門靜脈高壓。食管胃底靜脈曲張是門靜脈高壓的并發癥之一,表現為側支血管擴張,最常見于肝硬化,內鏡下可見曲張靜脈。歐美地區主要由酒精性肝病引起,而在世界范圍內則以乙型和丙型肝炎病毒感染為肝硬化的主要原因[15-16]。一旦發生肝硬化,逐漸增加的肝靜脈壓力梯度和惡化的肝功能可能導致食管胃底靜脈曲張形成,并可能發展至臨界點,一旦破裂可引起致命性大出血。食管胃底靜脈曲張破裂出血是肝硬化晚期的主要表現及死亡原因之一,常起病迅猛,病死率高,及時干預治療可減少曲張靜脈破裂出血的發生率,降低死亡率。曲張靜脈的直徑是其破裂出血最重要的預測因素,較大的精脈曲張直徑每年增加15%的患者首次出血的風險最高。失代償性肝硬化和內鏡下的紅痕征也是食管胃底靜脈曲張破裂出血的重要預測因素[17]。胃鏡雖然是診斷食管胃底靜脈曲張及出血的金標準,但為侵入性操作,依從性差,反復操作難度大,因此尋找簡便、非侵入性檢測方法預測食管胃底靜脈曲張程度及出血風險,成為臨床研究的熱點[18]。
目前,有多項研究證實RAS系統中的效應因子AngⅡ與肝纖維化、門脈高壓嚴重程度有密切關系。AngⅡ能夠刺激肝星狀細胞增殖,并向肌成纖維細胞轉化,能夠促進細胞外基質合成,如無有效的治療,將破壞肝臟的正常結構與功能,發展為肝硬化。研究發現AngⅡ水平在肝病患者中明顯升高,且與肝硬化程度呈正相關[19]。相關研究發現PGA指數在診斷酒精性肝病、病毒性肝炎的肝纖維化程度上有較高的敏感性和準確性。研究顯示:PGA≥3時,其肝纖維化診斷與病理組織學診斷符合率達86.25%,而PGA>6時,兩者符合率達92.18%[20]。且PGA是臨床常用的生化指標,各級醫院能夠開展,可廣泛推廣使用。
本研究發現,AngⅡ和PGA指數均與酒精性肝病患者食管胃底靜脈曲張的嚴重程度相關,二者均能預測未來半年內食管胃底靜脈曲張破裂出血的風險,檢測方便,依從性高,可重復性大,為臨床治療策略的制定和治療方法的選擇提供可靠依據,且操作簡便,易臨床推廣。但由于本項研究納入病例偏少,還有待于進一步擴大研究證實。此外,AngⅡ和PGA指數是否能應用于其他肝病(如病毒性肝病、血吸蟲肝病、自身免疫性肝病等),或預測其他并發癥發生率,也有待進一步相關研究。
[參考文獻]
[1] 中華醫學會肝病學分會脂肪肝和酒精性肝病學組,中國醫師協會脂肪性肝病專家委員會.酒精性肝病防治指南(2018年更新版)[J].中華肝臟病雜志,2018,26(3):188-194.
[2] Helmut KS,Ramon B,Helena C Pinto,et al.Alcoholic liver disease[J].Nature Reviews Disease Primers,2018,4(1):1-22.
[3] 屠軍,陳金聯,朱金水.Child-Pugh評分對肝硬化食管胃底靜脈曲張出血患者預后風險因素的臨床評估[J].臨床消化病雜志,2016,28(1):39-41.
[4] 郭蕓蕾,魯曉嵐,程妍,等.肝脾硬度聯合門靜脈寬度評估肝硬化食管胃底靜脈曲張出血風險[J].中華肝臟病雜志,2016,24(1):56-61.
[5] Singal AK,Bataller R,Ahn J,et al.ACG clinical guideline:Alcoholic liver disease[J].The American? Journal of? Gastroenterology,2018,113(2):175-180.
[6] Goldberg D,Ditah IC,Saeian K,et al.Changes in the prevalence of hepatitis C virus infection,nonalcoholic steatohepatitis,and alcoholic liver disease among patients with cirrhosis or liver failure on the waitlist for liver transplantation[J].Gastroenterology,2017,152(5):1090-1099.
[7] 方戴瓊,李蘭娟,郭靜,等.血管緊張素Ⅱ水平與肝硬化嚴重程度的相關性[J].中華肝臟病雜志,2016,24(10):794-796.
[8] Osna NA,Donohue JTM,Kharbanda KK.Alcoholic liver disease:Pathogenesis and current management[J].Alcohol Research:Current Reviews,2017,38(2):147-150.
[9] 李瓊,劉閃閃,徐麗紅,等.肝、脾硬度預測食管胃底靜脈曲張及出血風險[J].中國醫學影像技術,2018,34(4):563-567.
[10] Stickel F,Datz C,Hampe J,et al.Pathophysiology and management of alcoholic liver disease:Update 2016[J].Gut and? Liver,2017,11(2):173-180.
[11] Yang AM,Inamine T,Hochrath K,et al.Intestinal fungi contribute to development of alcoholic liver disease[J].The Journal of Clinical Investigation,2017,127(7):2829-2841.
[12] 楊志花,申鳳俊,黃會芳.慢性乙型肝炎和肝硬化患者AngⅡ、Ang(1-7)及AngⅡ/Ang(1-7)比值的變化[J].中華臨床醫師雜志,2016,10(8):1062-1065.
[13] Dubinkina VB,Tyakht AV,Odintsova VY,et al.Links of gut microbiota composition with alcohol dependence syndrome and alcoholic liver disease[J].Microbiome,2017,5(1):141-150.
[14] Lackner C,Spindelboeck W,Haybaeck J,et al.Histological parameters and alcohol abstinence determine long-term prognosis in patients with alcoholic liver disease[J].Journal of Hepatology,2017,66(3):610-618.
[15] Llorente C,Jepsen P,Inamine T,et al.Gastric acid suppression promotes alcoholic liver disease by inducing overgrowth of intestinal enterococcus[J].Nature Communications,2017,8(1):1-15.
[16] 夏婷,張瑾,姚佳慧,等.氧化應激在酒精性肝病中作用機制的研究進展[J].中國藥理學通報,2017,33(10):1353-1356.
[17] 楊冰冰,胡純秋,胡永迪,等.維生素D缺乏與酒精性肝病的相關性研究[J].安徽醫科大學學報,2019,54(8):1273-1276.
[18] 李苗苗.《2018年美國胃腸病學院酒精性肝病診洽臨床指南》椎薦意見[J].臨床肝膽病雜志,2018,34(3):498-499.
[19] 張艷芳,黃晶.酒精性肝纖維化的血清標志物研究進展[J].臨床肝膽病雜志,2018,34(3):623-626.
[20] 中華醫學會肝病學分會脂肪肝和酒精性肝病學組,中國醫師協會脂肪性肝病專家委員會.酒精性肝病防治指南(2018年更新版)[J].實用肝臟病雜志,2018,21(2):170-176.
(收稿日期:2019-9-10)

